Transkript
SCHWERPUNKT
HPV-Impfung – rund 10 Jahre nach Einführung in der Schweiz
Aktuelle Daten und Hilfen für die Beratung von Adoleszenten und Eltern
Mit der Zulassung des Impfstoffs gegen die onkogenen HPV-Typen 16 und 18 im Jahr 2006 verfügen wir seit bald zehn Jahren über eine effiziente Primärprophylaxe von anogenitalen Dysplasien der entsprechenden Impfvirustypen. Seit 2008 verfügen alle Schweizer Kantone über Impfprogramme, die sich in erster Linie an Mädchen zwischen 11 und 14 Jahren richten. Dennoch bleiben wichtige Fragen offen.
CHRISTINA SCHLATTER GENTINETTA
I Wird es gelingen, dank der Impfung die Inzidenz von Zervixkarzinomen zu senken?
I Ist eine Impfung bei über 16-Jährigen noch sinnvoll?
I Sollen auch Knaben geimpft werden? I Wie sind die beunruhigenden Berichte über
schwere unerwünschte Arzneimittelwirkungen zu bewerten? Der folgende Artikel gibt eine Übersicht über aktuelle Daten und bietet Hilfestellung bei der Beratung von Adoleszenten und ihren Eltern.
HPV-Typen und ihre Risiken
Die meisten Männer und Frauen kommen im Verlauf des Lebens mit HP-Viren in Kontakt. Die Ansteckung geschieht über intimen Hautkontakt, wobei das Präservativ nur unzureichenden Schutz bietet. Wir kennen mittlerweile ungefähr 200 verschiedene HPV-Typen. Für den Grossteil der HPV-bedingten Läsionen ist jedoch nur eine geringe Anzahl von Virustypen verantwortlich. Insgesamt sind 13 onkogene Virus-
Merkpunkte
I Der Langzeiteffekt der HPV-Impfung ist noch unklar. Der Nachweis einer Wirksamkeit gegen das invasive Zervixkarzinom wird in 5 bis 10 Jahren erwartet.
I Die Wirksamkeit der HPV-Impfung bei 12- bis 26-jährigen Frauen gegen CIN2+ 4 Jahre nach Einführung des Impfprogramms in Australien beträgt 46%.
I Wichtiger als das Alter zum Zeitpunkt der Impfung ist deren Durchführung bei sexuell-naiven Frauen.
I Das Hauptproblem global gesehen liegt in der Erreichbarkeit des Risikokollektivs.
I Gemäss vorliegenden Daten ist die Sicherheit der Impfung hoch.
typen bekannt. Dazu zählen neben den häufig vorkommenden Typen 16, 18, 31, 33, 45 (Abbildung) noch die HPV-Typen 35, 39, 51, 52, 56, 58, 59 und 68 (1, 2). Während HPV 16 und 18 zusammen ungefähr 70% der Zervixkarzinome verursachen, sind sie nur für 52% der HSIL-Läsionen an der Portio verantwortlich. Mit anderen Worten: Die Präkanzerosen scheinen ein breiteres Virusspektrum aufzuweisen als die invasiven Karzinome (3).
Die HPV-Impfung
In der Schweiz wurde der quadrivalente Impfstoff Gardasil® im Jahr 2006 zugelassen, der bivalente Impfstoff Cervarix® folgte 2010. Seither wurden in der Schweiz zirka 200 000 Personen gemäss Impfschema (siehe Kasten) geimpft. In der Zielgruppe der Mädchen zwischen 11 und 14 Jahren betrug die Durchimpfungsrate zwischen 2011 und 2014 zirka 51% (4). Weltweit wurden jedoch bereits ungefähr 175 Millionen Impfdosen verabreicht. Ein grosses Problem ist, dass diejenigen Länder mit der Hauptlast an Zervixkarzinomen – die Entwicklungsländer – bis heute kaum Zugang zum Impfstoff haben.
Wie «gut» ist die Wirksamkeit der Impfung?
Die Aussage «Die Impfung schützt zu 98%» ist genauso zutreffend wie die Aussage «Der Impfschutz beträgt 46%». Wichtig ist es zu fragen: Wen schützt die Impfung? Wovor schützt sie? Nach wie vor haben wir keine Daten zu einem effektiven Schutz vor dem invasiven Zervixkarzinom. Ergebnisse der entsprechenden Proof-of-Principle-Studie sind erst in 5 bis 10 Jahren zu erwarten (5). In der Per-Protocoll-Analyse (HPV-naive Frauen vor der Impfung, alle Impfungen zeitgerecht durchgeführt)
20 GYNÄKOLOGIE 5/2015
SCHWERPUNKT
der Future-II-Studie betrug die Wirksamkeit der Impfung für HPV-16/18-assoziierte höhergradige Dysplasien 98% (6). Wie wirksam ist die Impfung aber in der Praxis? Welchen Schutz vor zervikalen Dysplasien darf also eine junge Frau unabhängig vom kausalen HPV-Typ erwarten? Australien war 2007 das erste Land mit einem öffentlich finanzierten nationalen Impfprogramm. In den Schulen weist dieses Programm beeindruckende Impfraten von bis zu 84% für 12- bis 17-Jährige auf, zumindest für die erste Dosis. 4 Jahre nach Einführung der Impfung in Australien zeigt sich nun unter den 108 353 Frauen, die zwischen 2007 und 2011 zum ersten Pap-Screen kamen, eine Wirksamkeit für bioptisch gesichertes CIN2+ von 46%. Die «number needed to vaccinate» zur Verhinderung eines CIN2+ beträgt 125 (3). Dieser Wirksamkeitsnachweis mag auf den ersten Blick im Vergleich zu den oft zitierten Zulassungsdaten enttäuschen. Er ist aber sehr gut, wenn man bedenkt, dass die (bisherigen) Impftypen nur 52% der CIN-Läsionen ausmachen und die Wirksamkeit in der Intention-to-treat-Analyse für alle CIN2+ in der Future-II-Studie nur 17% betrug (6).
Wie sicher ist die HPV-Impfung?
Medien berichteten wiederholt über schwerwiegende Nebenwirkungen in Zusammenhang mit der HPV-Impfung. Insbesondere beziehen sich solche Meldungen auf die Multiple Sklerose. Aus Dänemark und Schweden liegen jedoch mittlerweile grosse Kohortendaten vor (fast 4 Mio. Frauen, davon 789 000 geimpft), welche im Anschluss an eine Impfung kein erhöhtes Risiko für Multiple Sklerose zeigen (4, 7–9). In der Schweiz gingen von 2007 bis 2014 167 Meldungen zu vermuteten Nebenwirkungen ein, 27% davon wurden als «medizinisch wichtig» beurteilt. Aufgrund eines gewissen Risikos für vagovasale Synkopen bei den jungen Mädchen empfiehlt man, die Impfung liegend oder sitzend zu verabreichen. Todesfälle wurden in der Schweiz keine gemeldet. Die initial geäusserten Befürchtungen zur Möglichkeit eines «type replacements» haben sich bis anhin nicht bestätigt. Auch eine grossflächig durchgeführte Impfung hat bisher die Prävalenz verschiedener Virustypen nicht beeinflusst, das ist wahrscheinlich auch mitbedingt durch die niedrige genetische Variabilität der HPV-Viren (10–12).
Ist es sinnvoll, Mädchen über 16 Jahre noch zu impfen?
Ein systemischer Review der Daten aus 46 Publikationen von 13 randomisierten Studien zeigt, dass die Catch-up-Impfung bei über 16-Jährigen keine zusätzlichen unerwünschten Arzneimittelwirkungen verursacht. Allerdings ist die Schutzwirkung nach 4 Jahren für CIN2+ in dieser Altersgruppe nur noch grenzwer-
Abbildung: Die Ursachen/Häufigkeit des Zervixkarzinoms je nach HPV-Typ (adaptiert nach 2)
Kasten:
Aktuelles Impfschema in der Schweiz
I Mädchen und Knaben: I Mädchen:
Gardasil®: Cervarix®:
Impfschema 0, 2, 6 Monate Impfschema 0, 1, 6 Monate
Mädchen bis 15 Jahre: In der Schweiz werden aus Kosteneffizienzgründen nur 2 Dosen verabreicht, ab 15 Jahren 3 Dosen.
Bis 2017 besteht noch eine begrenzte Kostenübernahme für die Catch-upImpfung von 15- bis 26-Jährigen.
tig gegeben mit einem relativen Risiko von 0,8 (95%KI: 0,62–1,02) (1). Entscheidend dürfte sicher weniger das Alter als die Sexualanamnese sein. Wesentlich ist die Komplettierung der Impfung vor dem ersten Intimkontakt.
Sollen Knaben auch geimpft werden?
Seit dem 5. März 2015 empfehlen in der Schweiz das BAG und die EKIF auch die Impfung von Knaben mit Gardasil®. Der Impfschutz der quadrivalenten Impfung für Kondylome ist gut belegt; zudem erhofft man sich einen positiven Effekt bei der Prävention von HPV-bedingten Zungengrund-, Tonsillen- und Analkarzinomen, deren Inzidenz steigend ist. Michael Douglas hat mit seinem Outing diesbezüglich sensibilisiert. Einschränkend ist zu erwähnen, dass gerade bei homosexuellen Männern diese Karzinome häufig durch Nichtimpftypen verursacht werden (13–15).
Ausblick
Im Dezember 2014 hat die FDA in den USA die Marktzulassung für Gardasil 9® erteilt. Es handelt sich dabei um einen 9-valenten HPV-Impfstoff, welcher im Vergleich zu Gardasil® zusätzlich fünf weitere HPVTypen enthält (31, 33, 45, 52 und 58). Der Impfstoff ist indiziert zur Prävention von Zervix-, Vulva-, Vaginalund Analkarzinomen und den entsprechenden präkanzerösen Läsionen. Zusätzlich schützt der Impfstoff
GYNÄKOLOGIE 5/2015
21
SCHWERPUNKT
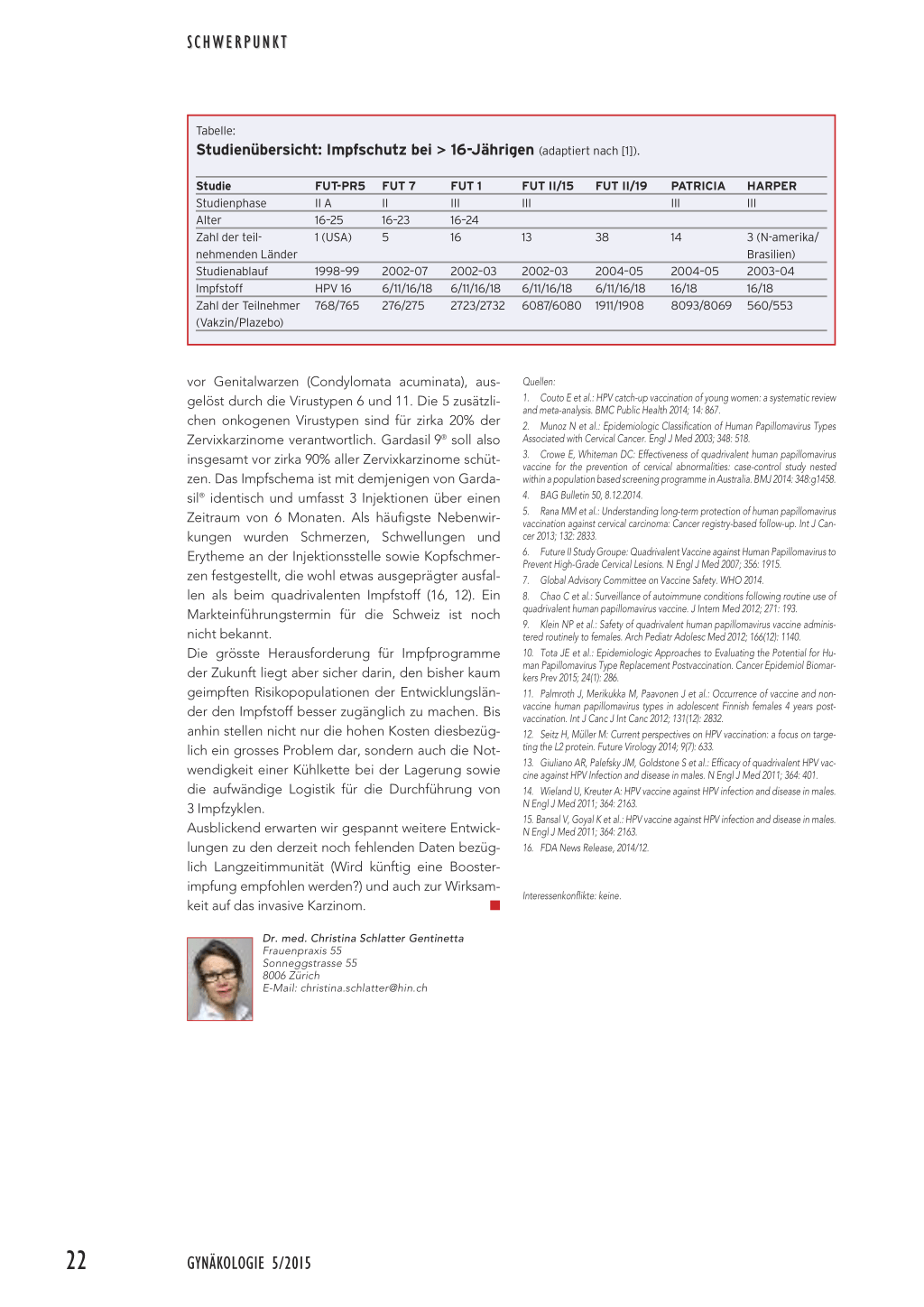
Tabelle:
Studienübersicht: Impfschutz bei > 16-Jährigen (adaptiert nach [1]).
Studie Studienphase Alter Zahl der teilnehmenden Länder Studienablauf Impfstoff Zahl der Teilnehmer (Vakzin/Plazebo)
FUT-PR5 II A 16–25 1 (USA)
1998–99 HPV 16 768/765
FUT 7 II 16–23 5
2002–07 6/11/16/18 276/275
FUT 1 III 16–24 16
2002–03 6/11/16/18 2723/2732
FUT II/15 FUT II/19 III
13 38
2002–03 2004–05 6/11/16/18 6/11/16/18 6087/6080 1911/1908
PATRICIA HARPER III III
14
2004–05 16/18 8093/8069
3 (N-amerika/ Brasilien) 2003–04 16/18 560/553
vor Genitalwarzen (Condylomata acuminata), aus-
gelöst durch die Virustypen 6 und 11. Die 5 zusätzli-
chen onkogenen Virustypen sind für zirka 20% der
Zervixkarzinome verantwortlich. Gardasil 9® soll also
insgesamt vor zirka 90% aller Zervixkarzinome schüt-
zen. Das Impfschema ist mit demjenigen von Garda-
sil® identisch und umfasst 3 Injektionen über einen
Zeitraum von 6 Monaten. Als häufigste Nebenwir-
kungen wurden Schmerzen, Schwellungen und
Erytheme an der Injektionsstelle sowie Kopfschmer-
zen festgestellt, die wohl etwas ausgeprägter ausfal-
len als beim quadrivalenten Impfstoff (16, 12). Ein
Markteinführungstermin für die Schweiz ist noch
nicht bekannt.
Die grösste Herausforderung für Impfprogramme
der Zukunft liegt aber sicher darin, den bisher kaum
geimpften Risikopopulationen der Entwicklungslän-
der den Impfstoff besser zugänglich zu machen. Bis
anhin stellen nicht nur die hohen Kosten diesbezüg-
lich ein grosses Problem dar, sondern auch die Not-
wendigkeit einer Kühlkette bei der Lagerung sowie
die aufwändige Logistik für die Durchführung von
3 Impfzyklen.
Ausblickend erwarten wir gespannt weitere Entwick-
lungen zu den derzeit noch fehlenden Daten bezüg-
lich Langzeitimmunität (Wird künftig eine Booster-
impfung empfohlen werden?) und auch zur Wirksam-
keit auf das invasive Karzinom.
I
Quellen: 1. Couto E et al.: HPV catch-up vaccination of young women: a systematic review and meta-analysis. BMC Public Health 2014; 14: 867. 2. Munoz N et al.: Epidemiologic Classification of Human Papillomavirus Types Associated with Cervical Cancer. Engl J Med 2003; 348: 518. 3. Crowe E, Whiteman DC: Effectiveness of quadrivalent human papillomavirus vaccine for the prevention of cervical abnormalities: case-control study nested within a population based screening programme in Australia. BMJ 2014: 348:g1458. 4. BAG Bulletin 50, 8.12.2014. 5. Rana MM et al.: Understanding long-term protection of human papillomavirus vaccination against cervical carcinoma: Cancer registry-based follow-up. Int J Cancer 2013; 132: 2833. 6. Future II Study Groupe: Quadrivalent Vaccine against Human Papillomavirus to Prevent High-Grade Cervical Lesions. N Engl J Med 2007; 356: 1915. 7. Global Advisory Committee on Vaccine Safety. WHO 2014. 8. Chao C et al.: Surveillance of autoimmune conditions following routine use of quadrivalent human papillomavirus vaccine. J Intern Med 2012; 271: 193. 9. Klein NP et al.: Safety of quadrivalent human papillomavirus vaccine administered routinely to females. Arch Pediatr Adolesc Med 2012; 166(12): 1140. 10. Tota JE et al.: Epidemiologic Approaches to Evaluating the Potential for Human Papillomavirus Type Replacement Postvaccination. Cancer Epidemiol Biomarkers Prev 2015; 24(1): 286. 11. Palmroth J, Merikukka M, Paavonen J et al.: Occurrence of vaccine and nonvaccine human papillomavirus types in adolescent Finnish females 4 years postvaccination. Int J Canc J Int Canc 2012; 131(12): 2832. 12. Seitz H, Müller M: Current perspectives on HPV vaccination: a focus on targeting the L2 protein. Future Virology 2014; 9(7): 633. 13. Giuliano AR, Palefsky JM, Goldstone S et al.: Efficacy of quadrivalent HPV vaccine against HPV Infection and disease in males. N Engl J Med 2011; 364: 401. 14. Wieland U, Kreuter A: HPV vaccine against HPV infection and disease in males. N Engl J Med 2011; 364: 2163. 15. Bansal V, Goyal K et al.: HPV vaccine against HPV infection and disease in males. N Engl J Med 2011; 364: 2163. 16. FDA News Release, 2014/12.
Interessenkonflikte: keine.
Dr. med. Christina Schlatter Gentinetta Frauenpraxis 55 Sonneggstrasse 55 8006 Zürich E-Mail: christina.schlatter@hin.ch
22 GYNÄKOLOGIE 5/2015