Transkript
LEBENSMITTELRECHT
Foto: zVg
Lebensmittel – keine Heilmittel
Schweizer Recht bei Nahrungsergänzungsmitteln
Monika Wymann, Ursula Deiss
Monika Wymann
«Wer Nahrungs
ergänzungsmittel in Verkehr bringt, ist selbst dafür verant-
»wortlich, dass diese
sicher sind.
Nahrungsergänzungsmittel sind Lebensmittel und keine Heilmittel. Damit ein Lebensmittel als Nahrungsergänzungsmittel in Verkehr gebracht werden kann, müssen spezifische Anforderungen erfüllt sein. Werbung, die Nahrungsergänzungsmitteln Eigenschaften der Heilung, der Linderung oder der Verhütung von Krankheiten zumisst, ist verboten.
Nach Schweizer Recht (1) sind Nahrungsergänzungsmittel Lebensmittel, die dazu bestimmt sind, die normale Ernährung zu ergänzen. Sie bestehen aus Einfach- oder Mehrfachkonzentraten von Vitaminen, Mineralstoffen oder sonstigen Stoffen mit ernährungsspezifischer oder physiologischer Wirkung und werden in dosierter Form in Verkehr gebracht. Nahrungsergänzungsmittel dürfen nur vorverpackt in Verkehr gebracht werden, ausser sie werden an Konsumentinnen und Konsumenten zum direkten Verzehr abgegeben (2). Sie müssen zur Aufnahme in abgemessenen kleinen Mengen, in Form von Kapseln, Pastillen, Tabletten, Pillen oder anderen ähnlichen Darreichungsformen oder in Form von Pulverbeuteln, Flüssigampullen, Flaschen mit Tropfeinsätzen oder ähnlichen Darreichungsformen von Flüssigkeiten und Pulvern, angeboten werden (3).
Spezifische Stoffe mit ernährungsspezifischer oder physiologischer Wirkung
Nahrungsergänzungsmittel müssen einen oder mehrere charakteristische Stoffe mit ernährungsspezifischer oder physiologischer Wirkung aufweisen. Sie dürfen ausschliesslich die in Anhang 1 Teil A, der Verordnung des EDI über Nahrungsergänzungsmittel (VNem) aufgeführten Vitamine und Mineralstoffe unter den dort aufgeführten Bedingungen enthalten. Die Zulässigkeit sonstiger Stoffe richtet sich nach Anhang 1 Teil B, dieser Verordnung. Während die Liste der zulässigen Vitamine und Mineralstoffe abschliessend ist, ist diejenige der zulässigen sonstigen Stoffe offen formuliert. Auch sie enthält jedoch Einschränkungen (4). Die in Anhang 1 der VNem festgelegten Höchstmengen für Vitamine, Mineralstoffe und sonstigen Stoffe dürfen pro empfohlene tägliche Verzehrsmenge nicht überschritten werden (5). Die zulässigen Verbindungen der Vitamine, Mineralstoffe und sonstigen Stoffe regelt Anhang 2 der VNem. Die VNem enthält weitere spezifische Anforderungen, so beispielsweise an in Nahrungsergänzungsmitteln verwendete neuartige Lebensmittel, die Verwendung lebender Bakterienkulturen oder den Zusatz basischer Mineralstoffe.
Den Nahrungsergänzungsmitteln dürfen weitere Lebensmittel zugegeben werden, wenn das End erzeugnis die in der VNem festgelegten Bedingungen trotzdem einhält.
Verbotene Stoffe
Nicht in Nahrungsergänzungsmitteln eingesetzt werden dürfen bestimmte Stoffe, wenn sie toxikologisch bedenklich sind oder eine pharmakologische Wirkung entfalten, wie sie laut der gesetzlichen Definition Arzneimitteln vorbehalten ist. Manche dieser Stoffe sind in den im Schweizer Lebensmittelrecht festgelegten, nicht abschliessenden Verbotslisten für Stoffe (6) und Pflanzen (7) aufgeführt. Häufig besitzen die eingesetzten Stoffe keine Verwendungsgeschichte als sicheres Lebensmittel/Nahrungsergänzungsmittel vor dem 15. Mai 1997 in der EU oder in der Schweiz und benötigen deshalb eine Bewilligung als neuartige Lebensmittel (Novel Food) (8). Grundsätzlich benötigen Nahrungsergänzungsmittel keine Bewilligung (Ausnahme: Novel Food, nicht gelistete gesundheitsbezogene Angaben, gentechnisch veränderte Organismen oder daraus gewonnene Stoffe). Wer Nahrungsergänzungsmittel in Verkehr bringt, ist selbst dafür verantwortlich, dass diese sicher sind. Im Rahmen der Selbstkontrolle ist zu gewährleisten, dass alle einschlägigen Bestimmungen der Lebensmittelgesetzgebung eingehalten werden. Die jeweils zuständige kantonale Vollzugsbehörde kontrolliert die Einhaltung der rechtlichen Vorgaben sowie die Beachtung der Selbstkontrollpflicht stichprobenweise. Der Lebensmittelbetrieb ist bei dieser meldepflichtig (9).
Produkte aus dem Internet – auf eigenes Risiko
Die gesetzlichen Vorschriften gelten auch für Produkte, die über das Internet vertrieben werden. Wer auf einer ausländischen Internetseite für den privaten persönlichen Gebrauch Nahrungsergänzungsmittel bestellt, tut dies jedoch auf eigenes Risiko. Solche im Ausland bestellten Produkte werden vom Geltungs-
6 Schweizer Zeitschrift für Ernährungsmedizin 1|2023
LEBENSMITTELRECHT
bereich des Schweizer Lebensmittelgesetzes (LMG) (10) nicht erfasst. Sie werden von der Schweizer Lebensmittelkontrolle nicht überwacht. Werden sie aber an Dritte weitergegeben, findet das LMG seine volle Anwendung. Das schweizerische Recht über Nahrungsergänzungsmittel orientiert sich an demjenigen der EU (11). Namentlich die Definition der Nahrungsergänzungsmittel (Art. 1 VNem) stimmt mit dem Recht der EU überein. Ein wesentlicher Unterschied zwischen dem Schweizer Recht und demjenigen der EU ergibt sich daraus, dass das Schweizer Recht sowohl für Vitamine und Mineralstoffe als auch für gewisse sonstige Stoffe Höchstmengen festlegt. In der EU sind zwar Bestrebungen im Gange, solche EU-weit harmonisierten Werte festzulegen, bisher konnte aber keine Einigung erzielt werden. Somit sind länderspezifische Regelungen möglich.
Das neue Schweizer Höchstmengenmodell
Seit dem 1. Juli 2020 besitzt die Schweiz ein neues Höchstmengenmodell für Vitamine und Mineralstoffe (siehe Tabellen 1 und 2). Die früheren Höchstmengen berücksichtigten in der Regel den Tagesbedarf eines Nährstoffs. Das neue Modell orientiert sich am Gesundheitsschutz und basiert auf aktuellen wissenschaftlichen Erkenntnissen. Die überarbeiteten Höchstwerte wurden für Nahrungsergänzungsmittel in Anhang 1 Teil A der VNem, für Lebensmittel für Sportlerinnen und Sportler in Anhang 11 der VLBE (siehe Tabelle 2 [12]) und zur Anreicherung von Lebensmitteln in Anhang 1 der VZVM übernommen (siehe Tabelle 1). Eine der Grundlagen für das neue Konzept war die Publikation des deutschen Bundesinstituts für Risikobewertung (BfR) «Höchstmengen für Vitamine und Mineralstoffe in Nahrungsergänzungsmitteln» (2018) (13). Das Konzept basiert auf dem Tolerable Upper Intake Level (UL) und auf Daten zum Verzehr der einzelnen Nährstoffe über die normale tägliche Ernährung. Die Menge eines Vitamins oder Mineralstoffs, welche für eine zusätzliche Zufuhr über Nahrungsergänzungsmittel und angereicherte Lebensmittel zur Verfügung steht, wurde durch Abzug der Zufuhr über die herkömmliche tägliche Ernährung (Basisaufnahme, BA) vom UL berechnet. Für die Abschätzung der Zufuhr der Nährstoffe über konventionelle Lebensmittel wurden die Ergebnisse der nationalen Verzehrstudie II von Deutschland verwendet. Es wurden grundsätzlich die Daten von Männern der Altersklasse 14 bis 80 Jahre, 90. Zufuhrperzentile, berücksichtigt (Ausnahme: Kalzium, Eisen und Jod). Die 90. Zufuhrperzentile entspricht der Menge, die von 90% der Bevölkerung nicht überschritten wird. Waren in der Verzehrsstudie II keine Verzehrsdaten vorhanden (Bor, Kupfer, Molybdän, Selen), wurden Daten aus weiteren Quellen verwendet. Für die Verteilung der Restmenge wurden die Stoffe in 4 Gruppen eingeteilt: – Gruppe 1: unkritische Stoffe; für die Stoffe dieser
Gruppe wurde kein Höchstwert mehr festgelegt
Abbildung: Modell zur Herleitung der Höchstwerte BA = Aufnahme mit konventionellen Lebensmitteln; RNEM = zur Verfügung für Nahrungsergänzungsmittel resp. Lebensmittel für Sportlerinnen und Sportler, Rang. LM: zur Verfügung für angereicherte Lebensmittel UL = Tolerable Upper Intake Level Die Differenz zwischen dem UL und der BA ist die Menge pro Nährstoff, welche für angereicherte Lebensmittel und Nahrungsergänzungsmittel resp. Lebensmittel für Sportlerinnen und Sportler zur Verfügung steht.
Tabelle 1:
Höchstmengen für Vitamine und Mineralstoffe in angereicherten Lebensmitteln (VZVM) vor und nach Inkrafttreten des neuen Höchstmengenmodells
Stoff Vitamin A Vitamin D Vitamin E Vitamin C Vitamin K Vitamin B1 (Thiamin) Vitamin B2 (Riboflavin) Niacin (Vitamin PP) Vitamin B6 Folsäure Vitamin B12 Biotin Pantothensäure Kalzium Phosphor Eisen Magnesium Zink Iod Selen Kupfer Mangan Chrom Molybdän Fluorid Kalium Chlorid
Lebensmittelrecht 2017 800 µg 15 µg 12 mg 100 mg 75 µg 1,1 mg 1,4 mg 16 mg 1,4 mg 300 µg 3 µg 50 µg 6 mg 1000 mg 700 mg 14 mg 375 mg 10 mg 150 µg 60 µg 1 mg 2 mg 40 µg 50 µg 3,5 mg 2000 mg 800 mg
Revision 2020 450 µg *1 23 µg 68 mg 250 mg 24 µg keine keine 200 mg 5 mg 250 µg keine keine keine
250 (700 *2) mg Nur als Begleition
7 mg 250 mg 1,8 mg 200 µg 55 µg 0,5 mg 1 mg 62 µg 100 µg
– 750 mg Nur als Begleition
*1Nur als ß-Carotin zulässig. Entspricht 2,7 mg ß-Carotin. *2Nur Ersatzprodukte für Milch und Milchprodukte.
Schweizer Zeitschrift für Ernährungsmedizin 1|2023 7
LEBENSMITTELRECHT
(z. B. Vitamin B1, B2, B12, Biotin, Pantothensäure). Im Rahmen der Selbstkontrolle muss sichergestellt werden, dass der Gesundheits- und Täuschungsschutz eingehalten wird. – Gruppe 2: Stoffe mit grossem Abstand UL zu BA (d. h. mit grosser Restmenge bzw. tiefem Risiko, den UL zu überschreiten) (β-Carotin, Folsäure, Niacin,
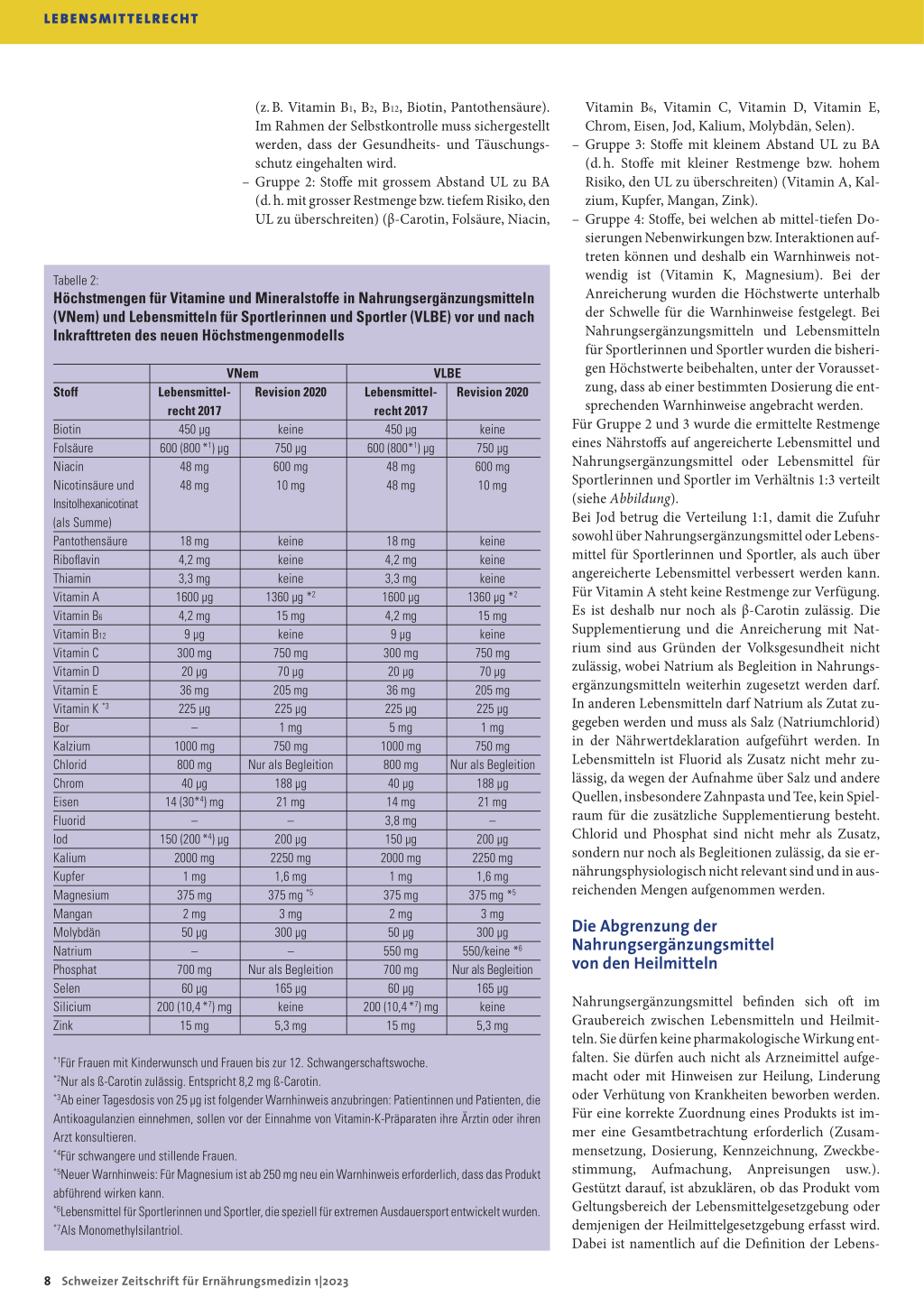
Tabelle 2:
Höchstmengen für Vitamine und Mineralstoffe in Nahrungsergänzungsmitteln (VNem) und Lebensmitteln für Sportlerinnen und Sportler (VLBE) vor und nach Inkrafttreten des neuen Höchstmengenmodells
VNem VLBE
Stoff
Lebensmittel- Revision 2020
Lebensmittel- Revision 2020
recht 2017
recht 2017
Biotin
450 µg
keine
450 µg
keine
Folsäure
600 (800 *1) μg
750 µg
600 (800*1) μg
750 µg
Niacin
48 mg
600 mg
48 mg
600 mg
Nicotinsäure und
48 mg
10 mg
48 mg
10 mg
Insitolhexanicotinat
(als Summe)
Pantothensäure
18 mg
keine
18 mg
keine
Riboflavin
4,2 mg
keine
4,2 mg
keine
Thiamin
3,3 mg
keine
3,3 mg
keine
Vitamin A
1600 µg
1360 µg *2
1600 µg
1360 μg *2
Vitamin B6
4,2 mg
15 mg
4,2 mg
15 mg
Vitamin B12
9 µg keine
9 µg keine
Vitamin C
300 mg
750 mg
300 mg
750 mg
Vitamin D
20 µg
70 µg
20 µg
70 µg
Vitamin E
36 mg
205 mg
36 mg
205 mg
Vitamin K *3
225 µg
225 µg
225 µg
225 µg
Bor
– 1 mg
5 mg
1 mg
Kalzium
1000 mg
750 mg
1000 mg
750 mg
Chlorid
800 mg
Nur als Begleition
800 mg Nur als Begleition
Chrom
40 µg
188 µg
40 µg
188 µg
Eisen
14 (30*4) mg
21 mg
14 mg
21 mg
Fluorid
–
–
3,8 mg
–
Iod
150 (200 *4) μg
200 µg
150 µg
200 µg
Kalium
2000 mg
2250 mg
2000 mg
2250 mg
Kupfer
1 mg
1,6 mg
1 mg
1,6 mg
Magnesium
375 mg
375 mg *5
375 mg
375 mg *5
Mangan
2 mg
3 mg
2 mg
3 mg
Molybdän
50 µg
300 µg
50 µg
300 µg
Natrium
–
–
550 mg
550/keine *6
Phosphat
700 mg
Nur als Begleition
700 mg Nur als Begleition
Selen
60 µg
165 µg
60 µg
165 µg
Silicium
200 (10,4 *7) mg
keine
200 (10,4 *7) mg
keine
Zink
15 mg
5,3 mg
15 mg
5,3 mg
*1Für Frauen mit Kinderwunsch und Frauen bis zur 12. Schwangerschaftswoche. *2Nur als ß-Carotin zulässig. Entspricht 8,2 mg ß-Carotin. *3Ab einer Tagesdosis von 25 µg ist folgender Warnhinweis anzubringen: Patientinnen und Patienten, die Antikoagulanzien einnehmen, sollen vor der Einnahme von Vitamin-K-Präparaten ihre Ärztin oder ihren Arzt konsultieren. *4Für schwangere und stillende Frauen. *5Neuer Warnhinweis: Für Magnesium ist ab 250 mg neu ein Warnhinweis erforderlich, dass das Produkt abführend wirken kann. *6Lebensmittel für Sportlerinnen und Sportler, die speziell für extremen Ausdauersport entwickelt wurden. *7Als Monomethylsilantriol.
Vitamin B6, Vitamin C, Vitamin D, Vitamin E, Chrom, Eisen, Jod, Kalium, Molybdän, Selen). – Gruppe 3: Stoffe mit kleinem Abstand UL zu BA (d. h. Stoffe mit kleiner Restmenge bzw. hohem Risiko, den UL zu überschreiten) (Vitamin A, Kalzium, Kupfer, Mangan, Zink). – Gruppe 4: Stoffe, bei welchen ab mittel-tiefen Dosierungen Nebenwirkungen bzw. Interaktionen auftreten können und deshalb ein Warnhinweis notwendig ist (Vitamin K, Magnesium). Bei der Anreicherung wurden die Höchstwerte unterhalb der Schwelle für die Warnhinweise festgelegt. Bei Nahrungsergänzungsmitteln und Lebensmitteln für Sportlerinnen und Sportler wurden die bisherigen Höchstwerte beibehalten, unter der Voraussetzung, dass ab einer bestimmten Dosierung die entsprechenden Warnhinweise angebracht werden. Für Gruppe 2 und 3 wurde die ermittelte Restmenge eines Nährstoffs auf angereicherte Lebensmittel und Nahrungsergänzungsmittel oder Lebensmittel für Sportlerinnen und Sportler im Verhältnis 1:3 verteilt (siehe Abbildung). Bei Jod betrug die Verteilung 1:1, damit die Zufuhr sowohl über Nahrungsergänzungsmittel oder Lebensmittel für Sportlerinnen und Sportler, als auch über angereicherte Lebensmittel verbessert werden kann. Für Vitamin A steht keine Restmenge zur Verfügung. Es ist deshalb nur noch als β-Carotin zulässig. Die Supplementierung und die Anreicherung mit Natrium sind aus Gründen der Volksgesundheit nicht zulässig, wobei Natrium als Begleition in Nahrungsergänzungsmitteln weiterhin zugesetzt werden darf. In anderen Lebensmitteln darf Natrium als Zutat zugegeben werden und muss als Salz (Natriumchlorid) in der Nährwertdeklaration aufgeführt werden. In Lebensmitteln ist Fluorid als Zusatz nicht mehr zulässig, da wegen der Aufnahme über Salz und andere Quellen, insbesondere Zahnpasta und Tee, kein Spielraum für die zusätzliche Supplementierung besteht. Chlorid und Phosphat sind nicht mehr als Zusatz, sondern nur noch als Begleitionen zulässig, da sie ernährungsphysiologisch nicht relevant sind und in ausreichenden Mengen aufgenommen werden.
Die Abgrenzung der Nahrungsergänzungsmittel von den Heilmitteln
Nahrungsergänzungsmittel befinden sich oft im Graubereich zwischen Lebensmitteln und Heilmitteln. Sie dürfen keine pharmakologische Wirkung entfalten. Sie dürfen auch nicht als Arzneimittel aufgemacht oder mit Hinweisen zur Heilung, Linderung oder Verhütung von Krankheiten beworben werden. Für eine korrekte Zuordnung eines Produkts ist immer eine Gesamtbetrachtung erforderlich (Zusammensetzung, Dosierung, Kennzeichnung, Zweckbestimmung, Aufmachung, Anpreisungen usw.). Gestützt darauf, ist abzuklären, ob das Produkt vom Geltungsbereich der Lebensmittelgesetzgebung oder demjenigen der Heilmittelgesetzgebung erfasst wird. Dabei ist namentlich auf die Definition der Lebens-
8 Schweizer Zeitschrift für Ernährungsmedizin 1|2023
LEBENSMITTELRECHT
mittel nach Art. 4 LMG und diejenige der Arzneimittel und Medizinprodukte in Art. 4 Heilmittelgesetz (14) abzustellen. Weitere Informationen zur Abgrenzung von Lebensmitteln und Arzneimitteln liefert der Abgrenzungsbericht (15).
Abgabe von Nahrungsergänzungsmitteln an Patientinnen und Patienten
Wer Nahrungsergänzungsmittel an Patientinnen und Patienten abgibt, muss lebensmittelrechtlich dieselben Anforderungen erfüllen, wie sie erfüllt sein müssen, wenn im Detailhandel solche Produkte an Konsumentinnen oder Konsumenten abgegeben werden. Vorverpackte Nahrungsergänzungsmittel müssen korrekt gekennzeichnet sein, sie müssen hinsichtlich der Zusammensetzung die Anforderungen der VNem erfüllen (Ziff. 1 oben), die abgebende Person ist zur Selbstkontrolle verpflichtet und es gelten auch alle anderen Anforderungen und Pflichten nach dem LMG (16).
Heilanpreisung nicht erlaubt
Weitere Informationen
Die Internetseite des Bundesamts für Lebensmittelsicherheit und Veterinärwesen (BLV) führt weitere detaillierte Informationen zu Nahrungsergänzungsmitteln auf.
Korrespondenzadressen: Monika Wymann, MLaw Wissenschaftliche Mitarbeiterin des Bundesamts für Lebensmittelsicherheit und Veterinärwesen (BLV), Rechtsdienst, Eidgenössisches Departement des Innern (EDI) Schwarzenburgstrasse 155 3003 Bern E-Mail: monika.wymann@blv.admin.ch Ursula Deiss, dipl. pharm., Lebensmittelchemikerin Wissenschaftliche Mitarbeiterin des Bundesamts für Lebensmittelsicherheit und Veterinärwesen (BLV), Abteilung Lebensmittel und Ernährung, Eidgenössisches Departement des Innern (EDI) Schwarzenburgstrasse 155 3003 Bern E-Mail: Ursula.Deiss@blv.admin.ch
Insbesondere hervorzuheben ist, dass bei solchen Abgaben das Heilanpreisungsverbot nach Art. 12 Abs. 2 Bst. c LGV zur Anwendung gelangt. So ist es zum Beispiel auch einer Ärztin oder einem Arzt nicht erlaubt, gegenüber Patientinnen und Patienten im Zusammenhang mit Nahrungsergänzungsmitteln heilende, lindernde oder krankheitsverhütende Eigenschaften zu versprechen. Auf dieses Verbot ist zurückzuführen, dass, wer Nahrungsergänzungsmittel an Ärztinnen oder Ärzte verkaufen will, diesen kein Werbe- oder Informationsmaterial über beispielsweise pharmakologische Wirkungen dieser Produkte zukommen lassen darf. Das Anpreisen solcher Wirkungen ist nur im Zusammenhang mit Heilmitteln erlaubt. Bei Lebensmitteln ist es verboten. Dies entspricht nicht nur der Vollzugspraxis der Lebensmittelkontrollbehörden, sondern auch der Gerichtspraxis des Schweizerischen Bundesgerichts und des Europäischen Gerichtshofs. Diese haben in ihren Urteilen (17) festgehalten, dass nährwert- und gesundheitsbezogene Angaben in kommerziellen Mitteilungen über Lebensmittel, die als solche an die Endverbraucherinnen oder die Endverbraucher abgegeben werden sollen, die lebensmittelrechtlichen Anforderungen erfüllen müssen, auch wenn sich diese Mitteilungen nicht an die Endverbraucherinnen und Endverbraucher, sondern ausschliesslich an medizinische Fachkreise richten. Begründet hat er dies unter anderem damit, dass die Kommunikation in einem solchen Fall zwischen den Lebensmittelunternehmen und den medizinischen Fachkreisen hauptsächlich auf die Endverbraucherinnen und Endverbraucher abzielt, damit sie das Lebensmittel, das Gegenstand der Kommunikation ist, auf Empfehlung dieser Fachkreise erwerben.
Direkter Link zu BLV: Nahrungsergänzungsmittel www.blv.admin.ch Referenzen: 1. Art. 1 der Verordnung des EDI über Nahrungsergänzungsmittel (VNem,
SR 817.022.14). 2. Art. 2 Abs. 1 VNem. 3. Art. 2 Abs. 2 VNem. 4. Art. 2 Abs. 3 VNem. 5. Art. 2 Abs. 5 VNem. 6. Anhang 4 der Verordnung des EDI über den Zusatz von Vitaminen,
Mineralstoffen und sonstigen Stoffen in Lebensmitteln (VZVM, SR 817.022.32). 7. Anhang 1 der Verordnung des EDI über Lebensmittel pflanzlicher Herkunft, Pilze und Speisesalz (VLpH, SR 817.022.17). 8. Art. 16 der Verordnung über Lebensmittel und Gebrauchsgegenstände (LGV, SR 817.02). 9. Art. 20 LGV 10. Bundesgesetz über Lebensmittel und Gebrauchsgegenstände (LMG, SR 817.0). 11. Richtlinie 2002/46/EG des europäischen Parlaments und des Rates vom 10. Juni 2022 zur Angleichung der Rechtsvorschriften der Mitgliedstaaten über Nahrungsergänzungsmittel, ABl. L 183 vom 12.7.2002, S. 51; zuletzt geändert durch Verordnung (EU) 2021/418 vom 9. März 2021, ABl. 83 vom 10.3.2021, S. 1. 12. Verordnung des EDI über Lebensmittel für Personen mit besonderem Ernährungsbedarf (VLBE, SR 817.022.104). 13. Weissenborn A. et al. Höchstmengen für Vitamine und Mineralstoffe in Nahrungsergänzungsmitteln. Journal of Consumer Protection and Food Safety 13:25-39, 2018. 14. Bundesgesetz über Arzneimittel und Medizinprodukte (HMG, SR 812.21). 15. Abgrenzungskriterien Heilmittel – Lebensmittel bezüglich oral einzunehmender Produkte. Bundesamt für Lebensmittelsicherheit und Veterinärwesen (BLV), Swissmedic und Bundesamt für Gesundheit (BAG). Die 3. aktualisierte Version wurde 2021 publiziert. 17. BGer_2C733/2020 vom 15. März 2021, E. 4 ff.; Urteil EuGH, Rs C-19/15 vom 14. Juli 2016.
10 Schweizer Zeitschrift für Ernährungsmedizin 1|2023