Transkript
Im Fokus: Tumoren im Kindesalter
Schmerztherapie bei Kindern mit malignen Tumoren
Das ganzheitliche Konzept in der pädiatrischen Onkologie
An Krebs erkrankte Kinder erleiden wie Erwachsene mitunter stärkste Schmerzen durch die Krankheit, Therapie und deren Folgen. Dabei sind in der Praxis teilweise ärztliche Vorbehalte und Unsicherheiten hinsichtlich der pädiatrischen Opioidtherapie zu überwinden. Wichtige Grundsätze der nichtmedikamentösen und medikamentösen Schmerztherapie werden im Folgenden aufgezeigt.
EVA BERGSTRÄSSER, DANIEL ZEHNDER
Eva Bergsträsser Daniel Zehnder
10
Fast alle an Krebs erkrankten Kinder leiden wie Erwachsene unter Schmerzen, die entweder durch die Krankheit selbst oder invasive Massnahmen, Therapiefolgen (Mukositis etc.) und die psychische Belastung hervorgerufen werden. Die psychische Belastung setzt sich aus einer Vielzahl von Faktoren zusammen, wie Entwicklungsstand des Kindes, Krankheits- und Therapieverständnis, soziales Umfeld und Einstellung des Umfeldes zur Erkrankung sowie soziokulturelle Faktoren. Das medizinische Personal trägt im Umgang mit potenziellen und tatsächlichen Schmerzen des Kindes und seines familiären Umfeldes eine grosse Verantwortung. Damit ist aber auch die Möglichkeit gegeben, dem Kind und seiner Familie vieles im Verlauf seiner Krankheit, Behandlung und Krankheitsverarbeitung zu erleichtern.
Grundsätzliche Aspekte in der Kinderonkologie
Eine wichtige Grundlage für diese Fragestellung liefert die deutsche Übersetzung der WHO-Empfehlungen «Cancer Pain and Palliative Care in Children» (1, 2). Nach wie vor bestehen viele, überwiegend unberechtigte Vorbehalte, Ängste und Missverständnisse bezüglich des Einsatzes von Opioiden bei starken Schmerzen (3). Dazu gehören: ▲ Ängste, dass Opioide zu einer Medikamentenab-
hängigkeit führen ▲ Unsicherheiten bei der Opioiddosierung bei Kin-
dern, was zu einer Zurückhaltung in der Verordnung und häufig Unterdosierung führt
Bemerkung: Zur Erleichterung der Lesbarkeit wurde die männliche Form gewählt, selbstverständlich sind beide Geschlechter gemeint. Wenn vom Kind die Rede ist, ist auch der Jugendliche angesprochen.
▲ unzureichende Kenntnisse des kindlichen Schmerz- und Krankheitserlebens
▲ Unsicherheiten darüber, welche Interventionen neben der Medikation zum verbesserten Umgang des Kindes mit unangenehmen/schmerzhaften Prozeduren beitragen.
Die Schmerzbehandlung, insbesondere die vorbeugende, ist ein äusserst wichtiger Baustein für das Vertrauen, welches das Kind zum Behandlungsteam entwickeln kann und welches es immer wieder überprüfen wird.
Die Schmerzmessung
Zur Schmerzbehandlung und Überprüfung ihres Erfolges ist die Einschätzung der Schmerzintensität von höchster Wichtigkeit (4). Für Kinder stehen altersspezifische, gut validierte Instrumente zur Selbst- und Fremdbestimmung der Schmerzintensität zur Verfügung (5). Dazu gehören: Neonatal Infant Pain Score (NIPS) bis zum Alter von 2½ Jahren, Children’s Hospital of Eastern Ontario Pain Scale (CHEOPS) für das Alter 2½ bis 4 Jahre, die Gesichterskala nach Bieri ab 5. Lebensjahr (6) und die bei Erwachsenen eingesetzte Visuell-Analog-Skala (VAS) für über 12-Jährige. Daneben sollte vor allem bei komplexen und chronischen Schmerzen eine umfassende Beurteilung des Schmerzes erfolgen (7). In der Erwachsenenonkologie wurde mit dem Edmonton Classification System for Cancer Pain (ECS-CP) ein wertvolles Instrument entwickelt, das eine Aussage über die Komplexität eines Schmerzes und seiner Prognose, im Sinne der Kontrollierbarkeit, erlaubt (8). Leider haben solche multidimensionalen Instrumente in der Pädiatrie bisher keinen Eingang in das alltägliche Schmerzmanagement gefunden. In der multizentrischen Validierungs-
ONKOLOGIE 4/2009
Im Fokus: Tumoren im Kindesalter
studie von Fainsinger et al. (8) konnte gezeigt werden, dass die Schmerzintensität (mittlerer bis starker Schmerz; gemessen nach VAS 0–10 in einem Bereich von 4 bis 10) mit der Dauer bis zur befriedigenden Schmerzkontrolle korreliert. Weitere prädiktive Faktoren wurden mit dem ECS-CP gefunden. Bei Kindern mit tumorbedingten Schmerzen deutet zumindest die Erfahrung darauf hin, dass die Schmerzintensität und das primäre Ansprechen auf eine adäquat dosierte Opioidtherapie einen ernst zu nehmenden Hinweis auf die Komplexität des Schmerzes und die Schwierigkeit der Kontrollierbarkeit geben können. Bei sehr kleinen Kindern können anhaltende Schmerzen oder schlecht kontrollierte Schmerzen zu einem «Rückzug» führen: Das bedeutet: ▲ Nicht unbedingt das vermehrte
Schreien weist auf Schmerzen hin, das bei akuten Schmerzen üblich ist, – sondern: ▲ das veränderte, häufig ganz ruhige Verhalten mit fehlendem Interesse, zu spielen oder mit der Umwelt in Kontakt zu treten, oder die Nahrungsverweigerung und Schlafstörungen.
Schmerztherapie im Alltag des krebskranken Kindes
Kinder wissen sehr genau, was ihnen wahrscheinlich und was ganz bestimmt sehr wehtut. Sie melden uns ihre Bedürfnisse für eine – am besten vorbeugende – Schmerzbehandlung unmissverständlich an. Dazu gehören – neben der Sicherheit spendenden Mutter, dem Nuggi oder Kuscheltier oder dem «Kraftstein», neben eingeübten Massnahmen (häufig Ablenkung, ein Lutscher, Vorlesen etc.) und Ritualen (bis drei zählen, «ich sage, wann du stechen darfst») – natürlich die medikamentös prophylaktische Schmerzbehandlung und begleitende Sedation. Um ein sinnvolles Prozedere zu entwickeln, muss individuell abgeklärt werden, ob ein Kind aufgrund seines Entwicklungsstands und seiner Persönlichkeit eher auf Ablenkungs- oder Kontrollstrategien anspricht.
Nichtmedikamentöse Schmerztherapie Wie angedeutet, spielen nichtmedikamentöse, häufig ritualisierte Massnah-
Bunte Perlen als «Starkmacher» zur Belohnung in schwierigen Situationen. Mit einer Belohnung sollen die Intervention und die Reaktion darauf nicht verharmlost werden, sondern das Bemühen des Kindes Wertschätzung erfahren.
men eine wichtige Rolle. Dazu gehören allgemein unterstützende Massnahmen (v.a. Einbezug der Familie in das gesamte Betreuungskonzept), kognitive Methoden (Ablenkung, Imagination), verhaltenstherapeutische (Belohnungssystem) und physikalische Massnahmen (Streicheln, Halten, Wiegen, vorsichtiges Massieren oder Auflagen/Wickel, das warme Kirschkernsäckchen oder «der kalte Lumpen»). Ein wichtiges Element stellt bei Kindern und Jugendlichen das Belohnungssystem dar, das in Tabelle 1 mit seinen verschiedenen Möglichkeiten aufgeführt ist. Belohnungen sollen das Kind zu bestimmten Aktivitäten oder erwünschtem Verhalten motivieren (positive Verstärkung in der Verhaltenstherapie). Zu diesen Aktivitäten gehören für manche Kinder schwer zu tolerierende, aber nicht zu umgehende, sich ständig wiederholende Interventionen wie Fingerpiks, Port-à-Cath-Anstechen, Verbandwechsel (etc). Mit einer Belohnung sollen die Intervention und die Reaktion darauf nicht verharmlost werden, sondern das Bemühen des Kindes Wertschätzung erfahren (Abbildung). Das Aushalten der schmerzhaften Verrichtung wird als Leistung des Kindes anerkannt; das Kind erhält in der Belohnung eine direkte Rückmeldung, worauf es stolz sein kann. Der Aufbau eines individuellen Belohnungs-/ Verstärkungssystems bedarf einer guten
Absprache mit den Eltern und einer schrittweise verlaufenden Entwicklung mit dem Kind. Häufig ist dazu eine psychologische/psychiatrische Fachperson notwendig. Wenn das Kind mit Panik reagiert, sind zunächst andere Schritte, die mit dem interdisziplinären Team und den Eltern abzustimmen sind, notwendig. Dabei geht es meist darum, die schmerzhafte Verrichtung gut vorzubereiten, damit sie möglichst rasch vollendet werden kann. Zudem soll dem Kind deutlich und ehrlich signalisiert werden, wann die medizinische Intervention vorbei ist. Weiter soll das Gefühl des kompletten Ausgeliefertseins schrittweise dahingehend verändert werden, dass das Kind einzelne Vorgehensweisen kontrollieren oder mitbestimmen kann (z.B. fragen, ob die Pflegende jeden Schritt verbal kommentieren oder nichts sagen soll).
Medikamentöse Schmerztherapie Diagnostische Eingriffe (Lumbalpunktion, Knochenmarkpunktion) werden meistens in Kurznarkosen durchgeführt. Krankheits- oder therapiebedingte Schmerzen werden bei Kindern wie bei Erwachsenen in Anlehnung an die von der WHO entwickelten «Schmerzleiter» in einem drei- bis vierstufigen System behandelt: ▲ Auf der ersten Stufe werden zur Be-
handlung leichter Schmerzen Nichtopioidanalgetika, bei Kindern vor al-
ONKOLOGIE 4/2009
11
Im Fokus: Tumoren im Kindesalter
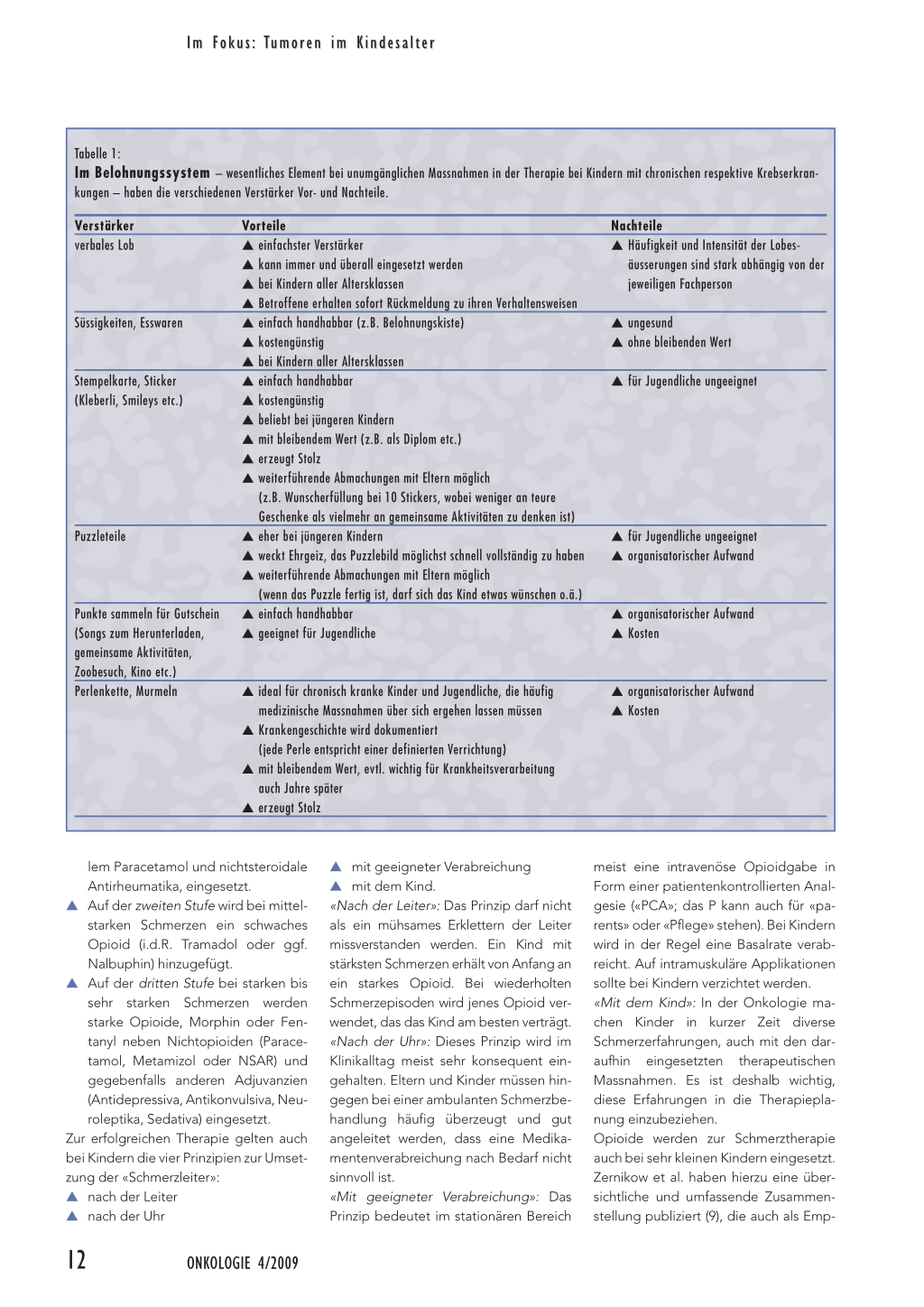
Tabelle 1:
Im Belohnungssystem – wesentliches Element bei unumgänglichen Massnahmen in der Therapie bei Kindern mit chronischen respektive Krebserkran-
kungen – haben die verschiedenen Verstärker Vor- und Nachteile.
Verstärker verbales Lob
Süssigkeiten, Esswaren
Stempelkarte, Sticker (Kleberli, Smileys etc.)
Puzzleteile
Punkte sammeln für Gutschein (Songs zum Herunterladen, gemeinsame Aktivitäten, Zoobesuch, Kino etc.) Perlenkette, Murmeln
Vorteile ▲ einfachster Verstärker ▲ kann immer und überall eingesetzt werden ▲ bei Kindern aller Altersklassen ▲ Betroffene erhalten sofort Rückmeldung zu ihren Verhaltensweisen ▲ einfach handhabbar (z.B. Belohnungskiste) ▲ kostengünstig ▲ bei Kindern aller Altersklassen ▲ einfach handhabbar ▲ kostengünstig ▲ beliebt bei jüngeren Kindern ▲ mit bleibendem Wert (z.B. als Diplom etc.) ▲ erzeugt Stolz ▲ weiterführende Abmachungen mit Eltern möglich
(z.B. Wunscherfüllung bei 10 Stickers, wobei weniger an teure Geschenke als vielmehr an gemeinsame Aktivitäten zu denken ist) ▲ eher bei jüngeren Kindern ▲ weckt Ehrgeiz, das Puzzlebild möglichst schnell vollständig zu haben ▲ weiterführende Abmachungen mit Eltern möglich (wenn das Puzzle fertig ist, darf sich das Kind etwas wünschen o.ä.) ▲ einfach handhabbar ▲ geeignet für Jugendliche
▲ ideal für chronisch kranke Kinder und Jugendliche, die häufig medizinische Massnahmen über sich ergehen lassen müssen
▲ Krankengeschichte wird dokumentiert (jede Perle entspricht einer definierten Verrichtung)
▲ mit bleibendem Wert, evtl. wichtig für Krankheitsverarbeitung auch Jahre später
▲ erzeugt Stolz
Nachteile ▲ Häufigkeit und Intensität der Lobes-
äusserungen sind stark abhängig von der jeweiligen Fachperson ▲ ungesund ▲ ohne bleibenden Wert ▲ für Jugendliche ungeeignet
▲ für Jugendliche ungeeignet ▲ organisatorischer Aufwand
▲ organisatorischer Aufwand ▲ Kosten
▲ organisatorischer Aufwand ▲ Kosten
lem Paracetamol und nichtsteroidale Antirheumatika, eingesetzt. ▲ Auf der zweiten Stufe wird bei mittelstarken Schmerzen ein schwaches Opioid (i.d.R. Tramadol oder ggf. Nalbuphin) hinzugefügt. ▲ Auf der dritten Stufe bei starken bis sehr starken Schmerzen werden starke Opioide, Morphin oder Fentanyl neben Nichtopioiden (Paracetamol, Metamizol oder NSAR) und gegebenfalls anderen Adjuvanzien (Antidepressiva, Antikonvulsiva, Neuroleptika, Sedativa) eingesetzt. Zur erfolgreichen Therapie gelten auch bei Kindern die vier Prinzipien zur Umsetzung der «Schmerzleiter»: ▲ nach der Leiter ▲ nach der Uhr
▲ mit geeigneter Verabreichung ▲ mit dem Kind. «Nach der Leiter»: Das Prinzip darf nicht als ein mühsames Erklettern der Leiter missverstanden werden. Ein Kind mit stärksten Schmerzen erhält von Anfang an ein starkes Opioid. Bei wiederholten Schmerzepisoden wird jenes Opioid verwendet, das das Kind am besten verträgt. «Nach der Uhr»: Dieses Prinzip wird im Klinikalltag meist sehr konsequent eingehalten. Eltern und Kinder müssen hingegen bei einer ambulanten Schmerzbehandlung häufig überzeugt und gut angeleitet werden, dass eine Medikamentenverabreichung nach Bedarf nicht sinnvoll ist. «Mit geeigneter Verabreichung»: Das Prinzip bedeutet im stationären Bereich
meist eine intravenöse Opioidgabe in Form einer patientenkontrollierten Analgesie («PCA»; das P kann auch für «parents» oder «Pflege» stehen). Bei Kindern wird in der Regel eine Basalrate verabreicht. Auf intramuskuläre Applikationen sollte bei Kindern verzichtet werden. «Mit dem Kind»: In der Onkologie machen Kinder in kurzer Zeit diverse Schmerzerfahrungen, auch mit den daraufhin eingesetzten therapeutischen Massnahmen. Es ist deshalb wichtig, diese Erfahrungen in die Therapieplanung einzubeziehen. Opioide werden zur Schmerztherapie auch bei sehr kleinen Kindern eingesetzt. Zernikow et al. haben hierzu eine übersichtliche und umfassende Zusammenstellung publiziert (9), die auch als Emp-
12 ONKOLOGIE 4/2009
Im Fokus: Tumoren im Kindesalter
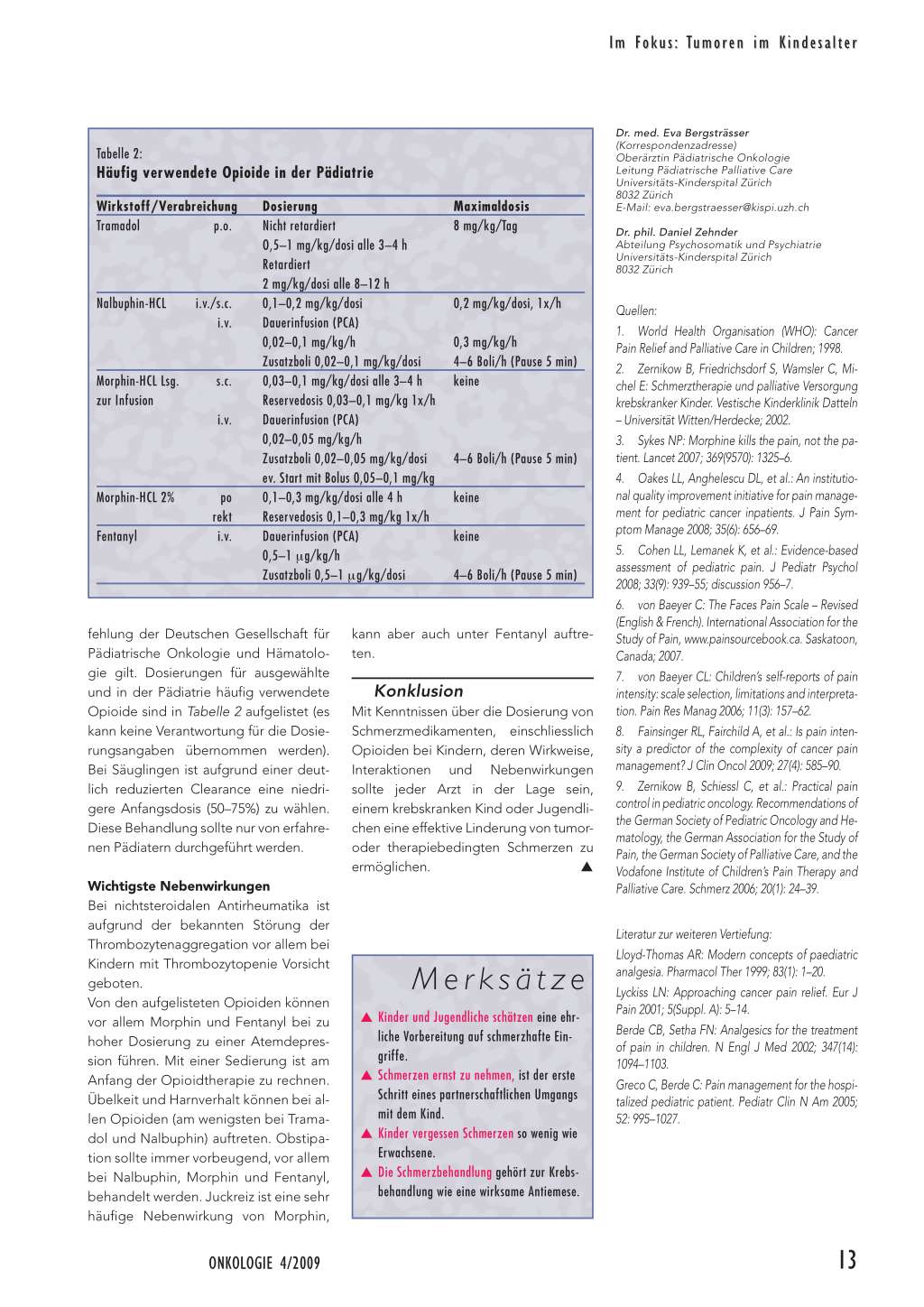
Tabelle 2:
Häufig verwendete Opioide in der Pädiatrie
Wirkstoff/Verabreichung
Tramadol
p.o.
Nalbuphin-HCL
i.v./s.c. i.v.
Morphin-HCL Lsg. zur Infusion
s.c. i.v.
Morphin-HCL 2% Fentanyl
po rekt i.v.
Dosierung Nicht retardiert O,5–1 mg/kg/dosi alle 3–4 h Retardiert 2 mg/kg/dosi alle 8–12 h 0,1–0,2 mg/kg/dosi Dauerinfusion (PCA) 0,02–0,1 mg/kg/h Zusatzboli 0,02–0,1 mg/kg/dosi 0,03–0,1 mg/kg/dosi alle 3–4 h Reservedosis 0,03–0,1 mg/kg 1x/h Dauerinfusion (PCA) 0,02–0,05 mg/kg/h Zusatzboli 0,02–0,05 mg/kg/dosi ev. Start mit Bolus 0,05–0,1 mg/kg 0,1–0,3 mg/kg/dosi alle 4 h Reservedosis 0,1–0,3 mg/kg 1x/h Dauerinfusion (PCA) 0,5–1 μg/kg/h Zusatzboli 0,5–1 μg/kg/dosi
Maximaldosis 8 mg/kg/Tag
0,2 mg/kg/dosi, 1x/h 0,3 mg/kg/h 4–6 Boli/h (Pause 5 min) keine
4–6 Boli/h (Pause 5 min) keine keine 4–6 Boli/h (Pause 5 min)
fehlung der Deutschen Gesellschaft für Pädiatrische Onkologie und Hämatologie gilt. Dosierungen für ausgewählte und in der Pädiatrie häufig verwendete Opioide sind in Tabelle 2 aufgelistet (es kann keine Verantwortung für die Dosierungsangaben übernommen werden). Bei Säuglingen ist aufgrund einer deutlich reduzierten Clearance eine niedrigere Anfangsdosis (50–75%) zu wählen. Diese Behandlung sollte nur von erfahrenen Pädiatern durchgeführt werden.
Wichtigste Nebenwirkungen Bei nichtsteroidalen Antirheumatika ist aufgrund der bekannten Störung der Thrombozytenaggregation vor allem bei Kindern mit Thrombozytopenie Vorsicht geboten. Von den aufgelisteten Opioiden können vor allem Morphin und Fentanyl bei zu hoher Dosierung zu einer Atemdepression führen. Mit einer Sedierung ist am Anfang der Opioidtherapie zu rechnen. Übelkeit und Harnverhalt können bei allen Opioiden (am wenigsten bei Tramadol und Nalbuphin) auftreten. Obstipation sollte immer vorbeugend, vor allem bei Nalbuphin, Morphin und Fentanyl, behandelt werden. Juckreiz ist eine sehr häufige Nebenwirkung von Morphin,
kann aber auch unter Fentanyl auftreten.
Konklusion
Mit Kenntnissen über die Dosierung von
Schmerzmedikamenten, einschliesslich
Opioiden bei Kindern, deren Wirkweise,
Interaktionen und Nebenwirkungen
sollte jeder Arzt in der Lage sein,
einem krebskranken Kind oder Jugendli-
chen eine effektive Linderung von tumor-
oder therapiebedingten Schmerzen zu
ermöglichen.
▲
Merksätze
▲ Kinder und Jugendliche schätzen eine ehrliche Vorbereitung auf schmerzhafte Eingriffe.
▲ Schmerzen ernst zu nehmen, ist der erste Schritt eines partnerschaftlichen Umgangs mit dem Kind.
▲ Kinder vergessen Schmerzen so wenig wie Erwachsene.
▲ Die Schmerzbehandlung gehört zur Krebsbehandlung wie eine wirksame Antiemese.
Dr. med. Eva Bergsträsser (Korrespondenzadresse) Oberärztin Pädiatrische Onkologie Leitung Pädiatrische Palliative Care Universitäts-Kinderspital Zürich 8032 Zürich E-Mail: eva.bergstraesser@kispi.uzh.ch
Dr. phil. Daniel Zehnder Abteilung Psychosomatik und Psychiatrie Universitäts-Kinderspital Zürich 8032 Zürich
Quellen:
1. World Health Organisation (WHO): Cancer Pain Relief and Palliative Care in Children; 1998.
2. Zernikow B, Friedrichsdorf S, Wamsler C, Michel E: Schmerztherapie und palliative Versorgung krebskranker Kinder. Vestische Kinderklinik Datteln – Universität Witten/Herdecke; 2002.
3. Sykes NP: Morphine kills the pain, not the patient. Lancet 2007; 369(9570): 1325–6.
4. Oakes LL, Anghelescu DL, et al.: An institutional quality improvement initiative for pain management for pediatric cancer inpatients. J Pain Symptom Manage 2008; 35(6): 656–69.
5. Cohen LL, Lemanek K, et al.: Evidence-based assessment of pediatric pain. J Pediatr Psychol 2008; 33(9): 939–55; discussion 956–7.
6. von Baeyer C: The Faces Pain Scale – Revised (English & French). International Association for the Study of Pain, www.painsourcebook.ca. Saskatoon, Canada; 2007.
7. von Baeyer CL: Children’s self-reports of pain intensity: scale selection, limitations and interpretation. Pain Res Manag 2006; 11(3): 157–62.
8. Fainsinger RL, Fairchild A, et al.: Is pain intensity a predictor of the complexity of cancer pain management? J Clin Oncol 2009; 27(4): 585–90.
9. Zernikow B, Schiessl C, et al.: Practical pain control in pediatric oncology. Recommendations of the German Society of Pediatric Oncology and Hematology, the German Association for the Study of Pain, the German Society of Palliative Care, and the Vodafone Institute of Children’s Pain Therapy and Palliative Care. Schmerz 2006; 20(1): 24–39.
Literatur zur weiteren Vertiefung:
Lloyd-Thomas AR: Modern concepts of paediatric analgesia. Pharmacol Ther 1999; 83(1): 1–20.
Lyckiss LN: Approaching cancer pain relief. Eur J Pain 2001; 5(Suppl. A): 5–14.
Berde CB, Setha FN: Analgesics for the treatment of pain in children. N Engl J Med 2002; 347(14): 1094–1103.
Greco C, Berde C: Pain management for the hospitalized pediatric patient. Pediatr Clin N Am 2005; 52: 995–1027.
ONKOLOGIE 4/2009
13