Transkript
SCHWERPUNKT
Medikamentöse Therapie der überaktiven Blase
Eine Übersicht über die neueren Ansätze
Dr. med. Christoph Schneider, PD Dr. med. Daniele Perucchini
Die Dranginkontinenz und die Drangsymptomatik werden heute unter dem Begriff «überaktive Blase» subsumiert. Zeichen der überaktiven Blase sind imperativer Harndrang, Dranginkontinenz, Nykturie und Pollakisurie. Dahinter steckt die Überaktivität des M. detrusor vesicae. Therapeutisch
wird versucht, mit Medikamenten die Häufigkeit der unwillkürlichen Detrusorkontraktionen zu verringern. In den letzten Jahren sind neue Medikamente zur Therapie der überaktiven Blase entwickelt und auf den Markt gebracht worden. Die wichtigsten sollen im Folgenden beschrieben werden.
Die International Continence Society (ICS) hat 2002 die Nomenklatur für die Harninkontinenz überarbeitet (1). In der neuen Definition werden die Begriffe vor allem symptomorientiert deskriptiv verwendet. Der Zusatz «urodynamisch verifiziert» zeigt die objektive Bestätigung der angegebenen Beschwerden an. Dabei wurde der Begriff «Syndrom der überaktiven Blase» (englisch: «overactive bladder syndrome», «OAB syndrome») eingeführt, definiert als Harndrang mit oder ohne Inkontinenz, gewöhnlich verbunden mit Pollakisurie und Nykturie, sofern gleichzeitig eine andere Harnwegspathologie (Harnwegsinfekt, Tumor, Steine etc.) ausgeschlossen werden kann.
Epidemiologie
Im Jahr 2001 wurden erstmals zwei grosse multinationale epidemiologische Studien – eine aus Europa und eine aus Asien – zur Inzidenz der überaktiven Blase publiziert. Bei der europäischen Studie wurden vom schwedischen Meinungsforschungsinstitut SIFO in Zusammenarbeit mit dem Gallup-Network 16 776 repräsentativ ausgewählte Personen im Alter ab 40 Jahren in Deutschland, Frankreich, Grossbritannien, Italien, Schweden und Spanien mittels Telefoninterview oder Direktbegegnung nach ihren Miktionsgewohnheiten befragt (2). Bei den 9728 teilnehmenden Frauen zeigte sich das Syndrom über-
NA
–
M1
+ M2/4 NA
+
M1
Ach –
Ach
M2/4
Zellmembran
β3 M2
AC
cAMP
Relaxation
Kontraktion
M3
PLC
Ca 2+
IP3
Ca2+ Kontraktion
Abbildung 1: Erregungsablauf an der Zellmembran einer Detrusorzelle. Eine Azetylcholin-vermittelte Aktivierung der M3 (Muskarin-3)-Rezeptoren führt direkt zu einer Kontraktion der glatten Detrusormuskulatur. Die Aktivierung der M2-Rezeptoren unterstützt durch eine Hemmung der β-adrenerg vermittelten Relaxation die Kontraktion der Detrusormuskulatur.
(nach Chapple, Urology 2000; 55: 33–46)
aktive Blase mit einer Prävalenz von 17,4 Prozent, wobei ein kontinuierlicher Anstieg der Prävalenz mit zunehmendem Lebensalter festgestellt werden konnte.
Pathophysiologie
In den letzten Jahren hat sich das Wissen über die Steuerung der Detrusorkontraktionen erheblich erweitert, wobei gleichzeitig die Komplexität dieser Mechanismen deutlich wurde. Ins Zentrum des Interesses sind die Muskarinrezeptoren und ihre Funktionen gerückt (3). Von den fünf heute bekannten Subtypen finden
sich zwei in der Blasenmuskulatur, nämlich die Muskarinrezeptoren M2 und M3. Eine Azetylcholin-vermittelte Aktivierung der M3-Rezeptoren führt direkt zu einer Kontraktion der glatten Detrusormuskulatur. Die Aktivierung der M2-Rezeptoren unterstützt durch eine Hemmung der β-adrenerg vermittelten Relaxation die Kontraktion der Detrusormuskulatur (vergleiche hierzu Abbildung 1).
Therapie
Die medikamentöse Therapie muss immer durch flankierende Massnahmen er-
8
GYNÄKOLOGIE 1/2004
SCHWERPUNKT
Medikamentöse Therapie der überaktiven Blase
gänzt werden, um dauerhafte Erfolge zu erzielen. Dazu gehören das Führen eines Miktionstagebuchs, ein intensives Blasentraining sowie eine gezielte Beckenboden-Physiotherapie. Ziel der medikamentösen Therapie mit den modernen Präparaten ist es, die Häufigkeit der unwillkürlichen Detrusorkontraktionen durch die Blockierung der Muskarinrezeptoren M2 und M3 zu reduzieren. Diese Medikamente werden als Muskarinrezeptorantagonisten, Antimuskarinika oder Anticholinergika bezeichnet. Da die Muskarinrezeptoren aber nicht nur in der Harnblase zu finden sind, ist mit teilweise stark störenden Nebenwirkungen zu rechnen, insbesondere an den Augen (Akkommodationsstörungen), an den Speicheldrüsen (Mundtrockenheit), am Herzen (Tachykardie) und am Gastrointestinaltrakt (Obstipation). Daraus ergeben sich auch die zu beachtenden Kontraindikationen bei diesen Substanzen: Dies sind vor allem Harnretention, Magenretention, schwere Colitis ulcerosa, toxisches Megakolon, unbehandeltes Engwinkelglaukom, Myasthenia gravis, Tachyarrhythmie. Ein Teil der Substanzen passiert auch die BlutHirn-Schranke und kann deshalb zu zentralnervösen Nebenwirkungen führen.
Anticholinergika im Vergleich
Die Tabelle gibt eine Übersicht über die uns zur Verfügung stehenden Medikamente. Im Folgenden soll auf die drei in der Schweiz wohl am häufigsten zur Anwendung kommenden Substanzen (Oxybutynin, Tolterodin und Trospiumchlorid) näher eingegangen werden. Oxybutynin, ein tertiäres Amin, hat sowohl antimuskarinische als auch direkt muskelrelaxierende und lokalanästhetische Wirkung. Tolterodin, auch ein tertiäres Amin, ist ein kompetitiver Muskarinrezeptorantagonist, welcher deutlich stärker an der Blase als an den Speicheldrüsen wirkt. Trospiumchlorid ist ein quarternäres Amin mit antimuskarinerger Wirkung. Keines dieser Medikamente besitzt eine Selektivität für einen der Muskarinrezeptor-Subtypen. Für alle
drei Substanzen existieren doppelblinde, plazebokontrollierte Studien, die eine signifikant bessere Wirkung gegenüber Plazebo zeigen. Gleichzeitig zeigten diese Studien aber auch einen grossen Plazeboeffekt in bis zu 33 Prozent der Patientinnen.
Vergleich zu Tolterodin (2 x 2 mg täglich) zeigte sich eine signifikant bessere Wirkung, aber ohne Unterschied im Auftreten von Nebenwirkungen (7). Tolterodin SR (slow release) wird in einer Dosierung von 4 mg einmal täglich angewendet. In einer doppelblinden,
Mediane Reduktion der Inkontinenz
0% -10% -20% -30% -40% -50% -60% -70% -80%
n = 417
n = 408
-57%
-71%
p = 0,036
Tolterodin SR
Tolterodin 2 x 2 mg
n = 410 -33%
Plazebo
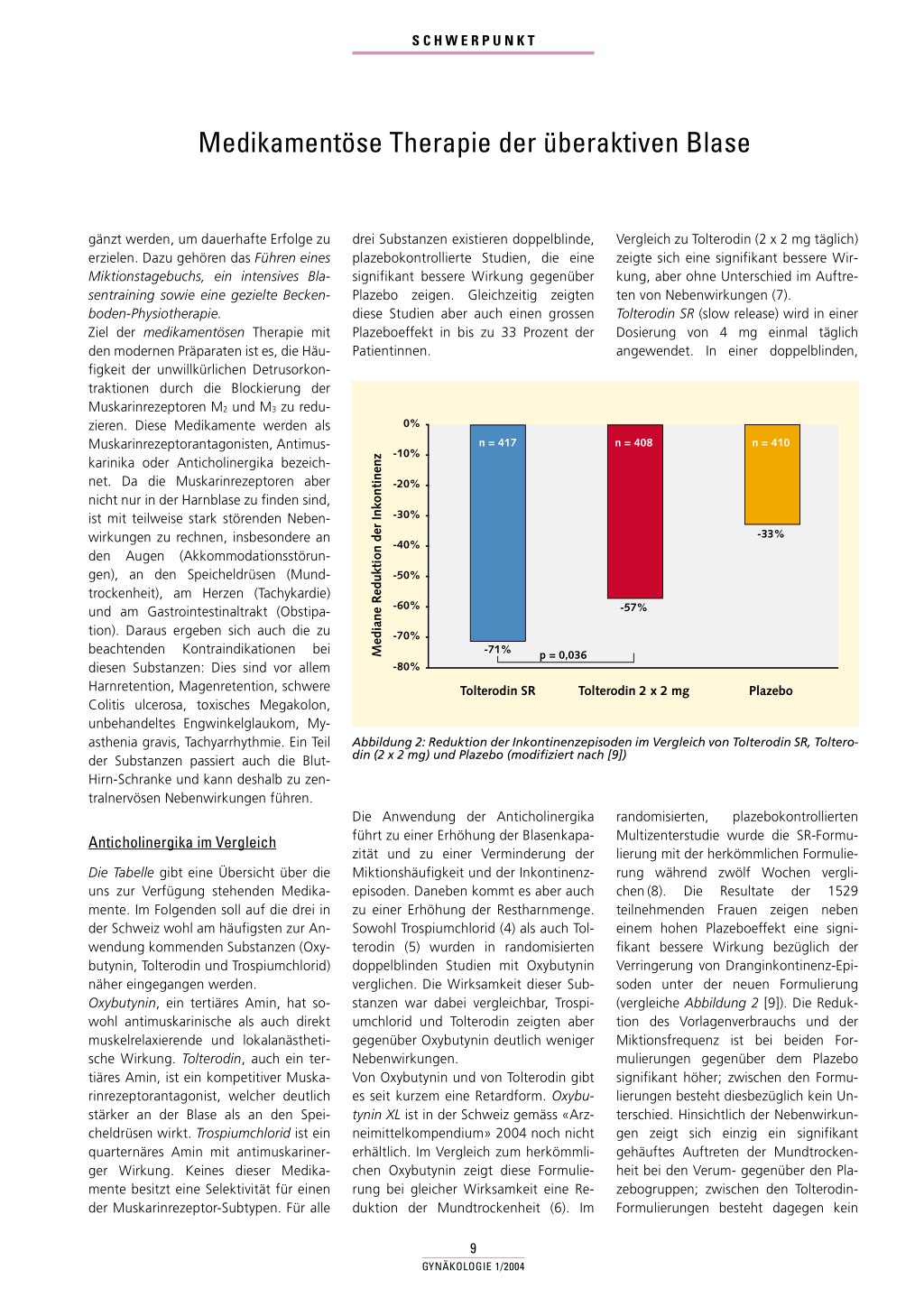
Abbildung 2: Reduktion der Inkontinenzepisoden im Vergleich von Tolterodin SR, Tolterodin (2 x 2 mg) und Plazebo (modifiziert nach [9])
Die Anwendung der Anticholinergika führt zu einer Erhöhung der Blasenkapazität und zu einer Verminderung der Miktionshäufigkeit und der Inkontinenzepisoden. Daneben kommt es aber auch zu einer Erhöhung der Restharnmenge. Sowohl Trospiumchlorid (4) als auch Tolterodin (5) wurden in randomisierten doppelblinden Studien mit Oxybutynin verglichen. Die Wirksamkeit dieser Substanzen war dabei vergleichbar, Trospiumchlorid und Tolterodin zeigten aber gegenüber Oxybutynin deutlich weniger Nebenwirkungen. Von Oxybutynin und von Tolterodin gibt es seit kurzem eine Retardform. Oxybutynin XL ist in der Schweiz gemäss «Arzneimittelkompendium» 2004 noch nicht erhältlich. Im Vergleich zum herkömmlichen Oxybutynin zeigt diese Formulierung bei gleicher Wirksamkeit eine Reduktion der Mundtrockenheit (6). Im
randomisierten, plazebokontrollierten Multizenterstudie wurde die SR-Formulierung mit der herkömmlichen Formulierung während zwölf Wochen verglichen (8). Die Resultate der 1529 teilnehmenden Frauen zeigen neben einem hohen Plazeboeffekt eine signifikant bessere Wirkung bezüglich der Verringerung von Dranginkontinenz-Episoden unter der neuen Formulierung (vergleiche Abbildung 2 [9]). Die Reduktion des Vorlagenverbrauchs und der Miktionsfrequenz ist bei beiden Formulierungen gegenüber dem Plazebo signifikant höher; zwischen den Formulierungen besteht diesbezüglich kein Unterschied. Hinsichtlich der Nebenwirkungen zeigt sich einzig ein signifikant gehäuftes Auftreten der Mundtrockenheit bei den Verum- gegenüber den Plazebogruppen; zwischen den TolterodinFormulierungen besteht dagegen kein
9
GYNÄKOLOGIE 1/2004
SCHWERPUNKT
Medikamentöse Therapie der überaktiven Blase
Tabelle:
Übersicht der Medikamente zur Therapie der überaktiven Blase
Medikamentengruppe Anticholinergika
Spasmolytikum NoradrenalinReuptake-Inhibitoren
Wirkstoff Tolterodin
Tolterodin Oxybutynin Emeproniumbromid Trospiumchlorid
Darifenacin
Solifenacin
Flavoxat Imipramin
Markenname Detrusitol SR® 4 mg Kaps. Detrusitol® 2 mg Tbl. Ditropan® 5 mg Tbl. Cetiprin® 200 mg Tbl. Spasmo-Urgenin® Neo 20 mg Drg. Noch in Phase-II/ IIIStudienphase Noch in Phase-II/ IIIStudienphase Urispas® 200 mg Drg. Tofranil® 10/25 mg Drg.
Dosierung/Tag 1 x 4 mg 2 x 2 mg 3 x 5 mg
3–4 x 200 mg 2 x 20 mg
3 x 200 mg 3 x 10–25 mg
signifikanter Unterschied, nur eine Tendenz zu seltenerem Auftreten in der SRForm. Eine Untersuchung an Freiwilligen (10) zeigte, dass die maximale Serumkonzentration der SR-Formulierung 75 Prozent der herkömmlichen Formulierung beträgt, womit das leicht verminderte Auftreten der Mundtrockenheit erklärt wird. Hier wurde ebenfalls deutlich, dass die minimale Serumkonzentration 1,5mal höher ist, was die bessere Wirkung erklärt. Die Fläche unter der Kurve über 24 Stunden (AUC24) ist aber identisch. Bezüglich klinischer Wirksamkeit ergab sich: Bereits nach einer Woche Einnahme von Tolterodin SR ist eine deutliche Besserung der Symptomatik zu erkennen; die maximale Wirkung ist aber erst nach zwölf Wochen erreicht (11). Eine Langzeitanwendung über zwölf Monate zeigte eine stabile Wirkung ohne schwere Nebenwirkungen; die störende Mundtrockenheit war im Verlauf abnehmend (12), was sicherlich auch der Compliance der Patientinnen förderlich war.
Weitere Substanzen in Sicht
In der nächsten Zukunft werden uns mit Darifenacin und Solifenacin zwei weitere Anticholinergika zur Verfügung stehen. Beide zeichnen sich durch eine recht selektive Blockierung der M3-Rezeptoren aus. Klinische Studien werden den Stellenwert dieser neuen Substanzen in der Therapie der überaktiven Blase aufzeigen. ◗
Korrespondenzadresse: Dr. med. Christoph Schneider Klinik für Gynäkologie Departement Frauenheilkunde UniversitätsSpital Zürich 8091 Zürich Tel. 01-255 11 11 E-Mail: christoph.schneider@usz.ch
Quellen: 1. Abrams P, Cardozo L, Fall M, Griffiths D, Rosier P, Ulmsten U, van Kerrebroeck P, Victor A, Wein A.: The standardisation of terminology of lower urinary tract function: Report from the standardisa-
tion sub-committee of the International Continence Society. Neurourol. Urodyn. 2002; 21: 167–178. 2. Milsom I, Abrams P, Cardozo L, Roberts RG, Thuroff J, Wein AJ.: How widespread are the symptoms of an overactive bladder and how are they managed? A population-based prevalence study. BJU Int. 2001; 87: 760–766. 3. Chapple CR, Yamanishi T, Chess-Williams R.: Muscarinic receptor subtypes and management of the overactive bladder. Urology 2002; 60: 82–89. 4. Madersbacher H, Stöhrer M, Richter R, Burgdorfer H, Hachen HJ, Murtz G.: Trospium chloride versus oxybutynin: a randomized, double-blind, multicentre trial in the treatment of detrusor hyperreflexia. Br J Urol 1995; 75: 452–456. 5. Van Kerrebroeck PE, Serment G, Dreher E.: Clinical efficacy and safety of tolterodine compared to oxybutynin in patients with overactive bladder. Neurourol Urodyn 1997; 16: 478–479. 6. Anderson RU, Mobley D, Blank B, Saltzstein D, Susset J, Brown JS.: Once-a-day controlled versus immediate-release oxybutynin chloride for urge incontinence. J Urol 1999; 161: 1809–1812. 7. Appell RA, Sand P, Dmochowski R, Anderson R, Zinner N, Lama D, Roach M, Miklos J, Saltzstein D, Boone T, Staskin DR, Albrecht D.: Prospective randomized controlled trial of extended-release oxybutynin chloride and tolterodine tartrate in the treatment of overactive bladder: results of the OBJECT study. Mayo Clin. Proc. 2001; 76: 358–363. 8. Van Kerrebroeck P, Kreder K, Jonas U, Zinner N, Wein A.: Tolterodine once-daily: superior efficacy and tolerability in the treatment of the overactive bladder. Urology 2001; 57: 414–421. 9. Swift S, Garely A, Dimpfl T, Payne C.: A oncedaily formulation of tolterodine provides superior efficacy and is well tolerated in women with overactive bladder. Int. Urogynecol. J. 2003; 14: 50–55. 10. Olsson B, Szamosi J.: Multiple dose pharmacokinetics of a new once daily extended release tolterodine formulation versus immediate release tolterodine. Clin. Pharmacokinet. 2001; 40: 227–235. 11. Siami P, Seidman LS, Lama D.: A multicenter, prospective, open-label study of tolterodine extended-release 4 mg for overactive bladder: the speed of onset of therapeutic assessment trial. Clin. Ther. 2002; 24: 616–628. 12. Kreder K, Mayne C, Jonas U.: Long-term safety, tolerability and efficacy of extended-release tolterodine in the treatment of overactive bladder. Euro. Urol. 2002; 41: 588–595.
10
GYNÄKOLOGIE 1/2004