Transkript
ENTZÜNDUNG UND ERNÄHRUNG
Die Rolle der Ernährung
«Low grade inflammation» und chronisch-degenerative Erkrankungen
Andreas Hahn, Wiebke Jonas und Isabel Behrendt
Andreas Hahn Wiebke Jonas Isabel Behrendt
Entzündungen, wie sie durch Infektionen oder Traumata hervorgerufen werden, sind durch einen akuten Verlauf mit ausgeprägten Symptomen und eine begrenzte Dauer gekenn zeichnet. Im Gegensatz dazu verläuft die chronische systemische Entzündung niederschwellig, symptomlos und über Jahre unbemerkt. Sie stellt einen wesentlichen Risikofaktor bei der Entstehung chronisch-degenerativer Erkrankungen dar. Nachfolgend ein kurzer Überblick, der beispielhaft einige Zusammenhänge aufzeigt.
Entzündungen sind für die Homöostase essenzielle Reaktionen, die den Organismus vor den Folgen von Infektionen und anderen Schädigungen schützen sollen. Sie zielen darauf ab, Pathogene zu beseitigen und den Heilungsprozess zu initiieren sowie eine Gewebereparatur einzuleiten, oder, wo das nicht möglich ist, das Gewebe zu zerstören. Die typischen Merkmale der akuten Entzündung (Rubor, Tumor, Dolor, Calor, Functio laesa) sind Zeichen der dabei stattfindenden immunologischen Reaktionen, die durch zahlreiche Zytokine und andere Mediatoren gesteuert werden. Das inflammatorische Geschehen kontrolliert sich normalerweise selbst und klingt über autoregulatorische Mechanismen wieder ab. Hierzu tragen neben antiinflammatorisch wirkenden Zytokinen u. a. spezifische Lipidmediatoren wie Maresine, Protektine und Resolvine bei. In den meisten Fällen bleiben Entzündungen lokal beschränkt; ist das nicht der Fall, treten systemische Symptome wie Fieber und Leukozytose auf. Auslöser einer akuten Entzündung sind Interaktionen der Mustererkennungsrezeptoren (Pattern Recognition Receptors; PRR) auf Immunzellen mit pathogenassoziierten molekularen Mustern (pathogen associated molecular pattern, PAMP), die auf vielen Erregern vorkommen und evolutionär hochkonserviert sind. Gleichermassen können schadensassoziierte molekulare Muster (damage associated molecular pattern, DAMP) eine Entzündungsreaktion einleiten. Diese Molekülstrukturen sind Teil des angeborenen Immunsystems und werden von geschädigten Körperzellen als Reaktion auf Traumata sowie chemische und metabolische Noxen freigesetzt, ohne dass eine Infektion vorliegt. Sie stellen somit endogene Signale dar, die ebenfalls an Mustererkennungsrezeptoren andocken und so eine Inflammation initiieren.
Akute versus chronische systemische Inflammation
Während sich akute und subakute Entzündungsprozesse durch ausgeprägte Symptome und eine begrenzte Dauer auszeichnen, handelt es sich bei der
chronischen systemischen Inflammation um einen persistierenden Vorgang, der niederschwellig und weitgehend unbemerkt abläuft (Tabelle 1) (1, 2). Daher wird diese Form der Entzündung auch als «silent inflammation» oder «low grade inflammation» bezeichnet. Da der Prozess zudem in engem Zusammenhang mit der Immunseneszenz, dem altersabhängigen Leistungsverlust des Immunsystems steht, ist er auch als «Inflammaging» bekannt, wobei die unterschiedlichen Begrifflichkeiten bislang nur unzureichend abgegrenzt werden. Die «low grade inflammation» ist charakterisiert durch erhöhte Konzentrationen proinflammatorischer Marker wie TNF-α oder IL-6, die aber weitaus niedriger liegen als bei akuten Infektionen. Auslöser der SCI sind typischerweise DAMP, die als Reaktion auf unterschiedliche Stressoren freigesetzt werden.
Ursachen
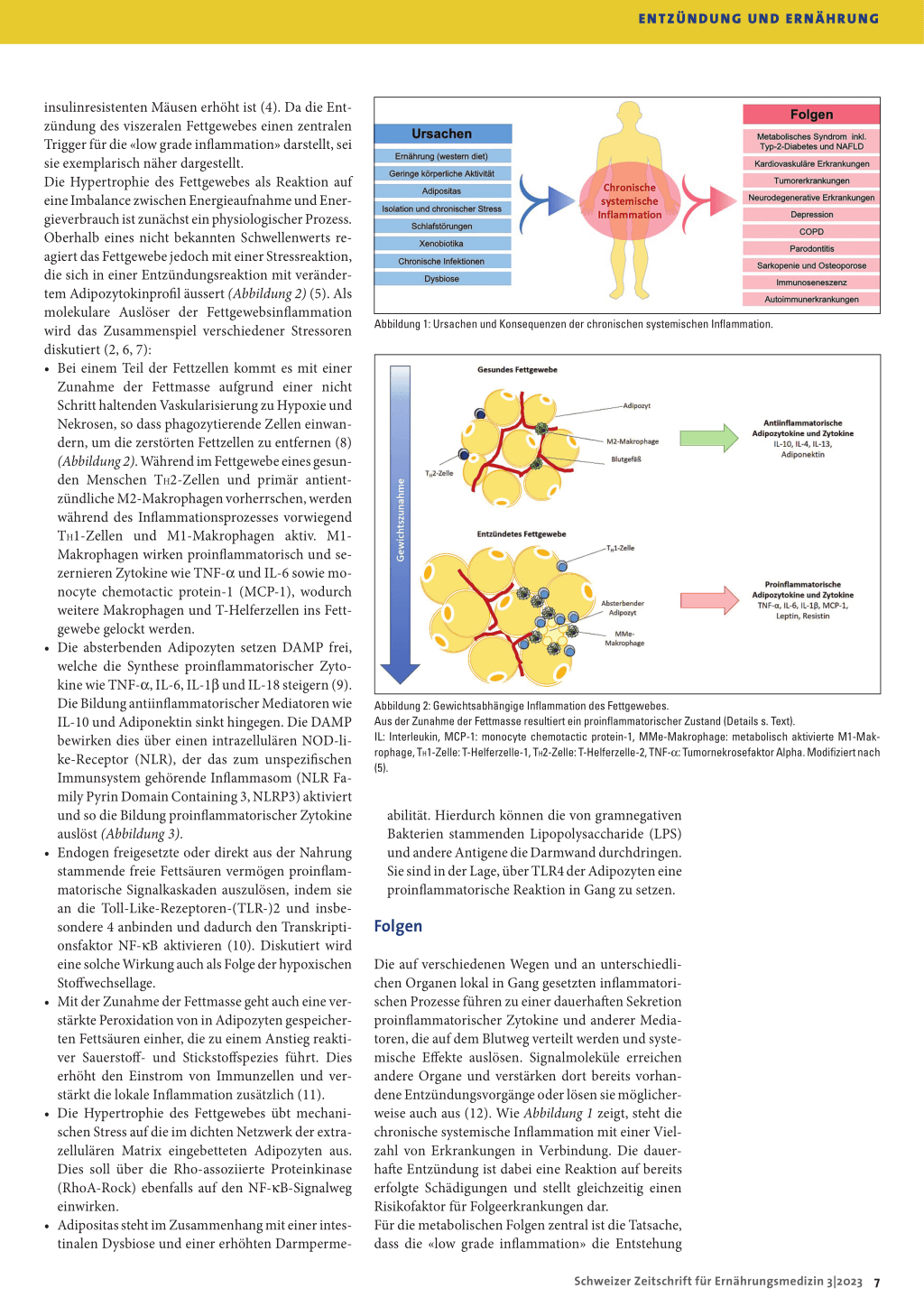
Die chronische systemische Inflammation beruht auf einem komplexen Ursachengefüge, das nicht in allen Details verstanden ist. Da die zelluläre Immunseneszenz mit einer vermehrten Bildung seneszenter CD8+-Zellen und einer gleichzeitig erhöhten Sekretion proinflammatorischer Zytokine einhergeht, begünstigen chronische Infektionen, beispielsweise mit dem Cytomegalievirus, die «low grade inflammation» (3), wenngleich der Einfluss nicht isoliert von Genetik und Umwelteinflüssen betrachtet werden kann (2). Abbildung 1 zeigt, welche ätiologischen Faktoren zum Tragen kommen. Plakativ vereinfacht lässt sich festhalten, dass ein bewegungsarmer Lebensstil, der mit einer ungünstigen Ernährungsweise im Sinne einer typischen «western diet» einhergeht, zu Adipositas führt und noch dazu durch psychosoziale Stressoren, Schlafmangel und eine hohe Exposition gegenüber Xenobiotika (z. B. Farbstoffe, Pestizide, Lösungmittel) gekennzeichnet ist, eine besonders ungünstige Konstellation darstellt. Bereits seit rund 30 Jahren ist bekannt, dass Adipo zyten das profinflammatorische Zytokin TNF-α sezernieren und dessen Expression bei adipösen und
6 Schweizer Zeitschrift für Ernährungsmedizin 3|2023
ENTZÜNDUNG UND ERNÄHRUNG
insulinresistenten Mäusen erhöht ist (4). Da die Ent-
zündung des viszeralen Fettgewebes einen zentralen
Trigger für die «low grade inflammation» darstellt, sei
sie exemplarisch näher dargestellt.
Die Hypertrophie des Fettgewebes als Reaktion auf
eine Imbalance zwischen Energieaufnahme und Ener-
gieverbrauch ist zunächst ein physiologischer Prozess.
Oberhalb eines nicht bekannten Schwellenwerts re-
agiert das Fettgewebe jedoch mit einer Stressreaktion,
die sich in einer Entzündungsreaktion mit veränder-
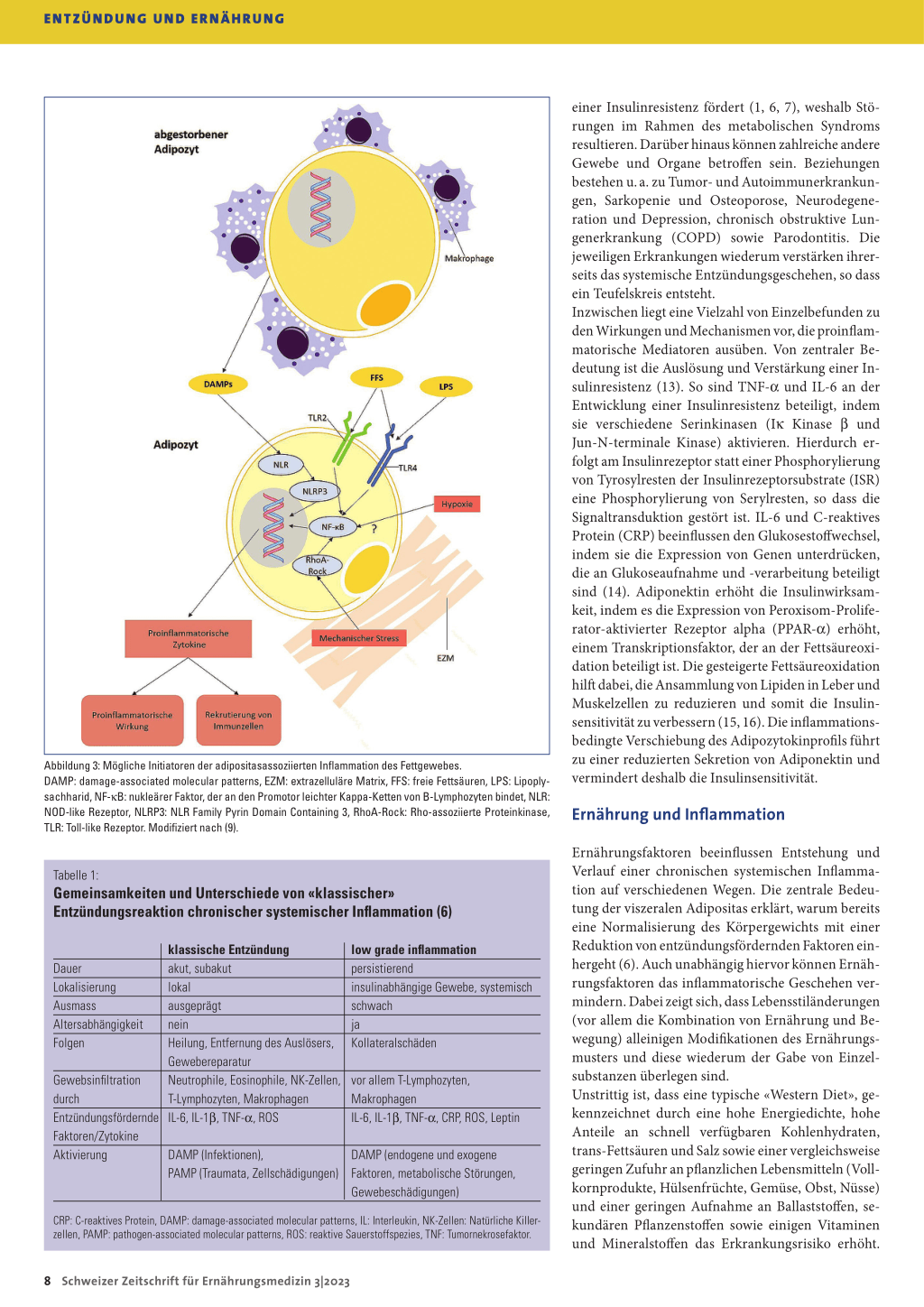
tem Adipozytokinprofil äussert (Abbildung 2) (5). Als
molekulare Auslöser der Fettgewebsinflammation wird das Zusammenspiel verschiedener Stressoren
Abbildung 1: Ursachen und Konsequenzen der chronischen systemischen Inflammation.
diskutiert (2, 6, 7):
• Bei einem Teil der Fettzellen kommt es mit einer
Zunahme der Fettmasse aufgrund einer nicht
Schritt haltenden Vaskularisierung zu Hypoxie und
Nekrosen, so dass phagozytierende Zellen einwan-
dern, um die zerstörten Fettzellen zu entfernen (8)
(Abbildung 2). Während im Fettgewebe eines gesun-
den Menschen TH2-Zellen und primär antient-
zündliche M2-Makrophagen vorherrschen, werden
während des Inflammationsprozesses vorwiegend
TH1-Zellen und M1-Makrophagen aktiv. M1-
Makrophagen wirken proinflammatorisch und se-
zernieren Zytokine wie TNF-α und IL-6 sowie mo-
nocyte chemotactic protein-1 (MCP-1), wodurch
weitere Makrophagen und T-Helferzellen ins Fett-
gewebe gelockt werden.
• Die absterbenden Adipozyten setzen DAMP frei,
welche die Synthese proinflammatorischer Zyto-
kine wie TNF-α, IL-6, IL-1b und IL-18 steigern (9).
Die Bildung antiinflammatorischer Mediatoren wie Abbildung 2: Gewichtsabhängige Inflammation des Fettgewebes.
IL-10 und Adiponektin sinkt hingegen. Die DAMP Aus der Zunahme der Fettmasse resultiert ein proinflammatorischer Zustand (Details s. Text).
bewirken dies über einen intrazellulären NOD-like-Receptor (NLR), der das zum unspezifischen Immunsystem gehörende Inflammasom (NLR Fa-
IL: Interleukin, MCP-1: monocyte chemotactic protein-1, MMe-Makrophage: metabolisch aktivierte M1-Mak-
rophage, TH1-Zelle: T-Helferzelle-1, TH2-Zelle: T-Helferzelle-2, TNF-a: Tumornekrosefaktor Alpha. Modifiziert nach (5).
mily Pyrin Domain Containing 3, NLRP3) aktiviert
und so die Bildung proinflammatorischer Zytokine
abilität. Hierdurch können die von gramnegativen
auslöst (Abbildung 3).
Bakterien stammenden Lipopolysaccharide (LPS)
• Endogen freigesetzte oder direkt aus der Nahrung
und andere Antigene die Darmwand durchdringen.
stammende freie Fettsäuren vermögen proinflam-
Sie sind in der Lage, über TLR4 der Adipozyten eine
matorische Signalkaskaden auszulösen, indem sie
proinflammatorische Reaktion in Gang zu setzen.
an die Toll-Like-Rezeptoren-(TLR-)2 und insbe-
sondere 4 anbinden und dadurch den Transkripti- Folgen
onsfaktor NF-κB aktivieren (10). Diskutiert wird
eine solche Wirkung auch als Folge der hypoxischen Die auf verschiedenen Wegen und an unterschiedli-
Stoffwechsellage.
chen Organen lokal in Gang gesetzten inflammatori-
• Mit der Zunahme der Fettmasse geht auch eine ver- schen Prozesse führen zu einer dauerhaften Sekretion
stärkte Peroxidation von in Adipozyten gespeicher- proinflammatorischer Zytokine und anderer Media-
ten Fettsäuren einher, die zu einem Anstieg reakti- toren, die auf dem Blutweg verteilt werden und syste-
ver Sauerstoff- und Stickstoffspezies führt. Dies mische Effekte auslösen. Signalmoleküle erreichen
erhöht den Einstrom von Immunzellen und ver- andere Organe und verstärken dort bereits vorhan-
stärkt die lokale Inflammation zusätzlich (11).
dene Entzündungsvorgänge oder lösen sie möglicher-
• Die Hypertrophie des Fettgewebes übt mechani- weise auch aus (12). Wie Abbildung 1 zeigt, steht die
schen Stress auf die im dichten Netzwerk der extra- chronische systemische Inflammation mit einer Viel-
zellulären Matrix eingebetteten Adipozyten aus. zahl von Erkrankungen in Verbindung. Die dauer-
Dies soll über die Rho-assoziierte Proteinkinase hafte Entzündung ist dabei eine Reaktion auf bereits
(RhoA-Rock) ebenfalls auf den NF-κB-Signalweg erfolgte Schädigungen und stellt gleichzeitig einen
einwirken.
Risikofaktor für Folgeerkrankungen dar.
• Adipositas steht im Zusammenhang mit einer intes- Für die metabolischen Folgen zentral ist die Tatsache,
tinalen Dysbiose und einer erhöhten Darmperme- dass die «low grade inflammation» die Entstehung
Schweizer Zeitschrift für Ernährungsmedizin 3|2023 7
ENTZÜNDUNG UND ERNÄHRUNG
Abbildung 3: Mögliche Initiatoren der adipositasassoziierten Inflammation des Fettgewebes. DAMP: damage-associated molecular patterns, EZM: extrazelluläre Matrix, FFS: freie Fettsäuren, LPS: Lipoplysachharid, NF-kB: nukleärer Faktor, der an den Promotor leichter Kappa-Ketten von B-Lymphozyten bindet, NLR: NOD-like Rezeptor, NLRP3: NLR Family Pyrin Domain Containing 3, RhoA-Rock: Rho-assoziierte Proteinkinase, TLR: Toll-like Rezeptor. Modifiziert nach (9).
Tabelle 1:
Gemeinsamkeiten und Unterschiede von «klassischer» Entzündungsreaktion chronischer systemischer Inflammation (6)
klassische Entzündung
low grade inflammation
Dauer
akut, subakut
persistierend
Lokalisierung
lokal
insulinabhängige Gewebe, systemisch
Ausmass ausgeprägt
schwach
Altersabhängigkeit nein
ja
Folgen
Heilung, Entfernung des Auslösers, Kollateralschäden
Gewebereparatur
Gewebsinfiltration Neutrophile, Eosinophile, NK-Zellen, vor allem T-Lymphozyten,
durch
T-Lymphozyten, Makrophagen
Makrophagen
Entzündungsfördernde IL-6, IL-1b, TNF-a, ROS
IL-6, IL-1b, TNF-a, CRP, ROS, Leptin
Faktoren/Zytokine
Aktivierung
DAMP (Infektionen),
DAMP (endogene und exogene
PAMP (Traumata, Zellschädigungen) Faktoren, metabolische Störungen,
Gewebeschädigungen)
CRP: C-reaktives Protein, DAMP: damage-associated molecular patterns, IL: Interleukin, NK-Zellen: Natürliche Killerzellen, PAMP: pathogen-associated molecular patterns, ROS: reaktive Sauerstoffspezies, TNF: Tumornekrosefaktor.
einer Insulinresistenz fördert (1, 6, 7), weshalb Störungen im Rahmen des metabolischen Syndroms resultieren. Darüber hinaus können zahlreiche andere Gewebe und Organe betroffen sein. Beziehungen bestehen u. a. zu Tumor- und Autoimmunerkrankungen, Sarkopenie und Osteoporose, Neurodegene ration und Depression, chronisch obstruktive Lungenerkrankung (COPD) sowie Parodontitis. Die jeweiligen Erkrankungen wiederum verstärken ihrerseits das systemische Entzündungsgeschehen, so dass ein Teufelskreis entsteht. Inzwischen liegt eine Vielzahl von Einzelbefunden zu den Wirkungen und Mechanismen vor, die proinflammatorische Mediatoren ausüben. Von zentraler Bedeutung ist die Auslösung und Verstärkung einer Insulinresistenz (13). So sind TNF-α und IL-6 an der Entwicklung einer Insulinresistenz beteiligt, indem sie verschiedene Serinkinasen (Iκ Kinase β und Jun-N-terminale Kinase) aktivieren. Hierdurch erfolgt am Insulinrezeptor statt einer Phosphorylierung von Tyrosylresten der Insulinrezeptorsubstrate (ISR) eine Phosphorylierung von Serylresten, so dass die Signaltransduktion gestört ist. IL-6 und C-reaktives Protein (CRP) beeinflussen den Glukosestoffwechsel, indem sie die Expression von Genen unterdrücken, die an Glukoseaufnahme und -verarbeitung beteiligt sind (14). Adiponektin erhöht die Insulinwirksamkeit, indem es die Expression von Peroxisom-Proliferator-aktivierter Rezeptor alpha (PPAR-α) erhöht, einem Transkriptionsfaktor, der an der Fettsäureoxidation beteiligt ist. Die gesteigerte Fettsäureoxidation hilft dabei, die Ansammlung von Lipiden in Leber und Muskelzellen zu reduzieren und somit die Insulinsensitivität zu verbessern (15, 16). Die inflammationsbedingte Verschiebung des Adipozytokinprofils führt zu einer reduzierten Sekretion von Adiponektin und vermindert deshalb die Insulinsensitivität.
Ernährung und Inflammation
Ernährungsfaktoren beeinflussen Entstehung und Verlauf einer chronischen systemischen Inflammation auf verschiedenen Wegen. Die zentrale Bedeutung der viszeralen Adipositas erklärt, warum bereits eine Normalisierung des Körpergewichts mit einer Reduktion von entzündungsfördernden Faktoren einhergeht (6). Auch unabhängig hiervor können Ernährungsfaktoren das inflammatorische Geschehen vermindern. Dabei zeigt sich, dass Lebensstiländerungen (vor allem die Kombination von Ernährung und Bewegung) alleinigen Modifikationen des Ernährungsmusters und diese wiederum der Gabe von Einzelsubstanzen überlegen sind. Unstrittig ist, dass eine typische «Western Diet», gekennzeichnet durch eine hohe Energiedichte, hohe Anteile an schnell verfügbaren Kohlenhydraten, trans-Fettsäuren und Salz sowie einer vergleichsweise geringen Zufuhr an pflanzlichen Lebensmitteln (Vollkornprodukte, Hülsenfrüchte, Gemüse, Obst, Nüsse) und einer geringen Aufnahme an Ballaststoffen, sekundären Pflanzenstoffen sowie einigen Vitaminen und Mineralstoffen das Erkrankungsrisiko erhöht.
8 Schweizer Zeitschrift für Ernährungsmedizin 3|2023
ENTZÜNDUNG UND ERNÄHRUNG
Demgegenüber können andere Kostformen den Entzündungsprozess vermindern. Gut hierzu eignen sich «klassische» mediterrane Ernährungsformen, wie sie lange Zeit auf den griechischen Inseln üblich waren. Sie zeichnen sich durch hohe Anteile der vorab genannten pflanzlichen Lebensmittel, hohe Gehalte an Monoenfettsäuren und – durch den Verzehr von Fisch – Omega-3-Fettsäuren aus. Dass solche Ernährungsweisen entzündlichen Vorgängen entgegenwirken können, ist u. a. aus der Ernährungstherapie der rheumatoiden Arthritis bekannt, hat aber auch für die «low grade inflammation» Bedeutung (18, 19). Auf mechanistischer Ebene wurden für eine Vielzahl von Lebensmittelinhaltsstoffe anti-inflammatorische Eigenschaften postuliert. Demgegenüber ist die Evidenz für die jeweiligen Effekte aus Humanstudien vielfach gering, was vor allem methodische Gründe hat. So wird der Bioeffekt eines Nährstoffs massgeblich bestimmt von dessen Dosierung und der Expositionsdauer auf der einen, sowie der Nährstoffversorgung vor Beginn der Nährstoffgabe auf der anderen Seite. Dieser für Nährstoffe charakteristische kontextabhängige Dosis-Wirkungs-Zusammenhang ist bei vielen Supplementierungsstudien nicht berücksichtigt, was ihre Aussagekraft deutlich einschränkt (20). In Interventionsstudien wurde häufiger gezeigt, dass bestimmte Ernährungsweisen mit Veränderungen des Blutspiegels an einzelnen Lebensmittelinhaltsstoffen einhergingen und gleichzeitig inflammatorische Parameter verändert waren. Derartige Daten erlauben allerdings meist keine kausalen Rückschlüsse.
Ausblick
Die chronische systemische Inflammation ist eine persistierende und niederschwellige Entzündungs reaktion, die den Gesamtorganismus betrifft. Sie ist gekennzeichnet durch erhöhte Konzentrationen an proinflammatorischen Zytokinen und anderen Mediatoren und stellt einen Risikofaktor für vielfältige Folgeerkrankungen dar, die den Prozess wiederum verstärken. Zu den Ursachen zählen neben Fehlernährung, Bewegungsmangel und Adipositas auch psychosoziale Faktoren, Umwelteinflüsse sowie Infektionen. Mit zunehmendem Verständnis des komplexen Geschehens erweitern sich die Möglichkeiten, präventiv und therapeutisch einzugreifen. Die zentrale Bedeutung kommt dabei Ernährung und Bewegung zu.
Referenzen: 1. Calder PC et al.: Dietary factors and low-grade inflammation in rela-
tion to overweight and obesity. Br J Nutr 2014; 106, Suppl 3: S5-S78. 2. Purman D et al.: Chronic inflammation in the etiology of disease
across the life span. Nature Medicine 2019; 25: 1822-1832. 3. Wang C et al.: Effects of aging, cytomegalovirus infection, and EBVin-
fection on human B cell repertoires. J Immunol 2014;192: 603–611. 4. Hotamisligil GS et al.: Adipose expression of tumor necrosis factor-
alpha: direct role in obesity-linked insulin resistance. Science 1993; 259: 87–91. 5. Tilg H, Moschen AR: Adipocytokines: mediators linking adipose tissue, inflammation and immunity. Nature Reviews Immunology 2006; 6: 772-783 6. Hahn A et al.: Ernährung – Physiologische Grundlagen, Prävention, Therapie. 4. Auflage, Wissenschaftliche Verlagsgesellschaft, Stuttgart, 2023. 7. Krüger K: Inflammation during obesity – pathophysiological concepts and effects of physical activity. Dtsch Z Sportmed 2017; 7-8: 163-168. 8. Murano I et al.: Dead adipocytes, detected as crown-likestructures, are prevalent in visceral fat depots of geneticallyobese mice. J Lipid Res. 2008; 49: 1562. 9. Reilly SM et al.: Adapting to obesity with adipose tissue inflammation. Nat Rev Endocrinol 2017; 13: 633-643. 10. Rogero MM et al.: Obesity, inflammation, toll-like receptor 4 and fatty acids, Nutrients 2018; 10, 432 11. León-Pedroza JI et al.: Low-grade systemic inflammation and the development of metabolic diseases: From the molecular evidence to the clinical practice. Cirugía y Cirujanos. 2015; 83: 543-551. 12. Gregor MF et al.: Inflammatory mechanisms in obesity. Annu Rev Immunol 2011; 29: 415-445. 13. Kojta I et al.: Obesity, Bioactive Lipids, and Adipose Tissue Inflammation in Insulin Resistance. Nutrients 2020; 12: 1305 14. Stanimirovic J et al.: Role of C-Reactive Protein in Diabetic Inflammation. Mediators Inflamm 2022; 2022: 1–15. 15. Achari, A. E. & Jain, S. K. (2017). Adiponectin, a Therapeutic Target for Obesity, Diabetes, and Endothelial Dysfunction. I J Mol Sci 2017; 18: 1321. 16. Petersen MC et al.: Mechanisms of Insulin Action and Insulin Resistance. Physiol Rev. 2018; 98: 2133–2223. 17. Christ A et al.: Western diet and the immune system: An inflammatory connection. Immunity 2019; 51: 794-811* 18. Al-Aubaidy HA et al.: Twelve-Week Mediterranean Diet Intervention Increases Citrus Bioflavonoid Levels and Reduces Inflammation in People with Type 2 Diabetes Mellitus. Nutrients 2021; 13: 1133 19. Mena M et al.: Inhibition of circulating immune cell activation: a molecular antiinflammatory effect of the Mediterranean diet. Am J Clin Nutr 2009; 89: 248–256. 20. Ströhle A et al.: Nährstoffsupplemente – Möglichkeiten und Grenzen. Teil 5: Supplemente in der Primärprävention – Methodologische Aspekte. Med Monatsschr Pharm 2014; 37: 13-26.
Co-Autorinnen M.Sc. Wiebke Jonas und Dr. Isabel Behrendt Leibniz Universität Hannover (LUH) Institut für Lebensmittelwissenschaft und Humanernährung
Korrespondenzadresse: Prof. Dr. Andreas Hahn Leibniz Universität Hannover (LUH) Institut für Lebensmittelwissenschaft und Humanernährung Am Kleinen Felde 30 D-30167 Hannover E-Mail: hahn@nutrition.uni-hannover.de
Schweizer Zeitschrift für Ernährungsmedizin 3|2023 9