Transkript
ERNÄHRUNG UND ENTZÜNDUNG
Alterung des Immunsystems
Immunseneszenz, Entzündungen und Ernährung
Svenja Nolte, Karsten Krüger
Svenja Nolte
Unter Immunseneszenz versteht man die allmähliche Abnahme der Funktion des Immunsys tems, die mit dem Alterungsprozess einhergeht. Zu den Merkmalen der Immunsenszenz ge hören eine Abnahme der Zahl und Funktion diverser Leukozyten-Subpopulationen, eine er höhte Anfälligkeit für Infektionen, eine verminderte Fähigkeit, eine wirksame Immunantwort auf Impfstoffe zu entwickeln, und möglicherweise auch eine erhöhte Neigung zur Entwicklung maligner neoplatischer Erkrankungen. Gleichzeitig entwickeln gealterte Zellen ein entzündli ches Profil, den Seneszenz-assoziierten sekretorischen Phänotyp (SASP), der auch die nichtautonome zelluläre Seneszenz und die Immundysfunktion fördert (1).
Karsten Krüger
Besonders deutliche alterungsassoziierte Veränderungen zeigen die T-Zellen, deren Subpopulationen und Diversität sich verändern. So kommt es zu einer progressiven Reduktion des T-Zell-Repertoires, was dazu führt, dass es immer weniger einzigartige T-Zellen zur Erkennung verschiedener Krankheitserreger gibt. Dazu kommt es zur Akkumulation von hochdifferenzierten Gedächtnis-T-Zellen bei gleichzeitigem Rückgang der Zahl der naiven T-Zellen, sodass eingeschränkt auf neue Krankheitserreger reagiert werden kann. Auch Oberflächenmarker, die auf T-Zellen exprimiert werden, verändern sich mit dem Alter, was zur Ausprägung altersspezifischer T-ZellPhänotypen führt. So nimmt beispielsweise der Anteil der CD8+ T-Zellen, die den co-inhibitorischen Rezeptor PD-1 exprimieren, mit dem Alter zu, was ihre Funktion beeinträchtigen kann (2). Es gibt weitere altersbedingte Veränderungen auf molekularer Ebene, die auf eine Einschränkung metabolischer Prozesse und einer mangelnden Balance zwischen pro- und anti-entzündlichen Prozessen hindeuten. Entsprechend sind mit zellulären Immunalterung eine Reduktion der Stoffwechselleistung und der Shift zu pro-entzündlichen Signalprozessen und Genexpressionsmustern verbunden, die sich unter anderem in der vermehrten Produktion von inflammatorischen Zytokinen zeigt. So verschiebt sich mit zunehmendem Alter die Balance zwischen entzündungsfördernden und entzündungshemmenden Zytokinen, wobei die Produktion von proinflammatorischen Zytokinen wie IL-6, IL-1b und TNF-α dominiert. Dies ist unter anderem durch eine Aktivierung des Inflammasoms bedingt, eines intrazellulären Multiproteinkomplexes, der zellulären Stress wahrnimmt und das Genexpressionsmuster der Zellen hinsichtlich pro-entzündlicher Prozesse verändert. Dieser Shift wird auch durch die proportional wachsende
Zahl von seneszenten Zellen begünstigt, zu denen auch die Terminal-differenzierte Effektor-Gedächtniszellen (T-EMRA) gehören (3). Das Ausmass der Immunalterung und des «Inflammaging», eines mittlerweile gebräuchlichen Begriffes zur Kombination von Entzündungs- und Alterungsprozessen, wird durch eine Vielzahl von Erkrankungen und Lebensstilfaktoren bi-direktional beeinflusst. Dazu gehören bedeutsame chronische Erkrankungen wie Diabetes, Fettleibigkeit und Herz-Kreislauf-Erkrankungen. Einerseits fördern gealterte Immunzellen die Entstehung einer endothelialen Dysfunktion und die Entstehung arteriosklerotischer Plaques, während chronisch erhöhte inflammatorische Zytokine vasoaktiv sind und auch den Glukose- und Lipidstoffwechsel stören. Umgekehrt können Stoffwechselstörungen auch inflammatorische Prozesse induzieren, da besonders ein expandierendes viszerales Fettgewebe zunächst metabolische Stresssignale, schliesslich auch inflammatorische Signalkaskaden aktivieren kann, welche nach einem Spill-over die systematische Entzündung triggert (4). Auch Lebensstilfaktoren, wie Schlafmangel, Rauchen, Alkoholkonsum und eine unbewegte Lebensweise, können das Risiko einer altersbedingten Entzündung erhöhen. Eine langfristig positive Energiebilanz und eine Ernährung mit einem hohen Anteil an gesättigten Fetten, Zucker und hochverarbeiteten Lebensmitteln scheinen dabei einen besonderen Einfluss zu haben (5).
Mikrobiom und Immunsystem
Die alterassoziierten Veränderungen des Immunsystems stehen in gewissen Abhängigkeiten zum Mikrobiom des Darms, denn das Darmgewebe beherbergt darmassoziiertes lymphatisches Gewebe (gut associated lymphoid tissue [GALT]). Man schätzt, dass beim
10 Schweizer Zeitschrift für Ernährungsmedizin 3|2023
ERNÄHRUNG UND ENTZÜNDUNG
Menschen etwa 70% der Immunzellen mit dem GALT funktionell assoziiert sind und dadurch der Kontakt mit der Darmmikrobiota eine wesentliche Bedeutung für das Funktionieren des Wirtsimmunsystems hat. Dass kommensale Bakterien der Mikrobiota wesentlich zur Entwicklung eines normal funktionierenden Immunsystems beitragen, zeigen keimfreie Tiermodelle, bei denen die lymphatischen Organe degenerieren und die Immunglobuline und Lymphozytenpopulationen reduziert sind (6). Auch das intestinale Mikrobiom unterzieht sich Veränderungen in seiner Zusammensetzung über die Lebensspanne des Menschen, weshalb es in den letzten Jahren als einer der Entscheidungsträger für Gesundheit und Krankheit diskutiert wird (7). Ein gesundes Darmmikrobiom eines Erwachsenen ist gekennzeichnet durch seine Stabilität, bis der Alterungsprozess beginnt und die Darmhomöstase beeinträchtigt wird (8). Neben einer geringeren Stabilität der intestinalen Mikrobiota nimmt mit der Alterung die Biodiversität ab, die sich besonders durch eine Reduktion der anti-inflammatorischen kurzkettigen Fettsäure produzierenden Bakterien auszeichnet (9). Zusätzlich führt die chronische niederschwellige Inflammation zum Wachstum von Pathobionten. Pathobionten machen in einem gesunden Darm nur einen geringen Teil aus, werden jedoch in einer pro-inflammatorischen Umgebung zum Wachstum angeregt, bis sie schliesslich die «guten», symbiotischen Darmbakterien in ihrer Zahl übertreffen (10). So kommt es insgesamt zu wechselseitigen Beeinflussungen zwischen systemischer Entzündung und Mikrobiom, die Bakterienpopulationen im Darm und ihre Syntheseprodukte wiederum die systemische Immunbalance beeinflussen.
«Healthy Aging» versus maladaptive Alterung
All diese Erkenntnisse sollen das Altern nicht per se als negativ-behafteten Prozess darstellen. Es kommt zwar in vielen physiologischen Systemen zu Remodelierungsprozessen, die mit Funktionseinschränkungen assoziiert sind; gleichwohl sind einige Umbauprozesse sicherlich funktioneller Natur (11). Weiterhin bestimmen verschiedene Lebensstilfaktoren die Geschwindigkeit der Progression der Immunalterung, so dass individuelle Einflüsse ein gesundes Altern zulassen und maladaptive Alterungsprozesse reduziert werden können. Wesentliche Einflussfaktoren stellen die Ernährung und körperliche Aktivität als zentrale Lebensstilmassnahmen dar, da diese einzeln und in Kombination signifikanten Einfluss auf Entzündung, Immunalterung und das Mikrobiom als einen der Mediatoren dieser Effekte haben (12).
Einfluss des Lebensstils auf die Immunalterung
Ein erster wichtiger Faktor ist eine ausgewogene Energiebilanz, da bekannt ist, dass Übergewicht und Adipositas in einer engen wechselseitigen Beziehung zur
systemischen Entzündung und der zellulären Immunalterung stehen. Dies liegt zum einen am entzündlichen Potenzial des viszeralen und ektopischen Fettgewebes, zum anderen an dem Zusammenhang zwischen dem Körperfett und der Proportion seneszenter T-Zellen, wie den T-EMRA-Zellen (13, 4). Entsprechend konnten viele Studien der vergangenen Jahre die Schlüsselrolle von einzelnen Ernährungsmustern zunächst auf die entzündlichen Komponenten der Immunalterung belegen. Weiterhin zeigen sich besonders durch die mediterrane Ernährungsweise, die DASH-Diät (Dietary Approaches to Stop Hypertension) und einer pflanzlichen Vollwertkost positiv-immunregulierende Einfüsse auf systemische Entzündungsprozesse. Die anti-entzündlichen Prozesse scheinen besonders von der erhöhten Aufnahme von Obst, Gemüse, Vollkornprodukten, Hülsenfrüchten, Nüssen, Samen und gesunden Fetten wie Olivenöl und fettem Fisch auszugehen. Diese Lebensmittel sind reich an Antioxidanzien, V itaminen, Mineralien und Ballaststoffen, die einerseits entzündungshemmende Wirkungen
«Auch das intestinale Mikrobiom unterzieht sich Veränderungen
in seiner Zusammensetzung über die Lebensspanne des Menschen,
»weshalb es in den letzten Jahren als einer der Entscheidungsträger
für Gesundheit und Krankheit diskutiert wird.
haben, positive Wirkungen auf die Immunfunktion haben und die Darmgesundheit verbessern (14). Der Verzehr von rotem und gepökeltem Fleisch, welches eher pro-entzündliche Wirkungen hat, wird gleichzeitig verringert. Die genannten Ernährungsweisen sind gleichzeitig mit einem geringeren Risiko für kardiovaskuläre Erkrankungen assoziiert, was eine indirekte oder direkte Folge der immunregulierenden Wirkung sein könnte (14).
Ernährung als Modulator der Immunalterung
Neben den allgemeinen Ernährungsweisen und einzelnen Lebensmittelgruppen beeinflussen einzelne Bestandteile der Ernährung die Immunfunktion. Da im Alter häufiger Mangelerscheinungen einzelner Mikro- und Makronährstoffen auftreten, wird dies durchaus auch relevant für das Immunaltern (15). Als Makronährstoffe liefern Kohlenhydrate und Proteine metabolische Substrate und Bausteine für die Biosynthese von Molekülen, die an der Immunantwort beteiligt sind, wie z. B. Aminosäuren für Immunglobuline, Zytokine, Rezeptoren und Akutphasenproteine. Viele Mikronährstoffe regulieren molekulare und zelluläre Aspekte der Immunreaktion, wozu besonders Eisen, Zink, Vitamin A und Vitamin D gehören. Selektive Nährstoffe bilden Substrate für die Synthese von Verbindungen, die an der Immunreaktion beteiligt sind, wie Arginin und Stickstoffmonoxid sowie Arachidonsäure und Eicosanoide. Einige Mineral-
Schweizer Zeitschrift für Ernährungsmedizin 3|2023 11
ERNÄHRUNG UND ENTZÜNDUNG
Lebensstileinflüsse auf das Mikrobiom im Alter
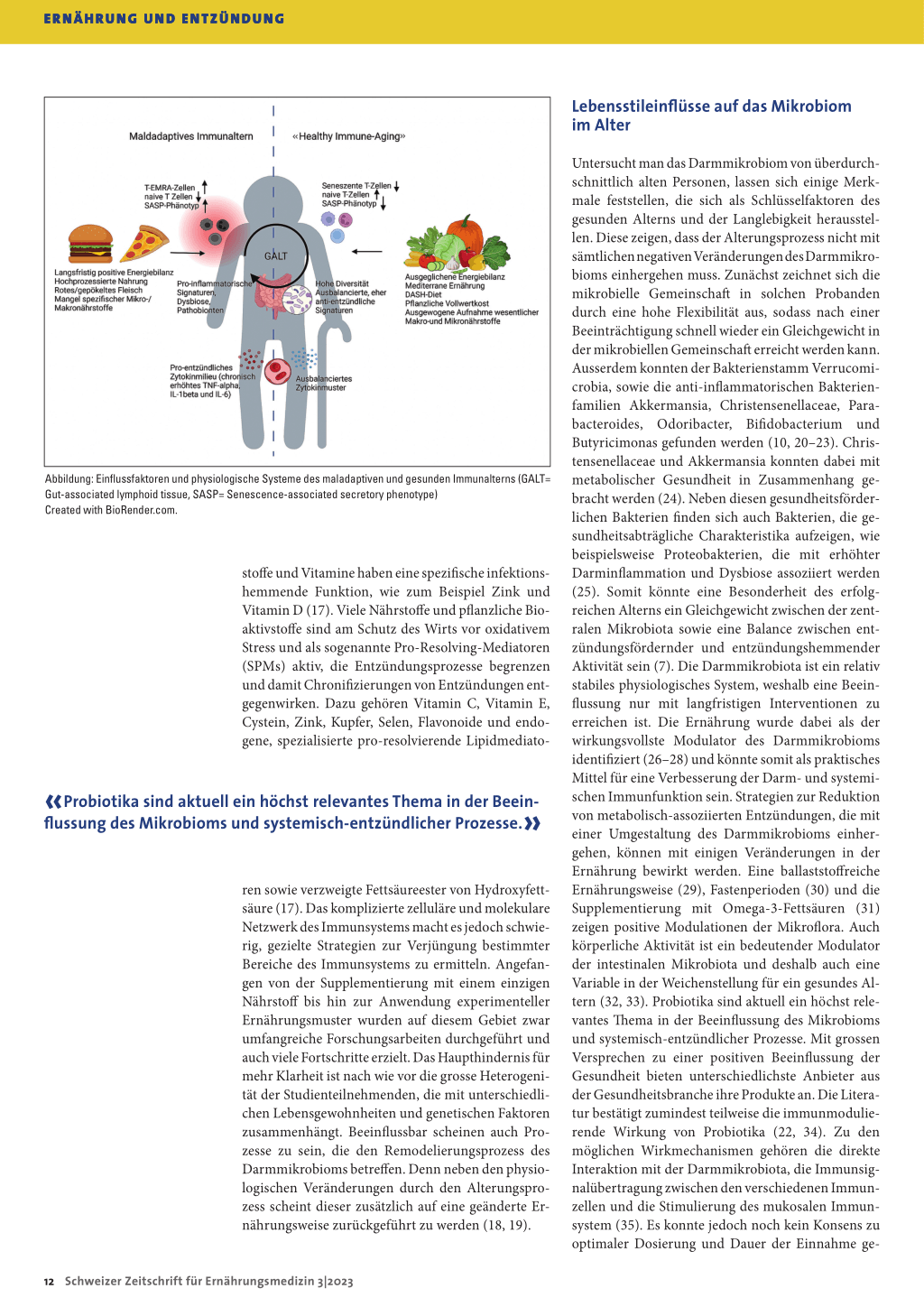
Abbildung: Einflussfaktoren und physiologische Systeme des maladaptiven und gesunden Immunalterns (GALT= Gut-associated lymphoid tissue, SASP= Senescence-associated secretory phenotype) Created with BioRender.com.
stoffe und Vitamine haben eine spezifische infektionshemmende Funktion, wie zum Beispiel Zink und Vitamin D (17). Viele Nährstoffe und pflanzliche Bioaktivstoffe sind am Schutz des Wirts vor oxidativem Stress und als sogenannte Pro-Resolving-Mediatoren (SPMs) aktiv, die Entzündungsprozesse begrenzen und damit Chronifizierungen von Entzündungen entgegenwirken. Dazu gehören Vitamin C, Vitamin E, Cystein, Zink, Kupfer, Selen, Flavonoide und endogene, spezialisierte pro-resolvierende Lipidmediato-
Probiotika sind aktuell ein höchst relevantes Thema in der Beein
« »flussung des Mikrobioms und systemisch-entzündlicher Prozesse.
ren sowie verzweigte Fettsäureester von Hydroxyfettsäure (17). Das komplizierte zelluläre und molekulare Netzwerk des Immunsystems macht es jedoch schwierig, gezielte Strategien zur Verjüngung bestimmter Bereiche des Immunsystems zu ermitteln. Angefangen von der Supplementierung mit einem einzigen Nährstoff bis hin zur Anwendung experimenteller Ernährungsmuster wurden auf diesem Gebiet zwar umfangreiche Forschungsarbeiten durchgeführt und auch viele Fortschritte erzielt. Das Haupthindernis für mehr Klarheit ist nach wie vor die grosse Heterogenität der Studienteilnehmenden, die mit unterschiedlichen Lebensgewohnheiten und genetischen Faktoren zusammenhängt. Beeinflussbar scheinen auch Prozesse zu sein, die den Remodelierungsprozess des Darmmikrobioms betreffen. Denn neben den physiologischen Veränderungen durch den Alterungsprozess scheint dieser zusätzlich auf eine geänderte Ernährungsweise zurückgeführt zu werden (18, 19).
Untersucht man das Darmmikrobiom von überdurchschnittlich alten Personen, lassen sich einige Merkmale feststellen, die sich als Schlüsselfaktoren des gesunden Alterns und der Langlebigkeit herausstellen. Diese zeigen, dass der Alterungsprozess nicht mit sämtlichen negativen Veränderungen des Darmmikro bioms einhergehen muss. Zunächst zeichnet sich die mikrobielle Gemeinschaft in solchen Probanden durch eine hohe Flexibilität aus, sodass nach einer Beeinträchtigung schnell wieder ein Gleichgewicht in der mikrobiellen Gemeinschaft erreicht werden kann. Ausserdem konnten der Bakterienstamm Verrucomicrobia, sowie die anti-inflammatorischen Bakterienfamilien Akkermansia, Christensenellaceae, Para bacteroides, Odoribacter, Bifidobacterium und Butyricimonas gefunden werden (10, 20–23). Christensenellaceae und Akkermansia konnten dabei mit metabolischer Gesundheit in Zusammenhang gebracht werden (24). Neben diesen gesundheitsförderlichen Bakterien finden sich auch Bakterien, die gesundheitsabträgliche Charakteristika aufzeigen, wie beispielsweise Proteobakterien, die mit erhöhter Darminflammation und Dysbiose assoziiert werden (25). Somit könnte eine Besonderheit des erfolg reichen Alterns ein Gleichgewicht zwischen der zentralen Mikrobiota sowie eine Balance zwischen entzündungsfördernder und entzündungshemmender Aktivität sein (7). Die Darmmikrobiota ist ein relativ stabiles physiologisches System, weshalb eine Beeinflussung nur mit langfristigen Interventionen zu erreichen ist. Die Ernährung wurde dabei als der wirkungsvollste Modulator des Darmmikrobioms identifiziert (26–28) und könnte somit als praktisches Mittel für eine Verbesserung der Darm- und systemischen Immunfunktion sein. Strategien zur Reduktion von metabolisch-assoziierten Entzündungen, die mit einer Umgestaltung des Darmmikrobioms einher gehen, können mit einigen Veränderungen in der Ernährung bewirkt werden. Eine ballaststoffreiche Ernährungsweise (29), Fastenperioden (30) und die Supplementierung mit Omega-3-Fettsäuren (31) zeigen positive Modulationen der Mikroflora. Auch körperliche Aktivität ist ein bedeutender Modulator der intestinalen Mikrobiota und deshalb auch eine Variable in der Weichenstellung für ein gesundes Altern (32, 33). Probiotika sind aktuell ein höchst relevantes Thema in der Beeinflussung des Mikrobioms und systemisch-entzündlicher Prozesse. Mit grossen Versprechen zu einer positiven Beeinflussung der Gesundheit bieten unterschiedlichste Anbieter aus der Gesundheitsbranche ihre Produkte an. Die Literatur bestätigt zumindest teilweise die immunmodulierende Wirkung von Probiotika (22, 34). Zu den möglichen Wirkmechanismen gehören die direkte Interaktion mit der Darmmikrobiota, die Immunsignalübertragung zwischen den verschiedenen Immunzellen und die Stimulierung des mukosalen Immunsystem (35). Es konnte jedoch noch kein Konsens zu optimaler Dosierung und Dauer der Einnahme ge-
12 Schweizer Zeitschrift für Ernährungsmedizin 3|2023
ERNÄHRUNG UND ENTZÜNDUNG
funden werden, in welchem Bezug die hohen interindividuellen Unterschiede der Wirkweise herausgestellt werden sollten (15). Neben der belegten Wirksamkeit bei Infektionen, die den oberen Respirationstrakt betreffen (35), zeigte sich der Verzehr von fermentierter Milch (Lactobacillus johnsonii La1) bei Alten als wirksam in der Bekämpfung von Infektionen und führte zu einer Verbesserung des Ernährungsund Immunstatus (36–38).
Fazit
Insgesamt zeigt die derzeitige Datenlage, dass sich durch das Alter auf verschiedenen Ebenen ein Umbauprozess des Immunsystems einstellt, der in vielen Bereichen zu einer reduzierten Funktion der Abwehrfunktion führt. Die Geschwindigkeit der Progression und damit auch das Ausmass der Dysfunktion ist stark mit dem Lebensstil assoziiert, wobei die Ernährung hier sowohl quantitativ (im Sinne einer ausgeglichenen Energiebilanz) als auch qualitativ (im Sinne einer ausgewogenen Ernährung mit einer ausreichenden Versorgung von Makro- und Mikronährstoffen) ein wesentlicher Modulator ist. Das Darmmikrobiom spielt in diesem Netzwerk eine zentrale Rolle, da es sich einerseits altersbedingt verändert, aber auch durch Lebensstilfaktoren beeinflussen lässt (Abbildung).
Korrespondenzadresse: Prof. Dr. Karsten Krüger Abteilung für Leistungsphysiologie und Sporttherapie Institut für Sportwissenschaft Kugelberg 62 D-35394 Giessen E-Mail: karsten.krueger@sport.uni-giessen.de Co-Autorin: Svenja Nolte, MSc., Doktorandin, Wissenschaftliche Mitarbeiterin, MSH Medical School Hamburg, Justus-Liebig-Universität Giessen Referenzen: 1. Lee KA et al.: Immune Senescence, Immunosenescence and Aging.
Front Aging. 2022 May 30;3:900028. 2. Mittelbrunn M et al.: Hallmarks of T cell aging. Nat Immunol. 2021
Jun;22(6):687-698. 3. Goronzy JJ et al.: Successful and Maladaptive T Cell Aging. Immu-
nity. 2017 Mar 21;46(3):364-378. 4. Bosslau TK et al.: Abdominal Obesity-Related Disturbance of Insulin
Sensitivity Is Associated with CD8+ EMRA Cells in the Elderly. Cells. 2021 Apr 23;10(5):998. 5. Strasser B et al.: The Effects of Lifestyle and Diet on Gut Microbiota Composition, Inflammation and Muscle Performance in Our Aging Society. Nutrients. 2021 Jun 15;13(6):2045. 6. Ahern PP et al. :Understanding immune-microbiota interactions in the intestine. Immunology. 2020 Jan;159(1):4-14. 7. Badal VD et al: The Gut Microbiome, Aging, and Longevity: A Systematic Review. Nutrients. 2020 Dec 7;12(12):3759. 8. Biagi E et al.: Through ageing, and beyond: gut microbiota and inflammatory status in seniors and centenarians. PLoS One. 2010 May 17;5(5):e10667. 9. Biagi E et al.: Aging of the human metaorganism: the microbial counterpart. Age (Dordr). 2012 Feb;34(1):247-67. 10. Biagi E et al.: Ageing and gut microbes: perspectives for health maintenance and longevity. Pharmacol Res. 2013 Mar;69(1):11-20. 11. Goronzy JJ et al.: Successful and Maladaptive T Cell Aging. Immunity. 2017 Mar 21;46(3):364-378. 12. Rosa-Neto JC et al.: Immunometabolism-fit: How exercise and training can modify T cell and macrophage metabolism in health and disease. Exerc Immunol Rev. 2022;28:29-46.
13. Krüger K: Inflammation during Obesity – Pathophysiological Concepts and Effects of Physical Activity. Dtsch Z Sportmed. 2017; 68: 163-169.
14. Itsiopoulos C et al.: The anti-inflammatory effects of a Mediterranean diet: a review. Curr Opin Clin Nutr Metab Care. 2022 Nov 1;25(6):415422.
15. Weyh C et al.: Physical Activity and Diet Shape the Immune System during Aging. Nutrients. 2020 Feb 28;12(3):622.
16. Calder PC et al.: Nutrition, Immunosenescence, and Infectious Disease: An Overview of the Scientific Evidence on Micronutrients and on Modulation of the Gut Microbiota. Adv Nutr. 2022 Oct 2;13(5):S1S26.
17. Brennan E et al.: Pro-resolving lipid mediators: regulators of inflammation, metabolism and kidney function. Nat Rev Nephrol. 2021 Nov;17(11):725-739.
18. Budden KF et al.: Emerging pathogenic links between microbiota and the gut-lung axis. Nat Rev Microbiol. 2017 Jan;15(1):55-63.
19. Labbé A et al.: Bacterial bile metabolising gene abundance in Crohn›s, ulcerative colitis and type 2 diabetes metagenomes. PLoS One. 2014 Dec 17;9(12):e115175.
20. Kim BS et al.: Comparison of the Gut Microbiota of Centenarians in Longevity Villages of South Korea with Those of Other Age Groups. J Microbiol Biotechnol. 2019 Mar 28;29(3):429-440.
21. Tuikhar N et al.: Comparative analysis of the gut microbiota in centenarians and young adults shows a common signature across genotypically non-related populations. Mech Ageing Dev. 2019 Apr;179:2335.
22. Wu L et al.: A Cross-Sectional Study of Compositional and Functional Profiles of Gut Microbiota in Sardinian Centenarians. mSystems. 2019 Jul 9;4(4):e00325-19.
23. Yu X et al.: Analysis of the intestinal microbial community structure of healthy and long-living elderly residents in Gaotian Village of Liuyang City. Appl Microbiol Biotechnol. 2015 Nov;99(21):9085-95.
24. Rizzatti G et al. Proteobacteria: A Common Factor in Human Diseases. Biomed Res Int. 2017;2017:9351507.
25. Boulangé CL et al.: Impact of the gut microbiota on inflammation, obesity, and metabolic disease. Genome Med. 2016 Apr 20;8(1):42.
26. Rinninella E et al.: Food Components and Dietary Habits: Keys for a Healthy Gut Microbiota Composition. Nutrients. 2019 Oct 7;11(10):2393.
27. Clarke SF et al.: Exercise and associated dietary extremes impact on gut microbial diversity. Gut. 2014 Dec;63(12):1913-20.
28. Kopf JC et al.: Role of whole grains versus fruits and vegetables in reducing subclinical inflammation and promoting gastrointestinal health in individuals affected by overweight and obesity: a randomized controlled trial. Nutr J. 2018 Jul 30;17(1):72.
29. Stekovic S et al.: Alternate Day Fasting Improves Physiological and Molecular Markers of Aging in Healthy, Non-obese Humans. Cell Metab. 2019 Sep 3;30(3):462-476.e6. Erratum in: Cell Metab. 2020 Apr 7;31(4):878-881.
30. Costantini L et al.: Impact of Omega-3 Fatty Acids on the Gut Microbiota. Int J Mol Sci. 2017 Dec 7;18(12):2645.
31. Fart F et al.: Differences in Gut Microbiome Composition between Senior Orienteering Athletes and Community-Dwelling Older Adults. Nutrients. 2020 Aug 27;12(9):2610.
32. Zhu Q et al.: Effects of exercise frequency on the gut microbiota in elderly individuals. Microbiologyopen. 2020 Aug;9(8):e1053.
33. Walsh NP. Nutrition and Athlete Immune Health: New Perspectives on an Old Paradigm. Sports Med. 2019 Dec;49(Suppl 2):153-168.
34. Waters JL et al.: The human gut bacteria Christensenellaceae are widespread, heritable, and associated with health. BMC Biol. 2019 Oct 28;17(1):83.
35. Maldonado Galdeano C, Cazorla SI, Lemme Dumit JM, Vélez E, Perdigón G: Beneficial Effects of Probiotic Consumption on the Immune System. Ann Nutr Metab. 2019;74(2):115-124. doi: 10.1159/000496426. Epub 2019 Jan 23. PMID: 30673668.
36. Fukushima Y et al.: Improvement of nutritional status and incidence of infection in hospitalised, enterally fed elderly by feeding of fermented milk containing probiotic Lactobacillus johnsonii La1 (NCC533). Br J Nutr. 2007 Nov;98(5):969-77.
37. Guillemard E et al.: Consumption of a fermented dairy product containing the probiotic Lactobacillus casei DN-114001 reduces the duration of respiratory infections in the elderly in a randomised controlled trial. Br J Nutr. 2010 Jan;103(1):58-68.
38. Turchet P et al.: Effect of fermented milk containing the probiotic Lactobacillus casei DN-114001 on winter infections in free-living elderly subjects: a randomised, controlled pilot study. J Nutr Health Aging. 2003;7(2):75-7.
Schweizer Zeitschrift für Ernährungsmedizin 3|2023 13