Transkript
LEBENSMITTELSICHERHEIT
Sicherheit von Vitaminen und Mineralstoffen
ANDREAS HAHN* UND ALEXANDER STRÖHLE*
Andreas Hahn
Dosis sola facit venenum – allein die Dosis macht das Gift. Diese grundlegende, bereits von Paracelus (1493–1541) formulierte Erkenntnis der Toxikologie gilt auch für Vitamine und Mineralstoffe. Sowohl ein Zuwenig als auch ein Zuviel dieser essenziellen Mikronährstoffe ist mit Nachteilen für die Gesundheit verbunden. Vor dem Hintergrund der Anreicherung von Lebensmitteln mit bestimmten Nährstoffen und der zunehmenden Bedeutung von Nährstoffsupplementen gewinnt deshalb die Frage an Bedeutung, welche Nährstoffmengen langfristig ohne Risiken aufgenommen werden können.
Alexander Ströhle
Hintergrund Erst Ende der Neunziger-
jahre des 19. Jahrhunderts
gelang dem niederländischen Hygieniker
und Tropenarzt Christiaan Eijkman (No-
belpreis 1929) bei seinen Forschungen
auf der indonesischen Insel Java der
Nachweis, dass für die Aufrechterhaltung
der normalen Körperfunktionen neben
Makronährstoffen (Kohlenhydrate, Fett,
Eiweiss) weitere organische Nahrungsbe-
standteile erforderlich sind. Mit dieser
Entdeckung der später von Kasimir Funk
als Vitamine bezeichneten Substanzklas-
se begann die Suche nach der notwendi-
gen Zufuhr an Mikronährstoffen für die
Aufrechterhaltung der Gesundheit. Zu-
nächst war der Fokus der Wissenschaft
darauf gerichtet, die zur Vermeidung
von Mangelerscheinungen erforderlichen
Mengen zu definieren; ab den Neunziger-
jahren des 20. Jahrhunderts trat die Frage
in den Vordergrund, welche Nährstoffauf-
nahme im Hinblick auf die langfristige
*Institut für Lebensmittelwissenschaft und Humanernährung, Leibniz Universität Hannover
Gesundheit und die Prävention chro- kompetente Zellen (u.a. Lymphozyten,
nisch-degenerativer Erkrankungen anzu- Neutrophile) mit Vitamin C gesättigt (4).
streben ist (1).
Diskutiert wird, dass 250 bis 300 mg Vit-
Wie Abbildung 1 am Beispiel von Vitamin C amin C pro Tag präventive Effekte im Hin-
verdeutlicht, variiert die wünschenswerte blick auf die Entwicklung eines grauen
Nährstoffzufuhr in Abhängigkeit vom je- Stars (Katarakt) ausüben (5, 6). Bei ≥ 400 mg
weiligen Zielkriterium (2). So genügt zur pro Tag ist jene Vitamin-C-Zufuhr erreicht,
Vermeidung von Skorbut – einer klassi- die in einer systematischen Auswertung
schen Vitamin-C-Mangelerkrankung – be- mehrerer grosser Kohortenstudien mit ins-
reits eine Menge von 10 mg Vitamin C pro gesamt 293 172 Teilnehmern mit einer
Tag; unter Berücksichtigung von Sicher- signifikanten Senkung des Risikos korona-
heitszuschlägen ergibt sich
daraus eine anzustrebende
Zufuhr von 30 mg Vitamin C
pro Tag für einen sicheren
Skorbutschutz. Um die
aufgrund von Beobach-
tungsstudien als präventiv
angesehene Plasmakon-
zentration an Vitamin C von
≥ 50 µmol/l zu erreichen,
bedarf es bereits ≥ 100 mg
Vitamin C täglich (3). Mit
mehr als 200 mg amTag wird
schliesslich eine weitgehen-
de Sättigung des Plasmas er- Abbildung 1: Dosis-Wirkungs-Beziehung zwischen der Vitamin-C-Zufuhr zielt; nun sind auch immun- und verschiedenen Endpunkten (2).
4/14
22
LEBENSMITTELSICHERHEIT
Abbildung 2: Dosis-Wirkungs-Kurve von Nährstoffen (16). Ausgehend von einer unzureichenden Zufuhr (linker Bereich der x-Achse) verbessern sich mit steigender Aufnahme eines Nährstoffs die Körperfunktionen; das Risiko für Mangelsymptome und entleerte Nährstoffspeicher sinkt. Mit weiter steigender Dosis wird ein Indifferenzbereich durchschritten, innerhalb dessen sich keine weitere Funktionsverbesserung ergibt, aber auch keine unerwünschten gesundheitlichen Effekte auftreten. Noch höhere Zufuhren führen zu einem sukzessiv zunehmenden Risiko für toxische Effekte; die Gefahr für unerwünschte Nebenwirkungen steigt.
Abbildung 3: Dosis-Wirkungs-Beziehung für die Ableitung der drei toxikologischen Kenngrössen LOAEL, NOAEL und UL (16, nach 25). Die Ableitung des UL (= höchste Nährstoffaufnahme) erfolgt auf Basis des NOAEL- beziehungsweise LOAEL-Werts unter Berücksichtigung eines Unsicherheitsfaktors. LOAEL: Lowest observed adverse effect level; NOAEL: No observed adverse effect level
rer Herzerkrankungen verbunden war (7). Eine Aufnahme von 500 bis 2000 mg Vitamin C am Tag führt schliesslich in den adjuvant-therapeutischen Bereich und wird beispielsweise zur Optimierung der Wundheilung nach operativen Eingriffen empfohlen (8). Vor diesem Hintergrund und angetrieben durch eine mediale Berichterstattung, die aus Vermutungen bisweilen Fakten und aus Fiktion gelegentlich Wahrheit entstehen lässt, kann es nicht verwundern, dass Vitamine und zunehmend auch Mineralstoffe in der Bevölkerung ein hohes Ansehen geniessen. Nicht selten resultiert daraus die Einnahme von Nährstoffsupplementen in der Erwartung eines zusätzlichen gesundheitlichen Nutzens. Verschiedene Untersuchungen zeigen, dass zwischen 25 und mehr als 40 Prozent der Erwachsenen nach eigenem Bekunden regelmässig solche Produkte konsumieren (9–15), insbesondere Vitamin- und Mineralstoffpräparate. Diese Entwicklung wirft nicht nur die Frage nach dem tatsächlichen Nutzen einer zusätzlichen Nährstoffzufuhr auf; sie erfordert gleichermassen einen Blick auf mögliche Risiken.
Dosis-Wirkungs-Beziehungen
bei essenziellen Mikronährstoffen
Abbildung 2 zeigt die typische Dosis-Wirkungs-Kurve eines essenziellen Nähr-
stoffs (16). Das völlige Fehlen der jeweiligen Substanz führt langfristig zum Tod. Mit steigender Zufuhr der Substanz sinkt das Risiko für Mangelerscheinungen; die klinischen Symptome verschwinden zusehends, und alle physiologischen Vorgänge normalisieren sich. Wird die Dosis erhöht, so folgt ein Indifferenzbereich, innerhalb dessen sich keine weitere Funktionsverbesserung ergibt, aber auch keine unerwünschten gesundheitlichen Effekte auftreten. Noch höhere Zufuhren steigern schliesslich das Risiko für unerwünschte Effekte und Erkrankungen durch Intoxikationen. Ziel der ernährungswissenschaftlichen Forschung ist es daher, die Zufuhr an Nährstoffen zu ermitteln, die – dem heutigen umfassenden Verständnis von Ernährung folgend – nicht nur Mangelerscheinungen vermeidet, sondern den langfristigen Erhalt der Gesundheit sicherstellt (2). Diese Erkenntnisse finden ihren Niederschlag in Empfehlungen für die Nährstoffzufuhr, im deutschen Sprachraum in Form der D-ACH-Referenzwerte (17). Gleichermassen gilt es aber auch, die Nährstoffmengen zu definieren, die im Sinne eines Vermeidens unerwünschter Wirkungen tolerierbar sind. Dabei spielt die akute Toxizität für die Praxis eine vernachlässigbare Rolle; relevant ist vielmehr die chronische Toxizität. Dies erfordert die Festlegung tolerierbarer
Höchstmengen für die langfristige Zufuhr, eine Aufgabe, die üblicherweise durch Expertenkommissionen auf Basis des jeweiligen Stands wissenschaftlicher Kenntnisse vorgenommen wird. Innerhalb der EU sowie der Schweiz wird dies im Allgemeinen von der Europäischen Behörde für Lebensmittelsicherheit (European Food Safety Authority, EFSA) beziehungsweise deren Vorläufergremium Scientific Committee on Food (SCF) der Europäischen Kommission übernommen. Im amerikanischen Raum ist das Food and Nutrition Board (FNB) des Institute of Medicine (IOM) für diese Aufgabe verantwortlich.
Toxikologische Bewertung
von Vitaminen und Mineralstoffen
Wissenschaftlich akzeptiert ist die grundsätzliche Feststellung, dass die Aufnahme von Nährstoffen bis zu einem bestimmten Schwellenwert nicht mit Risiken für Nebenwirkungen behaftet ist (18). Diese Schwellenwerte variieren innerhalb einer Population, unter anderem in Abhängigkeit von Gewicht, lean body mass, physiologischem Status und genetischen Faktoren, sodass theoretisch für jede Person ein individueller Wert definiert werden müsste; hierfür fehlt allerdings die Datenbasis. Aus diesem Grund werden Schwellenwerte wie der UL (s.u.) so festgelegt, dass sie auch die empfindlichsten Indivi-
23 4/14
LEBENSMITTELSICHERHEIT
duen berücksichtigen (19). Der Ansatz ist damit dem bei der Festlegung von Referenzwerten für die Nährstoffzufuhr vergleichbar, die bekanntlich so bemessen sind, dass die jeweils empfohlene Zufuhr «nahezu alle» Personen gesund erhält. In Anbetracht dessen, dass die Vulnerabilität gegenüber einer überhöhten Nährstoffzufuhr durch zahlreiche physiologische Faktoren beeinflusst wird, ist es allerdings angezeigt, diese bei der Festlegung von Schwellenwerten zu berücksichtigen und beispielsweise für Kinder, Schwangere oder Stillende entsprechend angepasste Werte zu definieren. Gleichermassen sind die Bioverfügbarkeit eines Nährstoffes, die Interaktionen mit anderen Nahrungsinhaltsstoffen und auch die Versorgungslage zu berücksichtigen (19). In toxikologischer Hinsicht bedeutsam ist
die Unterscheidung zwischen Gefährdung(spotenzial) («hazard») eines Stoffes auf der einen und Risiko («risk») auf der anderen Seite (20): Das Gefährdungspotenzial beschreibt die stoffimmanente Eigenschaft, adverse Wirkungen hervorzurufen. Unter Risiko wird hingegen die Möglichkeit eines Schadenseintrittsereignisses verstanden; es ergibt sich als Produkt von Schadensausmass und Wahrscheinlichkeit. Der Begriff «Risiko» berücksichtigt somit die zu erwartende Schadenshäufigkeit und das zu erwartende Schadensausmass. Im Grundsatz erfolgt die toxikologische Bewertung von Vitaminen und Mineralstoffen in einem vierstufigen Verfahren (18, 19, 21–23): 1. Erkennen des Gefährdungspotenzials
(«hazard identification»): Identifizie-
rung der bekannten oder potenziell nachteiligen Effekte eines Nährstoffs auf Basis der verfügbaren Informationen und Zusammenfassung der Belege. 2. Charakterisierung des Gefährdungspotenzials («hazard characterisation»): Qualitative und quantitative Einordnung der Nebenwirkungen. Hierbei erfolgt eine Dosis-Wirkungs-Bewertung, wobei der Zusammenhang zwischen Dosis einerseits und Häufigkeit und Schwere von unerwünschten Wirkungen andererseits ermittelt wird. Darauf basierend erfolgt unter Berücksichtigung der wissenschaftlichen Unsicherheiten die Festlegung eines UL (s.u.) für verschiedene Lebensphasen und Bevölkerungsgruppen. 3. Ermittlung der Exposition: Bestimmung der täglichen Gesamtaufnahme
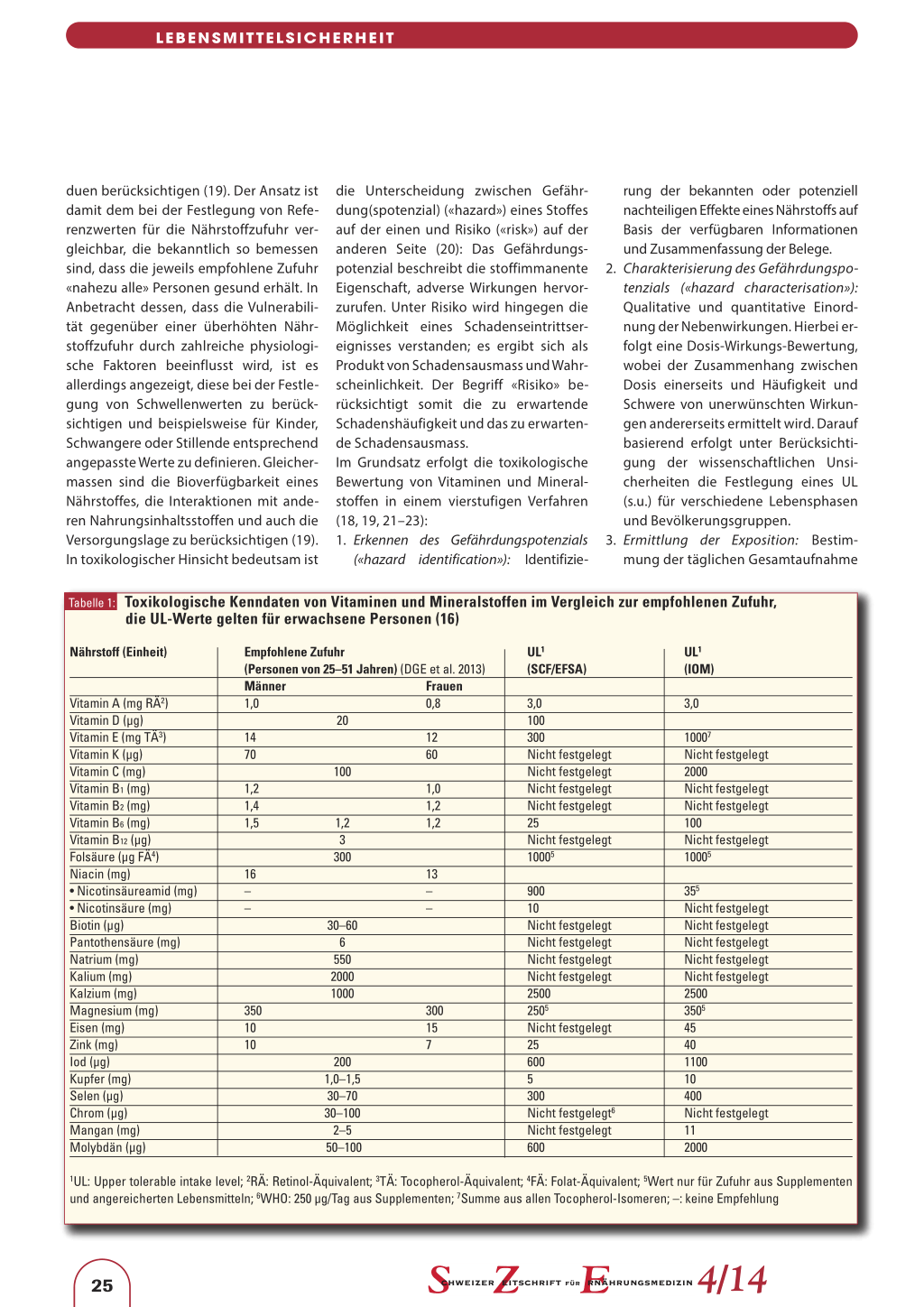
Tabelle 1: Toxikologische Kenndaten von Vitaminen und Mineralstoffen im Vergleich zur empfohlenen Zufuhr, die UL-Werte gelten für erwachsene Personen (16)
Nährstoff (Einheit)
Vitamin A (mg RÄ2) Vitamin D (µg) Vitamin E (mg TÄ3) Vitamin K (µg) Vitamin C (mg) Vitamin B1 (mg) Vitamin B2 (mg) Vitamin B6 (mg) Vitamin B12 (µg) Folsäure (µg FÄ4) Niacin (mg) • Nicotinsäureamid (mg) • Nicotinsäure (mg) Biotin (µg) Pantothensäure (mg) Natrium (mg) Kalium (mg) Kalzium (mg) Magnesium (mg) Eisen (mg) Zink (mg) Iod (µg) Kupfer (mg) Selen (µg) Chrom (µg) Mangan (mg) Molybdän (µg)
Empfohlene Zufuhr
(Personen von 25–51 Jahren) (DGE et al. 2013)
Männer
Frauen
1,0 0,8
20
14 12
70 60
100
1,2 1,0
1,4 1,2
1,5 1,2 1,2
3
300
16 13
––
––
30–60
6
550
2000
1000
350 300
10 15
10 7
200
1,0–1,5
30–70
30–100
2–5
50–100
UL1 (SCF/EFSA)
3,0 100 300 Nicht festgelegt Nicht festgelegt Nicht festgelegt Nicht festgelegt 25 Nicht festgelegt 10005
900 10 Nicht festgelegt Nicht festgelegt Nicht festgelegt Nicht festgelegt 2500 2505 Nicht festgelegt 25 600 5 300 Nicht festgelegt6 Nicht festgelegt 600
UL1 (IOM)
3,0
10007 Nicht festgelegt 2000 Nicht festgelegt Nicht festgelegt 100 Nicht festgelegt 10005
355 Nicht festgelegt Nicht festgelegt Nicht festgelegt Nicht festgelegt Nicht festgelegt 2500 3505 45 40 1100 10 400 Nicht festgelegt 11 2000
1UL: Upper tolerable intake level; 2RÄ: Retinol-Äquivalent; 3TÄ: Tocopherol-Äquivalent; 4FÄ: Folat-Äquivalent; 5Wert nur für Zufuhr aus Supplementen und angereicherten Lebensmitteln; 6WHO: 250 µg/Tag aus Supplementen; 7Summe aus allen Tocopherol-Isomeren; –: keine Empfehlung
25 4/14
LEBENSMITTELSICHERHEIT
an Nährstoffen in der Allgemeinbevölkerung. 4. Risikocharakterisierung («risk characterisation»): Ableitung einer Schlussfolgerung aus den Schritten 1 bis 3. Notwendig in diesem Zusammenhang ist zunächst die Definition dessen, was als «adverser Effekt» anzusehen ist. Nach einer Definition der Weltgesundheitsorganisation (WHO) bezieht dies alle Veränderungen in Morphologie, Physiologie, Wachstum, Entwicklung und Lebenserwartung mit ein, die zu Störungen der Funktion führen oder die Empfindlichkeit gegenüber nachteiligen Wirkungen anderer Umwelteinflüsse erhöhen. Dabei ist immer auch zu klären, ob ein Effekt als advers anzusehen ist oder nicht (24). Basierend auf dem dargestellten vierstufigen Verfahren haben SCF/EFSA und IOM die Toxizität von Vitaminen und Mineralstoffen systematisch bewertet und verschiedene toxikologische Kenngrössen abgeleitet (16): • Lowest observed adverse effect level (LOAEL): Niedrigste Nährstoffzufuhr, bei der erste unerwünschte Wirkungen zu beobachten sind. Für viele Vitamine konnte bisher kein LOAEL ermittelt werden. • No observed adverse effect level (NOAEL): Höchste untersuchte Dosis eines Nährstoffs, bei der noch keine unerwünschten gesundheitlichen Effekte zu beobachten sind. • Tolerable level of upper intake (UL): Höchste tägliche Nährstoffaufnahme aus allen Quellen, die bei dauerhafter Zufuhr keine gesundheitlich nachteiligen Effekte erwarten lässt. Entsprechend gilt: Liegt die Gesamtzufuhr eines Stoffs (aus Lebensmitteln des allgemeinen Verzehrs, angereicherten Produkten und Nährstoffpräparaten) im Bereich des UL, so kann die Aufnahme auch langfristig als gesundheitlich unbedenklich angesehen werden. Bei der Festlegung des UL werden die verfügbaren NOAEL- und LOAEL-Werte herangezogen und je nach Datengüte Unsicherheitsfaktoren berücksichtigt, sodass sich folgendes Konzept ergibt (25): UL = NOAEL (oder LOAEL)/Unsicherheitsfaktoren Es gilt also: UL < NOAEL < LOAEL. Welche Beziehungen sich zwischen der Zufuhr eines Nährstoffes und dem Risiko für Mangelerscheinungen beziehungsweise toxischen Wirkungen auf Populationsebene ergeben, zeigt Abbildung 3 (16). Langfristige Sicherheit von Vitaminen und Mineralstoffen Tabelle 1 gibt einen Überblick zu den ULWerten von Vitaminen und Mineralstoffen und stellt sie der empfohlenen Aufnahme gegenüber. Insgesamt betrachtet ist die Toxizität bei Vitaminen (mit Ausnahme von präformiertem Vitamin A und dem Niacinderivat Nikotinsäure) vergleichsweise gering, hingegen ist der Bereich zwischen erwünschter und uner- wünschter Wirkung bei einigen Mineralstoffen deutlich schmaler. Dies gilt vor allem für Zink und Eisen, aber auch für Kalzium. Bei der Betrachtung der Zahlen darf nicht übersehen werden, dass die aufgeführten UL-Werte unterschiedlichen Charakter besitzen. So gelten die für Magnesium etablierten Werte nur für die zusätzliche Zufuhr des Mineralstoffs über Supplemente; die normale Ernährung bleibt unberücksichtigt. Gleichermassen bezieht sich der UL für Folat nur auf synthetische Folsäure; in Lebensmitteln natürlicherweise vorkommende Folate gelten als unbedenklich. Der für Vitamin A etablierte UL bezieht sich lediglich auf präformiertes Vitamin A, nicht auf Provitamin-A-wirksame Karotinoide, eine Tatsa- Tabelle 2: Vitaminzufuhr in Deutschland (soweit Daten verfügbar) über die normale Ernährung (einschliesslich angereicherter Lebensmittel) in Relation zum UL Perzentile Vitamine Vitamin A (µg/Tag) Vitamin D [µg/Tag) Vitamin E (mg/Tag) Vitamin C (mg/Tag) Vitamin B1 (mg/Tag) Vitamin B2 (mg/Tag) Niacin (mg/Tag) Vitamin B6 (mg/Tag) Folat (µg/Tag) Vitamin B12 (µg/Tag) b-Carotin (mg/Tag) UL 30002,3 502 3002 20004 – – 9005/106 252 10002,7 – – Zufuhr über die normale Ernährung1 Männer Frauen 50 95 50 95 1800 4400 2,90 9,60 13,7 32,5 130 332 1,6 3,5 1,9 4,3 36,3 69,7 2,3 4,8 283 672 5,80 12,4 4,3 11,7 1500 3700 2,20 7,00 12,0 25,1 134 317 1,2 2,5 1,5 3,3 26,7 47,2 1,8 3,7 252 550 4,0 8,2 4,4 12,6 Mineralstoffe Kalzium (mg/Tag) Magnesium (mg/Tag) Eisen (mg/Tag) Jod (µg/Tag) Zink (mg/Tag) 25002 2502,8 459 6002 252 1052 2061 432 714 14,4 24,7 23310 41210 11,6 20,2 964 361 11,8 18510 9,1 1734 572 19,3 31010 15,1 1Daten für Deutschland; Nationale Verzehrsstudie II, einschliesslich angereicherter Lebensmittel (15) 2EFSA, SCF Tolerable Upper Intake Levels for vitamins and minerals (19) 3UL für präformiertes Vitamin A (Retinol and Retinylester) µg RE/Tag 4Food and Nutrition Board, Institute of Medicine (18, 23) 5UL for Nicotinamid 6UL for Nikotinsäure 7Wert für synthetische Folsäure 8Aufnahme nur aus Supplementen 9Food and Nutrition Board, Institute of Medicine 10unter Berücksichtigung von jodiertem Speisesalz 4/14 26 LEBENSMITTELSICHERHEIT che, die zu Fehlinterpretationen führen kann (s.u.). Toxikologische Risiken in der Praxis Wie die Übersicht in Tabelle 1 verdeutlicht, ist der Bereich zwischen empfohlener Aufnahme (D-A-CH-Referenzwert) und langfristig tolerierbarer Höchstmenge je nach Nährstoff sehr unterschiedlich ausgeprägt. In zahlreichen Fällen konnte mangels Daten zu einer toxischen Wirkung kein UL festgelegt werden, es finden sich allenfalls NOAEL-Werte. Entscheidend im Hinblick auf die Risikobewertung ist die Frage, inwieweit in der Praxis Nährstoffzufuhren zu beobachten sind, die den UL erreichen oder gar überschreiten. Beispielhaft seien hier die zuletzt in Deutschland erhobenen Daten der Nationalen Verzehrsstudie II herangezogen. Dabei ist nicht die mediane Zufuhr der Nährstoffe zu betrachten, sondern das Augenmerk auf die Personen mit der höchsten Nährstoffaufnahme zu richten, also die 95. Perzentile der errechneten Aufnahme. Wie die Analysen belegen, ist dabei – auch unter Berücksichtigung der Aufnahme angereicherter Lebensmittel mit der normalen Ernährung – keine Nährstoffzufuhr zu finden, die sich langfristig als Risiko erweist. Eine Ausnahme ergibt sich bei Vitamin A: Hier liegt die 95. Perzentile der Aufnahme deutlich oberhalb des UL von 3 mg/Tag (15). Bei der Interpretation dieser Befunde ist aber zu berücksichtigen, dass der UL sich ausschliesslich auf präformiertes Vitamin A bezieht, nicht auf Provitamin-A-wirksame Karotinoide. Diese werden bedarfsabhängig zu Vitamin A metabolisiert und besitzen selbst keine Vitamin-A-Toxizität. Zudem ist die Biokonversion der Provitamine insgesamt gering und unterliegt starken individuellen Schwankungen (26). Bei der Errechnung der Vitamin-AZufuhr auf Basis von Nährwerttabellen kommt es allerdings vielfach, so auch hier, zu einer Fehlinterpretation, weil der Provitamin-A-Gehalt in Nährwertdatenbanken aus Gründen der Vergleichbarkeit unmittelbar als Retinoläquivalent ausgewiesen wird. Mit anderen Worten: Die in Ernährungserhebungen errechnete Vitamin-A-Menge ergibt sich bei den übli- chen Auswerteverfahren als Summe aus vorgebildetem Vitamin A und ProvitaminA-aktiven Karotinoiden. Sie ist also nicht mit dem in toxikologischer Hinsicht relevanten Vitamin A selbst gleichzusetzen; die Aufnahme an Vitamin A selbst wird somit überschätzt. Dennoch stellt Vitamin A die Substanz dar, die unter Praxisbedingungen besondere Aufmerksamkeit erfordert: Durch den regelmässigen Verzehr von Leber ist ohne Weiteres eine den UL übersteigende Zufuhr des Vitamins erreichbar. Da eine erhöhte Zufuhr während der Schwangerschaft mit teratogenen Effekten verbunden ist, sollten Schwangere oder Frauen mit Kinderwunsch keine Leber konsumieren (27). Sicherheitsbewertung von Supplementen Während die allgemeine Ernährung somit in der Regel keine Risiken einer Überdosierung von Vitaminen und Mineralstoffen birgt, kann die Zufuhr von Nährstoffsupplementen eine potenzielle Gefährdung darstellen. Dies gilt in erster Linie dann, wenn a) hoch dosierte Präparate und/oder b) gleichzeitig mehrere Präparate mit denselben Inhaltsstoffen konsumiert werden. Aus diesem Grund wird innerhalb der Europäischen Union bereits seit geraumer Zeit diskutiert, gesetzlich Höchstmengen für Vitamine und Mineralstoffe in Nahrungsergänzungsmitteln festzulegen. Unterschiedliche nationale Vorstellungen im Hinblick auf das Risikomanagement haben dazu geführt, dass dies bis heute nicht erfolgt ist. So vertritt beispielsweise das deutsche Bundesinstitut für Risikobewertung (BfR) die Auffassung, bei der Festlegung von Höchstmengen müsse ein «Multiexpositionsfaktor» berücksichtigt werden, der der Tatsache Rechnung tragen soll, dass der Verbraucher bis zu vier Supplemente gleichzeitig verwende (28, 29). Aktuelle Daten zeigen, dass ein solches Multiexpositionsfaktor-Kriterium kaum zu rechtfertigen ist. So gaben in einer kürzlich publizierten Erhebung rund 89 Prozent aller Befragten an, nicht mehr als 1 oder 2 Produkte zu konsumieren. Zudem verwendeten 44 Prozent der Befragten das jewei- lige Supplement maximal ein Jahr und nur 6 Prozent mehr als 10 Jahre (30). Unabhängig von der politischen Frage, welches Mass an Sicherheit durch Höchstmengen erreicht werden soll, stellt sich die Ableitung sicherer Höchstmengen methodisch klar dar (16): Stark vereinfacht ist vom UL des jeweiligen Nährstoffs die Substanzmenge zu subtrahieren, die in der Bevölkerung über Lebensmittel des allgemeinen Verzehrs («normale» Lebensmittel wie Obst, Gemüse, Fleisch etc.) zugeführt wird. Aus Sicherheitsgründen wird auch hierbei nicht die durchschnittliche Aufnahme über die Nahrung zugrunde gelegt, sondern die 95. Perzentile der Zufuhr, also die bei den Personen mit der höchsten Aufnahme zu beobachtende Zufuhr. Die verbleibende Differenz zwischen UL und Zufuhr über normale Lebensmittel ist die Menge des Nährstoffs, die über angereicherte Lebensmittel und Supplemente insgesamt ohne Bedenken zusätzlich aufgenommen werden kann (31, 33). Zusammenfassung und Fazit Eine überhöhte Aufnahme an Vitaminen und Mineralstoffen ist ebenso wenig erwünscht wie eine unzureichende Zufuhr. Bei der toxikologischen Bewertung wird deutlich, dass Vitamine – mit Ausnahme von Vitamin A – in der Praxis eine vergleichsweise sichere Gruppe von Naturstoffen darstellen. Nur bei Mengen, die weit über den etablierten Zufuhrempfehlungen liegen, ist mit gesundheitlich unerwünschten Effekten zu rechnen. Im Gegensatz dazu weisen Mineralstoffe, und speziell Spurenelemente, ein kleines Toleranzfenster auf. Korrespondenzadresse: Prof. Dr. Andreas Hahn Leibniz Universität Hannover Institut für Lebensmittelwissenschaft und Humanernährung Am Kleinen Felde 30 D-30167 Hannover E-Mail: hahn@nutrition.uni-hannover.de Das Literaturverzeichnis befindet sich auf der folgenden Seite. 27 4/14 LEBENSMITTELSICHERHEIT Literatur: 1. Ströhle A, Behrendt I, Hadji P, Hahn A. Nährstoffsupplemente in der Gynäkologie. Eine Standortbestimmung. Frauenarzt 2014; 55: 38–46. 2. Ströhle A, Hahn A. Nährstoffsupplemente – Möglichkeiten und Grenzen. Teil 4: Supplemente in der Primärprävention – Konzeptionelle Aspekte. Med Monatsschr Pharm 2013; 36: 422–426. 3. Gey F. Vitamin E plus C and interacting conutrients required for optimal health. Biofactors 1998; 7: 113–174. 4. Ströhle A, Hahn A. [Vitamin C and immune function]. Med Monatsschr Pharm 2009; 32: 49–54. 5. Hankinson SE, Stampfer MJ, Seddon JM, Colditz GA et al. Nutrient intake and cataract extraction in women: a prospective study. BMJ 1992; 305: 335–339. 6. Yoshida M, Takashima Y, Inoue M, Iwasaki M et al. Prospective study showing that dietary vitamin C reduced the risk of age-related cataracts in a middleaged Japanese population. Eur J Nutr 2007; 46: 118–124. 7. Knekt P, Ritz J, Pereira MA, O’Reilly EJ et al. Antioxidant vitamins and coronary heart disease risk: a pooled analysis of 9 cohorts. Am J Clin Nutr 2004; 80: 1508–1520. 8. Ströhle A, Zänker K, Hahn A. Nutrition in oncology: the case of micronutrients (review). Oncol Rep. 2010; 24: 815–828. 9. Bailey RL, Gahche JJ, Lentino CV, Dwyer JT, Engel JS, Thomas PR, Betz JM, Sempos CT, Picciano MF. Dietary supplement use in the United States, 2003– 2006. J Nutr. 2011; 141: 261–266. 10. Balluz LS, Okoro CA, Bowman BA, Serdula MK, Mokdad AH. Vitamin or supplement use among adults, behavioral risk factor surveillance system, 13 states, 2001. Public Health Rep. 2005; 120: 117–231. 11. Beitz R, Mensink GB, Rams S, Döring A. [Use of vitamin and mineral supplements in Germany]. Bundesgesundheitsblatt Gesundheitsforschung Gesundheitsschutz. 2004; 47: 1057–1065. 12. Radimer K, Bindewald B, Hughes J, Ervin B, Swanson C, Picciano MF. Dietary supplement use by US adults: data from the National Health and Nutrition Examination Survey, 1999–2000. Am J Epidemiol. 2004; 160: 339–349. 13. Wolters M, Hahn A. Nährstoffsupplemente aus Sicht des Konsumenten. Ernährungs-Umschau 2001; 48: 136–141. 14. Hahn A. Nahrungsergänzungsmittel und ergänzende bilanzierte Diäten. (2. Aufl.) Stuttgart: Wissenschaftliche Verlagsgesellschaft 2006. 15. Max Rubner-Institut (Hrsg.): Nationale Verzehrs Studie II Ergebnisbericht, Teil 2 (2008), Bundesforschungsinstitut für Ernährung und Lebensmittel; www.was-esse-ich.de/uploads/media/NVSII_Abschlussbericht_Teil_2.pdf am 09.09.2014 16. Ströhle A, Hahn A. Nährstoffsupplemente – Möglichkeiten und Grenzen. Teil 6: Sicherheit und mögliche Risiken, Med Monatsschr Pharm. 2014; 37: 249– 256. 17. Deutsche Gesellschaft für Ernährung e.V. (DGE), Österreichische Gesellschaft für Ernährung (ÖGE), Schweizerische Gesellschaft für Ernährungsforschung (SGE), Schweizerische Vereinigung für Ernährung (SVE): Referenzwerte für die Nährstoffzufuhr. (1. Auflage, 5., korrigierter Nachdruck, Umschau, Braus 2013. 18. FNB (Food and Nutrition Board, Institute of Medicine, National Academy of Sciences). Dietary Reference Intakes: Calcium, Phosphorus, Magnesium, Vitamin D, and Fluoride. National Academy Press, Washington DC 1997. 19. EFSA; Scientific Committee on Food Scientific Panel on Dietetic Products, Nutrition and Allergies. Tolerable upper intake levels for vitamins and minerals, 2006. Online verfügbar unter www.efsa.europa.eu/de/ndatopics/docs/ndatolerableuil.pdf 20. Ulbig, R. F. Hertel, G.F. Böl (Hrsg.): Evaluierung der Kommunikation über die Unterschiede zwischen «risk» und «hazard», Abschlussbericht, Bundesinstitut für Risikobewertung 2009. http://www.bfr.bund.de/cm/350/evaluierung_der_kommunikation_ueber_die_unterschiede_zwischen_risk_ und_hazard.pdf am 09.09.2014) 21. FAO/WHO (Food and Agricultural Organisation of the UN/World Health Organisation) Expert Consultation. Application of risk analysis to food standards issues. Recommendations to the Codex Alimentarius Commission (ALINORM 95/9, Appendix 5) 1995. 22. FNB (Food and Nutrition Board, Institute of Medicine, National Academy of Sciences). Dietary Reference Intakes for Thiamin, Riboflavin, Niacin, Vitamin B6, Folate, Vitamin B12, Pantothenic Acid, Biotin, and Choline. National Academy Press, Washington DC 1998. 23. FNB (Food and Nutrition Board, Institute of Medicine, National Academy of Sciences). Dietary Reference Intakes for Vitamin C, Vitamin E, Carotenoids and Selenium. National Academy Press, Washington DC 2000. 24. WHO. Assessing human health risks of chemicals: derivation of guidance values for health-based exposure limits. Environmental Health Criteria, 170. Geneva 1994. 25. Mason P. One is okay, more is better? Pharmacological aspects and safe limits of nutritional supplements. Proc Nutr Soc. 2007 Nov; 66 (4): 493–507. 26. Tang G. Bioconversion of dietary provitamin A carotenoids to vitamin A in humans. Am J Clin Nutr. 2010; 91: 1468S–1473S. 27. Ströhle A, Wolters M, Hahn A. Nährstoffsupplemente – Möglichkeiten und Grenzen. Teil 2: Ausgewählte Risikogruppen – Supplemente in der Schwangerschaft, Med Monatsschr Pharm 2013; 36: 252–266. 28. Domke A, Grossklaus R, Niemann B, Przyrembel H, Richter K, Schmidt E, Weissenborn A, Wörner B, Ziegenhagen R. Verwendung von Vitaminen in Lebensmitteln. Bundesinstitut für Risikobewertung: Berlin, 2004. 29. Domke A, Grossklaus R, Niemann B, Przyrembel H, Richter K, Schmidt E, Weissenborn A, Wörner B, Ziegenhagen R: Verwendung von Mineralstoffen in Lebensmitteln. Bundesinstitut für Risikobewertung: Berlin, 2004. 30. Heinemann M, Willers J, Bitterlich N, Hahn A. Verwendung von Nahrungsergänzungsmitteln mit Vitaminen und Mineralstoffen – Ergebnisse einer deutschlandweiten Verbraucherbefragung, J. Verbr. Lebensm 2014, DOI 10.1007/s00003–014-0912-x 31. Flynn A, Moreiras O, Stehle P, Fletcher RJ, Müller DJ, Rolland V. Vitamins and minerals: a model for safe addition to foods. Eur J Nutr. 2003 Apr; 42 (2): 118–130. 32. Kloosterman J, Fransen HP, de Stoppelaar J, Verhagen H, Rompelberg C. Safe addition of vitamins and minerals to foods: setting maximum levels for fortification in the Netherlands. Eur J Nutr. 2007; 46: 220–229. 33. Rasmussen SE, Andersen NL, Dragsted LO, Larsen JC. A safe strategy for addition of vitamins and minerals to foods. Eur J Nutr. 2006; 45: 123–135. 4/14 28