Transkript
TNF-α-Hemmer gegen Arthrose?
Knorpeldegeneration führt sekundär zur Entzündung
EULAR
Arthrosen können sich zu sehr schmerzhaften Entzündungen entwickeln. In einer Reihe von niederländisch-belgischen Studien konnte gezeigt werden, dass TNF-α bei Arthrose am Entzündungsgeschehen beteiligt ist; daher könnte möglicherweise durch eine TNF-α-Hemmung die weitere Krankheitsprogression abgebremst werden.
Eine Arthrose ist zu Beginn eine nicht entzündliche Erkrankung. Allerdings kann sich das im Laufe einer aktivierten Arthrose schnell ändern: Durch die Knorpelzersetzung und den Knochenabrieb entzündet sich in der Gelenkhöhle die Gelenkinnenhaut, mit schmerzhaften Folgen. Diese Entzündungen und daraus abgeleitete Therapieansätze waren Gegenstand mehrerer am EULARKongress in London vorgestellter Untersuchungen.
TNF-α auch in Arthrosegelenken
So wollten die Forscher wissen, ob der Entzündungsfaktor TNF-α in geschwollenen Fingergelenken bei Arthrose nachzuweisen ist. Dazu wurden Patienten mit Fingergelenksarthrose radioaktiv markiertes Certolizumab pegol injiziert und dessen Verbleib mithilfe immunszintigrafischer Methoden detektiert. Ergebnis: Geschwollene Gelenke bei Fingergelenksarthrose sind deutlich mit der Aufnahme von markiertem Certolizumab pegol korreliert. «Das bedeutet, dass in diesen Gelenken viel TNF-α vorhanden war, was wiederum die Überlegungen für eine zytokinbasierte Therapie bei erosiver Arthrose unterstützt», so die Studienautorin Dr. Ruth Wittoek von der Universität Gent (B).
Schmerzreduktion bei geschwollenen Gelenken
Eine solche Therapie wollte man in zwei weiteren multizentrischen Studien testen, denn «obwohl die Arthrose eine erosive Erkrankung mit einem hohen Leidensdruck ist, sind bislang keine krankheitsmodifizierenden Therapien erhältlich», sagte Dr. Feline Kroon aus Leiden (NL). Für die erste Untersuchung wurden 90 Patienten (Durchschnittsalter 60 Jahre, 81% Frauen) mit aktiver entzündlicher Handarthrose randomisiert. Die Teilnehmer befanden sich in einem vorerosiven oder erosiven Stadium (ACR-Handarthrosekriterien) und mussten mit einer weiteren zukünftigen Verschlechterung ihrer Erkrankung rechnen. Während eine Hälfte mit dem TNF-α-Inhibitor Etanercept subkutan behandelt wurde (24 Wochen 50 mg/ Woche und die folgenden 24 Wochen 25 mg/Woche), erhielt die andere Hälfte der Teilnehmer Plazebo. Neben der Schmerzentwicklung wurden mit dem quantitativen Ghent University Scoring System (GUSS) auch strukturelle Veränderungen (Gelenkspalt, subchondrale Knochenarchitektur u.a.) registriert. Nach 24 Wochen konnte im VAS-Schmerz-Score in der Eta-
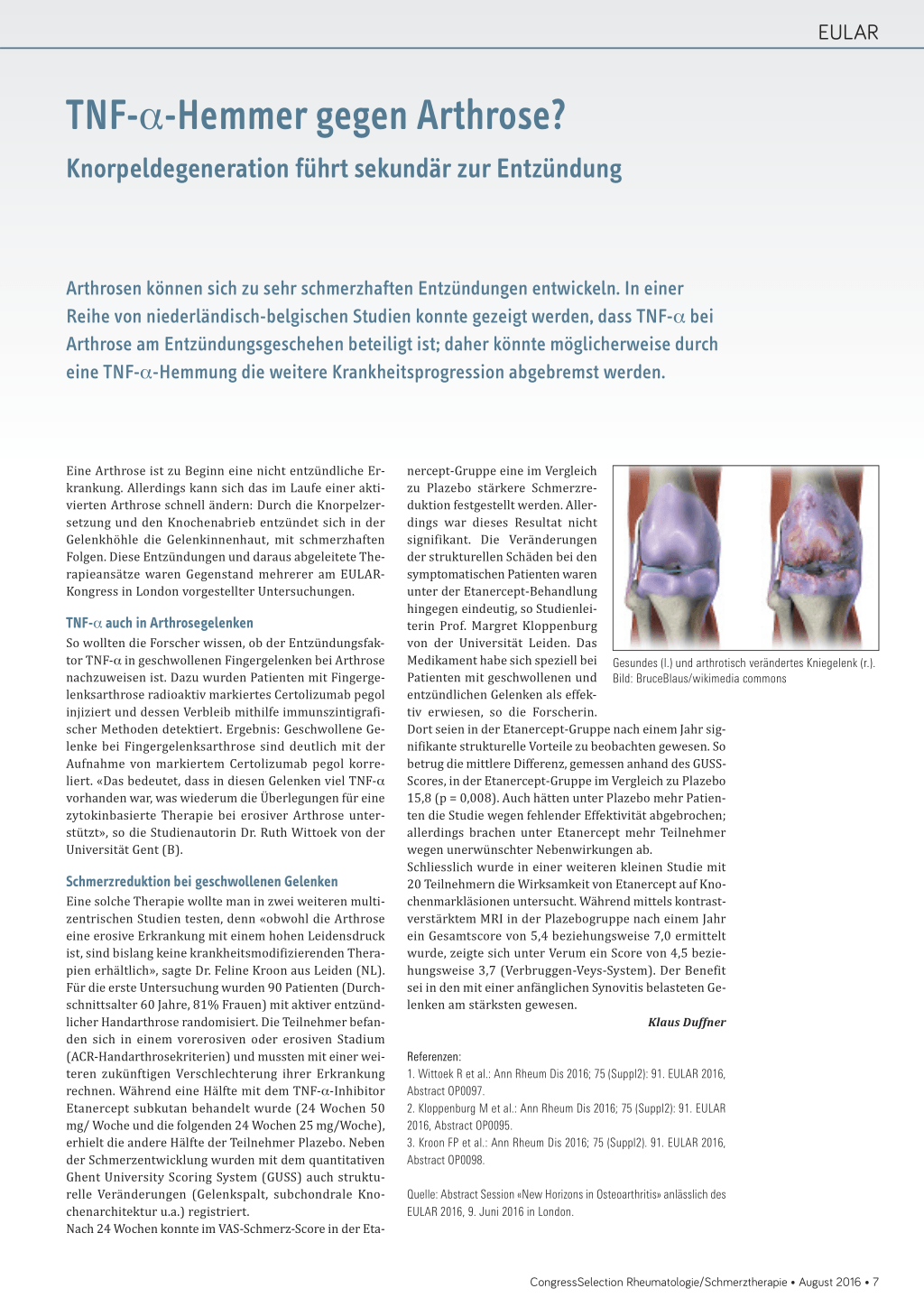
nercept-Gruppe eine im Vergleich zu Plazebo stärkere Schmerzreduktion festgestellt werden. Allerdings war dieses Resultat nicht signifikant. Die Veränderungen der strukturellen Schäden bei den symptomatischen Patienten waren unter der Etanercept-Behandlung hingegen eindeutig, so Studienleiterin Prof. Margret Kloppenburg von der Universität Leiden. Das Medikament habe sich speziell bei Gesundes (l.) und arthrotisch verändertes Kniegelenk (r.). Patienten mit geschwollenen und Bild: BruceBlaus/wikimedia commons entzündlichen Gelenken als effektiv erwiesen, so die Forscherin. Dort seien in der Etanercept-Gruppe nach einem Jahr signifikante strukturelle Vorteile zu beobachten gewesen. So betrug die mittlere Differenz, gemessen anhand des GUSSScores, in der Etanercept-Gruppe im Vergleich zu Plazebo 15,8 (p = 0,008). Auch hätten unter Plazebo mehr Patienten die Studie wegen fehlender Effektivität abgebrochen; allerdings brachen unter Etanercept mehr Teilnehmer wegen unerwünschter Nebenwirkungen ab. Schliesslich wurde in einer weiteren kleinen Studie mit 20 Teilnehmern die Wirksamkeit von Etanercept auf Knochenmarkläsionen untersucht. Während mittels kontrastverstärktem MRI in der Plazebogruppe nach einem Jahr ein Gesamtscore von 5,4 beziehungsweise 7,0 ermittelt wurde, zeigte sich unter Verum ein Score von 4,5 beziehungsweise 3,7 (Verbruggen-Veys-System). Der Benefit sei in den mit einer anfänglichen Synovitis belasteten Gelenken am stärksten gewesen.
Klaus Duffner
Referenzen: 1. Wittoek R et al.: Ann Rheum Dis 2016; 75 (Suppl2): 91. EULAR 2016, Abstract OP0097. 2. Kloppenburg M et al.: Ann Rheum Dis 2016; 75 (Suppl2): 91. EULAR 2016, Abstract OP0095. 3. Kroon FP et al.: Ann Rheum Dis 2016; 75 (Suppl2). 91. EULAR 2016, Abstract OP0098.
Quelle: Abstract Session «New Horizons in Osteoarthritis» anlässlich des EULAR 2016, 9. Juni 2016 in London.
CongressSelection Rheumatologie/Schmerztherapie • August 2016 • 7