Transkript
Im Fokus: Prostatakarzinom und Nierenzellkarzinom
Therapieoptionen beim fortgeschrittenen Nierenzellkarzinom
Update 2010
In den letzten fünf Jahren wurden in der Schweiz sechs neuartige, wirksame Medikamente für das fortgeschrittene Nierenzellkarzinom zugelassen. Für die bis anhin als wenig beeinflussbar geltende Erkrankung konnte damit ein deutlicher Behandlungsfortschritt erzielt werden. Dennoch bleiben viele Fragen zur optimalen Therapie, insbesondere zur besten Sequenz und zu allfälligen Kombinationsmöglichkeiten.
RICHARD CATHOMAS
Richard Cathomas
Das Nierenzellkarzinom (renal cell cancer: RCC) ist eine relativ seltene maligne Erkrankung. In der Schweiz erhalten jährlich knapp 900 Patienten diese Diagnose, etwa 500 Personen sterben daran. Der Anteil des Nierenzellkarzinoms an allen Krebsleiden beträgt 3%. Nierenzellkarzinome kommen gehäuft im Alter zwischen 60 und 80 Jahren vor; Männer erkranken dabei zweimal häufiger. Genetische Faktoren spielen bei der Entwicklung des Nierenzellkarzinoms eine grosse Rolle. Diese können hereditär oder spontan auftreten. Das von-HippelLindau-Syndrom ist die häufigste hereditäre Erkrankung, welche mit einem Nierenzellkarzinom assoziiert ist. Abgesehen von genetischen Faktoren stellen Übergewicht, Zigarettenrauchen, arterielle Hypertonie, Radiotherapie sowie Nierentransplantation und Dialyse Risikofaktoren für die Entstehung eines RCC dar. Bei der Präsentation finden sich gehäuft Hämaturie, eine abdominale Masse sowie unspezifische Symptome wie Schmerzen, Gewichtsverlust und Anämie. Die Frühentdeckung der Erkrankung hat in den letzten Jahren dank der Verbreitung von Ultraschall- und CT-Untersuchungen zugenommen. Fernmetastasen treten vor allem in der Lunge, in retroperitonealen und mediastinalen Lymphknoten, Knochen, Leber, Nebennieren und oft auch im ZNS auf. Die Metastasen sind aufgrund der Pathogenese stark vaskularisiert; bei Biopsien oder Operationen besteht dadurch eine erhöhte Blutungsgefahr.
Histologie, Pathogenese und die neuen Medikamente
Histologisch werden verschiedene RCC-Subtypen unterschieden, die vier häufigsten sind: ▲ das hellzellige (75%) ▲ das papillläre (Typ 1 und Typ 2, total ca. 15%) ▲ das chromophobe (5%) ▲ das onkozytäre (5%) Nierenzellkarzinom. Das von-Hippel-Lindau-Gen (VHL-Gen) spielt eine sehr wichtige Rolle bei der Entstehung des hellzelligen RCC. Es hat sich gezeigt, dass bei etwa 70% aller hellzelligen Nierenzellkarzinome eine Inaktivation des VHL-Gens durch Mutation oder Hypermethylierung vorliegt. Dies führt zu einem deutlichen Anstieg von Wachstumsfaktoren wie VEGF (vascular endothelial growth factor) und PDGF (platelet derived growth factor), welche für die Angiogenese und Proliferation verantwortlich sind (1). Diese Pathogenese erklärt die Wirksamkeit der Multitarget-Tyrosinkinasehemmer (TKI) Sunitinib, Pazopanib und Sorafenib beim hellzelligen Nierenzellkarzinom. Dabei sind das Ausmass sowie die Bandbreite der Hemmung der verschiedenen Tyrosinkinasen unterschiedlich, was zu Differenzen in der Wirksamkeit, aber auch in der Verträglichkeit führen kann. Selektiver hemmt Bevacizumab die Angiogenese; um eine gute Wirksamkeit zu erzielen, braucht es jedoch die Kombination mit Interferon-alpha. Über eine verwandte und doch etwas andere Signalkaskade wirken die mTOR-Inhibitoren (mammalian target of rapamycin) Temsirolimus und Everolimus: Einerseits wird durch die Blockade von mTOR eine
SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 4/2010
19
Im Fokus: Prostatakarzinom und Nierenzellkarzinom
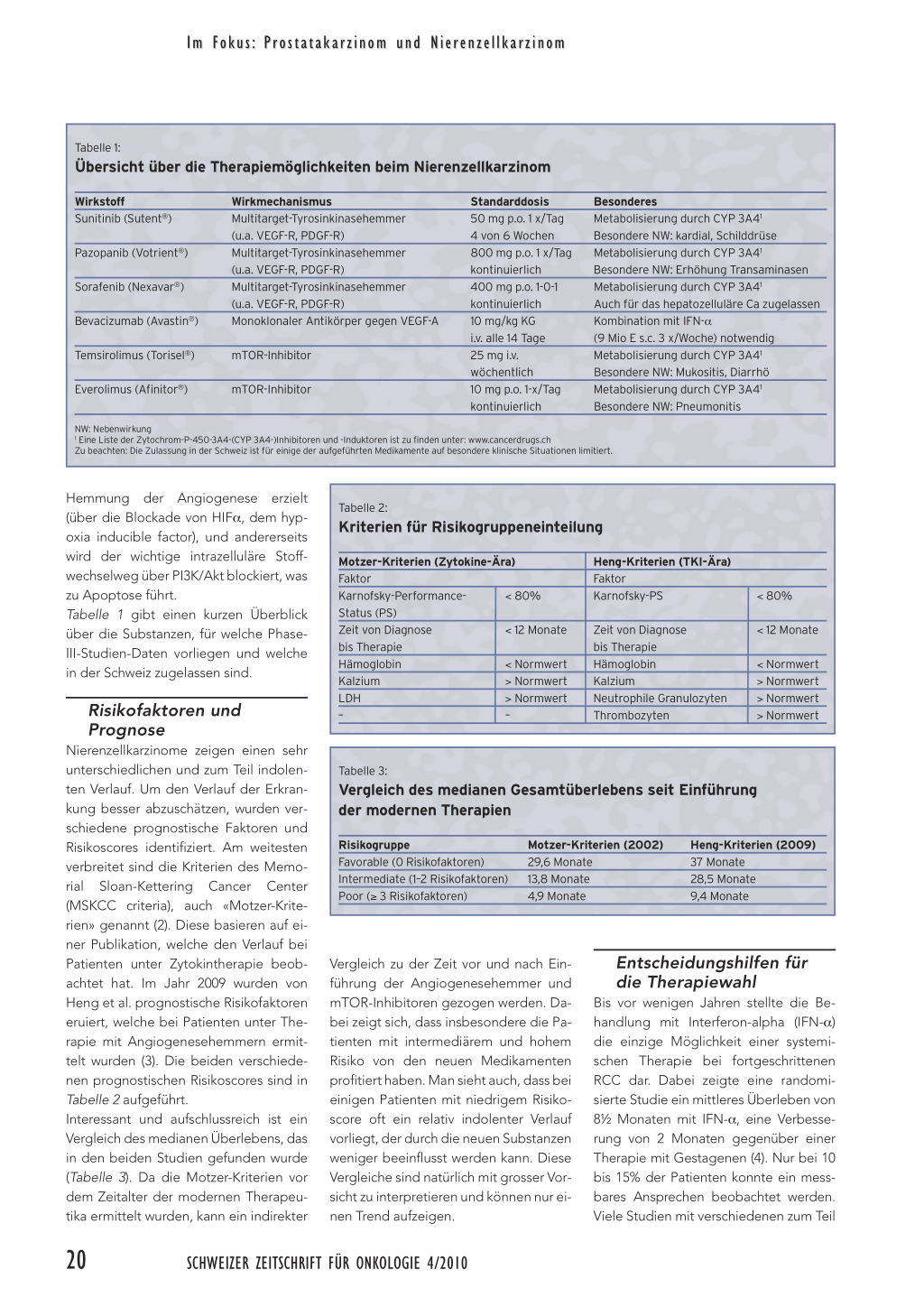
Tabelle 1:
Übersicht über die Therapiemöglichkeiten beim Nierenzellkarzinom
Wirkstoff Sunitinib (Sutent®) Pazopanib (Votrient®) Sorafenib (Nexavar®) Bevacizumab (Avastin®) Temsirolimus (Torisel®) Everolimus (Afinitor®)
Wirkmechanismus Multitarget-Tyrosinkinasehemmer (u.a. VEGF-R, PDGF-R) Multitarget-Tyrosinkinasehemmer (u.a. VEGF-R, PDGF-R) Multitarget-Tyrosinkinasehemmer (u.a. VEGF-R, PDGF-R) Monoklonaler Antikörper gegen VEGF-A
mTOR-Inhibitor
mTOR-Inhibitor
Standarddosis 50 mg p.o. 1 x/Tag 4 von 6 Wochen 800 mg p.o. 1 x/Tag kontinuierlich 400 mg p.o. 1-0-1 kontinuierlich 10 mg/kg KG i.v. alle 14 Tage 25 mg i.v. wöchentlich 10 mg p.o. 1-x/Tag kontinuierlich
Besonderes Metabolisierung durch CYP 3A41 Besondere NW: kardial, Schilddrüse Metabolisierung durch CYP 3A41 Besondere NW: Erhöhung Transaminasen Metabolisierung durch CYP 3A41 Auch für das hepatozelluläre Ca zugelassen Kombination mit IFN-α (9 Mio E s.c. 3 x/Woche) notwendig Metabolisierung durch CYP 3A41 Besondere NW: Mukositis, Diarrhö Metabolisierung durch CYP 3A41 Besondere NW: Pneumonitis
NW: Nebenwirkung 1 Eine Liste der Zytochrom-P-450-3A4-(CYP 3A4-)Inhibitoren und -Induktoren ist zu finden unter: www.cancerdrugs.ch Zu beachten: Die Zulassung in der Schweiz ist für einige der aufgeführten Medikamente auf besondere klinische Situationen limitiert.
Hemmung der Angiogenese erzielt (über die Blockade von HIFα, dem hypoxia inducible factor), und andererseits wird der wichtige intrazelluläre Stoffwechselweg über PI3K/Akt blockiert, was zu Apoptose führt. Tabelle 1 gibt einen kurzen Überblick über die Substanzen, für welche PhaseIII-Studien-Daten vorliegen und welche in der Schweiz zugelassen sind.
Risikofaktoren und Prognose
Nierenzellkarzinome zeigen einen sehr unterschiedlichen und zum Teil indolenten Verlauf. Um den Verlauf der Erkrankung besser abzuschätzen, wurden verschiedene prognostische Faktoren und Risikoscores identifiziert. Am weitesten verbreitet sind die Kriterien des Memorial Sloan-Kettering Cancer Center (MSKCC criteria), auch «Motzer-Kriterien» genannt (2). Diese basieren auf einer Publikation, welche den Verlauf bei Patienten unter Zytokintherapie beobachtet hat. Im Jahr 2009 wurden von Heng et al. prognostische Risikofaktoren eruiert, welche bei Patienten unter Therapie mit Angiogenesehemmern ermittelt wurden (3). Die beiden verschiedenen prognostischen Risikoscores sind in Tabelle 2 aufgeführt. Interessant und aufschlussreich ist ein Vergleich des medianen Überlebens, das in den beiden Studien gefunden wurde (Tabelle 3). Da die Motzer-Kriterien vor dem Zeitalter der modernen Therapeutika ermittelt wurden, kann ein indirekter
Tabelle 2:
Kriterien für Risikogruppeneinteilung
Motzer-Kriterien (Zytokine-Ära)
Faktor
Karnofsky-Performance-
< 80% Status (PS) Zeit von Diagnose < 12 Monate bis Therapie Hämoglobin < Normwert Kalzium > Normwert
LDH > Normwert
––
Heng-Kriterien (TKI-Ära) Faktor Karnofsky-PS
Zeit von Diagnose bis Therapie Hämoglobin Kalzium Neutrophile Granulozyten Thrombozyten
< 80% < 12 Monate < Normwert > Normwert > Normwert > Normwert
Tabelle 3:
Vergleich des medianen Gesamtüberlebens seit Einführung der modernen Therapien
Risikogruppe Favorable (0 Risikofaktoren) Intermediate (1–2 Risikofaktoren) Poor (≥ 3 Risikofaktoren)
Motzer-Kriterien (2002) 29,6 Monate 13,8 Monate 4,9 Monate
Heng-Kriterien (2009) 37 Monate 28,5 Monate 9,4 Monate
Vergleich zu der Zeit vor und nach Einführung der Angiogenesehemmer und mTOR-Inhibitoren gezogen werden. Dabei zeigt sich, dass insbesondere die Patienten mit intermediärem und hohem Risiko von den neuen Medikamenten profitiert haben. Man sieht auch, dass bei einigen Patienten mit niedrigem Risikoscore oft ein relativ indolenter Verlauf vorliegt, der durch die neuen Substanzen weniger beeinflusst werden kann. Diese Vergleiche sind natürlich mit grosser Vorsicht zu interpretieren und können nur einen Trend aufzeigen.
Entscheidungshilfen für die Therapiewahl
Bis vor wenigen Jahren stellte die Behandlung mit Interferon-alpha (IFN-α) die einzige Möglichkeit einer systemischen Therapie bei fortgeschrittenen RCC dar. Dabei zeigte eine randomisierte Studie ein mittleres Überleben von 8½ Monaten mit IFN-α, eine Verbesserung von 2 Monaten gegenüber einer Therapie mit Gestagenen (4). Nur bei 10 bis 15% der Patienten konnte ein messbares Ansprechen beobachtet werden. Viele Studien mit verschiedenen zum Teil
20 SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 4/2010
Im Fokus: Prostatakarzinom und Nierenzellkarzinom
aggressiven Chemotherapiekombinationen fielen negativ aus, einzig der Einsatz von hoch dosiertem Interleukin-2 (IL-2) konnte in wenigen Fällen (5%) eine komplette und lang anhaltende Remission erzielen (5). Das IL-2 hat sich aber wegen der sehr hohen Toxizität nicht an vielen Orten durchsetzen können. Zudem besteht grosse Unklarheit darüber, welche Patienten vom hoch dosierten IL-2 profitieren könnten, und auch eine dieses Jahr vorgestellte Studie konnte darüber noch keinen Aufschluss geben (6). Heute liegen breit abgestützte Daten zu mehreren neuen wirksamen Substanzen in der Erstlinientherapie vor. Die Fülle an neuen Daten und Medikamenten hat neben der deutlichen Verbesserung der Behandlungsmöglichkeiten aber auch zu Unsicherheiten darüber geführt, welche Therapie in welcher Situation zu bevorzugen sei. Allgemeine Richtlinien werden jährlich von verschiedenen Fachgesellschaften publiziert. Tabelle 4 gibt einen Überblick über die Behandlung, wie sie für das hellzellige Nierenzellkarzinom von der Europäischen Onkologiegesellschaft ESMO vorgeschlagen wird (7). Andere Gesellschaften haben sehr ähnliche Richtlinien. Vor dem Entscheid über eine systemische Therapie des fortgeschrittenen RCC sollten folgende Fragen beantwortet werden: ▲ Um welchen histologischen Subtyp
des Nierenzellkarzinoms handelt es sich? ▲ Wie ist die Risikogruppe einzuteilen? ▲ Besteht eine behandlungsbedürftige Situation? Grundsätzlich soll zwischen hellzelligen und nicht hellzelligen RCC unterschieden werden. Die Gruppeneinteilung erfolgt gemäss Motzer-Kriterien, es wird zwischen «good/intermediate»- sowie «poor risk»-Gruppen unterschieden. Beim fortgeschrittenen RCC besteht meist eine Behandlungsindikation; es gibt aber Fälle von asymptomatischen Patienten mit wenig Tumorlast (z.B. wenige kleine Lungenmetastasen) in der «good risk»-Gruppe, bei denen die Erkrankung einen sehr langsamen Verlauf zeigen kann. Es lohnt sich in diesen ausgewählten Fällen, mit dem Patienten eine «watch and wait»-Periode vor Beginn einer systemischen Therapie zu besprechen.
Tabelle 4:
Behandlungsalgorithmus für das hellzellige Nierenzellkarzinom 2010 (7)
Prädisponierende Faktoren
1. Wahl
Good/Intermediate Risk Group High Risk Group
1. Therapielinie Suntinib oder Pazopanib oder Bevacizumab + IFN-α Temsirolimus
Vorher Zytokine Vorher TKI Vorher Bevacizumab
2. Therapielinie Sorafenib oder Pazopanib Everolimus Sunitinib
Option
Hochdosis-Interleukin-2 Sunitinib
Sunitinib Andere Multitarget-TKI Andere Multitarget-TKI
Nicht hellzelliges Nierenzellkarzinom
Zur Behandlung von Patienten mit nicht hellzelligem Nierenzellkarzinom wurden nur wenige kleine Studien durchgeführt. Einerseits sind diese Patienten selten, andererseits wurden nicht hellzellige Histologien weitgehend aus den grossen Phase-III-Studien ausgeschlossen, sodass auch keine nützlichen Daten von Subgruppen aus diesen Untersuchungen vorliegen. Aufgrund des geschilderten Pathomechanismus ist die Blockade der Angiogenese beim nicht kleinzelligen RCC weniger sinnvoll, und die vorliegenden Resultate zeigen, dass mit Sunitinib oder Sorfenib auch nur in einer Minderheit der Fälle ein Ansprechen erzielt werden kann (8, 9). Es gibt aber Hinweise darauf, dass die Tumorprogression durch den Einsatz von TKI verlangsamt werden kann (8, 9). Etwas besser ist die Datenlage für den mTOR-Inhibitor Temsirolimus (10), und somit gilt heute bei Vorliegen eines nicht hellzelligen RCC Temsirolimus als Therapie der ersten Wahl.
Hellzelliges RCC mit «good/intermediate risk»
Erstlinientherapie Diese Gruppe stellt den Hauptanteil aller Patienten mit fortgeschrittenem RCC. In die randomisierten Phase-III-Studien mit Sunitinib, Pazopanib und Bevacizumab/ IFN-α (Bev/IFN) wurden fast ausschliesslich Patienten mit hellzelligem Nierenzellkarzinom aus der «good/intermediate risk»-Gruppe eingeschlossen. In den Studien mit Sunitinib (11) und Bev/IFN (12,
13) wurden die neuen Therapien mit IFN-α verglichen, die Studie mit Pazopanib (14) der Plazebogabe gegenübergestellt. Bei dieser letztgenannten Studie war knapp die Hälfte der Patienten mit Interferon vorbehandelt (202/435); die Studie muss somit etwas differenzierter beurteilt werden. Alle drei Substanzen haben einen ähnlichen Vorteil für das progressionsfreie Überleben (ca. 10 vs. 5 Monate) sowie für das Ansprechen (ca. 30 vs. 10%) gezeigt. In keiner der drei Studien konnte letzten Endes ein signifikanter Überlebensvorteil gefunden werden. Für die fehlende Signifikanz ist der grosse Anteil der Patienten mit Cross-over in den aktiven Studienarm verantwortlich. Die Wirksamkeit der drei Therapieoptionen scheint also ähnlich zu sein, wobei das Ansprechen unter Sunitinib am besten erscheint (47%-ige Ansprechrate). Einen Hinweis auf ähnliche Wirksamkeit liefert die am ASCO-Jahreskongress 2010 vorgestellte TORAVA-Studie: In dieser Phase-II-Studie mit 171 Patienten wurde Bevacizumab plus Temsirolimus versus Sunitinib versus Bev/IFN verglichen. Dabei scheint Bev/IFN einem TKI in der Wirksamkeit nicht unterlegen zu sein (15). Beim Entscheid über die Erstlinientherapie müssen also neben der Wirksamkeit zusätzliche Kriterien mit einbezogen werden: Das Nebenwirkungsspektrum sowie patientenbezogene Faktoren stehen hier im Vordergrund. Die Nebenwirkungen von Sunitinib sind gut bekannt und wurden an dieser Stelle schon ausführlich besprochen (vgl. SZO 3/2009, S. 24–27). Im Vordergrund stehen Fatigue, gastrointestinale Symptome
SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 4/2010
21
Im Fokus: Prostatakarzinom und Nierenzellkarzinom
(Dysgeusie, Diarrhö), kardiale Beschwerden (arterielle Hypertonie, Kardiotoxizität) sowie Hauttoxizität (insbesondere Hand-Fuss-Syndrom) und Schilddrüsendysfunktion. Durch entsprechende Information des Patienten sowie proaktives Management können viele der Nebenwirkungen gut kontrolliert werden. Ein Vergleich der Phase-III-Studien-Daten zeigt, dass Pazopanib möglicherweise etwas besser toleriert wird, insbesondere die Raten für Fatigue, Mukositis sowie Hand-Fuss-Syndrom sind verringert. Demgegenüber kommt es unter Pazopanib in bis zu 10% zu einem deutlichen Anstieg der Lebertransaminasen (Grad 3/4). Gemäss Studienlage ist die Rate an schwerer Asthenie und Müdigkeit unter der Therapie mit Bev/IFN am höchsten, zudem besteht unter dieser Therapie ein erhöhtes Risiko für thromboembolische Ereignisse. Das Interferon erhöht die Toxizität deutlich (grippeartige Symptome, Depression, Appetitlosigkeit) und muss daher oft dosisreduziert werden. Demgegenüber kommt es unter Bev/IFN nicht zu Hauttoxizität oder Mukositis/Dysgeusie. In die individuelle Beratung des Patienten können folgende Punkte einfliessen, welche allenfalls zur Entscheidungsfindung beitragen können: Patientenfaktoren, die für den Einsatz eines TKI (Sunitinib/Pazopanib) sprechen: ▲ Divertikulitis oder entzündliche Darm-
erkrankungen in der Anamnese (Risiko von GI-Perforation unter Bev/IFN) ▲ thromboembolische Ereignisse oder Status nach zerebrovaskulärem Insult in der Anamnese ▲ bessere Datenlage für Sunitinib bei älteren Patienten ▲ grosse Lungenmetastasen (Risiko von Hämoptysis unter Bev/IFN) ▲ Abneigung des Patienten gegen Infusionstherapie/subkutane Injektionen.
Patientenfaktoren, die für den Einsatz von Bevacizumab/IFN sprechen: ▲ reduzierte linksventrikuläre Funktion
vor Therapiebeginn (Kardiotoxizität von Sunitinib) ▲ eingeschränkte Mobilität (HandFuss-Syndrom unter Sunitinib ggf. sehr belastend) ▲ vorbestehende orale Probleme (Tabletteneinnahme erschwert, Gefahr
von verstärkter Mukositis unter Sunitinib) ▲ mangelnde Adhärenz der Patienten bezüglich Tabletteneinnahme. Wie aus der Aufzählung ersichtlich, müssen aufgrund der fehlenden Daten «weiche» Faktoren bei der Entscheidungsfindung helfen. Leider sind keine PhaseIII-Studien geplant, in denen TKI gegen Bev/IFN geprüft werden wird. Etwas mehr Klarheit dürften die Resultate einer Phase-III-Studie bringen, in der Sunitinib gegen Pazopanibmonotherapie verglichen wird.
Zweitlinientherapie: Frage der optimalen Sequenz Für die Wahl der weiteren Behandlung sollte die vorgängige Therapie beachtet werden: Bei Zytokinvorbehandlung zeigen die Phase-III-Studien mit Sorafenib (16) und neuerdings mit Pazopanib (14) eine signifikante Verbesserung des progressionsfreien Überlebens. Bei Progredienz nach vorausgegangener Therapie mit Sunitinib und/oder Sorafenib hat sich die Therapie mit Everolimus etabliert: Eine Phase-III-Studie zeigte für Everolimus als Zweitlinientherapie ein signifikant verbessertes PFS für Everolimus (4 vs. 1,9 Monate) gegenüber der Behandlung mit Plazebo (17). Es fand sich jedoch nur in 2% eine Partialremission, in 67% war die Krankheit stabil. Hierzu muss gesagt werden, dass in dieser Studie Everolimus nur gegen Plazebo und nicht gegen einen anderen TKI getestet wurde. Retrospektive Analysen zeigten, dass der Wechsel von Sorafenib auf Sunitinib oder umgekehrt ähnliche Resultate bringen kann. Vom klinischen Standpunkt her ist anzumerken, dass ein Wechsel des TKI bei Progredienz nach länger andauerndem Ansprechen oder Abbruch der Therapie wegen Toxizität eine gute Option darstellt. Bei primärer Resistenz auf TKI scheint der frühzeitige Einsatz von Everolimus demgegenüber sinnvoller. Eine weitere Verbesserung könnte in naher Zukunft der Einsatz der neuen Generation von TKI-Substanzen bringen: Mit Axitinib (deutlich höhere Affinität gegenüber VEGF-R und PDGF-R) zeigten sich in einer Phase-II-Studie (18) nach Versagen auf Sorafenib gute Ansprechraten (23%) und ein vielverspre-
chendes PFS (7,4 Monate). Hierzu läuft zurzeit eine Phase-III-Studie, in der Axitinib gegen Sorafenib in der Zweitlinientherapie geprüft wird. Auch sind Studien angelaufen, in denen primär der mTOR-Inhibitor und danach TKI (und vice versa) verabreicht wird (REOCRD-3), ebenso wie Switch-Studien, in denen die TKI gegeneinander ausgewechselt werden. Neben der sequenziellen Therapie sind in den letzten Jahren Kombinationen der verschiedenen Medikamente versucht worden. Dabei zeigte sich jedoch, dass eine Kombination von verschiedenen Angiogenesehemmern (Bevacizumab plus Sunitinib/Sorafenib) zu unerwartet starken Nebenwirkungen führt. Das Gleiche gilt für die Kombination von Sunitinib mit Temsirolimus. Vielversprechend erschien aufgrund von nicht überlappenden Toxizitäten der Ansatz einer Kombination von Bevacizumab mit mTOR-Inhibitoren: Die TORAVA-Studie zeigte jedoch auch hier eine erhöhte Toxizität, wenn Bevacizumab mit Temsirolimus kombiniert wird (15); die Daten der Kombination mit Everolimus (RECORD-2-Studie) sind ausstehend. Neben der erhöhten Toxizität zeigte sich bisher kein Hinweis auf eine verbesserte Wirksamkeit. Es scheint derzeit so, als ob die ideale Sequenz von Monotherapien und nicht die Kombinationstherapien eine optimale Therapie versprechen. Um diese optimale Sequenz zu bestimmen, wäre es wichtig, prädiktive Faktoren zu kennen, welche eine Aussage über das individuelle Therapieansprechen liefern könnten. Hier sind intensive Forschungsbemühungen im Gange, welche aber noch zu keinen verwertbaren Ergebnissen geführt haben.
Hellzelliges Nierenzellkarzinom mit «poor risk»
Weniger komplex ist die Datenlage für Hochrisikopatienten (= «poor risk» gemäss Motzer-Kriterien). In der einzigen randomisierten Phase-III-Studie wurde der mTOR-Inhibitor Temsirolimus gegenüber Interferon-alpha oder einer Kombination der zwei Medikamente getestet. Für Patienten in der Hochrisikogruppe zeigt sich mit Temsirolimus eine signifikante Verbesserung des Gesamtüberlebens gegenüber der Therapie mit
22 SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 4/2010
Im Fokus: Prostatakarzinom und Nierenzellkarzinom
Interferon-alpha (10,9 vs. 7,3 Monate) (19). Ein messbares Ansprechen oder eine Stabilisierung konnte in 32% für die Temsirolimuspatienten respektive in 16% für Patienten unter IFN-α gefunden werden. Diese Zahlen zeigen aber auch, dass bei Patienten mit schlechtem Risikoscore die Erkrankung weiterhin nur beschränkt beeinflusst werden kann.
Stellenwert der Tumornephrektomie im Zeitalter der neuen Therapien
In Anbetracht der neuen Möglichkeiten medikamentöser Behandlung stellt sich die Frage, ob bei Patienten mit metastasiertem RCC weiterhin eine Tumornephrektomie im Sinne eines Debulkings sinnvoll ist. In der Interferonära hatte sich gezeigt, dass ein derartiger Eingriff mit einer signifikanten Lebensverlängerung verbunden ist (11,1 vs. 8,1 Monate) (20). Zurzeit werden zwei randomisierte Studien durchgeführt, welche diese Frage zu klären versuchen. Eine kürzlich vorgestellte retrospektive Analyse zeigte einen Überlebensvorteil für Patienten mit Nephrektomie, auch wenn sie mit den neuen Substanzen behandelt werden (21). Dies trifft jedoch in erster Linie auf Patienten mit «good/intermediate risk» zu, während «poor risk»-Patienten nur marginal profitierten. Für die Klinik sollte gelten, dass eine Nephrektomie sinnvoll ist, sofern der Patient in gutem Allgemeinzustand ist und keine Hochrisikosituation vorliegt.
Zusammenfassung und Ausblick
In der Behandlung des Nierenzellkarzinoms konnten in den letzten Jahren sowohl für das lokalisierte Stadium (partielle Nephrektomie, andere minimalinvasive Verfahren) als auch für das fortgeschrittene Stadium grosse Fortschritte erzielt werden. Bei der systemischen Therapie besteht mittlerweile eine Auswahl an verschiedenen Therapien, was neue Fragen zur optimalen Sequenz oder Kombination aufgeworfen hat. Als Entscheidungshilfe müssen weiterhin histopathologische und klinische Kriterien benutzt werden, da eigentliche prädiktive Faktoren noch nicht gefunden wurden. Es ist zu erwarten, dass molekulare Erkenntnisse eine bedeutende Unterstützung
bei der Wahl der idealen und auf den in-
dividuellen Patienten ausgerichteten
Therapie sein werden. Bis dahin sollten
sich die Therapieentscheidungen an den
vorliegenden Daten sowie an den Be-
sonderheiten der verschiedenen Be-
handlungen orientieren.
▲
Dr. med. Richard Cathomas Leitender Arzt medizinische Onkologie Kantonsspital Graubünden 7000 Chur E-Mail: richard.cathomas@ksgr.ch
Interessenkonflikte: Teilnahme an Advisory Boards der Firmen GSK, Roche, Novartis und Pfizer.
Quellen:
1. Brugarolas J.: Renal-cell carcinoma – molecular pathways and therapies. N Engl J Med 2007; 356: 185–187.
2. Motzer RJ, Bacik J et al.: Interferon-alfa as a comparative treatment for clinical trials of new therapies against advanced renal cell carcinoma. J Clin Oncol 2002; 20: 289–296.
3. Heng DY, Xie W, Regan MM et al.: Prognostic factors for overall survival in patients with metastatic renal cell carcinoma treated with vascular endothelial growth factor-targeted agents: results from a large, multicenter study. J Clin Oncol 2009; 27: 5794–5799.
4. MRC Renal Cancer Collaborators: Interferonalfa and survival in metastatic renal cell carcinoma: early results of a randomised controlled trial. Lancet 1999; 353: 14–17.
5. Fyfe G, Fisher RI, Rosenberg SA et al.: Results of treatment of 255 patients with metastatic renal cell carcinoma who received high-dose recombinant interleukin-2 therapy. J Clin Oncol 1995; 13: 688–696.
6. McDermott DF, Ghebremichael MS, Signoretti S et al.: The high-dose aldesleukin (HD IL-2) SELECT trial in patients with metastatic renal cell carcinoma. J Clin Oncol 2010; 15s (supp; abstract 4514).
7. Escudier B, Kataja V.: Renal cell carcinoma: ESMO clinical practice guidelines for diagnosis, treatment and follow-up. Ann Oncol 2010; 21: v137–v139.
8. Choueiri TK, Plantade A et al.: Efficacy of sunitinib and sorafenib in metastatic papillary and chromophobe renal cell carcinoma. J Clin Oncol 2008; 26: 127–131.
9. Molina AM, Feldman DR et al.: Phase II trial of sunitinib in patients with metastatic non-clear cell renal cell carcinoma. Invest New Drugs 2010, August, epub ahead of print.
10. Dutcher JP, de Souza P et al.: Effect of temsirolimus versus interferon-alpha on outcome of patients with advanced renal cell carcinoma of diffe-
rent tumor histologies. Med Oncol 2009; 26: 202–209.
11. Motzer RJ, Hutson TE et al.: Sunitinib versus interferon-alfa in metastatic renal-cell carcinoma. N Engl J Med 2007; 356: 115–124.
12. Escudier B, Bellmunt J, Négrier S et al.: Phase III trial of bevacizumab plus interferon alfa-2a in patients with metastatic renal cell carcinoma (AVOREN): final analysis of overall survival. J Clin Oncol 2010; 28: 2137–2143.
13. Rini B, Halabi S, Rosenberg JE et al.: Phase III trial of bevacizumab plus interferon alfa versus interferon alfa monotherapy in patients with metastatic renal cell carcinoma: final results of CALGB 90206. J Clin Oncol 2010; 28: 2144–2150.
14. Sternberg CN, Davis ID, Mardiak J et al.: Pazopanib in locally advanced or metastatic renal cell carcinoma: results of a randomized phase III trial. J Clin Oncol 2010; 28: 1061–1068.
15. Escudier B, Negrier S, Gravis G et al.: Can the combination of temsirolimus and bevacizumab improve the treatment of metastatic renal cell carcinoma? Results of the randomized TORAVA phase II trial. J Clin Oncol 2010; 15s (supp; abstract 4516).
16. Escudier B, Eisen T et al.: Sorafenib in advanced clear-cell renal-cell carcinoma. N Engl J Med 2007; 356: 125–134.
17. Motzer RJ, Escudier B et al.: Efficacy of everolimus in advanced renal cell carcinoma: a doubleblind, randomised, placebo-controlled phase III trial. Lancet 2008; 372: 449–456.
18. Rini BI, Wilding G, Hudes G et al.: Phase II study of axitinib in sorafenib-refractory metastatic renal cell carcinoma. J Clin Oncol 2009; 27: 4462–4468.
19. Hudes G, Carducci M et al.: Temsirolimus, interferon-alfa or both for advanced renal-cell carcinoma. N Engl J Med 2007; 356: 2271–2281.
20. Flanigan RC, Salmon SE, Blumenstein BA et al.: Nephrectomy followed by interferon alfa-2b compared with interferona alfa-2b alone for metastatic renal cell cancer. N Engl J Med 2001; 345: 1655–1659.
21. Choueiri TK, Xie W, Kollmannsberger CK et al.: The impact of cytoreductive nephrectomy in patients with metastatic renal cell carcinoma (mRCC) treated with vascular endothelial growth factor (VEGF)-targeted therapy. ASCO Genitourinary Cancers Symposium 2010, abstract 311.
SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 4/2010
23