Transkript
Lang wirksame Antipsychotika: Indikation und Effektivität
FORTBILDUNG
Marion Ebersoldt Marc Walter Roland Vauth
Entsprechend den Leitlinien sind orale Antipsychotika Therapie der Wahl in der medikamentösen Behandlung der Schizophrenie. Lang wirksame Depotantipsychotika finden insbesondere in der Langzeittherapie der Schizophrenie Anwendung. Ergebnisse von Metaanalysen weisen darauf hin, dass sie das Rückfall- und Rehospitalisationsrisiko im Vergleich zur oralen Einnahmeform bei manchen Patienten senken können. Depotantipsychotika gewährleisten ausreichende Dosierungen, zeigen jedoch eine geringe Steuerbarkeit. Relevante Unterschiede beruhen weniger auf der Wirkstärke als vielmehr auf der Pharmakokinetik und auf unterschiedlichen Nebenwirkungsprofilen. Neben der Sicherung einer hinreichenden Adhärenz können sie individuell auch zu einer Verbesserung der Lebensqualität beitragen.
von Marion Ebersoldt1, Marc Walter2, Roland Vauth3
A ntipsychotika sind eine chemisch heterogene Gruppe von Pharmaka mit unterschiedlichen antipsychotischen Wirksamkeitspotenzen und Nebenwirkungsprofilen. In der Schweiz, in Deutschland und in den USA sind derzeit insgesamt 38 oral applizierbare, 1 inhalatives und 19 parenteral applizierbare Präparate (darunter 9 lang wirksame Depotformen) zugelassen. Aufgrund ihrer geringeren Steuerbarkeit finden Depotantipsychotika in der Regel in der Erhaltungstherapie Anwendung, sind jedoch auch teilweise für die Akutbehandlung zugelassen. Antipsychotika werden im Bereich psychotischer oder halluzinatorischer Zustände, aber auch zur Affektregulation (z.B. bei Paraphrenie) eingesetzt. Im Zulassungsbereich für Depotformen wurde der Schwerpunkt auf die Behandlung der Schizophrenie gelegt.
Stellenwert der Antipsychotika in der Schizophreniebehandlung Antipsychotika sind Mittel der Wahl bei der medikamentösen Behandlung der Schizophrenie (1, 2) und sollten im Rahmen eines individuellen und personenzentrierten Gesamtbehandlungsplanes in Kombination mit psycho- und soziotherapeutischen Verfahren (wie z.B. kognitiver Verhaltenstherapie, Psychoedukation, Familieninterventionen) verordnet werden. Behandlungsziele sind Symptomkontrolle, Rückfallverhütung, Verbesserung der Lebensqualität und Integration in normale Lebensbezüge. Schizophrenie ist eine häufige Erkrankung mit einer Lebenszeitprävalenz von zirka 1 Prozent, welche im jungen Erwachsenenalter beginnt und oft chronifiziert. Allgemeine Empfehlung ist, entsprechend den meisten Leitlinien, eine Antipsychotikabehandlung von Erster-
krankten über 1 Jahr, bei wiederholt Erkrankten über 5 Jahre (3–5). Angesichts der langen Behandlungsdauer ist es daher wichtig, für die Patienten eine komfortable und gut verträgliche, so auch besser akzeptierbare Behandlungsoption zu finden. Der Vergleich von konventionellen und atypischen Antipsychotika in der oralen Darreichungsform ergab eine vergleichbare Wirksamkeit hinsichtlich Symptomkontrolle mit Hinweis auf weniger Therapieabbrüche und eine bessere Rückfallprävention, auch auf weniger motorische Nebenwirkungen (insbesondere Spätdyskinsien) und eine bessere Wirksamkeit bei Negativsymptomatik für atypische Antipsychotika (4, 5).
Einführung und Verordnung lang wirksamer Depotantipsychotika Fluphenazin war der Wirkstoff des ersten Depotantipsychotikums aus der Gruppe der konventionellen Antipsychotika, welches 1967 als Prolixin in den USA eingeführt wurde. 2002 wurde Risperidon als erstes atypisches Depotantipsychotikum zugelassen. Weitere Präparateentwicklungen gingen nur zögerlich vonstatten, sodass derzeit in der Schweiz, in Deutschland und den USA nur insgesamt 9 Depotformen zur Verfügung stehen. Trotz guter Wirksamkeit und gewisser Vorteile nutzen in vielen Länder bis heute nur wenige Patienten mit Schizophrenie die Möglichkeit einer Depotmedikation, was offensichtlich auf eine zurückhaltende Einstellung der Therapeuten (8), eine begrenzte Verfügbarkeit von atypischen Depotpräparaten, teilweise aber auch auf eine mangelhafte Information der Patienten, eine fehlende Erfahrung mit Rückfällen und eine weiter bestehende Stigmatisierung der Injektionsform zurückzuführen ist (9–11). Depotinjektionen vermitteln den Patienten im Gegensatz zur oralen Medikation möglicherweise häufiger das Gefühl, nicht aktiv an der Therapieentscheidung und -durchführung mitwirken zu
&10 5/2013 PSYCHIATRIE NEUROLOGIE
FORTBILDUNG
Kasten 1:
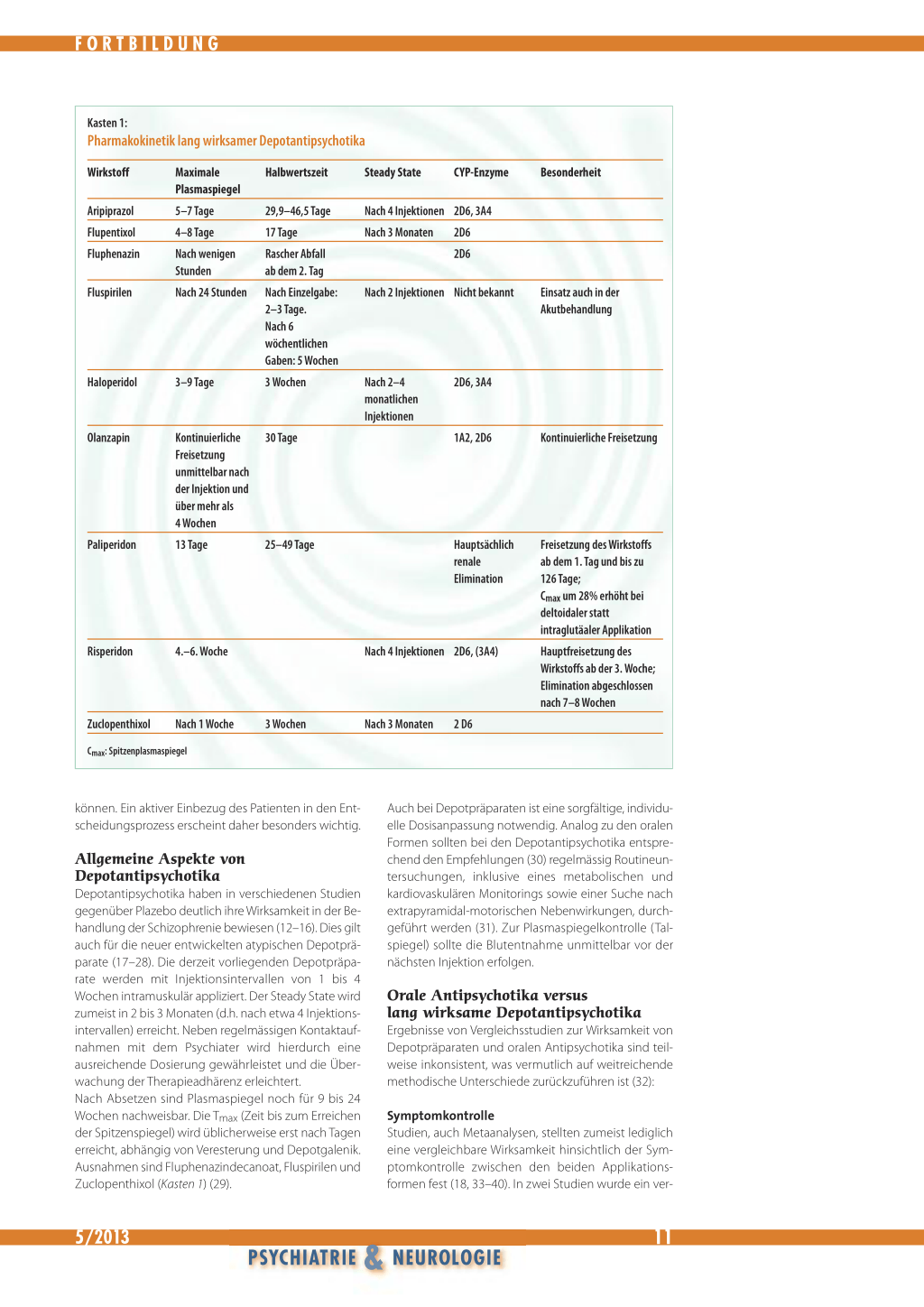
Pharmakokinetik lang wirksamer Depotantipsychotika
Wirkstoff Aripiprazol Flupentixol Fluphenazin Fluspirilen
Haloperidol Olanzapin
Paliperidon
Maximale Plasmaspiegel 5–7 Tage 4–8 Tage Nach wenigen Stunden Nach 24 Stunden
3–9 Tage
Halbwertszeit
29,9–46,5 Tage 17 Tage Rascher Abfall ab dem 2. Tag Nach Einzelgabe: 2–3 Tage. Nach 6 wöchentlichen Gaben: 5 Wochen 3 Wochen
Kontinuierliche Freisetzung unmittelbar nach der Injektion und über mehr als 4 Wochen
13 Tage
30 Tage 25–49 Tage
Steady State CYP-Enzyme
Nach 4 Injektionen 2D6, 3A4 Nach 3 Monaten 2D6
2D6
Nach 2 Injektionen Nicht bekannt
Nach 2–4 monatlichen Injektionen
2D6, 3A4 1A2, 2D6
Hauptsächlich renale Elimination
Risperidon
4.–6. Woche
Nach 4 Injektionen 2D6, (3A4)
Zuclopenthixol Nach 1 Woche
Cmax: Spitzenplasmaspiegel
3 Wochen
Nach 3 Monaten 2 D6
Besonderheit
Einsatz auch in der Akutbehandlung
Kontinuierliche Freisetzung
Freisetzung des Wirkstoffs ab dem 1. Tag und bis zu 126 Tage; Cmax um 28% erhöht bei deltoidaler statt intraglutäaler Applikation Hauptfreisetzung des Wirkstoffs ab der 3. Woche; Elimination abgeschlossen nach 7–8 Wochen
können. Ein aktiver Einbezug des Patienten in den Entscheidungsprozess erscheint daher besonders wichtig.
Allgemeine Aspekte von Depotantipsychotika Depotantipsychotika haben in verschiedenen Studien gegenüber Plazebo deutlich ihre Wirksamkeit in der Behandlung der Schizophrenie bewiesen (12–16). Dies gilt auch für die neuer entwickelten atypischen Depotpräparate (17–28). Die derzeit vorliegenden Depotpräparate werden mit Injektionsintervallen von 1 bis 4 Wochen intramuskulär appliziert. Der Steady State wird zumeist in 2 bis 3 Monaten (d.h. nach etwa 4 Injektionsintervallen) erreicht. Neben regelmässigen Kontaktaufnahmen mit dem Psychiater wird hierdurch eine ausreichende Dosierung gewährleistet und die Überwachung der Therapieadhärenz erleichtert. Nach Absetzen sind Plasmaspiegel noch für 9 bis 24 Wochen nachweisbar. Die Tmax (Zeit bis zum Erreichen der Spitzenspiegel) wird üblicherweise erst nach Tagen erreicht, abhängig von Veresterung und Depotgalenik. Ausnahmen sind Fluphenazindecanoat, Fluspirilen und Zuclopenthixol (Kasten 1) (29).
Auch bei Depotpräparaten ist eine sorgfältige, individuelle Dosisanpassung notwendig. Analog zu den oralen Formen sollten bei den Depotantipsychotika entsprechend den Empfehlungen (30) regelmässig Routineuntersuchungen, inklusive eines metabolischen und kardiovaskulären Monitorings sowie einer Suche nach extrapyramidal-motorischen Nebenwirkungen, durchgeführt werden (31). Zur Plasmaspiegelkontrolle (Talspiegel) sollte die Blutentnahme unmittelbar vor der nächsten Injektion erfolgen.
Orale Antipsychotika versus lang wirksame Depotantipsychotika Ergebnisse von Vergleichsstudien zur Wirksamkeit von Depotpräparaten und oralen Antipsychotika sind teilweise inkonsistent, was vermutlich auf weitreichende methodische Unterschiede zurückzuführen ist (32):
Symptomkontrolle Studien, auch Metaanalysen, stellten zumeist lediglich eine vergleichbare Wirksamkeit hinsichtlich der Symptomkontrolle zwischen den beiden Applikationsformen fest (18, 33–40). In zwei Studien wurde ein ver-
5/2013
&PSYCHIATRIE NEUROLOGIE
11
FORTBILDUNG
Kasten 2:
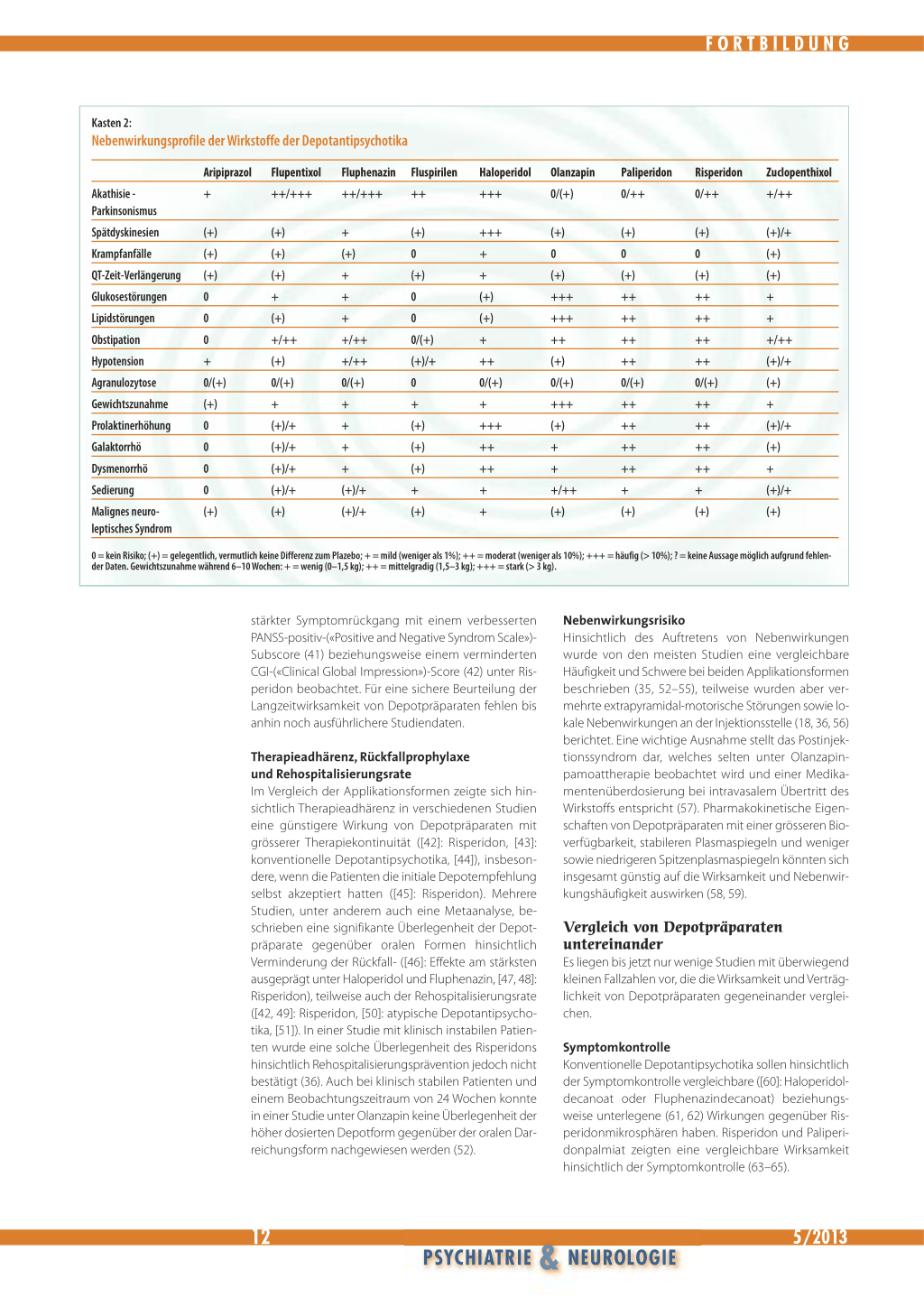
Nebenwirkungsprofile der Wirkstoffe der Depotantipsychotika
Akathisie Parkinsonismus Spätdyskinesien Krampfanfälle QT-Zeit-Verlängerung Glukosestörungen Lipidstörungen Obstipation Hypotension Agranulozytose Gewichtszunahme Prolaktinerhöhung Galaktorrhö Dysmenorrhö Sedierung Malignes neuroleptisches Syndrom
Aripiprazol Flupentixol + ++/+++
(+) (+) (+) (+) (+) (+) 0+ 0 (+) 0 +/++ + (+) 0/(+) 0/(+) (+) + 0 (+)/+ 0 (+)/+ 0 (+)/+ 0 (+)/+ (+) (+)
Fluphenazin Fluspirilen ++/+++ ++
+ (+) + + + +/++ +/++ 0/(+) + + + + (+)/+ (+)/+
(+) 0 (+) 0 0 0/(+) (+)/+ 0 + (+) (+) (+) + (+)
Haloperidol Olanzapin +++ 0/(+)
+++ (+) +0 + (+) (+) +++ (+) +++ + ++ ++ (+) 0/(+) 0/(+) + +++ +++ (+) ++ + ++ + + +/++ + (+)
Paliperidon 0/++
Risperidon 0/++
Zuclopenthixol +/++
(+) (+) (+)/+ 0 0 (+) (+) (+) (+) ++ ++ + ++ ++ + ++ ++ +/++ ++ ++ (+)/+ 0/(+) 0/(+) (+) ++ ++ + ++ ++ (+)/+ ++ ++ (+) ++ ++ + + + (+)/+ (+) (+) (+)
0 = kein Risiko; (+) = gelegentlich, vermutlich keine Differenz zum Plazebo; + = mild (weniger als 1%); ++ = moderat (weniger als 10%); +++ = häufig (> 10%); ? = keine Aussage möglich aufgrund fehlender Daten. Gewichtszunahme während 6–10 Wochen: + = wenig (0–1,5 kg); ++ = mittelgradig (1,5–3 kg); +++ = stark (> 3 kg).
stärkter Symptomrückgang mit einem verbesserten PANSS-positiv-(«Positive and Negative Syndrom Scale»)Subscore (41) beziehungsweise einem verminderten CGI-(«Clinical Global Impression»)-Score (42) unter Risperidon beobachtet. Für eine sichere Beurteilung der Langzeitwirksamkeit von Depotpräparaten fehlen bis anhin noch ausführlichere Studiendaten.
Therapieadhärenz, Rückfallprophylaxe und Rehospitalisierungsrate Im Vergleich der Applikationsformen zeigte sich hinsichtlich Therapieadhärenz in verschiedenen Studien eine günstigere Wirkung von Depotpräparaten mit grösserer Therapiekontinuität ([42]: Risperidon, [43]: konventionelle Depotantipsychotika, [44]), insbesondere, wenn die Patienten die initiale Depotempfehlung selbst akzeptiert hatten ([45]: Risperidon). Mehrere Studien, unter anderem auch eine Metaanalyse, beschrieben eine signifikante Überlegenheit der Depotpräparate gegenüber oralen Formen hinsichtlich Verminderung der Rückfall- ([46]: Effekte am stärksten ausgeprägt unter Haloperidol und Fluphenazin, [47, 48]: Risperidon), teilweise auch der Rehospitalisierungsrate ([42, 49]: Risperidon, [50]: atypische Depotantipsychotika, [51]). In einer Studie mit klinisch instabilen Patienten wurde eine solche Überlegenheit des Risperidons hinsichtlich Rehospitalisierungsprävention jedoch nicht bestätigt (36). Auch bei klinisch stabilen Patienten und einem Beobachtungszeitraum von 24 Wochen konnte in einer Studie unter Olanzapin keine Überlegenheit der höher dosierten Depotform gegenüber der oralen Darreichungsform nachgewiesen werden (52).
Nebenwirkungsrisiko Hinsichtlich des Auftretens von Nebenwirkungen wurde von den meisten Studien eine vergleichbare Häufigkeit und Schwere bei beiden Applikationsformen beschrieben (35, 52–55), teilweise wurden aber vermehrte extrapyramidal-motorische Störungen sowie lokale Nebenwirkungen an der Injektionsstelle (18, 36, 56) berichtet. Eine wichtige Ausnahme stellt das Postinjektionssyndrom dar, welches selten unter Olanzapinpamoattherapie beobachtet wird und einer Medikamentenüberdosierung bei intravasalem Übertritt des Wirkstoffs entspricht (57). Pharmakokinetische Eigenschaften von Depotpräparaten mit einer grösseren Bioverfügbarkeit, stabileren Plasmaspiegeln und weniger sowie niedrigeren Spitzenplasmaspiegeln könnten sich insgesamt günstig auf die Wirksamkeit und Nebenwirkungshäufigkeit auswirken (58, 59).
Vergleich von Depotpräparaten untereinander Es liegen bis jetzt nur wenige Studien mit überwiegend kleinen Fallzahlen vor, die die Wirksamkeit und Verträglichkeit von Depotpräparaten gegeneinander vergleichen.
Symptomkontrolle Konventionelle Depotantipsychotika sollen hinsichtlich der Symptomkontrolle vergleichbare ([60]: Haloperidoldecanoat oder Fluphenazindecanoat) beziehungsweise unterlegene (61, 62) Wirkungen gegenüber Risperidonmikrosphären haben. Risperidon und Paliperidonpalmiat zeigten eine vergleichbare Wirksamkeit hinsichtlich der Symptomkontrolle (63–65).
&12 5/2013 PSYCHIATRIE NEUROLOGIE
FORTBILDUNG
Therapieadhärenz, Rückfallprophylaxe und Rehospitalisierungsrate Eine Behandlung mit konventionellen Depotantipsychotika soll insgesamt vergleichbar häufig (66) oder auch seltener (60) zu Therapieabbrüchen führen als die Therapie mit Risperidon. Für Risperdon und Olanzapinpamoat wurde eine vergleichbare Therapieadhärenz festgestellt (67).
Nebenwirkungsrisiko Für konventionelle Depotantipsychotika wie Haloperidoldecanoat oder Fluphenazindecanoat wurden weniger Gewichtzunahmen und Prolaktinerhöhungen als für Risperidon berichtet (60). Ein Switch von Risperidon zu Paliperidonpalmiat schien sich mit einem Rückgang der Prolaktinwerte günstig auf Hyperprolaktinämien auszuwirken (Montalvo et al. [46–49]), insgesamt scheinen Depotrisperidon und Depotpaliperidon eine ähnlich gute Verträglichkeit aufzuweisen (64, 65). Die Verwendung von Olanzapinpalmeat war bei annähernd 0,07 Prozent der Injektionen oder 1,4 Prozent der behandelten Patienten mit dem Auftreten eines Postinjektionssyndroms mit klinisch relevanter Überdosierungssymptomatik assoziiert (68, 69), welches weder bei Risperidon noch bei Paliperidonpalmiat beobachtet wurde (70). Insgesamt scheinen atypische Depotantipsychotika im Vergleich zu konventionellen und in Analogie zu den oralen Präparaten tendenziell verstärkt metabolische Syndrome, Gewichtszunahmen und Prolaktinerhöhungen zu begünstigen, jedoch weniger extrapyramidal-motorische Störungen zu verursachen (Kasten 2). Es stehen weitere Studien bei diesen jungen Medikamenten aus.
Für welche Patientensubgruppe ist eine Behandlung mit Depotantipsychotika besonders indiziert? Die Zulassung für Depotpräparate erfolgte in der Schweiz und in Deutschland hauptsächlich für die (Langzeit-)Behandlung der Schizophrenie. Erweiterte Zulassungsbereiche erhielten folgende Substanzen: Flupentixol, welches in der Schweiz auch für andere Psychosen, zum Beispiel organische Psychosen, oder bei Paraphrenie zugelassen wurde; Haloperidol, welches in der Schweiz auch bei anderen Psychosen, in Deutschland auch bei maniformen Zuständen verwendet werden kann; Zuclopenthixol, welches in der Schweiz zusätzlich auch bei anderen paranoiden und halluzinatorischen Syndromen (insbesondere bei Unruhe, psychomotorischer Übererregtheit, Feindseligkeit und affektiven Reaktionen) eingesetzt werden kann. Fehlende Medikamentenadhärenz ist aufgrund krankheits-, therapie- und therapeutenbedingter Faktoren sehr häufig. Oftmals ist diese schwer zu erkennen und geht mit einer gehäuften Rückfall- und Rehospitalisierungsrate, auch mit gehäuften Suizidversuchen einher (71–73). Mindestens die Hälfte der Patienten mit Schizophrenie oder schizoaffektiven Störungen nehmen weniger als 70 Prozent der verschriebenen Dosen ein (74). Besonders Patienten mit einer partiellen oder fehlenden Medikamentenadhärenz, bei denen eine regelmässige Medikamenteneinnahme als dringend erforderlich erachtet wird, scheinen eine Zielgruppe für eine Depotmedikation und damit kontrollierte Medikamentenabgabe zu sein (75, 76).
Kasten 3:
Empfehlungen der Fachgesellschaften für den Einsatz von Depotpräparaten in der Behandlung der Schizophrenie*
Schweizer Gesellschaft für Psychiatrie und Psychotherapie (SGPP): Derzeit keine Behandlungsempfehlungen für Schizophrenie vorhanden.
Deutsche Gesellschaft für Psychiatrie, Psychotherapie und Nervenheilkunde (DGPPN), S3-Behandlungsleitlinie Schizophrenie (2006, [3]) Akutphase: Applikationsform des Antipsychotikums: Es sollte bei kooperativen Patienten die orale Applikationsform als am wenigsten invasive Massnahme gewählt werden, da dadurch bei ähnlicher guter Wirksamkeit die Patientenautonomie am besten gewährleistet wird, es sei denn, es besteht der Patientenwunsch nach einer anderen Darreichungsform (Empfehlungsgrad C). Langzeitbehandlung/ Rezidivprophylaxe: Typische Depotantipsychotika und das derzeit einzig verfügbare atypische Depotantipsychotikum Risperidon sind aufgrund ihrer gesicherten Applikation und guten Bioverfügbarkeit eine wirksame Alternative zur oralen Medikation und sollten grundsätzlich in der Langzeittherapie in Erwägung gezogen werden (Empfehlungsstärke A/B). Eine antipsychotische Depotmedikation empfiehlt sich besonders in den Fällen, in denen eine regelmässige orale antipsychotische Medikation nicht sichergestellt ist, eine gesicherte Applikation aber dringend notwendig erscheint (z.B. schwere Fremd- oder Eigengefährdung im Rezidiv), oder wenn die Depotapplikation eine Patientenpräferenz darstellt (Good Clinical Practice). Aufgrund fehlender überlegener Wirksamkeit einzelner typischer Depotantipsychotika untereinander sollte die Auswahl anhand des Nebenwirkungsprofils und des Injektionsintervalls vorgenommen werden (Empfehlungsstärke C). Bei der Entscheidung für ein antipsychotisches Depotpräparat ist das erwartungsgemäss als günstiger einzustufende Nebenwirkungsprofil des verfügbaren Depotantipsychotikums Risperidon (insbesondere im Hinblick auf das geringere Risiko von Spätdyskinesien) zu berücksichtigen (Empfehlungsstärke C).
World Federation of Societies of Biological Psychiatry (WFSBP), Guidelines for Biological Treatment of Schizophrenia (2013): Long-acting depot medication (5): Aufgrund guter Evidenz bestehen Empfehlungen für die antipsychotische Behandlung von Patienten mit Schizophrenie für folgende Depotantipsychotika: konventionelle Depotantipsychotika (Empfehlungsstärke 1), Risperdal- und Paliperidondepotpräparat (Empfehlungsstärke 1), Olanzapindepotpräparat (Empfehlungsstärke 2–3; bei Fehlen von Vergleichsstudien mit anderen Depotpräparaten). Derzeit besteht gute Evidenz für eine Anwendung von konventionellen Depotpräparaten in der Rückfallprophylaxe der Schizophrenie, jedoch wurde kein klarer Wirksamkeitsunterschied zwischen den konventionellen oralen und konventionellen Depotpräparaten nachgewiesen (Empfehlungsstärke 1). Für Risperdal gibt es eine gewisse Evidenz für eine Überlegenheit des Depotpräparates verglichen mit der oralen Darreichungsform (Empfehlungsstärke 4) und für eine Anwendung des Depotpräparates bei ersterkrankten und älteren Patienten mit Schizophrenie (Empfehlungsstärke 3). Für Paliperidon gibt es keine Evidenz für eine Überlegenheit des Depotpräparates verglichen mit der oralen Darreichungsform (Empfehlungsstärke 1). Depotpaliperidon scheint eine vergleichbare Wirksamkeit wie Depotrisperidon zu besitzen (Empfehlungsstärke 1). Das Postinjektionssyndrom mit Delir und Sedation sollte als eine mögliche schwere Nebenwirkung nach jeder Injektion mit Olanzapinpamoat erachtet werden. Jede Injektion mit Olanzapinpamoat sollte daher entsprechend den Empfehlungen des Herstellers erfolgen, danach sollte eine 3-stündige Überwachungszeit folgen (Empfehlungsstärke 4).
* Empfehlungsstärke in Abhängigkeit von der Evidenzebene
5/2013
&PSYCHIATRIE NEUROLOGIE
13
FORTBILDUNG
Kasten 4:
Vor- und Nachteile lang wirksamer Depotantipsychotika
Pro G Sicherstellung der Adhärenz durch kontrollierte Me-
dikamentenabgabe G Fraglich verminderte Rückfall- und Rehospitalisie-
rungsrate G Weniger Bedarf der Erinnerung an die Medikamen-
teneinnahme G Nach Absetzen oder Verpassen einer Dosis sind Plas-
maspiegel noch für Wochen vorhanden G Sichereres Erreichen der niedrigsten effektiven Dosis
(schrittweise Reduktion) G Vermeiden gastrointestinaler Absorptionsprobleme G Umgehen eines First-Pass-Lebermetabolismus G Günstigere Pharmakokinetik mit weniger und nied-
rigeren Spitzenplasmaspiegeln, dadurch vermutlich auch weniger Nebenwirkungen G Vermindertes Risiko einer versehentlichen oder absichtlichen Überdosierung G Bei manchen Patienten Verbesserung der Lebensqualität
Kontra G Geringere Flexibilität bei der Administration G Gefahr von Überdosierungen (insbesondere bei Olan-
zapinpamoat) G Dosisoptimierung als protrahierter und unsicherer
Prozess G Gelegentlich lokale Gewebereaktionen an der Injek-
tionsstelle (Schmerzen, Ödeme, Pruritus, Granulome) G Gefahr intraarterieller oder intravenöser Injektionen (Cave insbesondere bei öligen Injektionslösungen) G Verzögertes Auftreten störender Nebeneffekte auch nach Unterbrechung der Medikation G Oftmals negative Patientenwahrnehmung/Stigma der Injektionsform G Aufwendigere Administration und teurere Behandlungskosten
Heres et al. (77) identifizierten eine weitere Patientengruppe, die sich ebenfalls in besonderem Masse für eine Behandlung mit Depotantipsychotika zu eignen scheint: Patienten, die sich durch ein hohes Mass an Einsichtsfähigkeit, an Offenheit gegenüber der medikamentösen Therapie und eine weitreichende Kenntnis über die Erkrankungsmerkmale auszeichnen. Auch für ersterkrankte Patienten mit Schizophrenie wird der frühe Einsatz von Depotpräparaten diskutiert (78). Ziel einer solchen Behandlung wird sein, die Therapieadhärenz zu verbessern und damit auch die Rückfallprävention mit insgesamt günstigeren Gesamtergebnissen (45, 79–81). Aufgrund der schwachen Datenlage besteht derzeit allerdings keine allgemeine Behandlungsempfehlung mit Depotantipsychotika für diese Patientengruppe. Ein weiterer, eventuell zukünftiger und zurzeit diskutierter Einsatzbereich besteht in der Erhaltungstherapie bei bipolaren affektiven Störungen. Hier wurde eine gute Wirksamkeit auf maniforme Zustände beschrieben, jedoch keine (Risperidon) oder sogar verschlechternde Wirkung (konventionelle Antipsychotika) auf die depressive Komponente, sodass eine Kombinationstherapie unerlässlich erscheint (82). Kasten 3 zeigt eine Übersicht der Behandlungsempfehlungen für Antipsychotika (3). Neben diesen Empfehlungen existieren diverse andere Guidelines, zum Beispiel der World Federation of Societies of Biological Psychiatry (WFSBP) (5).
Depotantipsychotika und Lebensqualität Neben der Verbesserung der Psychopathologie und der sozialen Funktionen sollte die Optimierung des subjektiven Befindens und der Lebensqualität ein zentrales Ziel in der Langzeitbehandlung der Schizophrenie sein. Diverse Studien befassen sich mit Prädiktoren von Lebensqualität bei Patienten mit Schizophrenie. Es
scheint, dass insbesondere eine ausgeprägte Negativsymptomatik, psychosoziale Unannehmlichkeiten und Widerstände negative Einflüsse auf den sozialen Aktivitätsbereich, die Motivation und das Energieniveau haben (83, 84). Auch persistierende Positivsymptome und Nebenwirkungen der Medikamente beeinträchtigen das Funktionsniveau und die Lebensqualität (5, 85). Hierbei scheinen Erwartungshaltungen teilweise eine grössere Rolle zu spielen als tatsächliche Einschränkungen, sodass eine weitgehende Symptomkontrolle allein nicht unbedingt zur Wiederherstellung einer guten Lebensqualität ausreicht (86). Lang wirksame Depotantipsychotika scheinen insbesondere als Monotherapie (87) und bei längeren Injektionsintervallen (88) die Lebensqualität zu verbessern. Gewisse Hinweise bestehen, dass sich atypische Depotformen (Risperidon) günstiger auf das subjektive Wohlbefinden auswirken als konventionelle Depotformen (Haloperidol) (89).
Zusammenfassung Die Therapie der Wahl in der medikamentösen Behandlung der Schizophrenie sind entsprechend den Leitlinien orale Antipsychotika. Hauptzielgruppe für Depotantipsychotika sind insbesondere Patienten, bei denen eine intentionale oder auch nicht intentionale Malcompliance (z.B. aufgrund kognitiver Störungen) besteht und bei denen eine Therapieadhärenz so teils verbessert werden kann. Für konventionelle Depotantipsychotika konnte hinsichtlich der Wirksamkeit in der Behandlung der Schizophrenie keine klare Überlegenheit gegenüber den oralen Antipsychotika festgestellt werden. Für die atypischen Antipsychotika gibt es Hinweise für eine gewisse Überlegenheit der Depotform von Risperdal gegenüber den oralen Präparaten, die insbesondere mit einer Verbesserung der Rückfall- und Rehospitalisierungsprävention assoziiert sein soll.
&14 5/2013 PSYCHIATRIE NEUROLOGIE
FORTBILDUNG
Depot-Antipsychotika sind relativ sichere Präparate, die
sich hinsichtlich der Nebenwirkungen von oralen
Antipsychotika hauptsächlich durch mögliche Kompli-
kationen infolge der invasiven Applikationsweise unter-
scheiden (lokale Reaktionen, Postinjektionssyndrom
unter Olanzapinpamoat).
Manche Patienten ziehen eine Depotform vor, die eine
tägliche Medikamenteneinnahme überflüssig macht.
So beschrieben Studien teilweise positive Auswirkun-
gen von (atypischen) Depotpräparaten auf das soziale
Funktionsniveau und die Lebensqualität von Patienten,
die an einer Schizophrenie leiden.
Nutzen und Risiko einer Behandlung mit Depotantipsy-
chotika sollten individuell abgewogen werden (Kasten
4). Zu unterstreichen ist, dass Depotantipsychotika nicht
als «stand alone»-Therapie, sondern im Rahmen eines
individuellen Gesamtbehandlungsplanes in Kombina-
tion mit psycho- und soziotherpeutischen Verfahren an-
gewendet werden sollten.
G
Korrespondenzadresse:
Dr. med. Marion Ebersoldt
1 Abteilungsärztin
Ambulatorium für Psychotische Erkrankungen
Gesundheitszentrum Psychiatrie
E-Mail: marion.ebersoldt@upkbs.ch
Merksätze:
G Depotantipsychotika haben eine vergleichbare Wirksamkeit oder sogar Überlegenheit gegenüber oralen Antipsychotika hinsichtlich Rückfallprophylaxe und Verminderung der Rehospitalisierungsrate.
G Atypische Depotantipsychotika haben eher günstigere Nebenwirkungsprofile als konventionelle.
G Die Verträglichkeit und Sicherheit von Depot-Antipsychotika ist insgesamt vergleichbar mit den oralen Präparaten (Ausnahme: Olanzapinpalmoat).
2 Ärztlicher Zentrumsleiter, Zentrum für Psychotische Erkrankungen, Universitäre Psychiatrische Kliniken Basel
3 Ärztlicher Leiter der Ambulatorien für Psychotische Erkrankungen und Transkulturelle Psychiatrie Basel
Literaturverzeichnis auf Anfrage unter info@rosenfluh.ch
KONGRESSHINWEIS
5/2013
&PSYCHIATRIE NEUROLOGIE
15