Transkript
FORTBILDUNG
Neurologische Symptome:
Würmer und Wurmlarven im zentralen Nervensystem
Adulte Würmer oder Wurmlarven können ins zentrale Nervensystem (ZNS) gelangen und eine neurologische Symptomatik hervorrufen: Meist sind dies fokale Symptome, inklusive Krampfanfälle, häufig auch Zeichen einer (Meningo-)Enzephalitis oder Myelitis. Zunehmender internationaler Reiseverkehr und Immigranten aus tropischen Ländern bringen diese Krankheitsbilder auch nach Europa – nicht nur in spezialisierte Zentren, sondern potenziell in jede neurologische Praxis.
Gerd D. Burchard Jakob P. Cramer
5/2011
von Gerd D. Burchard und Jakob P. Cramer
Kurze Helminthologie
D er Mensch kann Endwirt der Helminthen sein, das heisst, er beherbergt die erwachsenen Würmer oder ist Zwischenwirt für die Larvenstadien. Dabei ist er häufig als Fehl- oder Zufallswirt betroffen und spielt keine Rolle bei der Verbreitung und Aufrechterhaltung des Infektionszyklus. Bei Infektionen mit dem Schweinebandwurm Taenia solium kann der Mensch sowohl Zwischen- als auch Endwirt sein. Die Würmer lassen sich grob einteilen in: ● Bandwürmer (Zestoden) ● Saugwürmer (Trematoden) ● Fadenwürmer (Nematoden). Die adulten Bandwürmer besitzen einen Kopf (Skolex) mit Saugnäpfen und teilweise einem Hakenkranz (Rostellum), sie bestehen aus einer Reihe von Proglottiden, die aneinandergereiht (bis zu mehreren tausend) eine Kette (Strobila) bilden. Die Körperform der Saugwürmer ist meist flach und lang bis gedrungen, meist heften sie sich mit Saugnäpfen an; Trematoden sind meist zwittrig (Ausnahme: Schistosomen = Pärchenegel). Nematoden sind lange, schmale, getrenntgeschlechtliche Würmer, die beim Menschen als Darm- oder Gewebenematoden (= Filarien) vorkommen. Würmer (Helminthen) sind «Makroparasiten»: Sie vermehren sich meist nicht innerhalb eines Wirtes, weil dann – teleologisch betrachtet – die Belastung für den Wirt zu gross würde und die Würmer sich die eigene Lebensgrundlage entziehen würden. Sie haben daher im Lauf der Evolution teilweise komplizierte Lebenszyklen entwickelt, um ihre Nachkommen (Eier, Larven) in neue Wirte zu bringen. Einzelne Würmer werden weltweit gefunden, viele aber wegen der Abhängigkeit von Zwischenwirten nur in bestimmten tropischen Klimaregionen.
Epidemiologie Eine wesentliche Entwicklung in der Reisemedizin der letzten Jahre ist die Etablierung von internationalen Surveillance-Netzwerken, ein Beispiel ist das GeoSenti-
nel-Netzwerk. Damit stehen grosse Datenbanken zur Verfügung, die Aussagen zur Häufigkeit importierter Erkrankungen ermöglichen (1). So zeigt sich, dass Wurmerkrankungen des ZNS von Touristen nur selten mitgebracht werden, hingegen häufiger von Immigranten. Deshalb muss heutzutage jeder Neurologe/ Psychiater im Zeitalter der Globalisierung mit diesen Erkrankungen rechnen (2–4).
Intrazerebrale Raumforderungen Eine Reihe von Helminthen kann zu intrazerebralen Raumforderungen führen (Kasten 1). Klinisch stehen dementsprechend fokale neurologische Symptome im Vordergrund, oft Krampfanfälle (5). Vermutungen, dass adulte Filarien (insbesondere Onchocerca volvulus, der Erreger der Flussblindheit) direkt ins Gehirn einwandern und zu Epilepsie führen, haben sich nicht bestätigen lassen (6).
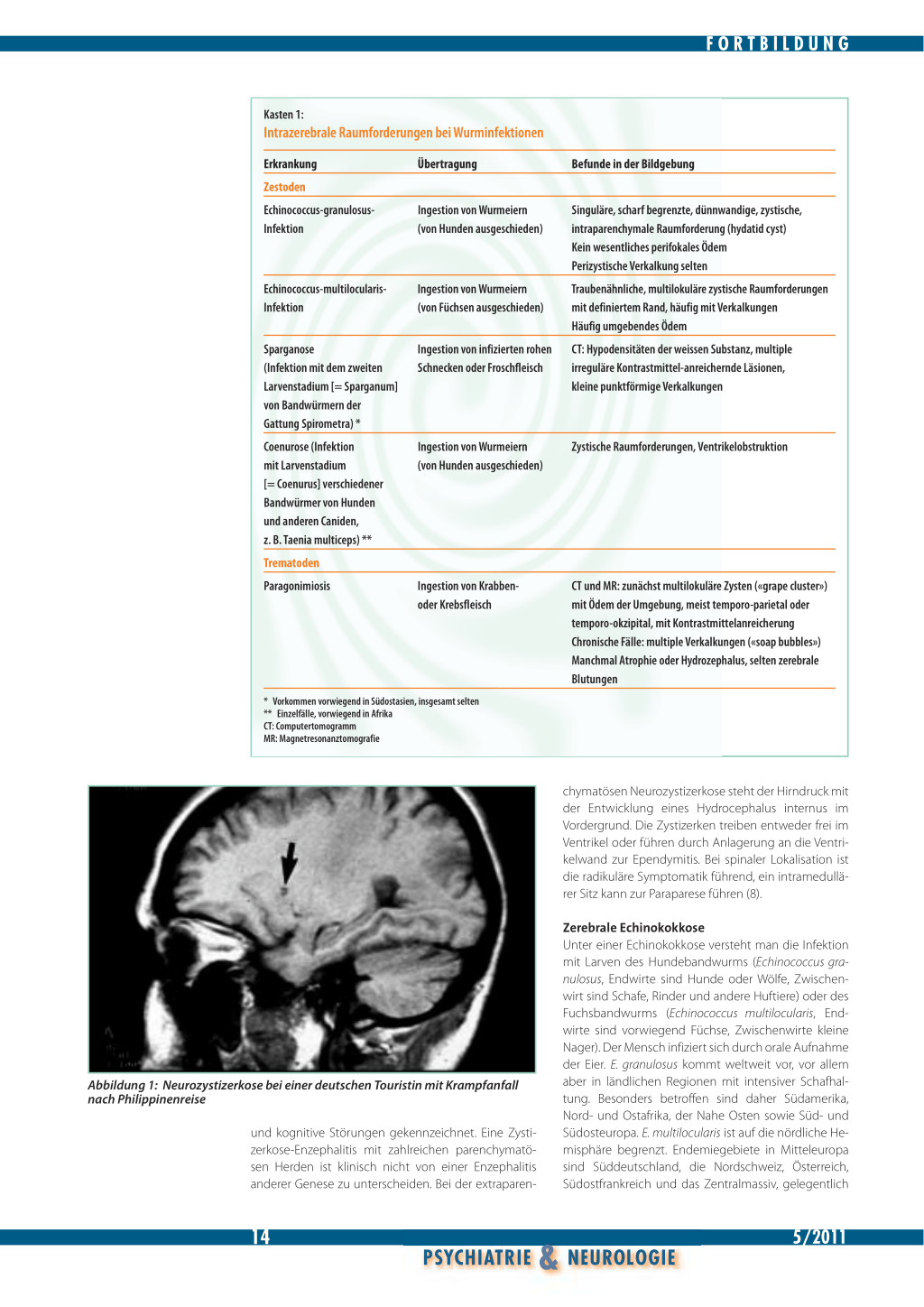
Neurozystizerkose Eine Zystizerkose ist die Infektion mit Larven des Schweinebandwurms Taenia solium. Die Infektion erfolgt durch Aufnahme von Wurmeiern mit verunreinigter Nahrung. Ein sehr seltener Übertragungsweg ist die interne Autoinfektion: Durch Hochwürgen von Proglottiden in den Magen werden Eier freigesetzt, aus denen dann die Hakenlarven schlüpfen können. Die Zystizerkose ist verbreitet in Gebieten mit niedrigem Hygienestandard, in denen häufig ungenügend gekochtes Schweinefleisch verzehrt wird. Weltweit ist die Neurozystizerkose die häufigste Ursache für eine im Erwachsenenalter einsetzende Epilepsie. Die Larven (Onkosphären) durchdringen die Darmwand, gelangen in Muskulatur, Herz und Subkutis sowie nicht selten ins Gehirn, wo sie sich innerhalb von 3 bis 4 Monaten zu 6 bis 15 mm grossen Zystizerken (Finnenblase mit einem einzelnen eingestülpten Skolex) entwickeln. Die Klinik ist abhängig von der Lokalisation der Zysten (7). Die parenchymatöse Neurozystizerkose (Abbildung 1) ist vor allem durch Krampfanfälle, Lähmungen
&PSYCHIATRIE NEUROLOGIE
13
FORTBILDUNG
Kasten 1:
Intrazerebrale Raumforderungen bei Wurminfektionen
Erkrankung Zestoden Echinococcus-granulosusInfektion
Übertragung
Ingestion von Wurmeiern (von Hunden ausgeschieden)
Echinococcus-multilocularisInfektion
Ingestion von Wurmeiern (von Füchsen ausgeschieden)
Sparganose (Infektion mit dem zweiten Larvenstadium [= Sparganum] von Bandwürmern der Gattung Spirometra) *
Coenurose (Infektion mit Larvenstadium [= Coenurus] verschiedener Bandwürmer von Hunden und anderen Caniden, z. B. Taenia multiceps) **
Trematoden
Paragonimiosis
Ingestion von infizierten rohen Schnecken oder Froschfleisch
Ingestion von Wurmeiern (von Hunden ausgeschieden)
Ingestion von Krabbenoder Krebsfleisch
* Vorkommen vorwiegend in Südostasien, insgesamt selten ** Einzelfälle, vorwiegend in Afrika CT: Computertomogramm MR: Magnetresonanztomografie
Befunde in der Bildgebung
Singuläre, scharf begrenzte, dünnwandige, zystische, intraparenchymale Raumforderung (hydatid cyst) Kein wesentliches perifokales Ödem Perizystische Verkalkung selten Traubenähnliche, multilokuläre zystische Raumforderungen mit definiertem Rand, häufig mit Verkalkungen Häufig umgebendes Ödem CT: Hypodensitäten der weissen Substanz, multiple irreguläre Kontrastmittel-anreichernde Läsionen, kleine punktförmige Verkalkungen
Zystische Raumforderungen, Ventrikelobstruktion
CT und MR: zunächst multilokuläre Zysten («grape cluster») mit Ödem der Umgebung, meist temporo-parietal oder temporo-okzipital, mit Kontrastmittelanreicherung Chronische Fälle: multiple Verkalkungen («soap bubbles») Manchmal Atrophie oder Hydrozephalus, selten zerebrale Blutungen
chymatösen Neurozystizerkose steht der Hirndruck mit der Entwicklung eines Hydrocephalus internus im Vordergrund. Die Zystizerken treiben entweder frei im Ventrikel oder führen durch Anlagerung an die Ventrikelwand zur Ependymitis. Bei spinaler Lokalisation ist die radikuläre Symptomatik führend, ein intramedullärer Sitz kann zur Paraparese führen (8).
Abbildung 1: Neurozystizerkose bei einer deutschen Touristin mit Krampfanfall nach Philippinenreise
und kognitive Störungen gekennzeichnet. Eine Zystizerkose-Enzephalitis mit zahlreichen parenchymatösen Herden ist klinisch nicht von einer Enzephalitis anderer Genese zu unterscheiden. Bei der extraparen-
Zerebrale Echinokokkose Unter einer Echinokokkose versteht man die Infektion mit Larven des Hundebandwurms (Echinococcus granulosus, Endwirte sind Hunde oder Wölfe, Zwischenwirt sind Schafe, Rinder und andere Huftiere) oder des Fuchsbandwurms (Echinococcus multilocularis, Endwirte sind vorwiegend Füchse, Zwischenwirte kleine Nager). Der Mensch infiziert sich durch orale Aufnahme der Eier. E. granulosus kommt weltweit vor, vor allem aber in ländlichen Regionen mit intensiver Schafhaltung. Besonders betroffen sind daher Südamerika, Nord- und Ostafrika, der Nahe Osten sowie Süd- und Südosteuropa. E. multilocularis ist auf die nördliche Hemisphäre begrenzt. Endemiegebiete in Mitteleuropa sind Süddeutschland, die Nordschweiz, Österreich, Südostfrankreich und das Zentralmassiv, gelegentlich
&14 5/2011 PSYCHIATRIE NEUROLOGIE
FORTBILDUNG
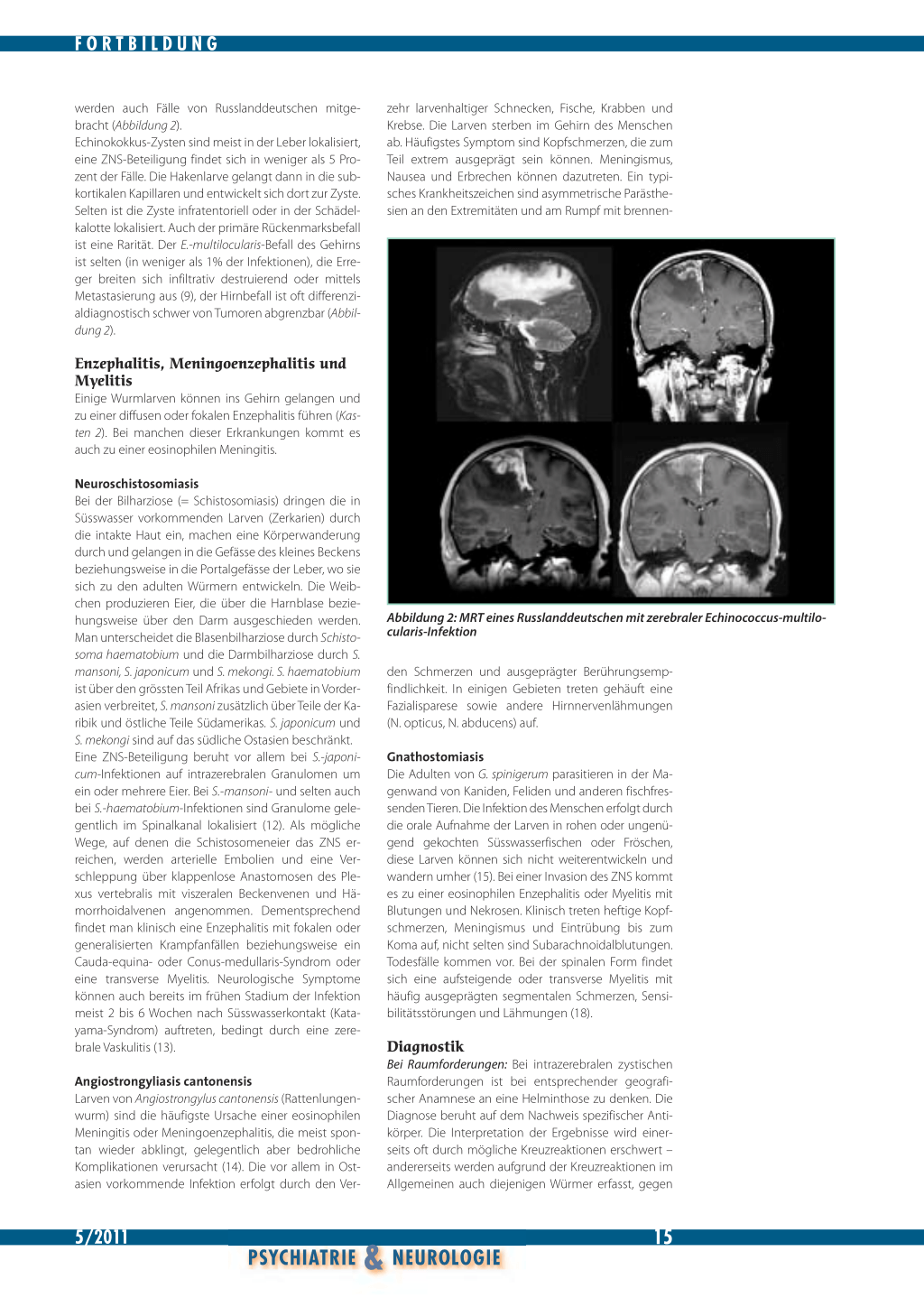
werden auch Fälle von Russlanddeutschen mitgebracht (Abbildung 2). Echinokokkus-Zysten sind meist in der Leber lokalisiert, eine ZNS-Beteiligung findet sich in weniger als 5 Prozent der Fälle. Die Hakenlarve gelangt dann in die subkortikalen Kapillaren und entwickelt sich dort zur Zyste. Selten ist die Zyste infratentoriell oder in der Schädelkalotte lokalisiert. Auch der primäre Rückenmarksbefall ist eine Rarität. Der E.-multilocularis-Befall des Gehirns ist selten (in weniger als 1% der Infektionen), die Erreger breiten sich infiltrativ destruierend oder mittels Metastasierung aus (9), der Hirnbefall ist oft differenzialdiagnostisch schwer von Tumoren abgrenzbar (Abbildung 2).
zehr larvenhaltiger Schnecken, Fische, Krabben und Krebse. Die Larven sterben im Gehirn des Menschen ab. Häufigstes Symptom sind Kopfschmerzen, die zum Teil extrem ausgeprägt sein können. Meningismus, Nausea und Erbrechen können dazutreten. Ein typisches Krankheitszeichen sind asymmetrische Parästhesien an den Extremitäten und am Rumpf mit brennen-
Enzephalitis, Meningoenzephalitis und Myelitis Einige Wurmlarven können ins Gehirn gelangen und zu einer diffusen oder fokalen Enzephalitis führen (Kasten 2). Bei manchen dieser Erkrankungen kommt es auch zu einer eosinophilen Meningitis.
Neuroschistosomiasis Bei der Bilharziose (= Schistosomiasis) dringen die in Süsswasser vorkommenden Larven (Zerkarien) durch die intakte Haut ein, machen eine Körperwanderung durch und gelangen in die Gefässe des kleines Beckens beziehungsweise in die Portalgefässe der Leber, wo sie sich zu den adulten Würmern entwickeln. Die Weibchen produzieren Eier, die über die Harnblase beziehungsweise über den Darm ausgeschieden werden. Man unterscheidet die Blasenbilharziose durch Schistosoma haematobium und die Darmbilharziose durch S. mansoni, S. japonicum und S. mekongi. S. haematobium ist über den grössten Teil Afrikas und Gebiete in Vorderasien verbreitet, S. mansoni zusätzlich über Teile der Karibik und östliche Teile Südamerikas. S. japonicum und S. mekongi sind auf das südliche Ostasien beschränkt. Eine ZNS-Beteiligung beruht vor allem bei S.-japonicum-Infektionen auf intrazerebralen Granulomen um ein oder mehrere Eier. Bei S.-mansoni- und selten auch bei S.-haematobium-Infektionen sind Granulome gelegentlich im Spinalkanal lokalisiert (12). Als mögliche Wege, auf denen die Schistosomeneier das ZNS erreichen, werden arterielle Embolien und eine Verschleppung über klappenlose Anastomosen des Plexus vertebralis mit viszeralen Beckenvenen und Hämorrhoidalvenen angenommen. Dementsprechend findet man klinisch eine Enzephalitis mit fokalen oder generalisierten Krampfanfällen beziehungsweise ein Cauda-equina- oder Conus-medullaris-Syndrom oder eine transverse Myelitis. Neurologische Symptome können auch bereits im frühen Stadium der Infektion meist 2 bis 6 Wochen nach Süsswasserkontakt (Katayama-Syndrom) auftreten, bedingt durch eine zerebrale Vaskulitis (13).
Angiostrongyliasis cantonensis Larven von Angiostrongylus cantonensis (Rattenlungenwurm) sind die häufigste Ursache einer eosinophilen Meningitis oder Meningoenzephalitis, die meist spontan wieder abklingt, gelegentlich aber bedrohliche Komplikationen verursacht (14). Die vor allem in Ostasien vorkommende Infektion erfolgt durch den Ver-
Abbildung 2: MRT eines Russlanddeutschen mit zerebraler Echinococcus-multilocularis-Infektion
den Schmerzen und ausgeprägter Berührungsempfindlichkeit. In einigen Gebieten treten gehäuft eine Fazialisparese sowie andere Hirnnervenlähmungen (N. opticus, N. abducens) auf.
Gnathostomiasis Die Adulten von G. spinigerum parasitieren in der Magenwand von Kaniden, Feliden und anderen fischfressenden Tieren. Die Infektion des Menschen erfolgt durch die orale Aufnahme der Larven in rohen oder ungenügend gekochten Süsswasserfischen oder Fröschen, diese Larven können sich nicht weiterentwickeln und wandern umher (15). Bei einer Invasion des ZNS kommt es zu einer eosinophilen Enzephalitis oder Myelitis mit Blutungen und Nekrosen. Klinisch treten heftige Kopfschmerzen, Meningismus und Eintrübung bis zum Koma auf, nicht selten sind Subarachnoidalblutungen. Todesfälle kommen vor. Bei der spinalen Form findet sich eine aufsteigende oder transverse Myelitis mit häufig ausgeprägten segmentalen Schmerzen, Sensibilitätsstörungen und Lähmungen (18).
Diagnostik Bei Raumforderungen: Bei intrazerebralen zystischen Raumforderungen ist bei entsprechender geografischer Anamnese an eine Helminthose zu denken. Die Diagnose beruht auf dem Nachweis spezifischer Antikörper. Die Interpretation der Ergebnisse wird einerseits oft durch mögliche Kreuzreaktionen erschwert – andererseits werden aufgrund der Kreuzreaktionen im Allgemeinen auch diejenigen Würmer erfasst, gegen
5/2011
&PSYCHIATRIE NEUROLOGIE
15
FORTBILDUNG
Kasten 2:
Meningoenzephalitis und Myelitis bei Wurminfektionen
Erkrankung
Übertragung
Befunde in der Bildgebung
Trematoden
Neuroschistosomiasis
Penetration der Haut durch
CCT und MRI unspezifisch, oft KM-anreichernde Läsionen
Zerkarien bei Süsswasserkontakt mit Ödem
Nematoden
Angiostrongyloidiasis
Genuss von rohen Schnecken
CT: normal oder Ödem, enhancing ring oder disc lesions MR: T1: leptomeningeales Enhancement, hohe Signalintensitäten im Globus pallidus, punktförmiges Enhancement in den Hemisphären nach Gadolinium
Gnathostomiasis
Genuss von ungekochtem Fisch, Schnecken, Hühnern
Hämorrhagische Gänge und vereinzelte Blutungsherde, fuzzy white matter lesions, Rückenmarksschwellung mit diffuser Signalverstärkung
Strongyloidiasis *
Penetration der Haut durch die Larven, z.B. beim Barfusslaufen auf feuchten Böden
Hyperintensitäten im MRI, die sich als Embolien durch Strongyloideslarven interpretieren lassen
Toxokariasis **
Ingestion von Eiern (von Hunden ausgeschieden)
Granulomatöse Läsionen im CCT
Trichinose
Genuss von ungekochtem Fleisch von Schweinen, Wildschweinen, gelegentlich auch Bären, Walrossen u.a.
Diffuse und fokale Enzephalopathie
Baylisascaris-procyonis-Infektion Aufnahme von Eiern aus (Spulwurm des Waschbären) *** Waschbärkot
(z.B. Kinder mit Geophagie)
Diffuse Veränderungen der weissen Substanz im MRT
* Bei Patienten mit Immundefizienz können Larven ins ZNS gelangen und zu neurologischen Symptomen führen, die von Kopfschmerzen, psychischen Auffälligkeiten, Meningismus, Krämpfen und Paralysen bis zum Koma reichen. Möglich sind begleitende bakterielle Infektionen, insbesondere mit Escherichia coli und Klebsiellen (purulente Meningitis). ** Neurologische Beteiligung bei Toxokariasis insgesamt eher selten (10) *** Bisher nur Fälle in Nordamerika (11) CCT: kranielle Computertomografie MRI: Magnetresonanztomografie
die keine spezifische Serologie zur Verfügung steht. Man wird also bei entsprechendem Verdacht zunächst einen serologischen Test auf je einen Vertreter der Zestoden, der Trematoden und der Nematoden veranlassen. In Einzelfällen sind falschnegative Tests möglich, so liegt die Sensitivität bei solitären Zystizerkose-Zysten bei nur 50 Prozent. Antigentests sind in Erprobung. Zum Teil finden sich pathognomonische Befunde in der Bildgebung: In frühen Stadien der Zystikerkose ist der Skolex innerhalb der Zyste nachweisbar: kleine dünnwandige Zyste mit exzentrischer Hyperintensität. Bei zerebraler Paragonimiasis sind meist auch pulmonale Veränderungen im Röntgenthorax nachweisbar (16). Bei Enzephalitis, Meningoenzephalitis und Myelitis: Bei einigen Wurminfektionen des ZNS kann typischerweise eine eosinophile Liquorpleozytose auftreten (17–19), insbesondere bei Angiostrongyloidiasis cantonensis, Gnathostomiasis, Toxokariasis, Schistosomiasis und ZNS-Trichinose. Die Diagnose beruht auf der entsprechenden Anamnese und dem Nachweis spezifischer Antikörper, eventuell auch im Liquor. Manchmal sind Wurmlarven im Liquor zu finden.
Bei diffuser oder fokaler Enzephalitits sind die Befunde in der Bildgebung häufig unspezifisch (z.B. bei Neuroschistosomiasis), manchmal sind granulomatöse Läsionen nachweisbar. Auch hier beruht die Diagnose also wesentlich auf der entsprechenden Anamnese und dem Nachweis spezifischer Antikörper. Eine Eosinophilie im Blutbild kann ein unspezifischer Hinweis sein, muss aber nicht nachweisbar sein. Bei transverser Myelitis ist in erster Linie an eine Schistosomiasis zu denken (meist untere thorakale oder obere lumbale Segmente), ausserdem an Gnathostomiasis, Angiostrongyloidiasis, Strongyloidiasis und spinale Zystizerkose. Bei der Neuroschistosomiasis sind häufig Schistosomen-Eier im Urin (bei S. haematobium) beziehungsweise im Stuhl (bei S. mansoni und S. japonicum) mittels Anreicherungsverfahren in spezialisierten Labors nachweisbar. Im Liquor finden sich keine Schistosomen-Eier. In der Bildgebung sind bei spinaler Schistosomiasis in etwa 75 Prozent intramedulläre Granulome darstellbar. Hinweise auf eine zerebrale Trichinose (20) können sein: vorausgehende gastrointestinale Beschwerden, periorbitale Ödeme, erhöhte Muskelenzymwerte. ●
&16 5/2011 PSYCHIATRIE NEUROLOGIE
FORTBILDUNG
Korrespondenzadresse:
Prof. Dr. Gerd Burchard
Universitätsklinikum Hamburg-Eppendorf
Sektion Tropenmedizin und Infektiologie
Bernhard-Nocht-Strasse 74
D-20259 Hamburg
Tel. 0049 40 42818391
Fax 0049 40 42818394
E-Mail: gerd.burchard@bni-hamburg.de
Literatur:
1. Odolini S, Parola P, Gkrania-Klotsas E, Caumes E, Schlagenhauf P, López-Vélez R, Burchard GD, Santos-O’Connor F, Weld L, von Sonnenburg F, Field V, de Vries P, Jensenius M, Loutan L, Castelli F.: Travel-related imported infections in Europe, EuroTravNet 2009. Clin Microbiol Infect. 2011 Jun 10.
2. Schmutzhard E.: Parasitäre Erkrankungen des Nervensystems. Der Nervenarzt 2010, 81: 162–171.
3. Lv S, Zhang Y, Steinmann P, Zhou XN, Utzinger J.: Helminth infections of the central nervous system occurring in Southeast Asia and the Far East. Adv Parasitol. 2010; 72: 351–408.
4. Shakir RA, Newman PK, Poser CM (Hrsg.), Tropical Neurology. WB Saunders Company Ltd. 1996.
5. Wagner RG, Newton CR.: Do helminths cause epilepsy? Parasite Immunol. 2009; 31(11): 697–705.
6. König R, Nassri A, Meindl M, Matuja W, Kidunda AR, Siegmund V, Bretzel G, Löscher T, Jilek-Aall L, Schmutzhard E, Winkler AS.: The role of Onchocerca volvulus in the development of epilepsy in a rural area of Tanzania. Parasitology. 2010; 137(10): 1559–68.
7. Carabin H, Ndimubanzi PC, Budke CM, Nguyen H, Qian Y, Cowan LD, Stoner JA, Rainwater E, Dickey M.: Clinical manifestations associated with neurocysticercosis: a systematic review. PLoS Negl Trop Dis. 2011; 5(5): e1152.
8. Nash TE, Garcia HH.: Diagnosis and treatment of neurocysticercosis. Nat Rev Neurol. 2011 Sep 13. doi: 10.1038/nrneurol.2011.135. [Epub ahead of print]
9. Isik N, Silav G, Cerçi A, Karabagli P, Elmaci I, Kalelioglu M.: Cerebral alveolar echinococcosis. A case report with MRI and review of the literature. J Neurosurg Sci. 2007; 51(3): 145–51.
10. Finsterer J, Auer H.: Neurotoxocarosis. Rev Inst Med Trop São Paulo. 2007; 49(5): 279–87.
11. Murray WJ, Kazacos KR.: Raccoon roundworm encephalitis. Clin Infect Dis. 2004; 39(10): 1484–92.
12. Ross AG, McManus DP, Farrar J, Hunstman RJ, Gray DJ, Li YS.: Neuroschistosomiasis. J Neurol. 2011 Jun 15.
13. Caumes E, Vidailhet M.: Acute neuroschistosomiasis: a cerebral vasculitis to treat with corticosteroids not praziquantel. J Travel Med. 2010; 17(5): 359.
14. Wang QP, Lai DH, Zhu XQ, Chen XG, Lun ZR.: Human angiostrongyliasis. Lancet Infect Dis. 2008; 8(10): 621–30.
15. Herman JS, Chiodini PL.: Gnathostomiasis, another emerging imported disease. Clin Microbiol Rev. 2009; 22(3): 484–92.
16. Kusner DJ, King CH.: Cerebral paragonimiasis. Semin Neurol. 1993; 13(2): 201–8.
17. Graeff-Teixeira C, da Silva AC, Yoshimura K.: Update on eosinophilic meningoencephalitis and its clinical relevance. Clin Microbiol Rev. 2009; 22(2): 322–48.
18. Katchanov J, Sawanyawisuth K, Chotmongkoi V, Nawa Y.: Neurognathostomiasis, a neglected parasitosis of the central nervous system. Emerg Infect Dis. 2011; 17(7): 1174–80.
19. Ramirez-Avila L, Slome S, Schuster FL, Gavali S, Schantz PM, Sejvar J, Glaser CA.: Eosinophilic meningitis due to Angiostrongylus and Gnathostoma species. Clin Infect Dis. 2009; 48(3): 322–7.
20. Mawhorter SD, Kazura JW.: Trichinosis of the central nervous system. Semin Neurol 1993; 13(2): 148–52.
Merkpunkte:
● Bei neu aufgetretener Epilepsie bei Tropenrückkehrern und Immigranten immer auch an Neurozystizerkose und an Bilharziose denken.
● Bei eosinophiler Meningitis denken an: Gnathostomiasis, Angiostrongyloidiasis, Zystizerkose und Bilharziose.
● Bei transverser Myelitis denken an Schistosomiasis und Gnathostomiasis.
5/2011
&PSYCHIATRIE NEUROLOGIE
17