Transkript
Fortbildung
Schmerz und Emotion
Kyrill Schwegler
24
Sind die Begriffe Schmerz und Emotion so zwanglos, wie es der Titel vorgibt, in Verbindung zu bringen, und dürfen sie in einem Atemzug genannt werden? Im Folgenden soll erörtert werden, wodurch eine solche Gegenüberstellung gerechtfertigt ist, die implizit suggeriert, dass beide Wahrnehmungen eng miteinander verknüpft sind, sich gegenseitig bedingen, ja sich gar decken.
S chmerz und Emotion sind eng verknüpft mit fundamentalen biologisch wie sozial verankerten Erfahrungen, die jedes Menschenleben prägen und ein breites Spektrum von gesunden bis pathologischen Entwicklungen und Zuständen bedingen können. Jeder Mensch kennt Schmerzen und weiss, dass schmerzhafte Erlebnisse von Emotionen begleitet sind. Dies lässt sich anhand von Redewendungen einfach zeigen. Der Volksmund spricht etwa von einem «schmerzvollen Abschied», von «Verlust- oder Herzschmerz» und so weiter, und meint damit, dass sich ein emotionales Erlebnis mit einer Schmerzerfahrung – hier einer seelischen – deckt, was nicht ausschliesst, dass diese durchaus auch auf einer körperlichen Ebene schmerzhaft wahrgenommen werden kann. Die Hypothese, welche sich hieraus ableiten lässt, lautet: Seelische Schmerzen sind nichts anderes als Emotionen. Damit wird gleichzeitig verdeutlicht, dass sich Seelisches im Körperlichen und vice versa darstellen beziehungsweise abbilden kann. Auch primär körperliche Schmerzen akuter peripher nozizeptiver Natur sind also von emotionalen Reaktionen begleitet und verfügen über eine «Gefühlsspur». Dieser Hinweis verdeutlicht, dass Schmerz und Emotion untrennbar
miteinander verwoben sind, was insbesondere für chronische nicht organische Schmerzen gilt, welche häufig mit einer emotionalen Störung vergesellschaftet sind. Es stellt sich die Frage wie diese Assoziation zustande kommt, wie sie sich auf dem Hintergrund einer neurobiologischen sowie psychologischen Betrachtungsweise erklären lässt und welche soziale Dimension sie hat?
Dimensionen des Schmerzes
Lange herrschte Unklarheit darüber, wie die äusserst komplexe Wahrnehmung «Schmerz» im zentralen Nervensystem zustande kommt beziehungsweise darüber, welche Areale im Hirn dabei involviert sind. Schmerz wurde vorwiegend als subkortikales Phänomen angesehen, ungeachtet der Tatsache, dass Patienten im Rahmen von nachweislich kortikalen Anfällen über Schmerzempfindungen berichteten. Erst die Entwicklungen der funktionellen Bildgebung machte es in den Neunzigerjahren des letzten Jahrhunderts technisch möglich, die zentralen Aktivierungsmuster im Rahmen peripherer Schmerzstimulation verlässlich sichtbar zu machen und für den Menschen darzustellen. Es wurde klar, dass sowohl kortikale Regionen wie die postzentralen somato-sensorischen Areale I und II (SI,
SII) und Anteile des limbischen und paralimbischen Systems, wie der anteriore zinguläre Kortex (ACC) beziehungsweise der insuläre Kortex (IC), und subkortikale Regionen wie der Thalamus (Th) und das Cerebellum (C) bei Schmerz aktiviert werden (1). Damit war die Rolle der einzelnen Hirnregionen in der Gesamtwahrnehmung Schmerz allerdings noch nicht geklärt. Phänomenologisch war bereits früher aufgrund klinischer Beobachtungen nicht anzuzweifeln, dass Schmerzen aus einem sensorischen, einem affektiven und einem kognitiv-bewertenden Teil bestehen beziehungsweise sich aus diesen Elementen zusammensetzen. Es wurden deskriptive Begriffe zur Charakterisierung dieser Dimensionen geschaffen, und es hat sich eingebürgert, von a) sensorisch-diskriminativen b) affektiv-motivationalen sowie c) kognitiv-evaluativen Aspekten
des Schmerzes zu sprechen (1). Die drei Umschreibungen werden der Tatsache gerecht, dass uns das zentrale Nervensystem aufgrund spezifischer dazu geeigneter Regionen befähigt, einerseits Schmerz detailliert und rational zu beschreiben (Lokalisation, Intensität, Qualität, Stärke etc.) (a), andererseits in Bezug auf emotionale und damit nicht der Ratio unterworfene Aspekte (unangenehm, ekelhaft, angsterregend, Leiden erzeugend) (b) zu erfassen und bewusst wahrzunehmen, und dass schliesslich die Möglichkeit besteht, den Schmerz in einen weiteren, abstrakteren Kontext zu stellen und kognitiv – also bewusst gedanklich – zu bewerten (c). In diesem Zusammenhang ist der Fallbericht von Ploner (2) mit dem Titel: «Pain affect without pain sensation in a patient with a postcentral leson» (Abbildung 1) zu nennen, welcher
Neurologie 3•2009
Fortbildung
Abbildung 1 (nach Ploner et al., 1999): Transaxiale MRISchnitte bei 42 mm (links) und 18 mm (rechts) paralell über der anterio-posterioren Kommissurenlinie. Die Skalen entsprechen den Koordinaten in mm entsprechend dem Talairach-Referenzrahmen (Talairach und Tournoux, 1988). Die Markierung (*) bezeichnet den Sulcus centralis.
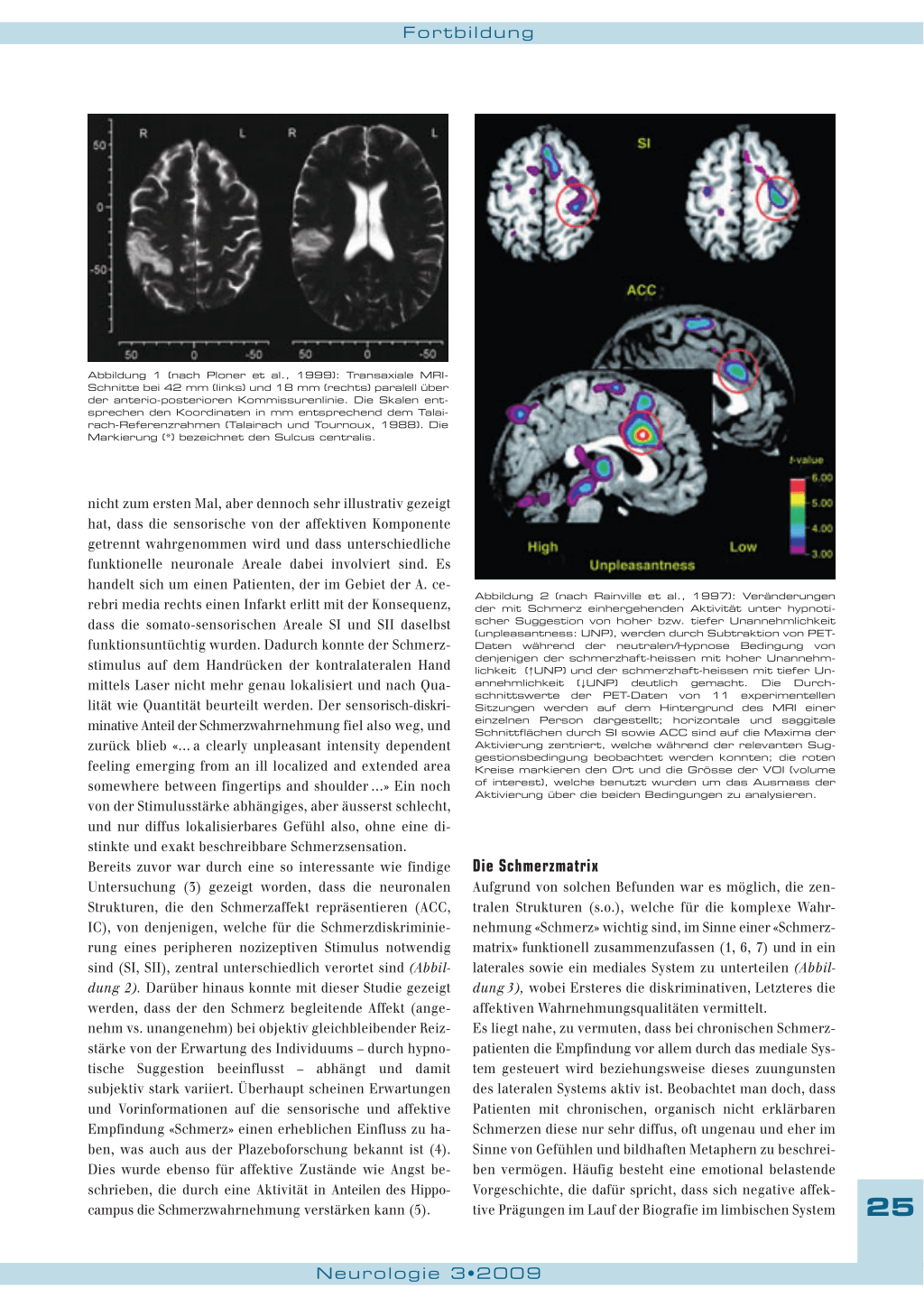
nicht zum ersten Mal, aber dennoch sehr illustrativ gezeigt hat, dass die sensorische von der affektiven Komponente getrennt wahrgenommen wird und dass unterschiedliche funktionelle neuronale Areale dabei involviert sind. Es handelt sich um einen Patienten, der im Gebiet der A. cerebri media rechts einen Infarkt erlitt mit der Konsequenz, dass die somato-sensorischen Areale SI und SII daselbst funktionsuntüchtig wurden. Dadurch konnte der Schmerzstimulus auf dem Handrücken der kontralateralen Hand mittels Laser nicht mehr genau lokalisiert und nach Qualität wie Quantität beurteilt werden. Der sensorisch-diskriminative Anteil der Schmerzwahrnehmung fiel also weg, und zurück blieb «… a clearly unpleasant intensity dependent feeling emerging from an ill localized and extended area somewhere between fingertips and shoulder …» Ein noch von der Stimulusstärke abhängiges, aber äusserst schlecht, und nur diffus lokalisierbares Gefühl also, ohne eine distinkte und exakt beschreibbare Schmerzsensation. Bereits zuvor war durch eine so interessante wie findige Untersuchung (3) gezeigt worden, dass die neuronalen Strukturen, die den Schmerzaffekt repräsentieren (ACC, IC), von denjenigen, welche für die Schmerzdiskriminierung eines peripheren nozizeptiven Stimulus notwendig sind (SI, SII), zentral unterschiedlich verortet sind (Abbildung 2). Darüber hinaus konnte mit dieser Studie gezeigt werden, dass der den Schmerz begleitende Affekt (angenehm vs. unangenehm) bei objektiv gleichbleibender Reizstärke von der Erwartung des Individuums – durch hypnotische Suggestion beeinflusst – abhängt und damit subjektiv stark variiert. Überhaupt scheinen Erwartungen und Vorinformationen auf die sensorische und affektive Empfindung «Schmerz» einen erheblichen Einfluss zu haben, was auch aus der Plazeboforschung bekannt ist (4). Dies wurde ebenso für affektive Zustände wie Angst beschrieben, die durch eine Aktivität in Anteilen des Hippocampus die Schmerzwahrnehmung verstärken kann (5).
Abbildung 2 (nach Rainville et al., 1997): Veränderungen der mit Schmerz einhergehenden Aktivität unter hypnotischer Suggestion von hoher bzw. tiefer Unannehmlichkeit (unpleasantness: UNP), werden durch Subtraktion von PETDaten während der neutralen/Hypnose Bedingung von denjenigen der schmerzhaft-heissen mit hoher Unannehmlichkeit (↑UNP) und der schmerzhaft-heissen mit tiefer Unannehmlichkeit (↓UNP) deutlich gemacht. Die Durchschnittswerte der PET-Daten von 11 experimentellen Sitzungen werden auf dem Hintergrund des MRI einer einzelnen Person dargestellt; horizontale und saggitale Schnittflächen durch SI sowie ACC sind auf die Maxima der Aktivierung zentriert, welche während der relevanten Suggestionsbedingung beobachtet werden konnten; die roten Kreise markieren den Ort und die Grösse der VOI (volume of interest), welche benutzt wurden um das Ausmass der Aktivierung über die beiden Bedingungen zu analysieren.
Die Schmerzmatrix
Aufgrund von solchen Befunden war es möglich, die zentralen Strukturen (s.o.), welche für die komplexe Wahrnehmung «Schmerz» wichtig sind, im Sinne einer «Schmerzmatrix» funktionell zusammenzufassen (1, 6, 7) und in ein laterales sowie ein mediales System zu unterteilen (Abbildung 3), wobei Ersteres die diskriminativen, Letzteres die affektiven Wahrnehmungsqualitäten vermittelt. Es liegt nahe, zu vermuten, dass bei chronischen Schmerzpatienten die Empfindung vor allem durch das mediale System gesteuert wird beziehungsweise dieses zuungunsten des lateralen Systems aktiv ist. Beobachtet man doch, dass Patienten mit chronischen, organisch nicht erklärbaren Schmerzen diese nur sehr diffus, oft ungenau und eher im Sinne von Gefühlen und bildhaften Metaphern zu beschreiben vermögen. Häufig besteht eine emotional belastende Vorgeschichte, die dafür spricht, dass sich negative affektive Prägungen im Lauf der Biografie im limbischen System
25
Neurologie 3•2009
Fortbildung
26
cortex:
lateral system: SI SII
medial system: insula ACC
thalamus: VPL, VPM VPI
VMpo MDvc, Pf CL
spinal cord:
lamina I
lamina V
deep
Abbildung 3 (nach Treede et al., 1999): Kortikale Areale, die Information aus dem Tractus spinothalamicus erhalten. Die spinothalamischen und thalamokorti-
kalen Hauptprojektionen werden vereinfacht für den Affen zusammengefasst (Vogt et al., 1979; Willis, 1985; Apkarian und Shi, 1994; Craig, 1996). Kortiko-kortikale Verbindungen werden nicht dargestellt. ACC, anteriorer
zingulärer Kortex; CL, centrolateraler Nucleus; MDvc, pars ventrocaudalis des mediodorsalen Nucleus; PF, parafasciculärer Nucleus; SI, primärer somato-
sensorischer Kortex; SII, sekundärer somatosensorischer Kortex; VMpo, pars posterioris des ventromedialen Nucleus; VPI, ventroposterioinferiorer Nucleus;
VPL, ventroposteriolateraler Nucleus; VPM ventroposteriomedialer Nucleus.
niedergeschlagen haben. Diese Ansicht lässt sich epidemiologisch dadurch stützen, dass Menschen mit Gewalt- und Missbrauchserfahrungen häufiger an nicht primär organischen Schmerzsyndromen erkranken (8, 9). Auch posttraumatische Belastungsstörungen sind zu einem hohen Prozentsatz mit chronischen Schmerzen vergesellschaftet (10–12). Ein solcher Zusammenhang könnte auch dadurch mit bedingt sein, dass traumatische Erfahrungen und damit negative Affekte, insbesondere auch Angst, bereits früh die Fähigkeit behindern, vertrauensvolle menschliche Bindungen einzugehen und zu halten. Diese Menschen sind also neurobiologisch anfälliger dafür, chronische Schmerzen zu entwickeln. Vielleicht gerade deshalb, weil sie sich grundsätzlich einsamer und verlassener fühlen. Meredith hat jedenfalls gezeigt, dass ein unsicherer Bindungstyp und chronische Schmerzen gehäuft assoziiert auftreten (13). Die Wahrnehmung von Schmerz hat also unbedingt auch eine soziale Komponente, die sich darin spiegelt, dass die emotionale Interaktion in sozialen Systemen – die auch trauma-
tisch sein kann – notwendigerweise einen Einfluss auf die Entwicklung der zentralen neurobiologischen Schmerzsysteme hat und dadurch wieder auf das soziale Verhalten Betroffener zurück wirkt. Hinweise dafür, dass sozialer Verlust und Ausschluss «schmerzhaft» sind und dabei die oben erwähnten Netzwerke eine wichtige Rolle spielen, finden sich in der Literatur (14, 15), was die eingangs aufgestellte Hypothese unterstützt, dass sich Seelisches im Körper abbildet – eine zentrale Forderung der Psychosomatik.
Soziale und Beziehungsaspekte von Schmerz: «The Pain-prone Patient»
Auf einer psychologischen Ebene wurden diese Phänomene bereits vor 50 Jahren in einer noch heute lesenswerten Publikation abgehandelt. Engel (16) beschrieb, wie Schmerz im Rahmen des gesunden und pathogenen entwicklungspsychologischen Prozesses die Rolle eines wichtigen Regulators einnimmt. Schmerzen sind notwendig, um die eigenen Grenzen in der Umwelt und damit auch diejenigen seines Körpers zu erfahren und überhaupt ein Körper- und Selbstbild zu entwickeln. Weiter spielen Schmer-
zen in der Beziehungsbildung eine
zentrale soziale Rolle. Erfährt ein
Kind Schmerz, und wird es getröstet
und damit seine Kränkung aufgeho-
ben, wird das Selbstwertgefühl ge-
stärkt. Weiter bekommt Schmerz
durch Bestrafung einer Missetat eine
moralische Wertung und wird zum
Signal für Schuld. Je nach Konstella-
tion – und dies kann der Anfang einer
pathologischen Entwicklung sein – ist
es möglich, dass Schmerz zu einem
wichtigen Sühnemittel wird.
Kinder psychisch kranker Eltern etwa
neigen dazu, die unbewusste «ewige
Schuld», diesen nicht helfen zu kön-
nen oder für deren Leiden gar verant-
wortlich zu sein, dadurch zu bewälti-
gen, dass sie sich ebenso unbewusst
«Sühne auferlegen», nicht selten in
Form von chronischen Schmerzen,
was das Schuldgefühl erträglicher
macht. Allerdings um den hohen Preis
einer masochistischen Haltung, wel-
che sich in der Folge auf das ganze
Wesen und damit auf sämtliche wich-
tigen Beziehungen übertragen wird.
Schliesslich spielen körperliche Schmer-
zen nach Engel bei Verlusten eine
wichtige Rolle. Sie dienen dazu, diese
nicht wahrnehmen zu müssen. Uner-
trägliche seelische Schmerzen wer-
den in den Körper projiziert und so
scheinbar neutralisiert.
◆
Dr. med. Kyrill Schwegler FMH Psychiatrie/Psychotherapie Vogelsangstrasse 52, 8032 Zürich
Interessenkonflikte: keine
Abbildung 1 mit freundlicher Genehmigung von Verlag und Autor. Aus: Ploner M, Freund HJ, Schnitzler A. Pain affect without pain sensation in a patient with a postcentral lesion. Pain. 1999 May; 81 (1–2): 211– 214. PubMed PMID: 10353510
Die Literaturliste ist zu finden in der Onlinefassung www.rosenfluh.ch/2009/psychiatrie-neurologie-nr.-03. 2009.html
Neurologie 3•2009
Fortbildung
Literatur: 1. Wall PD and Melzack R, Wall & Melzack's
Textbook of Pain. 2009, Elsevier. 2. Ploner M, Freund HJ, Schnitzler A. Pain affect
without pain sensation in a patient with a postcentral lesion. Pain, 1999. 81: 211– 214. 3. Rainville P et al. Pain Affect Encoded in Human Anterior Cingulate But Not Somatosensory Cortex. Science, 1997. 277: 968– 971. 4. Ploghaus A et al. Neural circuitry underlying pain modulation: expectation, hypnosis, placebo. Trends in Cognitive Sciences, 2003. 7: 197–200. 5. Ploghaus A et al. Exacerbation of pain by anxiety is associated with activity in a hippocampal network. Journal of Neuroscience, 2001. 21: 9896–9903. 6. Apkarian AV et al. Human brain mechanisms of pain perception and regulation in health and disease. European Journal of Pain, 2005. 9: 463–484.
7. Treede RD et al. The cortical representation of pain. Pain, 1999. 79: 105–111.
8. Linton SJ et al. A prospective study of the effects of sexual or physical abuse on back pain. Pain, 2002. 96: 347–351.
9. Linton SJ, Larden M, Gillow AM. Sexual abuse and chronic musculoskeletal pain: prevalence and psychological factors. Pain, 1997. 73: 47–53.
10. Asmundson GJ et al. PTSD and the experience of pain: research and clinical implications of shared vulnerability and mutual maintenance models. Can J Psychiatry, 2002. 47: 930–937.
11. Beckham JC et al. Chronic posttraumatic stress disorder and chronic pain in Vietnam combat veterans. Journal of Psychosomatic Research, 1997. 43: 379–389.
12. Sharp TJ, Harvey AG. Chronic pain and posttraumatic stress disorder: mutual maintenance? Clinical Psychology Review, 2001. 21: 857–877.
13. Meredith P, Ownsworth T, Strong J. A review of the evidence linking adult attachment theory and chronic pain: Presenting a conceptual model. Clinical Psychology Review, 2008. 28: 407–429.
14. Eisenberger NI, Lieberman MD, Williams KD. Does rejection hurt? An FMRI study of social exclusion. Science, 2003. 302: 290– 292.
15. Panksepp J. Neuroscience. Feeling the pain of social loss. Science, 2003. 302: 237– 239.
16. Engel GL. Psychogenic pain and pain-prone patient. Am J Med, 1959. 26: 899–918.
28
Neurologie 3•2009