Transkript
Referenzintervalle und Laboranforderungen
Problemlösungen für die pädiatrische Praxis
SCHWERPUNKT
«Kinder sind keine kleinen Erwachsenen» – dieses in vielfältiger Hinsicht strapazierte und daher fast schon zum Gemeinplatz verkommene Zitat des Entwicklungspsychologen Jean Piaget wird selbstverständlich auch auf die Labormedizin angewendet. In diesem Artikel werden spezifisch pädiatrische Probleme der Labordiagnostik, wie fehlende Referenzintervalle und limitierte Probenvolumina, erläutert und Lösungsansätze skizziert.
Von Christoph Seger
Selbst Anbieter von Labordienstleistungen scheuen nicht davor zurück, diese so wertvolle Aussage als Slogan zu nutzen, wenn es darum geht, eine Schwerpunktsetzung auf pädiatrische Labordiagnostik zu umwerben. In diesem Zusammenhang ist es durchaus legitim zu fragen: Pädiatrische Labordiagnostik – gibt es die denn überhaupt jenseits der Speziallaboratorien der Kinderkliniken in zentralen Versorgungszentren? Oder ist es nicht besser, einfach von der Berücksichtigung pädiatrischer Bedürfnisse in der Labormedizin zu sprechen? Im Folgenden wird versucht, dieser Frage anhand von zwei zentralen Aspekten der «pädiatrischen Labormedizin» auf den Grund zu gehen: einerseits dem Bezug individueller Laborergebnisse auf die in einer Referenzpopulation gefundenen Wertelagen – den sogenannten Referenzintervallen – und andererseits der Frage, wie die Begleitung beim Übergang von patientennaher Analytik beim Primärkontakt/in der Grundversorgung in die Spezialanalytik zentraler Versorgungszentren optimal gestaltet werden kann.
Generelle Referenzintervalle meist nicht möglich
Es ist allen Beteiligten klar: Das junge, sich entwickelnde Leben hat einen dynamischen Stoffwechsel, Reifungsprozesse begleiten den jungen Menschen in seinen zwei ersten Lebensjahrzehnten. So alt dieses qualitativ leicht fassbare biochemische Basiswissen ist, so problematisch ist in der quantitativen Welt der klinischen Chemie und Labormedizin offenbar seine Übersetzung in nach biologischer Reifung oder Lebensalter geschlechtsspezifisch stratifizierte Referenzintervalle (= Referenzbereiche) (1). Generell steht dem Anwender nur eine sehr limitierte Anzahl von Möglichkeiten zur Verfügung, derartige Vergleichswerte zu erhalten.
Im Regelfall, speziell im akkredierten Laborbereich, welcher sehr gerne auf IVD-CE-zertifizierte Kit-Lösungen namhafter Partner aus der IVD-Industrie zurückgreift, übernimmt man derartige Intervalle aus den analytischen Vorgabedokumenten des Herstellers. Dies gewinnt überall dort besondere Bedeutung, wo die Messmethode deutlichen Einfluss auf das quantitative Messergebnis hat, so zum Beispiel in weiten Bereichen der Endokrinologie (z.B. Steroide, Schilddrüsenhormone), aber auch in der auf immunologischen Messmethoden (Immunoassay) basierenden klinischen Chemie (z.B. Wachstumshormone), der Gerinnungsdiagnostik und in manchen Bereichen der Medikamentenspiegelmessung (z.B. Immunsuppressiva). Nur bei wenigen Ausnahmen – immer wenn die Messgrösse unabhängig von der Messmethode ist (z.B. bei Kennzahlen des weissen und roten Blutbildes) – ist es möglich, generalisierte Referenzintervalle anzugeben. Diese finden ab und an sogar den Weg in einschlägige Lehrbücher der Labormedizin oder der Pädiatrie. Bei diesen tabellarischen Aufbereitungen der Sekundärliteratur muss penibel darauf geachtet werden, welche Primärliteratur den oftmals elegant aufbereiteten Daten zugrunde liegt. Besonders heikel wird es, wenn Hersteller von IVD-CE-zertifizierten Testsystemen auf derartige Standardwerke Bezug nehmen und der Anwender sich in Sicherheit wiegt. So durfte der Autor dieser Zeilen in jüngster Vergangenheit feststellen, dass man einen sich bei einem auf Massenspektrometrie (LC-MS/MS) basierten kommerziellen Steroidassay auf ein ausserordentlich bekanntes und renommiertes Kompendium pädiatrischer Referenzintervalle berufen hat – die Nachschau in dieser Quelle hat jedoch ergeben, dass jeglicher Eintrag auf immunologischen Messmethoden beruht und daher für die LC-MS/MS-Messung sicherlich nur einen sehr groben Bezugsrahmen darstellen kann.
2/17
Referenzintervalle gelten häufig nur für eine bestimmte Analysenplattform.
7
SCHWERPUNKT
Abbildung 1: Die CALIPER-Homepage bietet Zugriff auf pädiatrische Referenzintervalle. (www.sickkids.ca/Caliperproject/intervals/index.html)
Immer öfter findet sich der Anbieter von Labordienstleistungen – sei es im öffentlichen Dienst, sei es im niedergelassenen Sektor – mit der Situation konfrontiert, dass ein IVD-Hersteller in seinen Produktunterlagen die von ihm (eigentlich verbindlich) vorgegebenen Referenzintervalle mit der Randnotiz unterläuft, dass der Nutzer angehalten ist, derartige Referenzintervalle selbst zu erarbeiten. Die damit verbundenen Probleme werden in den folgenden Absätzen abgehandelt.
Referenzintervalle bestimmen
Nur bei wenigen Ausnahmen, diese finden sich in der Regel im Bereich der Endokrinologie und bei neuen Testentwicklungen, sorgt ein Hersteller auch für die Erarbeitung von ausreichend wissenschaftlich fundierten Referenzintervallen. Als exemplarisch sei hier die Etablierung eines neuen IGF-1-Assays genannt, dessen veränderte (fortschrittliche) Testchemie eine komplette Neubewertung der Referenzintervalle erfordert hat (2). Ein offener Umgang mit diesem Thema, das heisst die aktive wissenschaftliche Publikation derartiger Unternehmungen, kann als ein hervorragendes Marketingmittel angesehen werden – ist doch kaum etwas überzeugender als der anerkannte Fachkollege.
Referenzintervalle
Referenzintervalle bilden die zentralen 95-Prozent-Perzentile der Referenzpopulation ab. Es besteht immer eine 5-prozentige Wahrscheinlichkeit, dass individuelle Werte eines klinisch Gesunden ausserhalb des Referenzintervalls zu liegen kommen. Die Auslenkung aus dem Referenzintervall kann nicht immer mit der Schwere einer Erkrankung/Pathologie korreliert werden; sie haben daher orientierenden Charakter.
Nur wiederholtes Testen (die Wahrscheinlichkeit, dass die Bestätigungsmessung aus einer unabhängigen Abnahme auch ausserhalb des Referenzintervalls liegt, ist kleiner 1/1000) oder die Zusammenschau mit pathophysiologisch korrelierten Messgrössen erlaubt es bereits bei minimaler Auslenkung, aus dem Referenzintervall pathophysiologisches Geschehen zu diagnostizieren.
Liegen derartige Daten nicht vor und ist der Referenzintervallvorschlag des Herstellers insuffizient belegt oder an einer offensichtlich ungeeigneten Referenzpopulation erarbeitet, muss versucht werden, die benötigte Information anderweitig zu erarbeiten. Dies ist bei gesunden Erwachsenen zwar ein gewisser Aufwand, aber in der Regel möglich, zum Beispiel als Nebenprodukt von Populationsquerschnittsstudien. Bei pädiatrischen Populationen sieht sich der forschende Diagnostiker hingegen mit deutlich höheren Hürden konfrontiert. Eine davon ist sicherlich die Frage, ob eine Entnahme von zusätzlichem Blutvolumen bei aparent gesunden Kindern einzig zur Erarbeitung von (dann vielleicht nur lokal gültigen) Referenzintervallen nicht ein grundsätzliches medizinethisches Veto impliziert. Vielleicht auch aus diesem Grund ist die Zahl internationaler Unternehmungen zur Etablierung von pädiatrischen Referenzintervallen, wenngleich hervorragend organisiert und ergebnisorientiert durchgeführt, durchaus überschaubar. Die IFCC (International Federation of Clinical Chemistry and Laboratory Medicine) hat mit der Gründung der Task Force on Paediatric Laboratory Medicine (TF-PLM) (www.ifcc.org/taskforce-paediatric-laboratory-medicine-web-pages/) vor mehr als zehn Jahren eine Plattform geschaffen, welche sich im Rahmen einer Initiative der Erarbeitung pädiatrischer Referenzintervalle widmet. Diese Initiative bündelt und koordiniert nationale und regionale Initiativen, um so wissenschaftlich sauber und nachvollziehbar zu verbesserten Referenzintervallen zu kommen. Das bedeutet unter anderem die Ergebnispublikation unter Peer-Review-Bedingungen – ein Aufwand, den die IVD-Industrie nur selten betreibt.
Das CALIPER*-Projekt
Einer der bedeutendsten Vorstösse in dieser Richtung gelang einem Konsortium kanadischer Forscher, bekannt unter dem Akronym CALIPER (Canadian Laboratory Initiative on Paediatric Reference Intervals) (3). Die multizentrische CALIPER-Gruppe (www.sick-kids.ca/ caliperproject/) konnte nach einer mehrjährigen Vorlaufzeit im vergangenen Jahrzehnt auf der Basis von rund 9000 Proben von gesunden Kindern für an die 100 Parameter, in der Hauptsache aus den Bereichen der klinischen Chemie, der Endokrinologie und der Immunologie, alters- und geschlechtsspezifische Referenzintervalle mittels der sogenannten direkten Methode, das heisst durch Etablierung eines Referenzkollektivs, erarbeiten. Die Bearbeitung der Rohwerte und die Etablierung der Referenzintervalle wurden in rund zwei Dutzend Publikationen der Fachöffentlichkeit transparent und nachvollziehbar präsentiert; alle erarbeiteten Referenzintervalle sind auf der CALIPER-Homepage inklusive Grafiken (Abbildung 1 und 2) der Öffentlichkeit zugänglich. Eingeschränkt wird die Nutzbarkeit der Daten im Moment durch die Tatsache, dass die Intervalle streng genommen nur für die Analysenplattform/die AssayChemie gelten, auf welcher sie erarbeitet worden sind
* Caliper: engl. Messschieber
8 2/17
SCHWERPUNKT
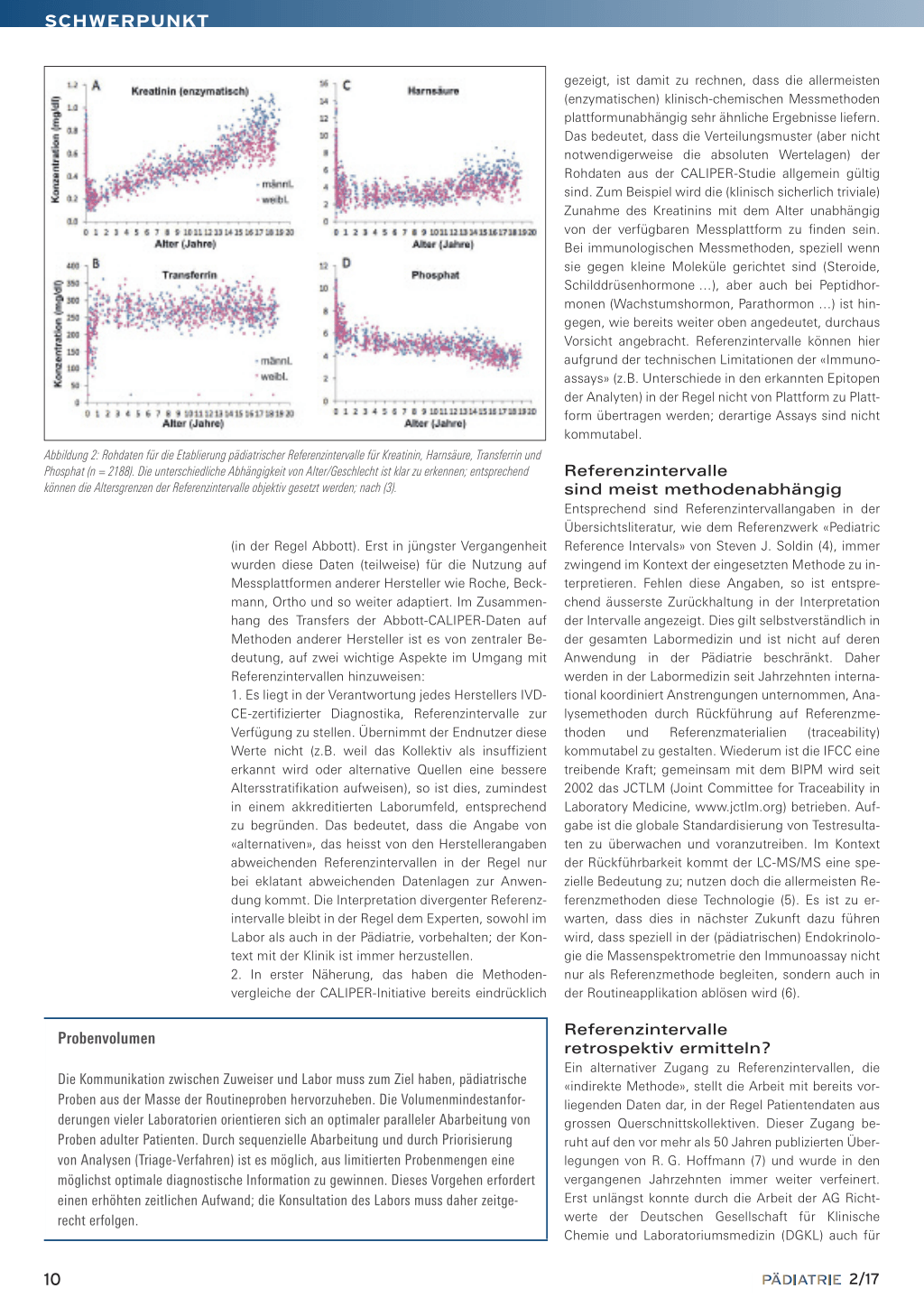
Abbildung 2: Rohdaten für die Etablierung pädiatrischer Referenzintervalle für Kreatinin, Harnsäure, Transferrin und Phosphat (n = 2188). Die unterschiedliche Abhängigkeit von Alter/Geschlecht ist klar zu erkennen; entsprechend können die Altersgrenzen der Referenzintervalle objektiv gesetzt werden; nach (3).
(in der Regel Abbott). Erst in jüngster Vergangenheit wurden diese Daten (teilweise) für die Nutzung auf Messplattformen anderer Hersteller wie Roche, Beckmann, Ortho und so weiter adaptiert. Im Zusammenhang des Transfers der Abbott-CALIPER-Daten auf Methoden anderer Hersteller ist es von zentraler Bedeutung, auf zwei wichtige Aspekte im Umgang mit Referenzintervallen hinzuweisen: 1. Es liegt in der Verantwortung jedes Herstellers IVDCE-zertifizierter Diagnostika, Referenzintervalle zur Verfügung zu stellen. Übernimmt der Endnutzer diese Werte nicht (z.B. weil das Kollektiv als insuffizient erkannt wird oder alternative Quellen eine bessere Altersstratifikation aufweisen), so ist dies, zumindest in einem akkreditierten Laborumfeld, entsprechend zu begründen. Das bedeutet, dass die Angabe von «alternativen», das heisst von den Herstellerangaben abweichenden Referenzintervallen in der Regel nur bei eklatant abweichenden Datenlagen zur Anwendung kommt. Die Interpretation divergenter Referenzintervalle bleibt in der Regel dem Experten, sowohl im Labor als auch in der Pädiatrie, vorbehalten; der Kontext mit der Klinik ist immer herzustellen. 2. In erster Näherung, das haben die Methodenvergleiche der CALIPER-Initiative bereits eindrücklich
gezeigt, ist damit zu rechnen, dass die allermeisten (enzymatischen) klinisch-chemischen Messmethoden plattformunabhängig sehr ähnliche Ergebnisse liefern. Das bedeutet, dass die Verteilungsmuster (aber nicht notwendigerweise die absoluten Wertelagen) der Rohdaten aus der CALIPER-Studie allgemein gültig sind. Zum Beispiel wird die (klinisch sicherlich triviale) Zunahme des Kreatinins mit dem Alter unabhängig von der verfügbaren Messplattform zu finden sein. Bei immunologischen Messmethoden, speziell wenn sie gegen kleine Moleküle gerichtet sind (Steroide, Schilddrüsenhormone …), aber auch bei Peptidhormonen (Wachstumshormon, Parathormon …) ist hingegen, wie bereits weiter oben angedeutet, durchaus Vorsicht angebracht. Referenzintervalle können hier aufgrund der technischen Limitationen der «Immunoassays» (z.B. Unterschiede in den erkannten Epitopen der Analyten) in der Regel nicht von Plattform zu Plattform übertragen werden; derartige Assays sind nicht kommutabel.
Referenzintervalle sind meist methodenabhängig
Entsprechend sind Referenzintervallangaben in der Übersichtsliteratur, wie dem Referenzwerk «Pediatric Reference Intervals» von Steven J. Soldin (4), immer zwingend im Kontext der eingesetzten Methode zu interpretieren. Fehlen diese Angaben, so ist entsprechend äusserste Zurückhaltung in der Interpretation der Intervalle angezeigt. Dies gilt selbstverständlich in der gesamten Labormedizin und ist nicht auf deren Anwendung in der Pädiatrie beschränkt. Daher werden in der Labormedizin seit Jahrzehnten international koordiniert Anstrengungen unternommen, Analysemethoden durch Rückführung auf Referenzmethoden und Referenzmaterialien (traceability) kommutabel zu gestalten. Wiederum ist die IFCC eine treibende Kraft; gemeinsam mit dem BIPM wird seit 2002 das JCTLM (Joint Committee for Traceability in Laboratory Medicine, www.jctlm.org) betrieben. Aufgabe ist die globale Standardisierung von Testresultaten zu überwachen und voranzutreiben. Im Kontext der Rückführbarkeit kommt der LC-MS/MS eine spezielle Bedeutung zu; nutzen doch die allermeisten Referenzmethoden diese Technologie (5). Es ist zu erwarten, dass dies in nächster Zukunft dazu führen wird, dass speziell in der (pädiatrischen) Endokrinologie die Massenspektrometrie den Immunoassay nicht nur als Referenzmethode begleiten, sondern auch in der Routineapplikation ablösen wird (6).
Probenvolumen
Die Kommunikation zwischen Zuweiser und Labor muss zum Ziel haben, pädiatrische Proben aus der Masse der Routineproben hervorzuheben. Die Volumenmindestanforderungen vieler Laboratorien orientieren sich an optimaler paralleler Abarbeitung von Proben adulter Patienten. Durch sequenzielle Abarbeitung und durch Priorisierung von Analysen (Triage-Verfahren) ist es möglich, aus limitierten Probenmengen eine möglichst optimale diagnostische Information zu gewinnen. Dieses Vorgehen erfordert einen erhöhten zeitlichen Aufwand; die Konsultation des Labors muss daher zeitgerecht erfolgen.
Referenzintervalle retrospektiv ermitteln?
Ein alternativer Zugang zu Referenzintervallen, die «indirekte Methode», stellt die Arbeit mit bereits vorliegenden Daten dar, in der Regel Patientendaten aus grossen Querschnittskollektiven. Dieser Zugang beruht auf den vor mehr als 50 Jahren publizierten Überlegungen von R. G. Hoffmann (7) und wurde in den vergangenen Jahrzehnten immer weiter verfeinert. Erst unlängst konnte durch die Arbeit der AG Richtwerte der Deutschen Gesellschaft für Klinische Chemie und Laboratoriumsmedizin (DGKL) auch für
10 2/17
SCHWERPUNKT
pädiatrische Kollektive eindrücklich gezeigt werden, dass aus durchaus überschaubar grossen retrospektiven Datensammlungen (rund 50 000–200 000 Einzelmessungen an einem tertiären Versorgungszentrum, Beobachtungszeitraum 5–10 Jahre) wertvolle kontinuierliche Referenzintervalldaten gewonnen werden können (8), welche durch entsprechend sinnvolle Interpretation natürlich auch einer Alters- und Geschlechtsstratifikation unterzogen werden können (9). Beide Zugänge, die «direkte» wie auch die «indirekte» Methode haben ihre Vor- und Nachteile. Der interessierte Leser sei an dieser Stelle auf eine aktuelle Diskussion hingewiesen, welche durch Empfehlungen der EFLM (10) zur Durchführung von «direkten Methoden» hervorgerufen worden ist (11).
Wie viel Probenmaterial muss es wirklich sein?
Wann immer einem Kleinkind oder gar einem Säugling Blut für die Erarbeitung von Laborresultaten entnommen wird, sieht sich der Praktiker oft mit der unangenehmen Frage konfrontiert: «Reicht das Material aus?» Im Rahmen der Grundversorgung kann er dieses Problem im Griff behalten; seine hauseigenen POC(Point-of-Care-)Gerätschaften sind ihm wohlbekannt und darauf optimiert, aus einer möglichst kleinen Probenmenge ein Maximum an Information zu erhalten, allerdings beschränkt auf wenige Notfallparameter (in der Regel Blutbild, CRP, Basisanalytik des Harns etc.). Sollte es für die weitere Abklärung einer Erkrankung nicht notwendig sein, den kleinen Patienten in die Obhut eines tertiären Versorgungszentrums mit einem in der Regel an die Bedürfnisse einer Pädiatrie gewöhnten Zentrallabor zu überstellen, sieht sich der Mediziner für gewöhnlich mit niedergelassenen Laboratorien konfrontiert. Da diese auf den raschen Durchsatz grosser Probenmengen optimiert sind, werden in der Regel Blutproben eines Auftrages parallel auf mehrere Analysegeräte verteilt. Die Verteilungsroutinen sind geregelt; die Labor-EDV verwaltet diesen Vorgang. Da Gerätschaften üblicherweise neben dem eigentlichen Messaliquot ein vorgegebenes Totvolumen in der Grössenordnung von mehreren Dutzend Mikroliter Probenvolumen aufweisen, ist diese Strategie nicht sehr materialsparend ausgelegt. Es stehen zwar in der Regel eigene Sekundärgefässe für mengenlimitierte Proben zur Verfügung, ein gewisses notwendiges Minimalvolumen kann aber nicht unterschritten werden. Werden notwendige Probenvolumina an den Zuweiser kommuniziert, enthalten diese oftmals einen zusätzlichen Sicherheitsaufschlag, falls eine Wiederholungsmessung, eine Verdünnungsmessung oder eine weiterführende Analytik notwendig sein sollte. All dies ist natürlich dem Anspruch entgegengerichtet, bei Kindern möglichst kleine Probenmengen einzusetzen. Auch muss konstatiert werden, dass die pädiatrische Probe im Routinelabor eklatant in der Minderzahl ist; die notwendige spezielle Behandlung im Sinne optimaler Probennutzung wird daher leicht übersehen.
Blut sparen durch sequenzielle Analysen
Aus dem soeben Gesagten sollte klar ersichtlich sein, welche Massnahmen geeignet sind, wertvolle pädiatrische Proben optimal der Laboranalytik zuzuführen. Seitens des Labors muss es die Möglichkeit geben, die parallele Abarbeitung durch (mit längeren Analysezeiten verbundenes) sequenzielles Abarbeiten zu ersetzen. Die notwendige Minimalmenge für die Messungen selbst muss berechnet werden können, verbleibendes Material aus dem Totvolumen soll gegebenenfalls Tests mit manuellen Abarbeitungsroutinen (z.B. Vitaminanalytik) zugeführt werden. Nach Möglichkeit sollte die Zahl der aus Blut gewonnenen Proben auf 1 bis 2 reduziert werden; zum Beispiel kann aus einer EDTA-Vollblutprobe, welche für ein Blutbild benötigt wird, nach erfolgreicher Analyse ein EDTA-Plasma gewonnen werden, aus welchem ein Gutteil der klinischchemischen Analytik abgearbeitet werden kann.
Prioritäten setzen
Der Kommunikation zwischen Zuweiser und Labor kommt daher bei der erfolgreichen Abarbeitung von pädiatrischem Probenmaterial eine zentrale Bedeutung zu. Wenn immer möglich, sollte der Zuweiser vorab das Labor kontaktieren, wenn er der Meinung ist, dass die verfügbare Probenmenge nicht mit der vom Labor kommunizierten Probenmenge übereinstimmt, das heisst ein Probenmangel sehr wahrscheinlich ist. In derartigen Fällen ist möglichst a priori, das heisst vor der Probengewinnung, im Rahmen einer zeitgerechten Konsultation ein Abarbeitungsplan zu erstellen; eine Prioritätenliste der Analysen sollte angelegt werden. Der Zuweiser ist dabei darauf hinzuweisen, dass es bei einer derartigen Vorgangsweise in der Regel nicht möglich sein wird, weiterführende Analytik oder Analysenachforderungen zu tätigen. Das Labor soll durch den Zuweiser möglichst deutlich und durchgängig auf derartige «Problemfälle» hingewiesen werden. Es ist durchaus angezeigt, pädiatrische Aufträge/Proben auffällig zu markieren und zusätzliche Hinweise auf die diagnostische Problemstellung oder auf die Limitation der Probenmenge zu geben. Klare Anweisungen, welche Analysen bei Probenmangel prioritär abzuarbeiten sind, werden es dem Labor erlauben, auf die individuellen Bedürfnisse des Zuweisers optimal einzugehen.
Zusammenfassung
• Die pädiatrischen Aspekte der Labordiagnostik betreffen nicht nur das hoch spezialisierte Labor der Kinderkliniken, sie sind im hektischen Treiben der Routinelaboratorien genauso von Bedeutung. Es ist sowohl seitens des Zuweisers als auch des Labors notwendig, auf die speziellen Aspekte der Proben von Kindern hinzuweisen.
• Durch Konsultationsgespräche zwischen Zuweiser und Labor muss es ermöglicht werden, aus minimalem Probenvolumen das Maximum an klinisch verwertbarer Information zu gewinnen.
• Eine zentrale Bedeutung kommt dem möglichst nach Alter und Geschlecht stratifizierten Referenz-
2/17
Zuweiser und Labor sollten Prioritäten setzen und einen Abarbeitungsplan erstellen.
11
SCHWERPUNKT
intervallen zu. Hier haben die letzten Jahre grosse inhaltliche Fortschritte gebracht, in vielen Bereichen ist aber noch Arbeit zu leisten, speziell in der Endokrinologie. • Abschliessend wird festgestellt, dass es wohl von Vorteil ist, die pädiatrische Labormedizin jenseits der hoch spezialisierten pädiatrischen Laboratorien der zentralen Versorgungseinheiten als einen integrativen Teil der Labormedizin zu begreifen – Probenmaterialien und Wertelagen, welche einer speziellen, gezielten Aufmerksamkeit des involvierten Fachpersonals bedürfen.
Korrespondenzadresse: PD Dr. rer. nat. Christoph Seger labormedizinisches zentrum Dr Risch AG Lagerstrasse 30 9470 Buchs E-Mail: christoph.seger@risch.ch
Literatur: 1. Sikaris KA: Physiology and its importance for reference intervals. Clin Biochem Rev 2014; 35: 3–14. 2. Bidlingmaier M et al.: Reference intervals for insulin-like growth factor-1 (IGF-I) from birth to senescence: results from a multicenter study using a new automated chemiluminescence IGF-I immunoassay conforming to recent international recommendations. J Clin Endocrinol Metab 2014; 99: 1712–1721. 3. Colantonio DA et al.: Closing the gaps in pediatric laboratory reference intervals: a CALIPER database of 40 biochemical markers in a healthy and multiethnic population of children. Clin Chem 2012; 58: 854–868. 4. Soldin SJ (ed.): Pediatric Reference Intervals. 6th edition 2007, AACC Press. 5. Kessler A: Mass spectrometry – a key technique for traceability in clinical chemistry. TrAC Trend Anal Chem 2016; 84: 74–79. 6. Vogeser M, Seger C: Mass spectrometry methods in clinical diagnostics – state of the art and perspectives. TrAC Trend Anal Chem 2016; 84: 1–4. 7. Hoffmann RG: Statistics in the practice of medicine. JAMA 1963; 185: 150–159. 8. Zierk J et al.: Age- and sex-specific dynamics in 22 hematologic and biochemical analytes from birth to adolescence. Clin Chem 2015; 61: 964–973. 9. Zierk J et al.: Pediatric reference intervals for alkaline phosphatase. Clin Chem Lab Med 2017; 55: 102–110. 10. Henny J et al.: Working Group Accreditation and ISO/CEN standards (WG-A/ISO) of the EFLM: Recommendation for the review of biological reference intervals in medical laboratories. Clin Chem Lab Med 2016; 54: 1893–1900. 11. Haeckel R et al.: Critical comments to a recent EFLM recommendation for the review of reference intervals. Clin Chem Lab Med 2017; 55: 341–347.
BUCHTIPP
«Mama, bin ich behindert?»
Mit dieser Frage schafft es der 10-jährige Leo, seine Mutter auch nach zehn Jahren Alltag mit ihrem Sohn für kurze Zeit aus der Fassung zu bringen. Da schreibt die Autorin bereits an ihrem Buch «Mein Löwenkind – vom Abenteuer, ein Kind mit Handicap grosszuziehen».
L eo wird als Säugling im Alter von vier Wochen adoptiert, nach einer schwierigen Schwangerschaft, Frühgeburt und Beatmung. Zunächst scheint er sich normal zu entwickeln, doch nach und nach müssen seine Eltern erkennen, dass er sich langsamer entwickelt als andere Kinder: «Vom Gift des Vergleichs und der Kraft der Illusion» lautet der Untertitel dieses Kapitels, in dem sich, wie in den anderen Kapiteln auch, sicher viele Eltern wiederfinden werden – und zwar nicht nur solche, die Kinder wie Leo haben.
Im Kindergartenalter erhält Leo die Diagnose
«frühkindliche Zerebralparese», wobei nur die
Kleinhirnfunktion und damit seine motorischen
Fähigkeiten eingeschränkt sind. Leo und seine
Eltern meistern letztlich alle Schwierigkeiten.
Der Leser begleitet die Familie vom Säuglings-
bis zum fortgeschrittenen Schulalter, als Leo mit
seinem Vater zu diskutieren beginnt, ob es wohl
wichtiger sei, einen Beruf oder eine Frau zu
haben …
Der Autorin ist es gelungen, den Elternalltag auf
den Punkt zu bringen. Was Leo und seine Eltern
in Kindergarten und Schule mit anderen
Kindern, Erzieherinnen und Lehrern erleben,
kennen auch Kinder ohne Handicap und ihre
Eltern – nur dass die Probleme durch Leos
Behinderung besonders scharf gezeichnet er-
scheinen. Ein berührendes und ermutigendes
Buch, das zum Lachen bringt, aber auch nach-
denklich macht. Lesenwert – nicht nur für Eltern
von Kindern mit einem Handicap.
RBO
Elena Pirin: Mein Löwenkind 216 Seiten, Patmos-Verlag ISBN 978-3-8436-0767-4: gebunden, Fr. 28.90 ISBN 978-3-8436-0768-1: eBook, Fr. 18.50
12
2/17