Transkript
Asthma bei Kindern
Fallstricke und Fingerzeige
PNEUMOLOGIE
Etwa 10 Prozent der Kleinkinder haben obstruktive Bronchitiden. Etwa 5 bis 8 Prozent der Schulkinder und ähnlich viele Jugendliche haben Asthma. Trotz dieser Häufigkeit sind viele Kinder mit Asthma nicht diagnostiziert und/oder insuffizient behandelt. Umgekehrt gibt es nicht selten Kinder, die eine Asthmadiagnose haben und entsprechend behandelt werden, obwohl bei ihnen ein anderes Problem vorliegt.
Von Stephan Illing
V om Kleinkindesalter bis zum Jugendlichen gibt es einen deutlichen Wandel in der Asthmasymptomatik, bei den typischen Auslösern, bei der Prognose und letztlich auch bei den therapeutischen Möglichkeiten. Einen akuten Asthmaanfall beim Schulkind oder Jugendlichen wird der Allgemeinarzt mit Sicherheit erkennen (Giemen mit verlängertem Exspirium, trockener Husten, Überblähung, Benutzung der Atemhilfsmuskulatur, bei schwerem Anfall Unruhe, Zyanose, Bewusstseinsstörung; cave «stille Obstruktion» mit leisem Atemgeräusch). Im Intervall oder bei chronischem Asthma sind die Kinder klinisch oft völlig unauffällig. In den meisten Situationen ist das Atemgeräusch normal, Einziehungen sieht man selten, eine Thoraxdeformierung kann auch andere Gründe haben. Indirekte Hinweise wie eine begleitende atopische Dermatitis haben nur vergleichsweise wenige ältere Kinder oder Jugendliche. Erst nach körperlicher Belastung oder Allergenkontakt zeigen sich Symptome. Die Sicherung der Asthmadiagnose erfolgt durch: • Anamnese: Wann? Wie oft? Welche Symptome? Welche Auslöser? Nachts? Vorhandene Umgebungsfaktoren wie Tiere, Schimmel und so weiter? Welche Therapie bisher? Effekt? • Lungenfunktionstest mit Laufbelastung (oder unspezifischer Provokationstest) und gegebenenfalls Broncholysetest • eventuell FeNO (fraktioniertes exhaliertes Stickstoffmonoxid) • Allergietestung • weitere Diagnostik wie Röntgenthorax, CO-Diffusion, invasive Diagnostik et cetera, nur in Einzelfällen, zum Bespiel, wenn prinzipielle Zweifel an der Asthmadiagnose bestehen oder bei atypischem Verlauf.
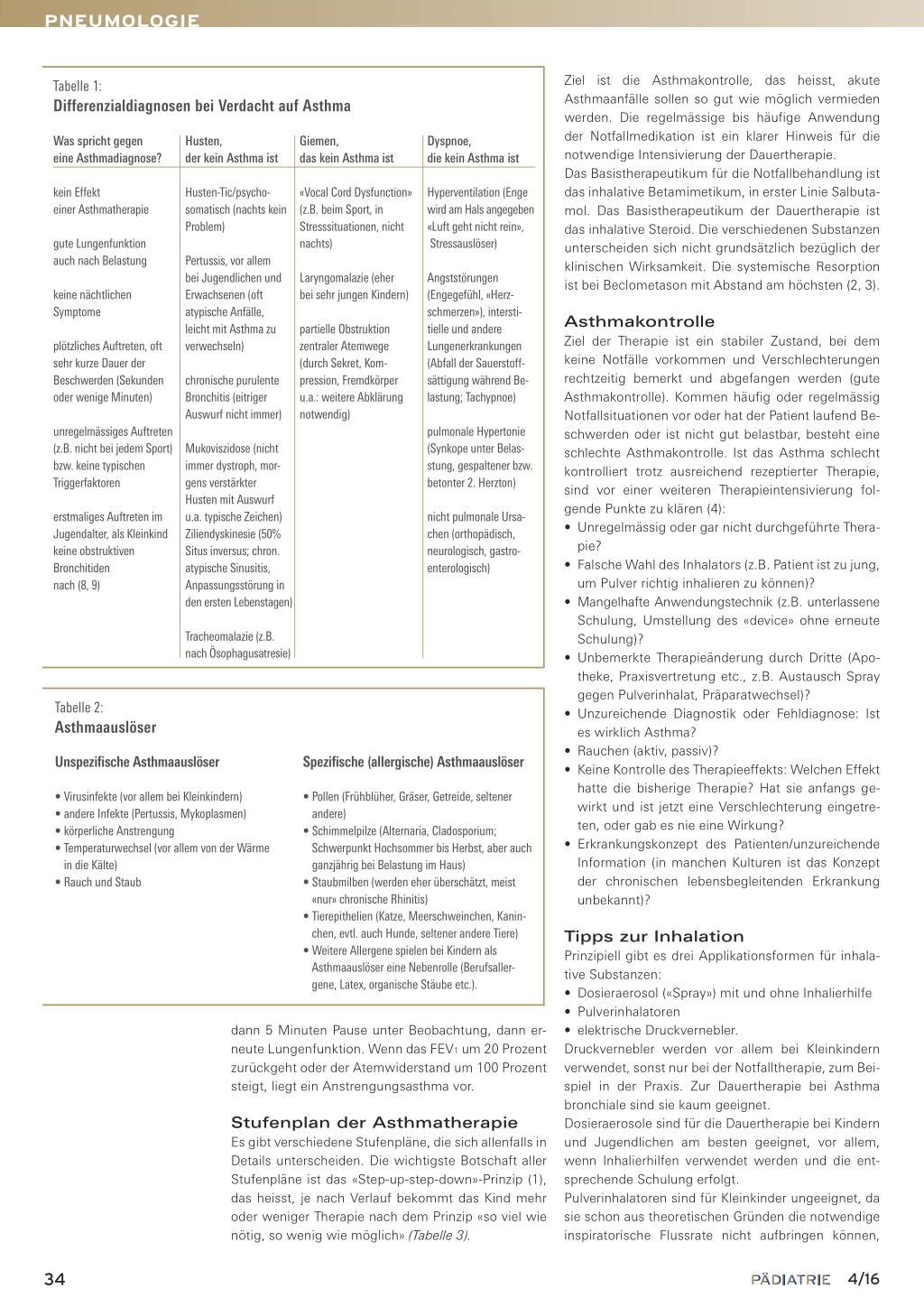
Differenzialdiagnosen bei Verdacht auf Asthma sind in Tabelle 1 zusammengefasst.
Asthmaauslöser
Bei Kleinkindern werden die allermeisten Episoden bronchialer Obstruktion durch Infekte ausgelöst, in erster Linie durch Virusinfekte. Auch später sind solche Virusinfektionen potente Asthmaauslöser. Die Infektfrequenz lässt ab dem Grundschulalter deutlich nach, sodass die infektbedingten Asthmaepisoden relativ an Bedeutung verlieren. Es gibt schon bei sehr kleinen Kindern Inhalationsallergien, doch sind das eher Ausnahmen. In Prick-Test und RAST lassen sich zwar immer wieder schon Sensibilisierungen zeigen, die aber oft keine klinische Relevanz haben. Ab dem Schulalter nimmt die Bedeutung allergischer Asthmaauslöser dann sehr deutlich zu. In jeder Altersstufe muss man zwischen unspezifischen und allergischen Auslösern unterscheiden (Tabelle 2).
Sinnvolle Diagnostik für Auslöser
Die Allergietestung richtet sich nach der Anamnese beziehungsweise der alterstypischen «Hitliste»: Pollenallergene, Tierepithelien und Staubmilben sind am häufigsten, aber auch Alternaria, weitere Schimmelpilze und alle anderen Inhalationsallergene können eine Rolle spielen. Nahrungsmittelreaktionen (z.B. auf Obst) kommen als Kreuzreaktion vor (z.B. bei Birkenpollenallergie) oder führen nicht nur zu Asthma, sondern auch zu Urtikaria und gastrointestinalen Symptomen. Die Diagnostik mit Laufbelastung wird folgendermassen durchgeführt: Lungenfunktion in Ruhe, dann 8 Minuten Laufen im Joggingtempo unter Beobachtung (Husten oder Giemen bereits während des Laufens? Dyspnoe? Atemtechnik? Keine «Schleichbelastung»?),
4/16
Man muss zwischen unspezifischen und allergenen Auslösern unterscheiden.
33
PNEUMOLOGIE
Tabelle 1: Differenzialdiagnosen bei Verdacht auf Asthma
Was spricht gegen
Husten,
Giemen,
eine Asthmadiagnose? der kein Asthma ist das kein Asthma ist
Dyspnoe, die kein Asthma ist
kein Effekt einer Asthmatherapie
gute Lungenfunktion auch nach Belastung
keine nächtlichen Symptome
plötzliches Auftreten, oft sehr kurze Dauer der Beschwerden (Sekunden oder wenige Minuten)
unregelmässiges Auftreten (z.B. nicht bei jedem Sport) bzw. keine typischen Triggerfaktoren
erstmaliges Auftreten im Jugendalter, als Kleinkind keine obstruktiven Bronchitiden nach (8, 9)
Husten-Tic/psychosomatisch (nachts kein Problem)
Pertussis, vor allem bei Jugendlichen und Erwachsenen (oft atypische Anfälle, leicht mit Asthma zu verwechseln)
chronische purulente Bronchitis (eitriger Auswurf nicht immer)
«Vocal Cord Dysfunction» (z.B. beim Sport, in Stresssituationen, nicht nachts)
Laryngomalazie (eher bei sehr jungen Kindern)
partielle Obstruktion zentraler Atemwege (durch Sekret, Kompression, Fremdkörper u.a.: weitere Abklärung notwendig)
Mukoviszidose (nicht immer dystroph, morgens verstärkter Husten mit Auswurf u.a. typische Zeichen) Ziliendyskinesie (50% Situs inversus; chron. atypische Sinusitis, Anpassungsstörung in den ersten Lebenstagen)
Hyperventilation (Enge wird am Hals angegeben «Luft geht nicht rein», Stressauslöser)
Angststörungen (Engegefühl, «Herzschmerzen»), interstitielle und andere Lungenerkrankungen (Abfall der Sauerstoffsättigung während Belastung; Tachypnoe)
pulmonale Hypertonie (Synkope unter Belasstung, gespaltener bzw. betonter 2. Herzton)
nicht pulmonale Ursachen (orthopädisch, neurologisch, gastroenterologisch)
Tracheomalazie (z.B. nach Ösophagusatresie)
Tabelle 2: Asthmaauslöser
Unspezifische Asthmaauslöser
• Virusinfekte (vor allem bei Kleinkindern) • andere Infekte (Pertussis, Mykoplasmen) • körperliche Anstrengung • Temperaturwechsel (vor allem von der Wärme • in die Kälte) • Rauch und Staub
Spezifische (allergische) Asthmaauslöser
• Pollen (Frühblüher, Gräser, Getreide, seltener • andere) • Schimmelpilze (Alternaria, Cladosporium; •Schwerpunkt Hochsommer bis Herbst, aber auch • ganzjährig bei Belastung im Haus) • Staubmilben (werden eher überschätzt, meist • «nur» chronische Rhinitis) • Tierepithelien (Katze, Meerschweinchen, Kanin•chen, evtl. auch Hunde, seltener andere Tiere) • Weitere Allergene spielen bei Kindern als •Asthmaauslöser eine Nebenrolle (Berufsaller•gene, Latex, organische Stäube etc.).
dann 5 Minuten Pause unter Beobachtung, dann erneute Lungenfunktion. Wenn das FEV1 um 20 Prozent zurückgeht oder der Atemwiderstand um 100 Prozent steigt, liegt ein Anstrengungsasthma vor.
Stufenplan der Asthmatherapie
Es gibt verschiedene Stufenpläne, die sich allenfalls in Details unterscheiden. Die wichtigste Botschaft aller Stufenpläne ist das «Step-up-step-down»-Prinzip (1), das heisst, je nach Verlauf bekommt das Kind mehr oder weniger Therapie nach dem Prinzip «so viel wie nötig, so wenig wie möglich» (Tabelle 3).
Ziel ist die Asthmakontrolle, das heisst, akute Asthmaanfälle sollen so gut wie möglich vermieden werden. Die regelmässige bis häufige Anwendung der Notfallmedikation ist ein klarer Hinweis für die notwendige Intensivierung der Dauertherapie. Das Basistherapeutikum für die Notfallbehandlung ist das inhalative Betamimetikum, in erster Linie Salbutamol. Das Basistherapeutikum der Dauertherapie ist das inhalative Steroid. Die verschiedenen Substanzen unterscheiden sich nicht grundsätzlich bezüglich der klinischen Wirksamkeit. Die systemische Resorption ist bei Beclometason mit Abstand am höchsten (2, 3).
Asthmakontrolle
Ziel der Therapie ist ein stabiler Zustand, bei dem keine Notfälle vorkommen und Verschlechterungen rechtzeitig bemerkt und abgefangen werden (gute Asthmakontrolle). Kommen häufig oder regelmässig Notfallsituationen vor oder hat der Patient laufend Beschwerden oder ist nicht gut belastbar, besteht eine schlechte Asthmakontrolle. Ist das Asthma schlecht kontrolliert trotz ausreichend rezeptierter Therapie, sind vor einer weiteren Therapieintensivierung folgende Punkte zu klären (4): • Unregelmässig oder gar nicht durchgeführte Thera-
pie? • Falsche Wahl des Inhalators (z.B. Patient ist zu jung,
um Pulver richtig inhalieren zu können)? • Mangelhafte Anwendungstechnik (z.B. unterlassene
Schulung, Umstellung des «device» ohne erneute Schulung)? • Unbemerkte Therapieänderung durch Dritte (Apotheke, Praxisvertretung etc., z.B. Austausch Spray gegen Pulverinhalat, Präparatwechsel)? • Unzureichende Diagnostik oder Fehldiagnose: Ist es wirklich Asthma? • Rauchen (aktiv, passiv)? • Keine Kontrolle des Therapieeffekts: Welchen Effekt hatte die bisherige Therapie? Hat sie anfangs gewirkt und ist jetzt eine Verschlechterung eingetreten, oder gab es nie eine Wirkung? • Erkrankungskonzept des Patienten/unzureichende Information (in manchen Kulturen ist das Konzept der chronischen lebensbegleitenden Erkrankung unbekannt)?
Tipps zur Inhalation
Prinzipiell gibt es drei Applikationsformen für inhalative Substanzen: • Dosieraerosol («Spray») mit und ohne Inhalierhilfe • Pulverinhalatoren • elektrische Druckvernebler. Druckvernebler werden vor allem bei Kleinkindern verwendet, sonst nur bei der Notfalltherapie, zum Beispiel in der Praxis. Zur Dauertherapie bei Asthma bronchiale sind sie kaum geeignet. Dosieraerosole sind für die Dauertherapie bei Kindern und Jugendlichen am besten geeignet, vor allem, wenn Inhalierhilfen verwendet werden und die entsprechende Schulung erfolgt. Pulverinhalatoren sind für Kleinkinder ungeeignet, da sie schon aus theoretischen Gründen die notwendige inspiratorische Flussrate nicht aufbringen können,
34 4/16
PNEUMOLOGIE
aber auch in den anderen Altersstufen ist die Fehlanwendungsrate trotz Schulung recht gross. Inhalierhilfen («Spacer») für Dosieraerosole dienen dazu, Sprühstoss und Inhalation zeitlich zu entkoppeln, denn nur bei sehr guter Koordination gelingt es, das mit zirka 50 km/h startende Inhalat im Rachenraum umzulenken und im Bronchialbaum zu deponieren. Lokale Nebenwirkungen topischer Steroide wie Heiserkeit und Mundsoor lassen sich durch die Verwendung einer Inhalierhilfe praktisch vollständig vermeiden. Anforderungen an die Inhalierhilfe sind: • einfache Handhabung • einfach und gut zu reinigen • möglichst universelle Anwendbarkeit, das heisst,
Sprays verschiedener Hersteller können in gleicher Weise verwendet werden.
Geeignet sind unter anderem Vortex® (Pari, Aluminiumgehäuse ohne statische Aufladung) oder Aerochamber®, weniger geeignet sind präparatspezifische Spacer ohne Ventil. Pulverinhalatoren benötigen zur Freisetzung des Medikaments einen relativ hohen inspiratorischen Flow und vor allem eine andere Inhalationstechnik als Dosieraerosole, sodass eine neue Anwendungsschulung notwendig ist. Dies erklärt auch die hohe Fehlanwendungsrate. Typische Anwendungsfehler sind (5): • keine Ausatmung vor Aktivierung (12–77%) • kein Anhalten des Atems (6–54%) • keine kräftige und tiefe Einatmung (2–48%) • falsche Dosis durch Fehlbedienung (2–46%) • kein korrektes Halten des Gerätes (7–44%) • falsche Reihenfolge der Anwendungsschritte (2–45%).
Die Lungendeposition ist bei den einzelnen Applikationsformen unterschiedlich, aber in allen Fällen relativ gering, das heisst, ein erheblicher Teil der Dosis geht verloren beziehungsweise landet im Gastrointestinaltrakt. Die Lungendeposition von Dosieraerosolen (HFA-Sprays) liegt bei 20 bis 60 Prozent je nach Technik/Inhalierhilfe/Altersstufe, bei Kleinkindern mit Inhalierhilfe und Maske bei maximal 25 Prozent. Die Lungendeposition bei Pulverinhalatoren (6) beträgt bis zu 30 Prozent beim Turbohaler® und 8 bis 15 Prozent beim Diskus®. Pulverinhalatoren werden wegen der schlechteren Bioverfügbarkeit höher dosiert, in der Regel um 100 Prozent im Vergleich zu Sprays. Dies schlägt sich zum Teil auch in den Therapiekosten nieder. Daher sollte im Einzelfall genau überprüft werden, welche Therapieform sowohl von der Effektivität als auch von den Kosten her günstiger ist.
Keine Angst vor Steroiden!
Von Patienten beziehungsweise Eltern werden die Nebenwirkungen der Steroidtherapie oft stark überbewertet oder hinterfragt. Die Bereitschaft zu einer wirksamen Dauertherapie hängt ganz entscheidend von der Gesprächsführung ab. Den meisten Menschen ist nicht klar, dass Kortison ein lebensnotwendiges Hormon ist, und dass die vorgeschlagene inhalative Dosis im Vergleich zur selbst produzierten Menge sehr klein ist.
Relevante Wachstumsstörungen, ungewollte Gewichtszunahme, verminderte Knochendichte, Beeinflussung des Glukosestoffwechsels et cetera kommen bei Standarddosierung eines inhalativen Steroids nicht vor. Bei fehlerhafter sehr hoher Dosierung können inhalative Steroide substanzabhängig durchaus solche systemische Nebenwirkungen haben. Die «Nebenwirkungen» der unterlassenen Steroidtherapie sind wesentlich gravierender: • Die längerfristige Monotherapie mit einem (lang
wirksamen) Betamimetikum ist ein Kunstfehler. Die Asthmamortalität ist um ein Vielfaches höher. • Eine langfristig unterlassene Asthmatherapie kann zur Zunahme der peripheren Obstruktion führen. • Bei einigen Patienten kommt es zur fixierten Obstruktion. Diese Gruppe hat meist keine akuten Asthmaanfälle, sondern unterschwellige Beschwerden und kann relativ früh ein Cor pulmonale entwickeln.
Ein unbehandeltes Asthma hat verschiedene Folgen (7): • Es ist die häufigste Ursache von krankheitsbeding-
ten Schulausfällen. • Die Hospitalisierungsrate ist durch leitlinienge-
rechte Therapie mindestens zu halbieren.
Tabelle 3: Medikamentöse Stufentherapie Generell gilt die Devise: so viel wie nötig, so wenig wie möglich.
Stufe 42 inhalatives rasch wirkendes Beta-2-Sympathomimetikum1
Stufe 32 inhalatives rasch wirkendes Beta-2-Sympathomimetikum1
Stufe 2 inhalatives rasch wirkendes Beta-2-Sympathomimetikum1
Stufe 1 inhalatives rasch wirkendes Beta-2-Sympathomimetikum1
ICS in hoher Dosis, wenn nicht ausreichend plus eine oder mehrere der folgenden Optionen: • inhalatives, lang wirksames Beta-2-Sympathomimetikum • (ggf. als fixe Kombination) • Montelukast • Retard-Theophyllin • systemisches Glukokortikoid (intermittierend oder • dauerhaft) in der niedrigsten noch effektiven Dosis.
ICS in hoher Dosis, wenn nicht ausreichend plus eine der folgenden Optionen: • Steigerung der Dosis des inhalativen Glukokortikoids • inhalatives, lang wirksames Beta-2-Sympathomimetikum4 • Montelukast5 • Retard-Theophyllin.
Therapie der 1. Wahl: niedrig dosierte ICS-Alternativtherapien: • Montelukast5 • Cromoglycinsäure • Versuch über 4 bis 8 Wochen möglich.
keine3
ICS: inhalative Glukokortikosteroide 1 Alternativen: Anticholinergika (z.B. Ipratropiumbromid), Theophyllin in Lösung, eventuell auch kombinierte Medikation mit rasch wirksamen Beta-2-Sympathomimetika. 2 Vor Dosissteigerung des IGCS beziehungsweise vor Add-on-Therapie oder Gabe oraler Glukokortikosteroide: Vorstellung in einem pädiatrisch-allergologisch-pneumologishcen Schwerpunkt (Praxis/Zentrum). 3 Eine vorübergehende antientzündliche Therapie zum Beispiel bei rezidivierenden, infektgetriggerten Bronchialobstruktionen im Säuglings- oder Kleinkindesalter sowie bei kurzfristigem Allergenkontakt (z.B. Birkenpollen, sporadischer Tierkontakt) älterer Kinder ist möglich, wird aber kontrovers diskutiert. 4 Im Vorschulalter kaum Wirksamkeits- oder Sicherheitsdaten, deshalb hier nur in Ausnahmefällen. 5 Als Monotherapie ab dem 2. Lebensjahr zugelassen, bei Kleinkindern (1–6 Jahre) ist Montelukast den lang wirksamen Beta-2-Sympathomimetika vorzuziehen.
Quelle: Gesellschaft für pädiatrische Pneumologie
4/16
35
PNEUMOLOGIE
• Das Todesfallrisiko wird durch Dauertherapie um 50 bis 90 Prozent reduziert (je nach Studie und Art der Therapie).
• Schweres unzureichend behandeltes Asthma hat negative Auswirkung, auf das Wachstum.
Zusammenfassung
Asthma ist bei Kindern und Jugendlichen häufig. Die Sicherung der Diagnose umfasst die Abgrenzung von anderen Erkrankungen und die Vermeidung von Fehldiagnosen. Das Spektrum reicht von psychosomatisch bedingten Atemstörungen bis zu schwerwiegenden chronischen beziehungsweise genetisch bedingten pulmonalen Grunderkrankungen. Ziele der Asthmatherapie sind eine gute Erkrankungskontrolle und die Vermeidung von Notfallsituationen. Wichtigstes Basistherapeutikum bei der Dauertherapie ist ein inhalatives Steroid. Bei Kindern sollten primär Dosieraerosole mit Inhalierhilfe verwendet werden. Bei guter Schulung ist die Asthmatherapie fast nebenwirkungsfrei und sehr wirksam.
Literatur: 1. Cope S: International differences in asthma guidelines for children. Int Arch Allergy Immunol 2009; 148(4): 265–278. 2. Allen D: Effects of inhaled steroids in growth, bone metabolism, and adrenal function. Advances in pediatrics 2006; 53: 101–110. 3. Allen D: Inhaled corticosteroids: past lessons and future issues (Review). J Allergy Clin Immunol 2003; 112(Suppl): S1–40. 4. Haughney J: Achieving asthma control in practice: understanding the reasons for poor control. Respiratory Medicine 2008; 102(12): 1681–1693. 5. Lavorini F: Effect of incorrect use of dry powder inhalers on management of patients with asthma and COPD. Respiratory Medicine 2008; 102(4): 593–604. 7. Spahn J: Weighing the risks of treatment versus nontreatment in pediatric asthma. Pediatr Clin N Am 2003; 50(3): 677–695. 8. Niggemann B: Functional symptoms confused with allergic disorders in children and adolescents. Pediatr Allergy Immunol 2002; 13(5): 312–318. 9. Seear M: How accurate is the diagnosis of exercise induced asthma among Vancouver schoolchildren. Arch Dis Child 2005; 90(9): 898–902.
Dieser Beitrag erschien zuerst in der Zeitschrift «Der Allgemeinarzt» 20/2015. Der bearbeitete Abdruck erfolgt mit freundlicher Genehmigung von Verlag und Autor. Es werden in dieser bearbeiteten Version nur Medikamente genannt, die in der Schweiz zugelassen sind.
Korrespondenzadresse: Dr. med. Stephan Illing Pädiatrische Pneumologie/Allergologie/Infektiologie Olgahospital/Klinikum Stuttgart Kriegsbergstr. 62 D-70174 Stuttgart E-Mail: s.illing@klinikum-stuttgart.de
36 4/16