Transkript
Im Fokus: Gastroenterologische Tumoren
Therapeutische Optionen beim Cholangiokarzinom
Systemische Therapiemöglichkeiten im Fokus
Der vorliegende Artikel gibt einen Überblick über die aktuellen Therapieoptionen beim Cholangiokarzinom. Der Fokus liegt insbesondere auf den systemischen Therapieoptionen in der adjuvanten sowie metastasierten Situation.
KIRA-LEE KOSTER, CHRISTIAN WEISSHAUPT
SZO 2021; 5: 20–23.
Kira-Lee Koster Christian Weisshaupt
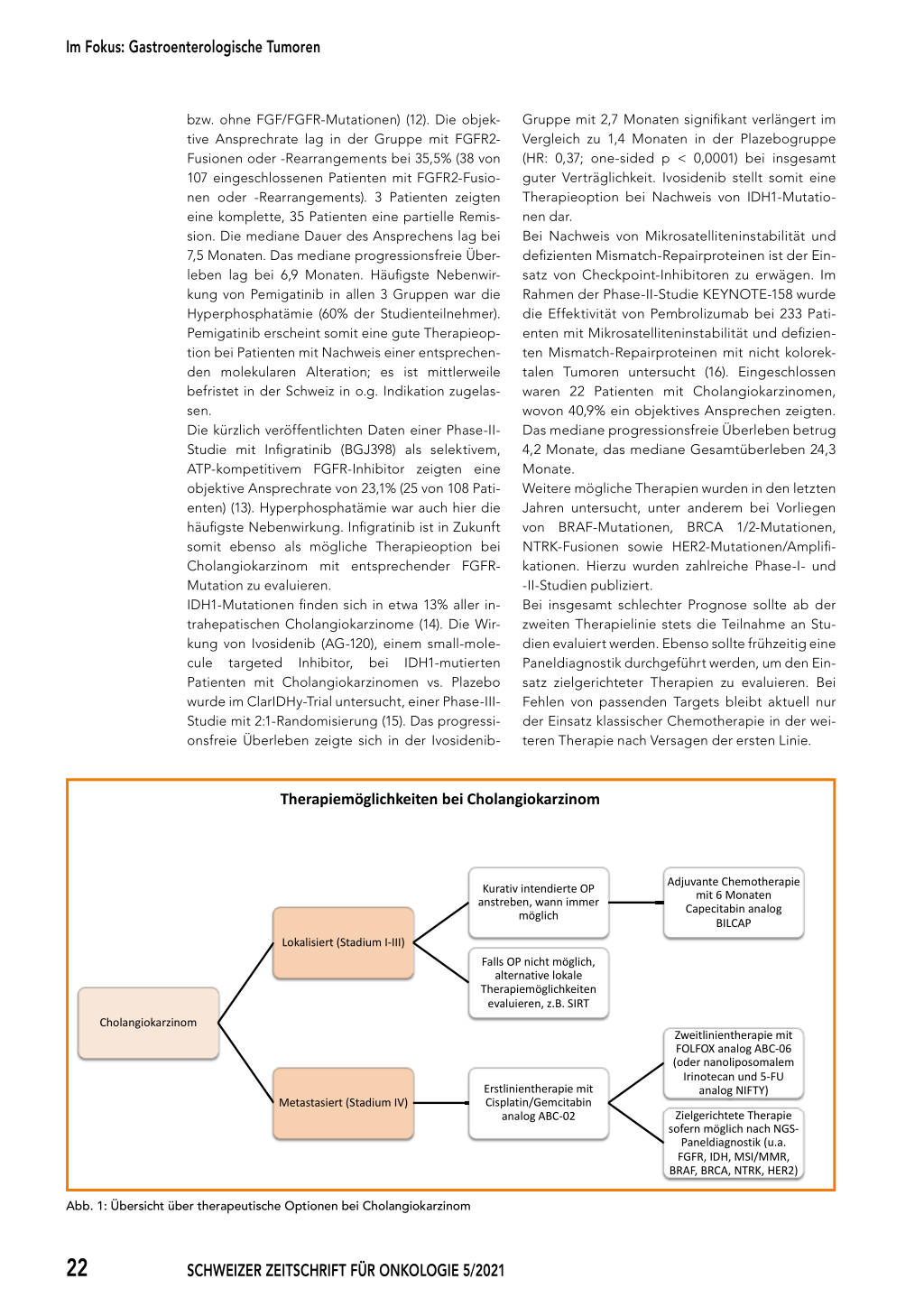
Das Cholangiokarzinom ist mit < 1% aller Krebserkrankungen eine seltene Tumorentität. Cholangiokarzinome machen 10 bis 15% aller primären Lebertumore aus, die Einteilung erfolgt in intrahepatische, extrahepatische perihiläre (Klatskintumore) und distale Cholangiokarzinome sowie Gallenblasenkarzinome. Je nach Lage zeigen die Cholangiokarzinome eine unterschiedliche Biologie und erfordern eine unterschiedliche Behandlung. Die Erkrankung tritt gehäuft im höheren Lebensalter auf und kann durch diverse Risikofaktoren begünstigt werden: primär sklerosierende Cholangitis, chronische Infektionen, Parasitenbefall, Hepatound Choledocholithiasis sowie Choledochuszysten und das Caroli-Syndrom (1). Cholangiokarzinome können lange symptomlos bleiben, sodass sie erst in sehr fortgeschrittenen ABSTRACT Therapeutic options in cholangiocarcinoma Cholangiocarcinoma is a rare cancer entity, difficult to diagnose due to often initially asymp tomatic patients, especially in intrahepatic manifestations and presenting with unspecific symptoms. Surgical treatment is the only curative therapeutic option and should be performed whenever possible. A complete resection (R0) is absolutely necessary in the curative setting. An adjuvant treatment with 6 months of Capecitabine (according to the BILCAP-study) should be discussed with the patient. In the metastatic setting, the recommended first line treatment is a chemotherapy with Cisplatin and Gemcitabine (according to the ABC-02study). NGS-testing should be performed early to recognize targetable genomic alterations for the further therapy lines. In case of no targetable genetic alterations, FOLFOX (according to the ABC-06-study) is recommended as second line treatment. Recently nanoliposomal Iri notecan combined with 5-fluorouracil has shown efficacy as well in the second line treat ment and might be taken into account as another possible second line treatment-option. In the presence of targetable genetic alterations e.g. FGFR- or IDH-mutations or in the presence of microsatellite-instability, the second line treatment should be performed with the suitable targeted therapy. Patients with Cholangiocarcinoma should be treated in clinical trials when ever possible. Although several new therapeutic options, especially targeted therapies, have been identified in the last years, the outcome remains poor in the metastatic situation. Keywords: Cholangiocarcinoma, chemotherapy, targeted therapy, NGS-testing oder metastasierten Stadien entdeckt werden und eine kurative Behandlung häufig nicht mehr möglich ist. Mögliche Symptome sind Ikterus, Cholangitis, Erbrechen, Übelkeit, Inappetenz sowie rechtsseitige Oberbauchschmerzen. Weiterhin auftreten können Aszites, Gewichtsverlust, Asthenie und Fatigue (2). Aufgrund der unspezifischen Symptome ist die Diagnosestellung ohne Bildgebung kaum möglich. Diagnosestellung und Staging Zur Diagnosestellung und zum Staging sollte eine Schnittbilddiagnostik mittels Computertomographie (CT) oder Magnetresonanztomographie (MRT) erfolgen (3). Eine invasivere Diagnostik zur Zytologiegewinnung (Endoskopische retrograde Cholangiographie [ERC]/Endosonographie [EUS]) muss nur in unklaren Fällen erfolgen, bei lokalisiertem Cholan giokarzinom ohne relevante Cholestase ist nach Möglichkeit ein operatives Vorgehen anzustreben (2). Eine ERC oder eine Magnetresonanztomographiegestützte Cholangiographie (MRC) ist bei extrahepatischen perihilären Karzinomen wichtig zur genauen Lokalisation des Tumors in der Gallengangsgabelung zur Einteilung nach Bismuth für die Abschätzung der Resektabilität. Wenn bezüglich Cholestase keine Notfallsituation vorliegt, sollte vor einem allfälligen Stenting die Bildgebung unbedingt abgeschlossen werden, da die Tumorlokalisation sonst nicht mehr korrekt möglich ist. Bei inoperabler Erkrankung oder im metastasierten Stadium ist eine histologische oder zumindest zytologische Diagnostik notwendig. Systemische Therapiemöglichkeiten Lokal begrenzte Stadien (I–III) Bei lokal begrenzten, resektablen Stadien sollte die Operation in kurativer Intention angestrebt und eine R0-Resektion unbedingt versucht werden. 20 SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 5/2021 Im Fokus: Gastroenterologische Tumoren Erstmalig konnte mit der randomisierten Phase-IIIStudie BILCAP der Nutzen einer adjuvanten Chemotherapie mit 6 Monaten Capecitabin im Vergleich zur reinen Nachsorge gezeigt werden (4). Obwohl sich in der ITT-Population kein signifikant besseres Gesamtüberleben (median 51,1 Monate) im Vergleich zur Beobachtungsgruppe (36,4 Monate) gezeigt hat (Hazard Ratio [HR]: 0,81; p = 0,097) und die Studie ihren primären Endpunkt somit nicht erreicht hat, konnte in einer protokollspezifischen Sensitivitätsanalyse mit Adjustierung nach Geschlecht, Lymphknotenstatus und Differenzierungsgrad ein verbessertes Gesamtüberleben gezeigt werden (OS-HR: 0,71; p = 0,010), mit 53 Monaten in der Capecitabin-Gruppe vs. 36 Monaten in der Beobachtungsgruppe (adjustierte HR: 0,75; p = 0,028). In der PRODIGE12-ACCORD18-UNICANCER-Studie, ebenso eine randomisierte Phase-III-Studie, wurden Gemcitabin und Oxaliplatin im adjuvanten Setting mit Nachsorge verglichen. Hier konnte kein Überlebensvorteil nachgewiesen werden (5). Gemcitabin und Cisplatin adjuvant vs. Capecitabin adjuvant werden in der aktuell noch laufenden ACTICCA-Studie untersucht, die Studie rekrutiert noch (NCT02170090). Eine adjuvante Radiotherapie sollte derzeit nur im Rahmen klinischer Studien durchgeführt werden, da randomisierte Phase-III-Daten fehlen. Metastasierte Erkrankung (Stadium IV) Bei metastasierter Erkrankung kann die Therapie nur noch in palliativer Intention erfolgen. Vor Therapiebeginn sollte in diesem Stadium unbedingt eine histologische oder zumindest zytologische Bestätigung der Diagnose erfolgen. Dies ist auch relevant für weitere Untersuchungen im Hinblick auf zielgerichtete Therapien ab der zweiten Therapielinie. Optionen zur Erstlinientherapie Indikationsstellung und Therapieauswahl sollten den Allgemeinzustand sowie die Komorbiditäten der Patientinnen und Patienten berücksichtigen. Behandlungsstandard in der ersten palliativen Therapielinie ist eine Kombinationschemotherapie mit Gemcitabin und Cisplatin gemäss der britischen ABC-02-Studie (6). Das mittlere Gesamtüberleben lag bei 11,7 Monaten in der Cisplatin/ Gemcitabin-Gruppe im Vergleich zu 8,1 Monaten in der Gemcitabin-Gruppe (HR: 0,64; p < 0,001). Das Auftreten von unerwünschten Ereignissen war in beiden Gruppen ähnlich mit Ausnahme von Neutropenien, die in der Gruppe der Kombinationschemotherapie häufiger auftraten. Die Anzahl an Neutropenie-assoziierten Infektionen war jedoch in beiden Gruppen gleich. Insgesamt wurde ein gut verträgliches Schema von Gemcitabin und Cisplatin gewählt mit Gabe von Gemcitabin 1000 mg/ m2 und Cisplatin 25 mg/m2 an d1 und d8 mit Wiederholung an d22. Bei Nierenfunktionsstörungen sollte der Einsatz von Oxaliplatin anstelle von Cisplatin erwogen werden (3). Weitere Therapielinien Nach Progression im Rahmen der Erstlinientherapie wurde die Gabe von FOLFOX als Zweitlinientherapie im Rahmen der ABC-06-Studie, ebenso eine randomisierten Phase-III-Studie, untersucht (7). Das mediane Gesamtüberleben in der untersuchten Gruppe mit aktiver Symptomkontrolle und FOLFOX betrug 6,2 vs. 5,3 Monate in der Gruppe mit aktiver Symptomkontrolle (adjustierte HR: 0,69; p = 0,031). Auch zeigten sich die Gesamtüberlebensraten nach 6 und 12 Monaten mit Zugabe von FOLFOX verbessert (nach 6 Monaten 50,6% und nach 12 Monaten 25,9%) im Vergleich zur alleinigen Symptomkontrolle (35,5% nach 6 Monaten und 11,4% nach 12 Monaten). Die Gabe von FOLFOX als Zweitlinientherapie sollte in Betracht gezogen und mit den Patienten besprochen werden. Nanoliposomales Irinotecan in Kombination mit 5-Fluorouracil (5-FU) und Leucovorin vs. 5-FU und Leucovorin nach Progression auf Gemcitabin und Cisplatin wurde im Rahmen der Phase-IIb-Studie NIFTY untersucht (8). Das mediane progressionsfreie Überleben (BICR) lag bei 7,1 vs. 1,4 Monaten (HR: 0,56; p = 0,0019), das mediane Gesamtüberleben lag bei 8,6 vs. 5,5 Monaten (HR: 0,68; p = 0,0349). Obwohl dies eine rein koreanische Studie war, kann nanoliposomales Irinotecan in Kombination mit 5-FU und Leucovorin somit bei Versagen der Erstlinientherapie als mögliche Zweitlinientherapie evaluiert werden. Verschiedene zielgerichtete Therapien wurden in der zweiten Therapielinie untersucht. Die Durchführung einer breiten molekularen Paneldiagnostik sollte frühzeitig erwogen werden, um allenfalls mögliche zielgerichtete Therapiemöglichkeiten einsetzen zu können (9). Die im Next Generation Sequencing (NGS) gefundenen Mutationen unterscheiden sich je nach Lage/Tumortyp: IDH-Mutationen sowie FGFRRearrangements finden sich bei intrahepatischen Cholangiokarzinomen häufiger, HER2-Veränderungen in extrahepatischen Cholangiokarzinomen sowie Gallenblasenkarzinomen (10). FGFR2-Fusionen sind unter den FGFR-Veränderungen bei intrahepatischem Cholangiokarzinom am häufigsten (11). In der Phase-II-Studie FIGHT-202 wurde der Einsatz von Pemigatinib, einem selektiven, oralen FGFR -1-, 2- und -3-Inhibitor bei Patientinnen und Patienten mit FGFR2-Fusionen oder -Rearrangements getestet (im Vergleich zu anderen SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 5/2021 21 Im Fokus: Gastroenterologische Tumoren bzw. ohne FGF/FGFR-Mutationen) (12). Die objektive Ansprechrate lag in der Gruppe mit FGFR2Fusionen oder -Rearrangements bei 35,5% (38 von 107 eingeschlossenen Patienten mit FGFR2-Fusionen oder -Rearrangements). 3 Patienten zeigten eine komplette, 35 Patienten eine partielle Remission. Die mediane Dauer des Ansprechens lag bei 7,5 Monaten. Das mediane progressionsfreie Überleben lag bei 6,9 Monaten. Häufigste Nebenwirkung von Pemigatinib in allen 3 Gruppen war die Hyperphosphatämie (60% der Studienteilnehmer). Pemigatinib erscheint somit eine gute Therapieoption bei Patienten mit Nachweis einer entsprechenden molekularen Alteration; es ist mittlerweile befristet in der Schweiz in o.g. Indikation zugelassen. Die kürzlich veröffentlichten Daten einer Phase-IIStudie mit Infigratinib (BGJ398) als selektivem, ATP-kompetitivem FGFR-Inhibitor zeigten eine objektive Ansprechrate von 23,1% (25 von 108 Patienten) (13). Hyperphosphatämie war auch hier die häufigste Nebenwirkung. Infigratinib ist in Zukunft somit ebenso als mögliche Therapieoption bei Cholangiokarzinom mit entsprechender FGFRMutation zu evaluieren. IDH1-Mutationen finden sich in etwa 13% aller intrahepatischen Cholangiokarzinome (14). Die Wirkung von Ivosidenib (AG-120), einem small-molecule targeted Inhibitor, bei IDH1-mutierten Patienten mit Cholangiokarzinomen vs. Plazebo wurde im ClarIDHy-Trial untersucht, einer Phase-IIIStudie mit 2:1-Randomisierung (15). Das progressionsfreie Überleben zeigte sich in der Ivosidenib- Gruppe mit 2,7 Monaten signifikant verlängert im Vergleich zu 1,4 Monaten in der Plazebogruppe (HR: 0,37; one-sided p < 0,0001) bei insgesamt guter Verträglichkeit. Ivosidenib stellt somit eine Therapieoption bei Nachweis von IDH1-Mutationen dar. Bei Nachweis von Mikrosatelliteninstabilität und defizienten Mismatch-Repairproteinen ist der Einsatz von Checkpoint-Inhibitoren zu erwägen. Im Rahmen der Phase-II-Studie KEYNOTE-158 wurde die Effektivität von Pembrolizumab bei 233 Patienten mit Mikrosatelliteninstabilität und defizienten Mismatch-Repairproteinen mit nicht kolorektalen Tumoren untersucht (16). Eingeschlossen waren 22 Patienten mit Cholangiokarzinomen, wovon 40,9% ein objektives Ansprechen zeigten. Das mediane progressionsfreie Überleben betrug 4,2 Monate, das mediane Gesamtüberleben 24,3 Monate. Weitere mögliche Therapien wurden in den letzten Jahren untersucht, unter anderem bei Vorliegen von BRAF-Mutationen, BRCA 1/2-Mutationen, NTRK-Fusionen sowie HER2-Mutationen/Amplifikationen. Hierzu wurden zahlreiche Phase-I- und -II-Studien publiziert. Bei insgesamt schlechter Prognose sollte ab der zweiten Therapielinie stets die Teilnahme an Studien evaluiert werden. Ebenso sollte frühzeitig eine Paneldiagnostik durchgeführt werden, um den Einsatz zielgerichteter Therapien zu evaluieren. Bei Fehlen von passenden Targets bleibt aktuell nur der Einsatz klassischer Chemotherapie in der weiteren Therapie nach Versagen der ersten Linie. Therapiemöglichkeiten bei Cholangiokarzinom Cholangiokarzinom Lokalisiert (Stadium I-III) Kurativ intendierte OP anstreben, wann immer möglich Falls OP nicht möglich, alternative lokale Therapiemöglichkeiten evaluieren, z.B. SIRT Metastasiert (Stadium IV) Erstlinientherapie mit Cisplatin/Gemcitabin analog ABC-02 Abb. 1: Übersicht über therapeutische Optionen bei Cholangiokarzinom 22 SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 5/2021 Adjuvante Chemotherapie mit 6 Monaten Capecitabin analog BILCAP Zweitlinientherapie mit FOLFOX analog ABC-06 (oder nanoliposomalem Irinotecan und 5-FU analog NIFTY) Zielgerichtete Therapie sofern möglich nach NGS- Paneldiagnostik (u.a. FGFR, IDH, MSI/MMR, BRAF, BRCA, NTRK, HER2) Im Fokus: Gastroenterologische Tumoren Lokale Therapiemöglichkeiten Bei inoperablem intrahepatischem Cholangiokarzinom sollten lokale Therapiemöglichkeiten als alternative oder zusätzliche Behandlungsmöglichkeit individuell evaluiert werden, einen klaren Standard gibt es nicht. Eine mögliche Therapie ist die selektive interne Radiotherapie (SIRT). In einer Metaanalyse aus 9 Beobachtungsstudien zeigten sich Überlebensraten von 55,7% nach einem Jahr, 33,1% nach 2 Jahren sowie 20,2% nach 3 Jahren (17). Bei «masseformenden» Tumoren zeigten sich bessere therapeutische Ergebnisse als bei infiltrativem Wachstum (medianes Überleben 19,9 vs. 8,1 Monate; p = 0,002), ebenso bei SIRT als Erstlinientherapie im Vergleich zu vorbehandelten Patienten (medianes Überleben 24 vs. 11,5 Monate; p = 0,048). Auch eine begleitende Chemotherapie zur SIRT zeigte im Vergleich zu Patienten, die keine Therapie erhielten, einen Vorteil (medianes Überleben 19,5 vs. 5,5 Monate; p = 0,042). Neben der SIRT können weitere transarterielle sowie ablative Verfahren zum Einsatz kommen, die ebenfalls evaluiert werden sollten. Schlussfolgerung Cholangiokarzinome sind eine seltene Tumorentität mit schlechter Prognose. Fehlen angehbare genomische Alterationen, sind die Therapiemöglichkeiten eingeschränkt. Die untersuchten Standardtherapien gehen in dieser häufig polymorbiden Patientengruppe mit einer hohen Toxizität einher, diese kann therapielimitierend sein. Bei gegebener Resektabilität sollte unbedingt eine R0-Resektion angestrebt werden, die operative Therapie ist der einzige kurative Ansatz. Eine anschliessende adjuvante Chemotherapie mit 6 Monaten Capecitabin sollte mit den Patienten besprochen werden. In der metastasierten Situation ist die Kombinationschemotherapie mit Cisplatin und Gemcitabin etablierte Erstlinientherapie. Schon früh sollte eine Paneldiagnostik durchgeführt werden, um für die weiteren Therapielinien allfällig mögliche zielgerichtete Therapien planen und anfragen zu können. Bei Fehlen von angehbaren Mutationen wird in der zweiten Therapielinie die Gabe von FOLFOX als Standardtherapie empfohlen. Kira-Lee Koster Dr. med. Christian Weisshaupt (Korrespondenzadresse) E-Mail: christian.weisshaupt@kssg.ch Kantonsspital St. Gallen Klinik für Medizinische Onkologie und Hämatologie CH-9007 St. Gallen Interessenkonflikte: Keine Merkpunkte ■ Cholangiokarzinome sind eine seltene Tumorentität und schwer zu diagnostizieren bei unspezifischer Symptomatik. Methode der Wahl zur Diagnosestellung ist die Schnittbilddiagnostik. ■ Bei kurativ resezierbarer Situation sollte unbedingt eine R0-Resektion angestrebt werden, die operative Therapie ist der einzige kurative Ansatz. ■ Nach vollständiger Resektion des Tumors sollte mit den Patienten eine adjuvante Therapie mit 6 Monaten Capecitabin gemäss BILCAP-Studie diskutiert werden. ■ Die Erstlinientherapie in der palliativen Situation besteht gemäss den Daten der ABC-02-Studie aus Cisplatin und Gemcitabin. ■ Schon früh sollte eine molekulargenetische Paneldiagnostik durchgeführt werden, um ab der zweiten Therapielinie allenfalls zielgerichtete Therapien einsetzen zu können. ■ Bei nicht operablem intrahepatischem Cholangiokarzinom sollten lokale Therapie möglichkeiten evaluiert werden. Literaturverzeichnis 1. Ghouri YA et al.: Cancer review: Cholangiocarcinoma. J Carcinog. 2015;14:1. 2. Maligne biliäre Tumoren. Onkopedia. Accessed September 12, 2021. https:// www.onkopedia.com/de/onkopedia/guidelines/maligne-biliaere-tumoren 3. Valle JW et al.: Biliary cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2016;27(suppl 5):v28-v37. 4. Primrose JN et al.: Capecitabine compared with observation in resected biliary tract cancer (BILCAP): a randomised, controlled, multicentre, phase 3 study. Lancet Oncol. 2019;20(5):663-673. 5. Edeline J et al.: Gemcitabin and Oxaliplatin Chemotherapy or Surveillance in Resected Biliary Tract Cancer (PRODIGE 12-ACCORD 18-UNICANCER GI): A Randomized Phase III Study. J Clin Oncol Off J Am Soc Clin Oncol. 2019;37(8):658-667. 6. Valle J et al.: Cisplatin plus Gemcitabin versus Gemcitabin for biliary tract cancer. N Engl J Med. 2010;362(14):1273-1281. 7. Lamarca A et al.: Second-line FOLFOX chemotherapy versus active symptom control for advanced biliary tract cancer (ABC-06): a phase 3, open-label, randomised, controlled trial. Lancet Oncol. 2021;22(5):690-701. 8. Yoo C et al.: Liposomal irinotecan (nal-IRI) in combination with fluorouracil (5FU) and leucovorin (LV) for patients with metastatic biliary tract cancer (BTC) after progression on Gemcitabin plus cisplatin (GemCis): Multicenter comparative randomized phase 2b study (NIFTY). J Clin Oncol. 2021;39(15_ suppl):4006-4006. 9. Mosele F et al.: Recommendations for the use of next-generation sequencing (NGS) for patients with metastatic cancers: a report from the ESMO Precision Medicine Working Group. Ann Oncol. 2020;31(11):1491-1505. 10. Valle JW et al.: New Horizons for Precision Medicine in Biliary Tract Cancers. Cancer Discov. 2017;7(9):943-962. 11. Arai Y et al.: Fibroblast growth factor receptor 2 tyrosine kinase fusions define a unique molecular subtype of cholangiocarcinoma. Hepatology. 2014;59(4):1427-1434. 12. Abou-Alfa GK et al.: Pemigatinib for previously treated, locally advanced or metastatic cholangiocarcinoma: a multicentre, open-label, phase 2 study. Lancet Oncol. 2020;21(5):671-684. doi:10.1016/S1470-2045(20)30109-1. 13. Javle M et al.: Infigratinib (BGJ398) in previously treated patients with advanced or metastatic cholangiocarcinoma with FGFR2 fusions or rearrangements: mature results from a multicentre, open-label, single-arm, phase 2 study. Lancet Gastroenterol Hepatol. Published online August 3, 2021:S2468-1253(21)001965. 14. Boscoe AN et al.: Frequency and prognostic significance of isocitrate dehydrogenase 1 mutations in cholangiocarcinoma: a systematic literature review. J Gastrointest Oncol. 2019;10(4):751-765. 15. Abou-Alfa GK et al.: Ivosidenib in IDH1-mutant, chemotherapy-refractory chol angiocarcinoma (ClarIDHy): a multicentre, randomised, double-blind, placebocontrolled, phase 3 study. Lancet Oncol. 2020;21(6):796-807. 16. Marabelle A et al.: Efficacy of Pembrolizumab in Patients With Noncolorectal High Microsatellite Instability/Mismatch Repair-Deficient Cancer: Results From the Phase II KEYNOTE-158 Study. J Clin Oncol. 2020;38(1):1-10. 17. Cucchetti A et al.: Improving patient selection for selective internal radiation therapy of intra-hepatic cholangiocarcinoma: A meta-regression study. Liver Int. 2017;37(7):1056-1064. SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 5/2021 23