Transkript
Im Fokus: Sarkome und seltene Malignome
Strategisches Vorgehen bei Verdacht auf Knochensarkom
Fallbeispiel Ewing-Sarkom: Biopsie? Chemotherapie? Bestrahlung? Oder einfach «nur» operieren?
Sarkome sind bösartige Knochen- und Weichteiltumore und umfassen mehr als 100 verschiedene Typen mit eigener Biologie, welche entsprechend individualisierte Therapieformen erfordern. Im Folgenden wird anhand eines Fallbeispiels das therapeutische, insbesondere chirurgische Vorgehen beschrieben.
KOUROSH MODARESSI, FELIX NIGGLI, BRUNO FUCHS
Kourosh Modaressi
Felix Niggli
Bruno Fuchs
Die muskuloskeletale Onkologie befasst sich mit der Behandlung der relativ seltenen Tumoren des Bindegewebes (Knochen und Weichteile), auch Sarkome genannt. Die Behandlungsstrategie der Sarkome sollte bereits vor einer Tumorbiopsie, das heisst anlässlich der Erstvorstellung in einer möglichst auf Sarkombehandlung spezialisierten Klinik durchdacht werden. Nur so kann gewährleistet werden, dass bereits der bioptische Zugang in einer für die spätere Tumorresektion korrekten Art erfolgt. Nur durch eine adäquate Behandlung von Beginn an, welche hauptsächlich aus einer Kombination von Chirurgie, Radiotherapie und Chemotherapie besteht und eine entsprechend hohe Interdisziplinarität erfordert, kann für jeden einzelnen Patienten die Prognose schliesslich optimiert werden (1). Mit der im Untertitel erwähnten Fragestellung wurde uns ein zehnjähriger Junge zugewiesen, welcher beim Tennisspielen ziehende Schmerzen im Bereich der rechten Schulter beklagte. Strikt nach unserem Behandlungsalgorithmus für Sarkome (Tabelle 1) wurden radiologische Abklärungen mittels konventionellen Röntgens und MRI durchgeführt. Diese zeigten einen hochgradigen Verdacht auf einen malignen Knochentumor.
ABSTRACT
Diagnosis and Treatment of malignant musculoskeletal tumors
The diagnosis and treatment of malignant musculoskeletal tumors require an interdisciplinary team approach. A concerted and coordinated effort among specialists within a sarcoma center provides the best base to establish the optimal treatment strategy. Surgical treatment includes a wide armamentarium, which needs to be individualized to for each patient’s situation.
Keywords: Bone tumour, soft tissue sarcoma, interdisciplinarity.
Allgemeines
Sarkome umfassen zirka 1% aller Malignome, wobei vielfach Kinder und Jugendliche betroffen sind (2, 3). Es existieren mehr als 100 verschiedene (inkl. molekulare) Sarkomtypen mit unterschiedlicher Biologie, welche entsprechend individualisierte Therapieformen erfordern. Die molekulare Genetik hat das Wissen über die Sarkome in den letzten Jahren erweitert und damit neue Therapiemöglichkeiten eröffnet. Folglich kann den Sarkompatienten ohne exzellent koordinierte, interdisziplinäre Teamarbeit im Rahmen eines SarkomBoards keine optimale Therapie zuteil werden (die Mortalität bliebe unverändert hoch). Selbstverständlich wurden auch bei unserem zehnjährigen Jungen die jeweiligen Behandlungsschritte interdisziplinär am Sarkom-Board besprochen.
Interdisziplinäre Teamarbeit
Das Sarkom-Board (www.sarkomboard.ch) in Zürich setzt sich aus Experten der Fachbereiche Medizinische und Pädiatrische Onkologie, Orthopädische Onkologie, Radiologie, Radio-Onkologie (inkl. Protonentherapie), Pathologie, Thoraxchirurgie, Wiederherstellungschirurgie und Viszeralchirurgie zusammen. Diese Spezialistengruppe trifft sich wöchentlich am Universitätsspital Zürich mit dem Ziel, die beste Strategie zur Diagnostik und Therapie von Sarkompatienten vor Beginn der Behandlung festzulegen.
Fallbeispiel: Zehnjähriger mit Ewing-Sarkom
Biopsie Im beschriebenen Fall wurde zunächst die Indikation zur Stanzbiopsie durch den klavikulären Anteil des M. Deltoideus gestellt, welche problemlos in Kurznarkose und schmerzlos für den Patienten erfolgen konnte.
12 SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 2/2012
Im Fokus: Sarkome und seltene Malignome
Grundsätzlich werden Nadel- oder Stanzbiopsien von offenen Biopsien unterschieden, welche weiter in Inzisions- und Exzisionsbiopsien unterteilt werden (4). Bei einer Inzisionsbiopsie wird ein kleiner, aber repräsentativer Teil des Tumors gewonnen. Mehrfachpunktionen sollten vermieden werden, weil dadurch vermutlich die Streuung des Tumors erhöht werden könnte. Bei offenen Inzisionsbiopsien wird der Tumor eröffnet und ein zirka 1 x 1 x 1 cm grosses Gewebestück gewonnen. Unvermeidbar ist die zelluläre Kontamination der Biopsiestelle. Deshalb gibt es für die Biopsiedurchführung Leitlinien (5, 6), um die spätere operative Resektion optimal gestalten zu können (4, 5). Im beschriebenen Fall zeigte die histologische Aufarbeitung kleine, runde, blaue Tumorzellen. Immunhistochemisch waren diese CD99-positiv. Molekulargenetisch wurde die Fusion zwischen dem EWS- und FLI1-Gen mittels «Real-Time-PCR» und fluoreszierender In-situ-Hybridisierung (FISH) nachgewiesen, entsprechend einer Translokation zwischen Chromosom 11 und 22. Damit wurde die Diagnose eines EwingSarkoms gestellt.
Tabelle 1: Behandlungschema Sarkome
Therapeutisches Vorgehen
Die durch chirurgische Eingriffe dominierte Knochentumorbehandlung konnte bis in die Sechzigerjahre nur bescheidene Heilungserfolge erzielen. Erst mit Einführung der Chemotherapie neben bereits vorhandener Strahlentherapie konnte die langfristige Prognose der Knochentumore signifikant verbessert werden. Es ist deshalb heute Standard, die Therapie in die drei Phasen ▲ neoadjuvante Chemotherapie ▲ lokale Tumorkontrolle und ▲ postoperative Chemotherapie zu gliedern. Da Ewing-Sarkome besondere Empfindlichkeit gegenüber alkylierenden Substanzen, Anthrazyklinen, Vincristin, Actinomycin D und Etoposid aufweisen, erfolgt die primäre Chemotherapie mit einer entsprechenden Kombination dieser Substanzen. Nach vier- bis fünfmonatiger Chemotherapie steht die lokale Tumorkontrolle an. Mehrheitlich erfolgt diese mit einer Tumorresektion. Strahlentherapie wird bei unvollständigen Resektionen oder bei besonderer Lokalisation wie beispielsweise im Wirbelsäulenbereich in Betracht gezogen. An die Lokaltherapie schliesst sich eine adjuvante Chemotherapie über mehrere Monate an. Für Hochrisikopatienten wird derzeit der Einsatz von Hochdosistherapien mit autologer Stammzelltransplantation geprüft (7). Neuere Substanzen, welche allenfalls additiv zum Beispiel zur Apoptoseinduktion von Tumorrestzellen, zur Hemmung der Angiogenese oder zur Blockade des Insulin-like-growth-factor-1-Rezeptor gegeben werden können, sind in klinischen Studien
Tabelle 2: Definition der Resektionen (R-Klassifikation) Tabelle 3: Grading-System (UICC, 2003)
SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 2/2012
13
Im Fokus: Sarkome und seltene Malignome
tung erfolgen, wenn bei einer etwaigen Erstoperation eine solche eingelegt worden war. Nicht immer ist eine Kompartmentresektion (Resektion des Muskels/der Muskelgruppe vom Ursprung bis zum Ansatz) zwingend notwendig. Dies ist nur bei einer Tumorkontamination des gesamten Kompartimentes indiziert.
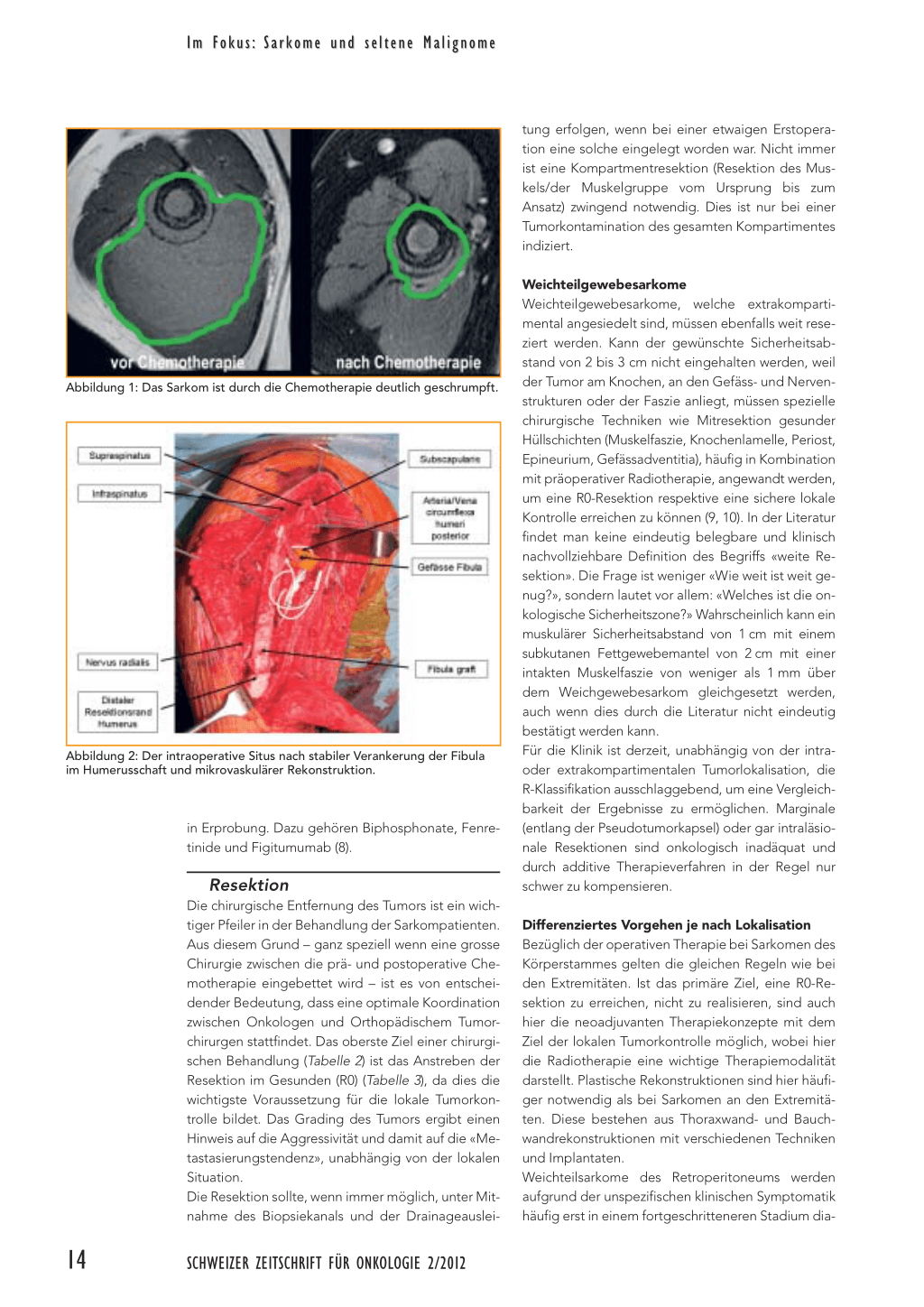
Abbildung 1: Das Sarkom ist durch die Chemotherapie deutlich geschrumpft.
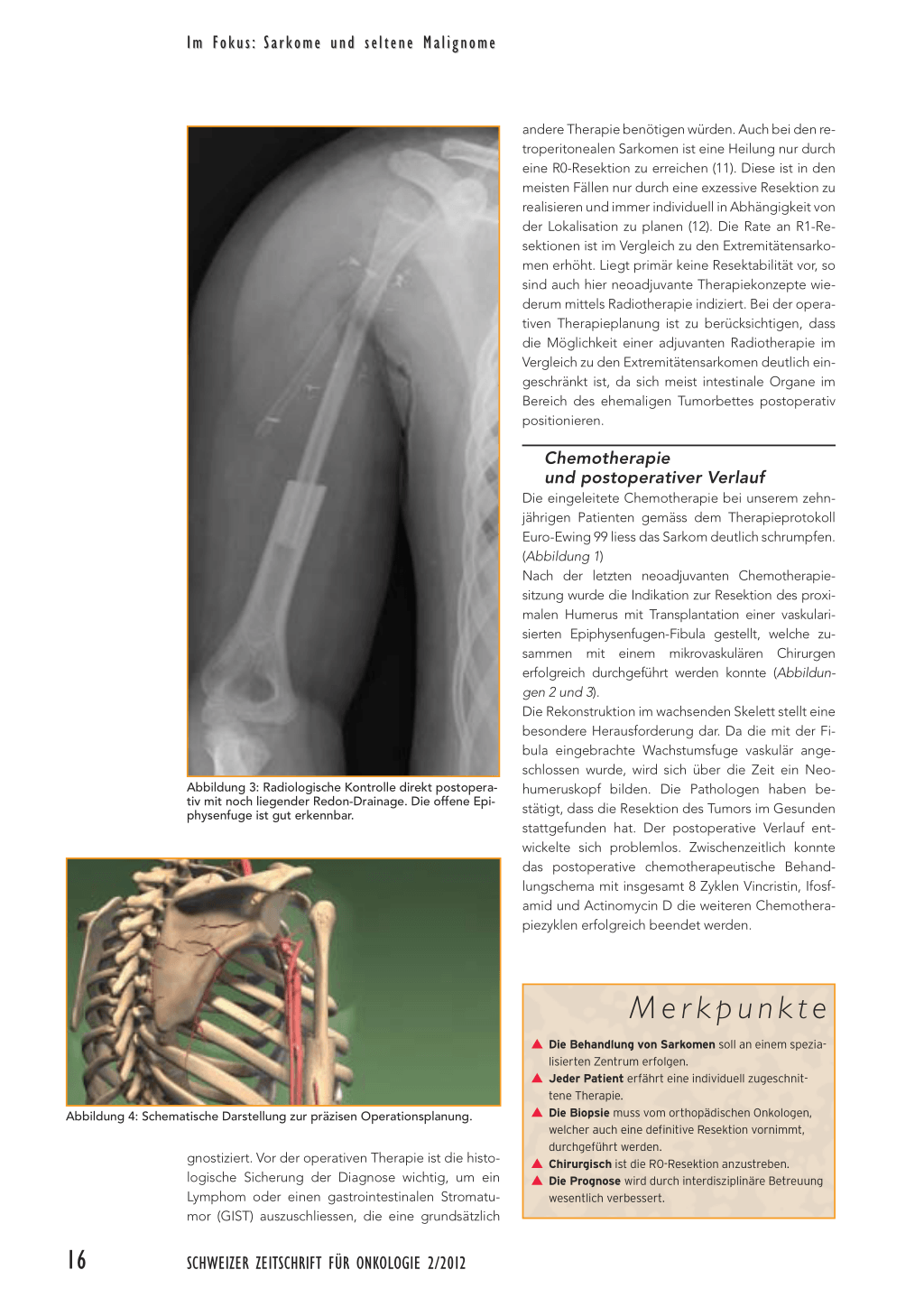
Abbildung 2: Der intraoperative Situs nach stabiler Verankerung der Fibula im Humerusschaft und mikrovaskulärer Rekonstruktion.
in Erprobung. Dazu gehören Biphosphonate, Fenretinide und Figitumumab (8).
Resektion
Die chirurgische Entfernung des Tumors ist ein wichtiger Pfeiler in der Behandlung der Sarkompatienten. Aus diesem Grund – ganz speziell wenn eine grosse Chirurgie zwischen die prä- und postoperative Chemotherapie eingebettet wird – ist es von entscheidender Bedeutung, dass eine optimale Koordination zwischen Onkologen und Orthopädischem Tumorchirurgen stattfindet. Das oberste Ziel einer chirurgischen Behandlung (Tabelle 2) ist das Anstreben der Resektion im Gesunden (R0) (Tabelle 3), da dies die wichtigste Voraussetzung für die lokale Tumorkontrolle bildet. Das Grading des Tumors ergibt einen Hinweis auf die Aggressivität und damit auf die «Metastasierungstendenz», unabhängig von der lokalen Situation. Die Resektion sollte, wenn immer möglich, unter Mitnahme des Biopsiekanals und der Drainageauslei-
Weichteilgewebesarkome Weichteilgewebesarkome, welche extrakompartimental angesiedelt sind, müssen ebenfalls weit reseziert werden. Kann der gewünschte Sicherheitsabstand von 2 bis 3 cm nicht eingehalten werden, weil der Tumor am Knochen, an den Gefäss- und Nervenstrukturen oder der Faszie anliegt, müssen spezielle chirurgische Techniken wie Mitresektion gesunder Hüllschichten (Muskelfaszie, Knochenlamelle, Periost, Epineurium, Gefässadventitia), häufig in Kombination mit präoperativer Radiotherapie, angewandt werden, um eine R0-Resektion respektive eine sichere lokale Kontrolle erreichen zu können (9, 10). In der Literatur findet man keine eindeutig belegbare und klinisch nachvollziehbare Definition des Begriffs «weite Resektion». Die Frage ist weniger «Wie weit ist weit genug?», sondern lautet vor allem: «Welches ist die onkologische Sicherheitszone?» Wahrscheinlich kann ein muskulärer Sicherheitsabstand von 1 cm mit einem subkutanen Fettgewebemantel von 2 cm mit einer intakten Muskelfaszie von weniger als 1 mm über dem Weichgewebesarkom gleichgesetzt werden, auch wenn dies durch die Literatur nicht eindeutig bestätigt werden kann. Für die Klinik ist derzeit, unabhängig von der intraoder extrakompartimentalen Tumorlokalisation, die R-Klassifikation ausschlaggebend, um eine Vergleichbarkeit der Ergebnisse zu ermöglichen. Marginale (entlang der Pseudotumorkapsel) oder gar intraläsionale Resektionen sind onkologisch inadäquat und durch additive Therapieverfahren in der Regel nur schwer zu kompensieren.
Differenziertes Vorgehen je nach Lokalisation Bezüglich der operativen Therapie bei Sarkomen des Körperstammes gelten die gleichen Regeln wie bei den Extremitäten. Ist das primäre Ziel, eine R0-Resektion zu erreichen, nicht zu realisieren, sind auch hier die neoadjuvanten Therapiekonzepte mit dem Ziel der lokalen Tumorkontrolle möglich, wobei hier die Radiotherapie eine wichtige Therapiemodalität darstellt. Plastische Rekonstruktionen sind hier häufiger notwendig als bei Sarkomen an den Extremitäten. Diese bestehen aus Thoraxwand- und Bauchwandrekonstruktionen mit verschiedenen Techniken und Implantaten. Weichteilsarkome des Retroperitoneums werden aufgrund der unspezifischen klinischen Symptomatik häufig erst in einem fortgeschritteneren Stadium dia-
14 SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 2/2012
Im Fokus: Sarkome und seltene Malignome
andere Therapie benötigen würden. Auch bei den retroperitonealen Sarkomen ist eine Heilung nur durch eine R0-Resektion zu erreichen (11). Diese ist in den meisten Fällen nur durch eine exzessive Resektion zu realisieren und immer individuell in Abhängigkeit von der Lokalisation zu planen (12). Die Rate an R1-Resektionen ist im Vergleich zu den Extremitätensarkomen erhöht. Liegt primär keine Resektabilität vor, so sind auch hier neoadjuvante Therapiekonzepte wiederum mittels Radiotherapie indiziert. Bei der operativen Therapieplanung ist zu berücksichtigen, dass die Möglichkeit einer adjuvanten Radiotherapie im Vergleich zu den Extremitätensarkomen deutlich eingeschränkt ist, da sich meist intestinale Organe im Bereich des ehemaligen Tumorbettes postoperativ positionieren.
Abbildung 3: Radiologische Kontrolle direkt postoperativ mit noch liegender Redon-Drainage. Die offene Epiphysenfuge ist gut erkennbar.
Chemotherapie und postoperativer Verlauf
Die eingeleitete Chemotherapie bei unserem zehnjährigen Patienten gemäss dem Therapieprotokoll Euro-Ewing 99 liess das Sarkom deutlich schrumpfen. (Abbildung 1) Nach der letzten neoadjuvanten Chemotherapiesitzung wurde die Indikation zur Resektion des proximalen Humerus mit Transplantation einer vaskularisierten Epiphysenfugen-Fibula gestellt, welche zusammen mit einem mikrovaskulären Chirurgen erfolgreich durchgeführt werden konnte (Abbildungen 2 und 3). Die Rekonstruktion im wachsenden Skelett stellt eine besondere Herausforderung dar. Da die mit der Fibula eingebrachte Wachstumsfuge vaskulär angeschlossen wurde, wird sich über die Zeit ein Neohumeruskopf bilden. Die Pathologen haben bestätigt, dass die Resektion des Tumors im Gesunden stattgefunden hat. Der postoperative Verlauf entwickelte sich problemlos. Zwischenzeitlich konnte das postoperative chemotherapeutische Behandlungschema mit insgesamt 8 Zyklen Vincristin, Ifosfamid und Actinomycin D die weiteren Chemotherapiezyklen erfolgreich beendet werden.
Abbildung 4: Schematische Darstellung zur präzisen Operationsplanung.
gnostiziert. Vor der operativen Therapie ist die histologische Sicherung der Diagnose wichtig, um ein Lymphom oder einen gastrointestinalen Stromatumor (GIST) auszuschliessen, die eine grundsätzlich
Merkpunkte
▲ Die Behandlung von Sarkomen soll an einem spezia-
lisierten Zentrum erfolgen.
▲ Jeder Patient erfährt eine individuell zugeschnit-
tene Therapie.
▲ Die Biopsie muss vom orthopädischen Onkologen,
welcher auch eine definitive Resektion vornimmt, durchgeführt werden.
▲ Chirurgisch ist die R0-Resektion anzustreben. ▲ Die Prognose wird durch interdisziplinäre Betreuung
wesentlich verbessert.
16 SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 2/2012
Im Fokus: Sarkome und seltene Malignome
Fazit
Die zwingende Notwendigkeit einer interdiszi-
plinären Teamarbeit wird an diesem Fallbeispiel
deutlich. Diese Interdisziplinarität wird in Zukunft im-
mer wichtiger, wenn die neuesten molekularen Er-
rungenschaften in Diagnose, Monitoring und (chirur-
gischer) Therapie Einzug halten.
▲
Dr. med. Kourosh Modaressi Oberarzt Tumorchirurgie; spez. Knochen- und Weichteilchirurgie Universitätsklinik Balgrist 8008 Zürich E-Mail: kourosh.modaressi@balgrist.ch
Prof. Dr. med. Felix Niggli Abteilungsleiter Kinderonkologie Universitäts-Kinderklinik 8032 Zürich E-Mail: felix.niggli@kispi.uzh.ch
Prof. Dr. med. Dr. sc. nat. Bruno Fuchs Abteilungsleiter Tumorchirurgie Universitätsklinik Balgrist 8008 Zürich E-Mail: bruno.fuchs@balgrist.ch
Quellen:
1. Gustafson P, Dreinhofer KE, Rydholm A.: Soft tissue sarcoma should be treated at a tumor center. A comparison of quality of surgery in 375 patients. Acta Orthop Scand 1994; 65(1): 47–50.
2. Greenlee RT, Hill-Harmon MB, Murray T, Thun M.: Cancer statistics. Cancer J Clin 2001; 51: 15–36.
3. Mankin HJ, Hornicek FJ: Diagnosis, classification, and management of soft tissue sarcomas. Cancer Control 2005; 12(1): 5–21.
4. Bruns J, Yazigee O, et al.: Bioptische Sicherung muskuloskelettaler Tumoren. Der Onkologe 2006; 12: 119–27.
5. Deutsche Gesellschaft für Orthopädie und orthopädische Chirurgie und des Berufsverbandes für Orthopädie: Leitlinie: Diagnostik muskuloskelettaler Malignome (033/034).
6. Fuchs B: Die Biopsie von Knochen- und Weichteiltumoren. Schweizerisches Krebsbulletin – Bulletin Swiss du Cancer 2008; 8(4): 293–95.
7. Ladenstein R, Pötschger U et al.: Primary disseminated multifocal Ewing sarcoma: results of the Euro-EWING 99 trial. J Clin Oncol. 2010; 28(20): 3284–91.
8. Potratz J, Jürgens H, Craft A, Dirksen U. Ewing sarcoma: biology-based therapeutic perspectives. Pediatr Hematol Oncol. 2012(1): 12–27.
9. Peter C, Wunder JS.: Peripheral Nerve Considerations in the Management of Extremity Soft Tissue Sarcomas. In: Tunn PU (Hrsg.): Treatment of Bone and Soft Tissue Sarcomas. Berlin, Heidelberg 2009.
10. Mahendra A, Wunder JA.: Management of Vascular Involvement in Extremity Soft Tissue Sarcoma. In: Tunn PU (Hrsg.): Treatment of Bone and Soft Tissue Sarcomas. Berlin, Heidelberg 2009.
11. Mendenhall WM, Zlotecki RA, et al.: Retroperitoneal soft tissue sarcoma. Cancer 2005; 104(4): 669–75.
12. Dickinson IC, Whitwell DJ, Battituta D et al. Surgical margin and its influence on survival in soft tissue sarcoma. J Surg 2006; 76 (3): 104–09.
SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 2/2012
17