Transkript
Im Fokus: Kolorektalkarzinom
Medikamentöse Behandlung des metastasierten kolorektalen Karzinoms
Aktuelle rationale Therapien Die medikamentöse Behandlung des kolorektalen Karzinoms hat in den letzten zehn Jahren eindrückliche Fortschritte gemacht. So stehen heute neben dem altbewährten Fluorouracil neue Zytostatika zur Verfügung wie Irinotecan und Oxaliplatin. Auf der Basis randomisierter klinischer Studien lassen sich aktuelle rationale Therapiestrategien formulieren, wie in diesem Beitrag dargestellt. Die Therapiepalette hat sich erweitert um die monoklonalen Antikörper Bevacizumab und Cetuximab, welche in neuen klinischen Vergleichsstudien untersucht und erfolgreich eingesetzt wurden.
BERNHARD C. PESTALOZZI, DIRK JÄGER, CHRISTIAN TAVERNA
Der 1957 synthetisierte Antimetabolit 5-Fluorouracil stellte während Jahrzehnten das einzige Medikament in der Behandlung von Patienten mit kolorektalem Karzinom dar. In klinischen Studien der Siebzigerund Achtzigerjahre wurde die Wirksamkeit von 5-Fluorouracil durch die kontinuierliche Applikation und die biochemische Modulation mit Leukovorin verbessert. Erst in den Neunzigerjahren haben sich die therapeutischen Möglichkeiten erheblich erweitert durch die Entwicklung oraler Vorstufen des 5-Fluorouracils sowie vor allem durch den Topoisomerase-I-Inhibitor Irinotecan und das Platinderivat Oxaliplatin.
Capecitabine
Wegen unsicherer Resorption kann 5-Fluorouracil nicht oral verabreicht werden. Da es zudem eine kurze Halbwertszeit hat und besser wirkt bei kontinuierlicher Applikation, wurden orale Vorstufen entwickelt, mit denen vergleichbare Wirkspiegel erreicht werden können. Heute steht in der Schweiz nur Capecitabine (Xeloda®) als orale Vorstufe von 5-Fluorouracil zur Verfügung. Capecitabine ist in zwei grossen randomisierten Studien gegenüber dem konventionellen Mayo-Regime mit Bolus-5-Fluorouracil getestet worden (1, 2). Dabei zeigte sich eine gewisse Verbesserung bezüglich der Ansprechrate
(RR, response rate) und ein vergleichbares progressionsfreies Überleben (PFS, progression free survival) beziehungsweise Gesamtüberleben (OS, overall survival). Die gastrointestinale und hämatologische Toxizität von Capecitabine war geringer als diejenige des Mayo-Regimes. Dafür trat häufiger ein meist mildes Hand-Fuss-Syndrom auf. Capecitabine ist als Monotherapie geeignet für Patienten, bei denen Kombinationsbehandlungen riskant erscheinen und deren Compliance mit der Tabletteneinnahme gewährleistet ist. Capecitabine kann mit Irinotecan beziehungsweise Oxaliplatin kombiniert werden, was in mehreren Phase-II-Studien gezeigt wurde. Allerdings fehlen vergleichende Studien, welche erlauben würden, generell das kontinuierlich zu infundierende und mit Leukovorin ergänzte 5-Fluorouracil durch das orale Capecitabine zu ersetzen.
Irinotecan
Irinotecan (CPT-11, Campto®) ist ein TopoisomeraseI-Inhibitor, dessen Wirkprinzip darauf beruht, Brüche in der DNS zu initiieren. In einer langen Serie von klinischen Studien – Phase I (Dosisfindung), Phase II (Wirksamkeit) und Phase III (randomisierte Vergleichsstudie) – wurde die Wirksamkeit von Irinotecan beim kolorektalen Karzinom nachgewiesen. Iri-
ONKOLOGIE 2/2004
17
Im Fokus: Kolorektalkarzinom
notecan verbessert danach das Überleben im Vergleich zur «best supportive care». Irinotecan ist wirksam auch bei Resistenz auf 5-Fluorouracil. Besser als die Monotherapie mit Irinotecan ist die Kombination mit 5-Fluorouracil und Leukovorin (4). Das Regime von Irinotecan mit Bolus-5-Fluorouracil und Leukovorin wird als IFL bezeichnet (4). Auch in Kombination mit Irinotecan ist die kontinuierliche Gabe des 5-Fluorouracils der BolusApplikation vorzuziehen (3, 5). In drei grossen randomisierten Studien wurden 5-Fluorouracil und Leukovorin gegen dieselben Medikamente plus Irinotecan verglichen (3–5). In allein drei Studien wurden die Remissionsraten, die progressionsfreie Überlebenszeit und das Überleben verbessert (Tabelle). In den USA wurde das IFL-Regime ab dem Jahr 2000 zur Standardtherapie (4), während in Europa die kontinuierliche 5-Fluorouracil-Applikation vorgezogen wird (3, 5). Die deutsche Arbeitsgruppe für Internistische Onkologie (AIO) verwendet wöchentlich eine 24-stündige Infusion, während in Frankreich alle zwei Wochen eine 48-stündige Infusion zur Anwendung kommt (de Gramont [3]). Diese 5-Fluorouracil-Applikation mit einbis zweitägiger Infusion scheint wirksamer und weniger toxisch zu sein als die Bolus-Applikation. Bei etwa 20 Prozent der Patienten kommt es zu schwerer Diarrhö (Kolitis), was besonders in Kombination mit Neutropenie gefährlich werden kann. Irinotecan soll nur von Spezialisten angewendet werden, die mit der Substanz und ihren erwünschten und unerwünschten Wirkungen vertraut sind. Irinotecan kann auch zu Alopezie und Fatigue führen.
Oxaliplatin
Oxaliplatin (Eloxatine®) ist ein Platin-Analog, das DNS-Addukte bildet. Oxaliplatin ist in der Monotherapie nur wenig wirksam beim kolorektalen Karzinom, deshalb wird es immer mit 5-Fluorouracil und Leukovorin kombiniert. Die Zugabe von Oxaliplatin zu 5-Fluorouracil und Leukovorin gegenüber diesen beiden Substanzen allein wurde in drei grossen Studien geprüft (Tabelle [6–8]). In allen Studien zeigte sich eine Verbesserung der Ansprechrate und des progressionsfreien Überlebens. Die Verlängerung der
Überlebenszeit war nicht statistisch signifikant. Erst die grosse amerikanische Studie von Goldberg, welche die Überlegenheit von FOLFOX (FOLinsäure = Leukovorin, 5-Fluorouracil, OXaliplatin) gegenüber dem IFL-Regime ergab, führte dazu, dass FOLFOX heute auch in den USA als ein wichtiger Standard in der Behandlung des metastasierten kolorektalen Karzinoms gilt (9). Die Hauptnebenwirkung von Oxaliplatin ist die Neurotoxizität. Eine reversible sensomotorische Neuropathie tritt in Abhängigkeit der kumulativen Dosis auf und wirkt dosislimitierend. Zudem muss der Patient auf eine meist selbstlimitierende akute kälteassoziierte Neuropathie aufmerksam gemacht werden, die sich vorzugsweise als pharyngo-laryngeale Dysästhesie oder periphere Parästhesie manifestiert. Oxaliplatin ist nur mässig hämatotoxisch und führt selten zu Alopezie.
Oxaliplatin oder Irinotecan?
Die Überlegenheit des Oxaliplatin-haltigen FOLFOX über das Irinotecan-haltige IFL-Regime (9) beweist keineswegs, dass Oxaliplatin grundsätzlich wirksamer als Irinotecan ist. Die besseren Therapieergebnisse könnten nämlich darauf zurückzuführen sein, dass die Bolus-Applikation des 5-Fluorouracils im IFL der kontinuierlichen Applikation im FOLFOX unterlegen ist. Für diese Interpretation spricht die Studie von Tournigand, welche auch Irinotecan mit dem kontinuierlich infundierten 5-Fluorouracil zu FOLFIRI kombiniert (10). In dieser Studie wurde die Sequenz FOLFIRI, gefolgt von FOLFOX, bei Progression verglichen mit der umgekehrten Sequenz, FOLFOX, gefolgt von FOLFIRI. Im Gesamtüberleben ergab sich kein Unterschied zwischen diesen Sequenzen, die also als gleichwertig anzusehen sind. Das Zweitlinien-FOLFOX (n= 81) zeigte ein etwas besseres Ansprechen (14 vs. 4%) und ein besseres progressionsfreies Überleben (4,1 vs. 2,5 Monate) als das ZweitlinienFOLFIRI (n = 69). Die Antwort auf die Frage «Oxaliplatin oder Irinotecan?» lautet also: beide, hintereinander.
Synthese
Auf der Basis dieser Studien ergeben sich zum heutigen Zeitpunkt folgende Schlüsse (13):
1. Die so genannten «Doublets» (FOLFOX oder FOLFIRI) sind die wirksamsten Kombinationen.
2. Die Triplets (Oxaliplatin, Irinotecan, 5-Fluorouracil gleichzeitig) sind bisher nicht erfolgreicher, aber erheblich toxischer.
3. 5-Fluorouracil ist weiterhin ein zentraler Bestandteil der wirksamsten Regimes.
4. Kontinuierlich infundiertes 5-Fluorouracil ist der wirksamste Partner, kombiniert mit Irinotecan und mit Oxaliplatin – besser als Bolus-Fluorouracil. Das monatliche Bolus-5Fluorouracil-Regime (so genanntes Mayo-Regime) gilt nicht mehr als Standard.
5. Mediane Überlebenszeiten von 20 Monaten können erreicht werden, wenn alle drei Medikamente für eine sequenzielle Behandlung zur Verfügung stehen (14).
6. Die Wirksamkeit einer Zweit- oder Drittlinientherapie auf das Überleben gilt als gesichert.
Neue monoklonale Antikörper: Cetuximab und Bevacizumab
Cetuximab ist ein humanisierter monoklonaler Antikörper gegen den Membranrezeptor «epithelial growth factor receptor» (EGFR). In einer Phase-III-Studie konnte gezeigt werden, dass bei Irinotecan-resistenten Karzinomen die Kombination von Irinotecan mit Cetuximab ein nochmaliges Ansprechen ergeben kann (Tabelle [11]). Auch das progressionsfreie Überleben, nicht aber das Überleben, wurde davon beeinflusst. Cetuximab (Erbitux®) ist in der Schweiz zugelassen, jedoch nur in Kombination mit Irinotecan und für die spezielle Situation der Irinotecan-resistenten Karzinome. An der Jahresversammlung der amerikanischen Onkologen 2003 (ASCO) wurden überraschende Resultate der Kombination von Bevacizumab mit IFL (Irinotecan, 5-Fluorouracil, Leukovorin) vorgestellt (12). Bevacizumab ist ein monoklonaler humanisierter Antikörper gegen den Wachstumsfaktor der Angiogenese «vascular endothelial growth factor» (VEGF). In einer grossen randomisierten Studie von 815 Patienten mit fortgeschrittenem
18 ONKOLOGIE 2/2004
Im Fokus: Kolorektalkarzinom
Kolorektalkarzinom war die Kombination von IFL mit Bevacizumab derjenigen mit Plazebo bezüglich Ansprechen, Zeit bis zur Progression und Überleben signifikant überlegen (Tabelle [12]). Nebenwirkungen von Bevacizumab sind arterielle Hypertonie und selten Gastrointestinalblutungen. Bevacizumab (Avastin®) soll bald auch in der Schweiz erhältlich werden. Da es bisher nur in Kombination mit IFL getestet wurde, wird es wohl als Zweitlinien-Medikament nach FOLFOX eingesetzt werden. Neben weiteren Antikörpern werden zurzeit auch andere Substanzen beim kolorektalen Karzinom untersucht: die Thyrosinkinasehemmer Gefitinib (ZD1839, Iressa®), Erlotinib (OSI-774, Tarceva®) sowie PTK/ZK 22586. Auch neue Zytostatika wie Epothilone B und die Inhibitoren der Zyllooxygenase II (Cox-II-Inhibitoren) werden studiert. Die Kosten dieser neuen Therapiemöglichkeiten werden für das Gesundheitswesen eine besondere Herausforderung darstellen.
Zusammenfassend ist festzuhalten, dass
uns die Entwicklung der letzten zehn
Jahre eine erfreuliche Erweiterung der
therapeutischen Möglichkeiten in der
Behandlung des kolorektalen Karzinoms
beschert hat.
▲
PD Dr. med. Bernhard C. Pestalozzi PD Dr. med. Dirk Jäger
Dr. med. Christian Taverna Klinik und Poliklinik für Onkologie
UniversitätsSpital
8091 Zürich
(Schlüsselwörter: kolorektales Karzinom, Irinotecan, Oxaliplatin, Capecitabine, Bevacizumab)
Quellen:
1. Van Cutsem E, Twelves C, Cassidy J, et al.: Oral capecitabine compared with intravenous fluorouracil plus leucovorin in patients with metastatic colorectal cancer: Results of a large phase III study. J Clin Oncol 2001; 19: 4097–4106.
2. Hoff PM, Ansari R, Batist G, et al.: Comparison of oral capecitabine versus intravenous fluorouracil plus leucovorin as first-line treatment in 605 patients with metastatic colorectal cancer: Results of a randomized phase III study. J Clin Oncol 2001; 19: 2282–2292.
3. Douillard JY, Cunningham D, Roth AD, et al.: Irinotecan combined with fluorouracil compared with fluorouracil alone as first-line treatment for metastatic colorectal cancer: A multicentre randomised trial. Lancet 2000; 355: 1041–1047.
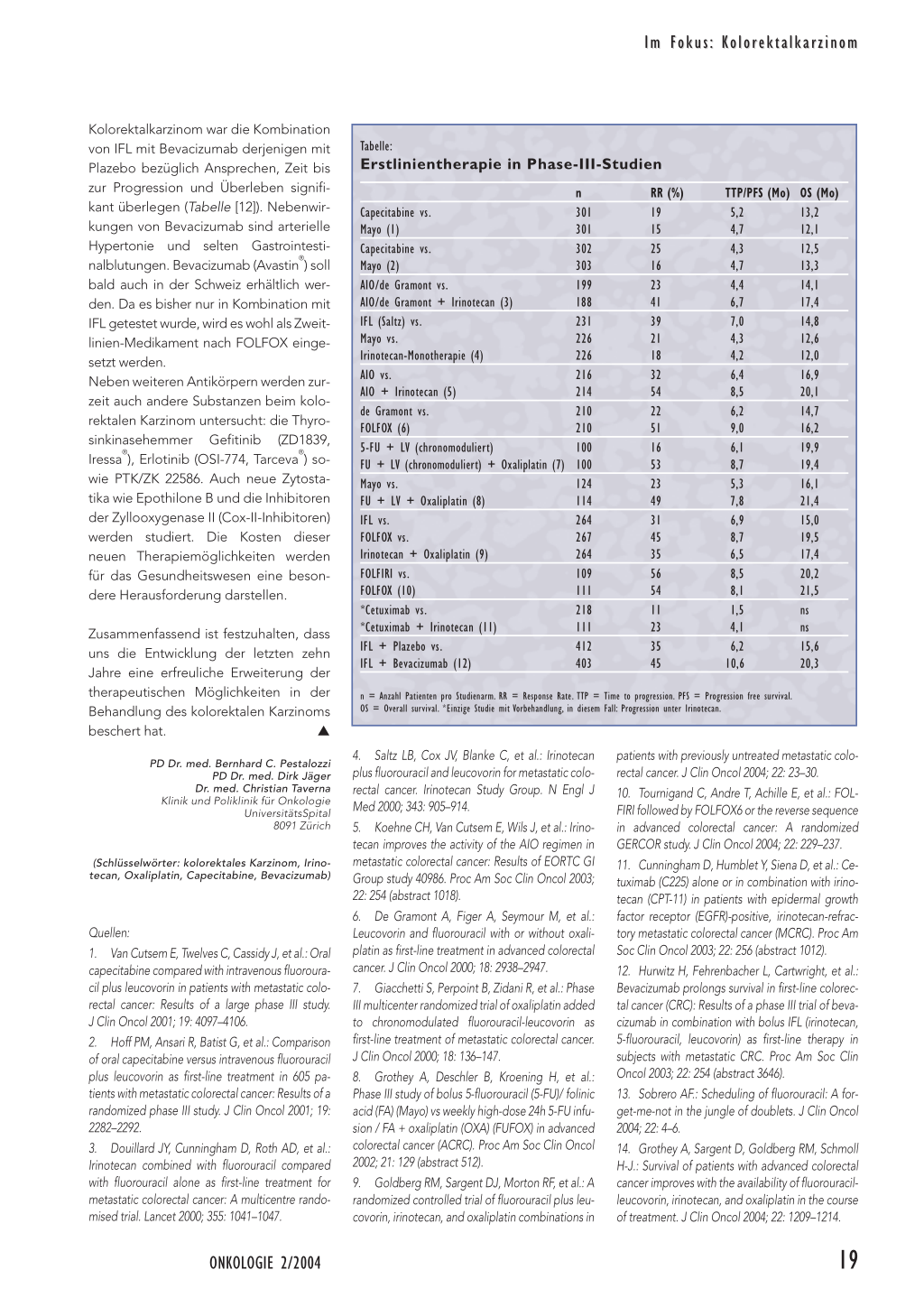
Tabelle: Erstlinientherapie in Phase-III-Studien
n
Capecitabine vs. Mayo (1)
301 301
Capecitabine vs. Mayo (2)
302 303
AIO/de Gramont vs. AIO/de Gramont + Irinotecan (3)
199 188
IFL (Saltz) vs. Mayo vs.
231 226
Irinotecan-Monotherapie (4)
226
AIO vs.
216
AIO + Irinotecan (5)
214
de Gramont vs.
210
FOLFOX (6)
210
5-FU + LV (chronomoduliert)
100
FU + LV (chronomoduliert) + Oxaliplatin (7) 100
Mayo vs. FU + LV + Oxaliplatin (8)
124 114
IFL vs. FOLFOX vs.
264 267
Irinotecan + Oxaliplatin (9)
264
FOLFIRI vs.
109
FOLFOX (10)
111
*Cetuximab vs.
218
*Cetuximab + Irinotecan (11)
111
IFL + Plazebo vs.
412
IFL + Bevacizumab (12)
403
RR (%)
19 15
25 16
23 41
39 21 18
32 54
22 51
16 53
23 49
31 45 35
56 54
11 23
35 45
TTP/PFS (Mo) OS (Mo)
5,2 13,2 4,7 12,1
4,3 12,5 4,7 13,3
4,4 14,1 6,7 17,4
7,0 14,8 4,3 12,6 4,2 12,0
6,4 16,9 8,5 20,1
6,2 14,7 9,0 16,2
6,1 19,9 8,7 19,4
5,3 16,1 7,8 21,4
6,9 15,0 8,7 19,5 6,5 17,4
8,5 20,2 8,1 21,5
1,5 ns 4,1 ns
6,2 15,6 10,6 20,3
n = Anzahl Patienten pro Studienarm. RR = Response Rate. TTP = Time to progression. PFS = Progression free survival. OS = Overall survival. *Einzige Studie mit Vorbehandlung, in diesem Fall: Progression unter Irinotecan.
4. Saltz LB, Cox JV, Blanke C, et al.: Irinotecan plus fluorouracil and leucovorin for metastatic colorectal cancer. Irinotecan Study Group. N Engl J Med 2000; 343: 905–914.
5. Koehne CH, Van Cutsem E, Wils J, et al.: Irinotecan improves the activity of the AIO regimen in metastatic colorectal cancer: Results of EORTC GI Group study 40986. Proc Am Soc Clin Oncol 2003; 22: 254 (abstract 1018).
6. De Gramont A, Figer A, Seymour M, et al.: Leucovorin and fluorouracil with or without oxaliplatin as first-line treatment in advanced colorectal cancer. J Clin Oncol 2000; 18: 2938–2947.
7. Giacchetti S, Perpoint B, Zidani R, et al.: Phase III multicenter randomized trial of oxaliplatin added to chronomodulated fluorouracil-leucovorin as first-line treatment of metastatic colorectal cancer. J Clin Oncol 2000; 18: 136–147.
8. Grothey A, Deschler B, Kroening H, et al.: Phase III study of bolus 5-fluorouracil (5-FU)/ folinic acid (FA) (Mayo) vs weekly high-dose 24h 5-FU infusion / FA + oxaliplatin (OXA) (FUFOX) in advanced colorectal cancer (ACRC). Proc Am Soc Clin Oncol 2002; 21: 129 (abstract 512).
9. Goldberg RM, Sargent DJ, Morton RF, et al.: A randomized controlled trial of fluorouracil plus leucovorin, irinotecan, and oxaliplatin combinations in
patients with previously untreated metastatic colorectal cancer. J Clin Oncol 2004; 22: 23–30.
10. Tournigand C, Andre T, Achille E, et al.: FOLFIRI followed by FOLFOX6 or the reverse sequence in advanced colorectal cancer: A randomized GERCOR study. J Clin Oncol 2004; 22: 229–237.
11. Cunningham D, Humblet Y, Siena D, et al.: Cetuximab (C225) alone or in combination with irinotecan (CPT-11) in patients with epidermal growth factor receptor (EGFR)-positive, irinotecan-refractory metastatic colorectal cancer (MCRC). Proc Am Soc Clin Oncol 2003; 22: 256 (abstract 1012).
12. Hurwitz H, Fehrenbacher L, Cartwright, et al.: Bevacizumab prolongs survival in first-line colorectal cancer (CRC): Results of a phase III trial of bevacizumab in combination with bolus IFL (irinotecan, 5-fluorouracil, leucovorin) as first-line therapy in subjects with metastatic CRC. Proc Am Soc Clin Oncol 2003; 22: 254 (abstract 3646).
13. Sobrero AF.: Scheduling of fluorouracil: A forget-me-not in the jungle of doublets. J Clin Oncol 2004; 22: 4–6.
14. Grothey A, Sargent D, Goldberg RM, Schmoll H-J.: Survival of patients with advanced colorectal cancer improves with the availability of fluorouracilleucovorin, irinotecan, and oxaliplatin in the course of treatment. J Clin Oncol 2004; 22: 1209–1214.
ONKOLOGIE 2/2004
19