Transkript
SCHWERPUNKT
Screening auf Ovarialund Endometriumkarzinome
Welche Untersuchungen sind sinnvoll?
Ovarial- und Endometriumkarzinome sind in fortgeschrittenen Stadien mit einer hohen Mortalität verbunden. Naheliegend ist, dass ein systematisches Screening helfen könnte, asymptomatische Frühstadien zu identifizieren. Die aktuelle Datenlage zeigt leider, dass ein Screening bei asymptomatischen Frauen zu keiner Senkung der karzinomspezifischen Mortalität führt. Dennoch gibt es beim Ovarialkarzinom mögliche Hinweise für den Nutzen eines multimodalen Screenings unter bestimmten Voraussetzungen.
JANNA PAPE, DANIEL FINK, ELEFTHERIOS PIERRE SAMARTZIS
Janna Pape
Jährlich werden zirka 600 neue Ovarialkarzinomerkrankungen in der Schweiz diagnostiziert, weltweit rund 250 000 pro Jahr. Die Symptome sind meist unspezifisch oder fehlen, sodass die Diagnose meist in einem späteren Tumorstadium (≥ FIGO III) gestellt wird (1). Endometriumkarzinome stellen in unseren Breitengraden die häufigste maligne gynäkologische Erkrankung dar und sind nach Mamma-, Kolon- und Bronchialkarzinom das vierthäufigste Karzinom der Frau. Es gilt zwar als Karzinom der älteren Frau, jedoch tritt es gelegentlich auch in jüngeren Jahren auf, insbesondere bei Vorliegen von familiären Tumorsyndromen wie dem Lynch-Syndrom (2).
Daniel Fink Eleftherios Pierre Samartzis
Screening von Ovarialkarzinomen in der Allgemeinpopulation
Das Ovarialkarzinom weist in der Allgemeinpopulation eine insgesamt niedrige Inzidenz auf, sodass ein generelles Screening schwierig ist. Zwei diagnostische Mittel stehen hierbei hauptsächlich zur Verfügung: der transvaginale Ultraschall und der Tumormarker CA-125. Vier gross angelegte, prospektive, klinische Studien untersuchten ihre Effek-
Merkpunkte
I Sowohl beim Ovarial- als auch beim Endometriumkarzinom konnten gross angelegte Studien für ein Screening mittels transvaginalen Ultraschalls und zusätzlicher Tumormarkerbestimmung (CA-125) keinen Überlebensvorteil nachweisen.
I Einen möglichen Vorteil eines multimodalen Screenings zeigte die britische UKCTOCSStudie in einer Subgruppenanalyse nach Ausschluss der bei Erstuntersuchung diagnostizierten Ovarialkarzinomfälle.
I Die gynäkologische Vorsorge bleibt für diese zwei gynäkologischen Karzinome klar symptomorientiert und unterstreicht die Bedeutung einer ausführlichen Aufklärung über mögliche (wenn auch zum Teil unspezifische) Frühzeichen.
I In nachgewiesenen genetischen Risikosituationen ist das risikoreduzierende operative Vorgehen für die Prävention des Ovarial- und/oder Endometriumkarzinoms die einzige wirkungsvolle Massnahme.
tivität entweder einzeln oder in Kombination (vgl.Tabelle):
Die Studie SCSOCS (Shizuoka Cohort Study of Ovarian Cancer Screening) Mehr als 80 000 asymptomatische postmenopausale Patientinnen wurden in dieser japanischen Studie (3) untersucht und entweder in eine Screeninggruppe mit jährlichen CA-125-Bestimmungen und vaginalem Ultraschall (TVUS) (n = 41 688) oder in eine Kontrollgruppe ohne Massnahmen (n = 40 799) randomisiert. Es wurden insgesamt nur 35 Ovarialkarzinome entdeckt, hierbei ergab sich ein Trend zu einem höheren Anteil früherer Tumorstadien in der Screeninggruppe (63 vs. 38%). Ergebnisse zur Gesamtmortalität sind bisher nicht publiziert.
Die Kentucky-Ovarian-Cancer-Screening-Studie Diese nicht randomisierte Kohortenstudie (4) untersuchte den Effekt eines jährlichen Ultraschallscreenings auf das Tumorstadium bei Diagnosestellung bei mehr als 37 000 Frauen in einem Zeitraum über 23 Jahre. Rekrutiert wurden Frauen über 25 Jahre mit positiver Familienanamnese oder asymptomatische Frauen über 50 Jahre. Als pathologische Kriterien galten Zysten mit soliden Anteilen oder mit einem Volumen > 20 cm3 bei prämenopausalen und > 10 cm3 bei postmenopausalen Patientinnen. Die weitere Abklärung erfolgte mittels Verlaufsultraschall nach 4 bis 6 Wochen und gegebenenfalls invasiver Abklärung (1,4% der Fälle). Als Kontrollgruppe diente eine gleich grosse Kohorte aus derselben Gegend. Insgesamt wurden 76 Karzinome in der gescreenten Kohorte entdeckt, 70% im FIGO-Stadium I/II (27% in der Kontrollgruppe). Auch die 5-Jahres-Überlebensrate von Frauen mit invasiven Ovarialkarzinomen lag in der Untersuchungsgruppe signifikant höher als in der Vergleichskohorte (74,8 vs. 53,7%).
12 GYNÄKOLOGIE 1/2020
SCHWERPUNKT
Limitationen dieser Studie sind jedoch die fehlende Randomisierung sowie der Einschluss von Borderlinetumoren in die Karzinomgruppe. Ferner wurde die Studie nur in einem Zentrum mit hoher sonografischer Expertise durchgeführt, sodass die Resultate nicht ohne Weiteres für eine generelle Screeningempfehlung extrapolierbar sind.
Die Studie PLCO (Prostate, Lung, Colorectal and Ovarian Cancer Screening) In dieser Studie (5, 6) wurden über 78 000 asymptomatische Frauen zwischen 55 und 74 Jahren in den Jahren 1993 bis 2001 untersucht. In der Screeninggruppe (n = 34 253) wurde jährlich der Tumormarker CA-125 bestimmt sowie ein Ultraschall durchgeführt. Die Kontrollgruppe (n= 34 304) erhielt kein Screening. Als pathologische Kriterien wurden ein CA-125 > 35 U/ml, ein Ovarialvolumen > 10 cm3, Ovarialzysten > 10 cm3 oder Ovarialzysten mit soliden oder papillären Anteilen gewertet. Über das weitere Prozedere entschied jeweils der behandelnde Arzt. Insgesamt wurden in der Screeninggruppe 212 (davon 27,8% FIGO I/II) und in der Kontrollgruppe 176 Ovarialkarzinome registriert. In der Screeninggruppe kam es zu 3285 falsch positiven Befunden, davon wurde zirka ein Drittel der Fälle (n = 1080) invasiv abgeklärt; bei 15% bestanden schwerwiegende Komplikationen. Eine Reduktion der Mortalität konnte in der primären Analyse nicht gezeigt werden (Screeninggruppe 3,1 vs. Kontrollgruppe 2,6/10 000 Frauen), jedoch eine erhöhte untersuchungsbedingte Morbidität (7).
Die Studie UKCTOCS (UK Collaborative Trial of Ovarian Cancer Screening) In dieser Studie (8) wurden zwischen 2001 und 2005 mehr als 200 000 asymptomatische Frauen zwischen 50 und 74 Jahren eingeschlossen. Die Studienteilnehmer wurden in drei Gruppen randomisiert: Screeninggruppe 1 (n = 50 639) wurde jährlich mittels Ultraschall untersucht, Screeninggruppe 2 (n = 50 640) erhielt ein kombiniertes Screening mit CA-125-Bestimmung und Ultraschalluntersuchung. In der Kontrollgruppe (n = 101 359) erfolgten keine Massnahmen. Zu beachten ist dabei auch, dass der Algorithmus zur Bestimmung des individuellen Risikos auf mehreren seriellen CA-125-Bestimmungen im Vergleich zur Baseline beruht. Nur ein positiver Wiederholungsbefund führte zu einer invasiven Abklärung. Die Studiengruppen zeigten folgende Resultate: In der Screening-Gruppe 1 kam es in 845 Fällen (1,8%) zu invasiven Abklärungen. 45 primäre Ovarialkarzinome (inkl. 20 Borderlinetumoren) wurden entdeckt, was einem positiven Vorhersagewert von 5,3% entspricht.
Das kombinierte Screening in der Screeninggruppe 2 zeigte mit 43,3% einen deutlich höheren positiven Vorhersagewert: Mittels invasiver Abklärungen (n = 97 entsprechend 0,2%) wurden 42 primäre Ovarialkarzinome (inkl. 8 Borderlinetumoren) diagnostiziert. In beiden Screeningstrategien waren knapp die Hälfte der Befunde Frühkarzinome im FIGO-Stadium I/II. Im medianen Follow-up von 11,1 Jahren wurden insgesamt 1282 Ovarialkarzinome entdeckt: 314 (0,6%) im reinen Ultraschallscreening, 338 (0,7%) im kombinierten Screening und 630 in der Kontrollgruppe. Die Mortalität konnte um 11% nach reinem Ultraschallscreening und um 15% nach kombiniertem Screening gesenkt werden, jedoch war dieses Ergebnis nicht signifikant. Diese Studie stellte jedoch einen wichtigen Punkt fest: Nach Ausschluss der Frauen, die bereits im initialen Screening ein Ovarialkarzinom aufwiesen, ergab sich in der multimodalen Screeninggruppe eine Reduktion der Todesfälle aufgrund Ovarialkarzinomen um insgesamt 20% bei einer Mortalitätsreduktion von 8% in den Jahren 0 bis 7 und 28% in den Jahren 7 bis 14. Weitere Langzeitauswertungen werden zeigen, ob sich dieser Trend über einen längeren Beobachtungszeitraum fortsetzt. Wenn sich der Nutzen eines Screenings in der Langzeitauswertung dieser Studie bestätigt, bleibt auch zu klären, in welchem Alter damit begonnen werden sollte. Diese Resultate könnten somit möglicherweise für den Nutzen eines Screenings unter bestimmten Voraussetzungen sprechen, jedoch sind diese Daten im längeren Follow-up zu bestätigen.
Aktuelle Schlussfolgerung Einen eindeutigen Nutzen und eine verminderte Mortalität durch ein generelles Screening mittels transvaginaler Sonografie und Bestimmung des CA125 konnten die bisherigen oben beschriebenen Studien folglich nicht erbringen. Im Gegenteil, zumindest in der PLCO-Studie führten falsch positive Ergebnisse zu einem signifikant höheren Morbiditäts- und Mortalitätsrisiko durch unnötige operative Interventionen. Die Daten der UKCTOCS-Studie könnten für einen möglichen Nutzen einer seriellen algorithmischen CA-125-Untersuchung sprechen, allerdings konnte das nur in der Subgruppenanalyse nach präspezifiziertem Ausschluss der bei Studienbeginn initial diagnostizierten Ovarialkarzinome gezeigt werden, wobei der primäre Endpunkt der Studie, nämlich der Nachweis eines Überlebensvorteils im untersuchten Gesamtkollektiv, verfehlt wurde. Zu einem generellen Screening zur Früherkennung eines Ovarialkarzinoms kann somit anhand der zurzeit vorliegenden Daten nicht geraten werden. Umso wichtiger bleiben daher das frühzeitige Erkennen von möglichen, häufig sehr unspezifischen Sympto-
GYNÄKOLOGIE 1/2020
13
SCHWERPUNKT
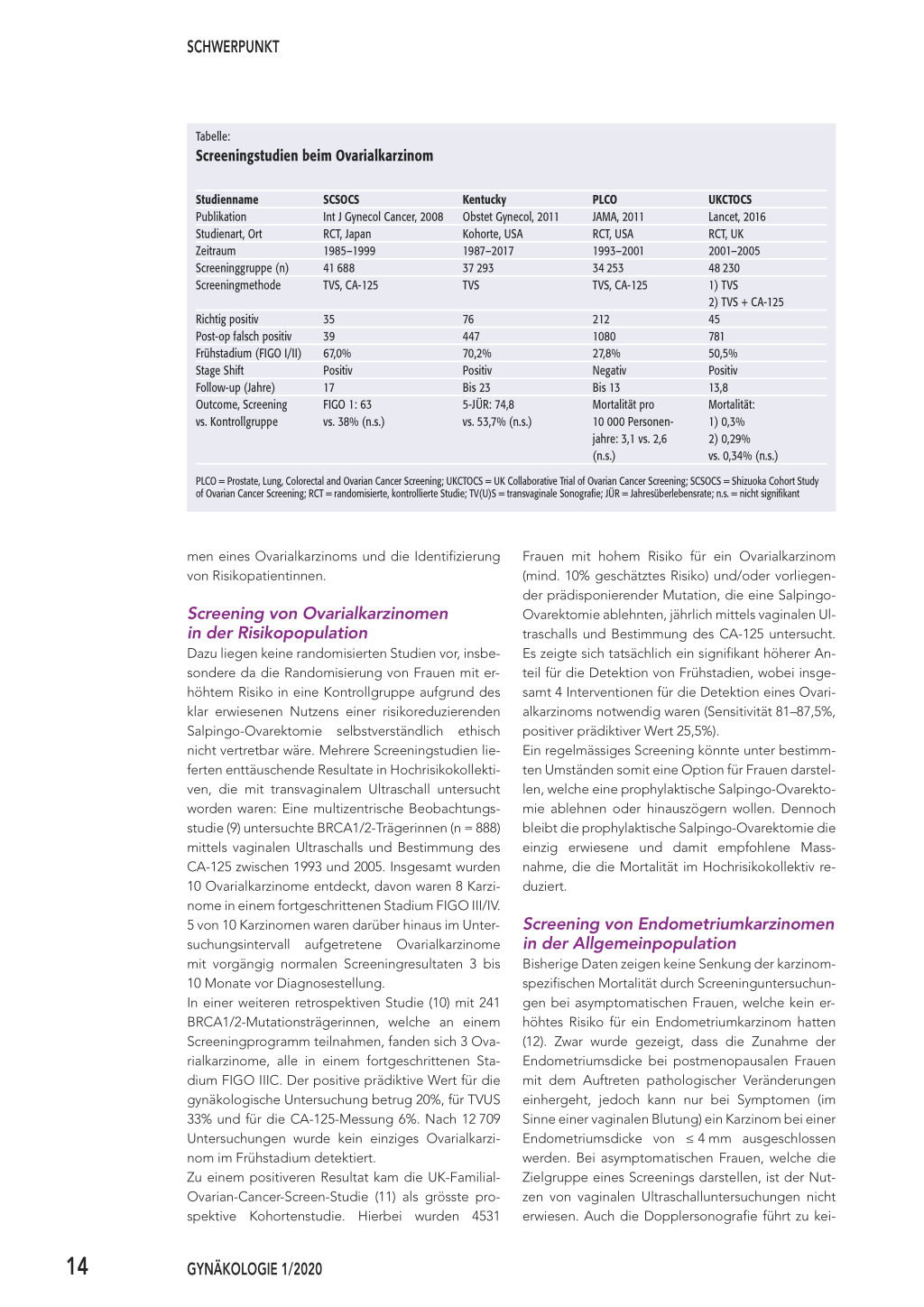
Tabelle:
Screeningstudien beim Ovarialkarzinom
Studienname Publikation Studienart, Ort Zeitraum Screeninggruppe (n) Screeningmethode
SCSOCS Int J Gynecol Cancer, 2008 RCT, Japan 1985–1999 41 688 TVS, CA-125
Kentucky Obstet Gynecol, 2011 Kohorte, USA 1987–2017 37 293 TVS
Richtig positiv Post-op falsch positiv Frühstadium (FIGO I/II) Stage Shift Follow-up (Jahre) Outcome, Screening vs. Kontrollgruppe
35 39 67,0% Positiv 17 FIGO 1: 63 vs. 38% (n.s.)
76 447 70,2% Positiv Bis 23 5-JÜR: 74,8 vs. 53,7% (n.s.)
PLCO JAMA, 2011 RCT, USA 1993–2001 34 253 TVS, CA-125
212 1080 27,8% Negativ Bis 13 Mortalität pro 10 000 Personenjahre: 3,1 vs. 2,6 (n.s.)
UKCTOCS Lancet, 2016 RCT, UK 2001–2005 48 230 1) TVS 2) TVS + CA-125 45 781 50,5% Positiv 13,8 Mortalität: 1) 0,3% 2) 0,29% vs. 0,34% (n.s.)
PLCO = Prostate, Lung, Colorectal and Ovarian Cancer Screening; UKCTOCS = UK Collaborative Trial of Ovarian Cancer Screening; SCSOCS = Shizuoka Cohort Study of Ovarian Cancer Screening; RCT = randomisierte, kontrollierte Studie; TV(U)S = transvaginale Sonografie; JÜR = Jahresüberlebensrate; n.s. = nicht signifikant
men eines Ovarialkarzinoms und die Identifizierung von Risikopatientinnen.
Screening von Ovarialkarzinomen in der Risikopopulation
Dazu liegen keine randomisierten Studien vor, insbesondere da die Randomisierung von Frauen mit erhöhtem Risiko in eine Kontrollgruppe aufgrund des klar erwiesenen Nutzens einer risikoreduzierenden Salpingo-Ovarektomie selbstverständlich ethisch nicht vertretbar wäre. Mehrere Screeningstudien lieferten enttäuschende Resultate in Hochrisikokollektiven, die mit transvaginalem Ultraschall untersucht worden waren: Eine multizentrische Beobachtungsstudie (9) untersuchte BRCA1/2-Trägerinnen (n = 888) mittels vaginalen Ultraschalls und Bestimmung des CA-125 zwischen 1993 und 2005. Insgesamt wurden 10 Ovarialkarzinome entdeckt, davon waren 8 Karzinome in einem fortgeschrittenen Stadium FIGO III/IV. 5 von 10 Karzinomen waren darüber hinaus im Untersuchungsintervall aufgetretene Ovarialkarzinome mit vorgängig normalen Screeningresultaten 3 bis 10 Monate vor Diagnosestellung. In einer weiteren retrospektiven Studie (10) mit 241 BRCA1/2-Mutationsträgerinnen, welche an einem Screeningprogramm teilnahmen, fanden sich 3 Ovarialkarzinome, alle in einem fortgeschrittenen Stadium FIGO IIIC. Der positive prädiktive Wert für die gynäkologische Untersuchung betrug 20%, für TVUS 33% und für die CA-125-Messung 6%. Nach 12 709 Untersuchungen wurde kein einziges Ovarialkarzinom im Frühstadium detektiert. Zu einem positiveren Resultat kam die UK-FamilialOvarian-Cancer-Screen-Studie (11) als grösste prospektive Kohortenstudie. Hierbei wurden 4531
Frauen mit hohem Risiko für ein Ovarialkarzinom (mind. 10% geschätztes Risiko) und/oder vorliegender prädisponierender Mutation, die eine SalpingoOvarektomie ablehnten, jährlich mittels vaginalen Ultraschalls und Bestimmung des CA-125 untersucht. Es zeigte sich tatsächlich ein signifikant höherer Anteil für die Detektion von Frühstadien, wobei insgesamt 4 Interventionen für die Detektion eines Ovarialkarzinoms notwendig waren (Sensitivität 81–87,5%, positiver prädiktiver Wert 25,5%). Ein regelmässiges Screening könnte unter bestimmten Umständen somit eine Option für Frauen darstellen, welche eine prophylaktische Salpingo-Ovarektomie ablehnen oder hinauszögern wollen. Dennoch bleibt die prophylaktische Salpingo-Ovarektomie die einzig erwiesene und damit empfohlene Massnahme, die die Mortalität im Hochrisikokollektiv reduziert.
Screening von Endometriumkarzinomen in der Allgemeinpopulation
Bisherige Daten zeigen keine Senkung der karzinomspezifischen Mortalität durch Screeninguntersuchungen bei asymptomatischen Frauen, welche kein erhöhtes Risiko für ein Endometriumkarzinom hatten (12). Zwar wurde gezeigt, dass die Zunahme der Endometriumsdicke bei postmenopausalen Frauen mit dem Auftreten pathologischer Veränderungen einhergeht, jedoch kann nur bei Symptomen (im Sinne einer vaginalen Blutung) ein Karzinom bei einer Endometriumsdicke von ≤ 4 mm ausgeschlossen werden. Bei asymptomatischen Frauen, welche die Zielgruppe eines Screenings darstellen, ist der Nutzen von vaginalen Ultraschalluntersuchungen nicht erwiesen. Auch die Dopplersonografie führt zu kei-
14 GYNÄKOLOGIE 1/2020
SCHWERPUNKT
ner Verbesserung der Detektionsrate für maligne und prämaligne Veränderungen. Vaginale Ultraschalluntersuchungen zum Zweck einer Früherkennung eines Endometriumkarzinoms sollten daher bei asymptomatischen Frauen nicht durchgeführt werden.
Screening von Endometriumkarzinomen in der Hochrisikopopulation
Auch bei erhöhtem Risiko (Adipositas, Diabetes mellitus, Hormontherapie, metabolisches Syndrom, PCO-Syndrom) sind Ultraschalluntersuchungen nicht empfohlen (13). Ein Screening unter Tamoxifen in der adjuvanten endokrinen Therapie des Mammakarzinoms ergab hohe Raten an falsch positiven Befunden und eine extrem niedrige Detektionsrate für Karzinome. Problematisch ist insbesondere die Uneinigkeit über die Endometriumsdicke als Grenzwert für eine histopathologische Abklärung (zwischen 5 und 10 mm). Der Nutzen von Tamoxifen überwiegt hier insgesamt klar das Risiko für ein Endometriumkarzinom (relativer Risikoanstieg von 2 bis 3) (14). Bezüglich des Nutzens von jährlichem Endometriumsampling im Hochrisikokollektiv ist die Datenlage schwach. Ein wesentlicher Nachteil ist auch die Invasivität der Methode, wobei die endometriale im Vergleich zur zervikalen Zytologie schwieriger zu interpretieren ist. Der zytologische Abstrich der Zervix kann gelegentlich zur Entdeckung eines klinisch okkulten Endometriumkarzinoms führen, jedoch ist diese Methode bei einer Sensitivität von nur 30% nicht für das Screening geeignet.
Anlage für Lynch-Syndrom und Cowden-Syndrom Der Stellenwert des Endometriumkarzinom-Screenings bei Lynch-Syndrom- und Cowden-SyndromAnlageträgerinnen mit sehr hohem Lebenszeitrisiko ist ungeklärt. Eine verbesserte Überlebensrate unter regelmässiger Überwachung wurde bislang nicht nachgewiesen, wobei das unter anderem auf die ohnehin gute Prognose (5-Jahres-Überlebensrate 75–83%) und die Notwendigkeit langfristiger prospektiver Datenerhebungen zum Nachweis eines Überlebensvorteils zurückzuführen ist. Es gibt allerdings Hinweise, dass bei Vorliegen eines Lynch-Syndroms jährliche Endometriumbiopsien dem transvaginalen Ultraschall bei der Identifizierung eines Endometriumkarzinoms und prämaligner Veränderungen überlegen ist (15). Prinzipiell sollte bei Lynchund Cowden-Syndrom-Anlageträgerinnen ab dem 40. Lebensjahr bzw. 5 Jahre vor dem frühesten Erkrankungsalter in der Familie eine prophylaktische Hysterektomie und bei Lynch-Syndrom-Patientinnen gegebenenfalls zusätzlich eine beidseitige Adnexektomie besprochen werden (12).
Fazit für die Praxis
Sowohl beim Ovarial- als auch beim Endometrium-
karzinom lassen sich derzeit keine Vorteile eines ge-
nerellen Screenings auf das Gesamtüberleben nach-
weisen. Somit bleibt das empfohlene Vorgehen
symptomorientiert und unterstreicht die Wichtigkeit
einer ausführlichen Aufklärung über mögliche Früh-
zeichen und auch zum Teil unspezifische Symptome.
Im Falle eines nachgewiesenen genetischen Risikos
bleibt das risikoreduzierende operative Vorgehen
beim Ovarial- und Endometriumkarzinom die einzige
erwiesene protektive Massnahme.
I
Dr. med. Janna Pape Prof. Dr. med. Daniel Fink Dr. med Eleftherios P. Samartzis (Korrespondenzadresse) E-Mail: eleftherios.samartzis@usz.ch
Klinik für Gynäkologie Universitätsspital Zürich 8091 Zürich
Quellen : 1. Jayson, G.C., et al.: Ovarian cancer. Lancet. 2014; 384(9951): 1376–1388. 2. Morice, P., et al.: Endometrial cancer. Lancet. 2016; 387(10023): 1094–1108. 3. Kobayashi, H., et al.: A randomized study of screening for ovarian cancer: a multicenter study in Japan. Int J Gynecol Cancer. 2008; 18(3): 414–420. 4. van Nagell, J.R., Jr., et al.: Survival of Women With Type I and II Epithelial Ovarian Cancer Detected by Ultrasound Screening. Obstet Gynecol. 2018; 132(5): 1091–1100. 5. Buys, S.S., et al.: Effect of screening on ovarian cancer mortality: the Prostate, Lung, Colorectal and Ovarian (PLCO) Cancer Screening Randomized Controlled Trial. JAMA. 2011; 305(22): 2295–2303. 6. Buys, S.S., et al.: Ovarian cancer screening in the Prostate, Lung, Colorectal and Ovarian (PLCO) cancer screening trial: findings from the initial screen of a randomized trial. Am J Obstet Gynecol. 2005; 193(5): 1630–1639. 7. Temkin, S.M., et al.: Outcomes from ovarian cancer screening in the PLCO trial: Histologic heterogeneity impacts detection, overdiagnosis and survival. Eur J Cancer. 2017; 87: 182–188. 8. Jacobs, I.J., et al.: Ovarian cancer screening and mortality in the UK Collaborative Trial of Ovarian Cancer Screening (UKCTOCS): a randomised controlled trial. Lancet. 2016; 387(10022): 945–956. 9. Hermsen, B.B., et al.: No efficacy of annual gynaecological screening in BRCA1/2 mutation carriers; an observational follow-up study. Br J Cancer. 2007; 96(9): 1335–1342. 10. van der Velde, N.M., et al.: Time to stop ovarian cancer screening in BRCA1/2 mutation carriers? Int J Cancer. 2009; 124(4): 919–923. 11. Rosenthal, A.N., et al.: Results of annual screening in phase I of the United Kingdom familial ovarian cancer screening study highlight the need for strict adherence to screening schedule. J Clin Oncol. 2013; 31(1): 49–57. 12. Emons, G., et al.: Interdisciplinary Diagnosis, Therapy and Follow-up of Patients with Endometrial Cancer. Guideline (S3-Level, AWMF Registry Nummer 032/034OL, April 2018) – Part 1 with Recommendations on the Epidemiology, Screening, Diagnosis and Hereditary Factors of Endometrial Cancer. Geburtshilfe Frauenheilkd. 2018; 78(10): 949–971. 13. Lancaster, J.M., et al.: Society of Gynecologic Oncology statement on risk assessment for inherited gynecologic cancer predispositions. Gynecol Oncol. 2015; 136(1): 3–7. 14. Gerber, B., et al.: Effects of adjuvant tamoxifen on the endometrium in postmenopausal women with breast cancer: a prospective long-term study using transvaginal ultrasound. J Clin Oncol. 2000; 18(20): 3464–3470. 15. ACOG Practice Bulletin No. 147: Lynch syndrome. Obstet Gynecol. 2014; 124(5): 1042–1054.
GYNÄKOLOGIE 1/2020
15