Transkript
SCHWERPUNKT
Das Screening auf Zervix-, Vulva- und Analkarzinom
Für wen sind welche Untersuchungen sinnvoll?
Das seit Jahrzehnten etablierte Zervixkarzinom-Screening hat in der industrialisierten Welt im Verlauf der Jahre zu einem deutlichen Rückgang der Inzidenz und Mortalität des Gebärmutterhalskrebses geführt. Unter Berücksichtigung der Erfolge dieses Screenings, des vergleichbaren Gewebeaufbaus zervikal und anal (Transformationszone) sowie der ähnlichen Empfänglichkeit des Gewebes für HPV-Infektionen bietet sich die erweiterte, die Vulva- und Analregion beinhaltende Vorsorgeuntersuchung im Rahmen der Jahreskontrolle geradezu an.
GIAN-PIERO GHISU, DANIEL FINK
Gian-Piero Ghisu Daniel Fink
Rationale für die Screeninguntersuchung im Allgemeinen
Für ein Vulva- oder Analkarzinom-Screening im klassischen Sinne bestehen bisher keine Empfehlungen, dabei besteht hier durchaus Handlungsbedarf, insbesondere in einer Hochrisikopopulation. Die Anzahl der in der Schweiz neu diagnostizierten Zervix- und Analkarzinome (1) sowie Vulvakarzinome (2) ist in Tabelle 1 zusammengefasst (die Zahlen umfassen die Fälle unabhängig vom HPV-Status). Beim Analkarzinom fällt auf, dass die Erkrankung Frauen mehr als zweimal häufiger trifft als Männer. Zudem sticht hervor auf, dass die Anzahl neu diagnostizierter Vulvakarzinome etwa derjenigen der Zervixkarzinome entspricht oder diese sogar leicht übersteigt.
Merkpunkte
I Das Zervixkarzinom-Screening hat zu einer deutlichen Senkung von Inzidenz und Mortalität des Gebärmutterhalskrebses geführt, wodurch sein Nutzen als unbestritten gilt.
I Für das Vulva- und Analkarzinom-Screening bestehen keine Empfehlungen; eine Untersuchung dieser Regionen bietet sich vor allem aufgrund der HPV-Assoziation einiger der Erkrankungen im Rahmen der gynäkologischen Vorsorgeuntersuchung allerdings an.
I Das Zervixkarzinom-Screening kann zytologisch oder – ab dem 30. Lebensjahr – mittels HPV-Testung erfolgen, wobei Letztere von der Grundversicherung noch nicht übernommen wird; der Stellenwert des HPV-Tests im Rahmen der vulvären und analen Vorsorgeuntersuchungen ist unklar.
I Eine Vulvoskopie sollte bei Patientinnen mit sichtbaren Anomalien an der Vulva und bei fokalen Beschwerden unklarer Ätiologie wie Juckreiz, Schmerz oder Brennen erfolgen, wobei zu beachten ist, dass ein grosser Teil der Patientinnen mit vulvärer Dysplasie asymptomatisch ist.
I Zur Hochrisikopopulation, welche von einem «Analkarzinom-Screening» profitieren könnte, gehören HIV-positive Frauen bzw. Frauen mit HIV-positivem Partner, Immunsupprimierte, Frauen mit (Zustand nach) HSIL bzw. Malignom der Zervix, der Vulva und der Vagina sowie Frauen mit perinealen HPV-assoziierten Läsionen.
Präventive Möglichkeiten Gemäss WHO (und ursprünglich durch Gerald Caplan 1964 beschrieben) wird die Prävention nach ihrem Zeitpunkt der Durchführung in eine primäre, sekundäre und tertiäre Prävention gegliedert (3). Die primäre Prävention zielt auf die Vermeidung der Entstehung eines Karzinoms und seiner Vorstufen (z. B. HPV-Impfung, Nikotinstopp). Die sekundäre Prävention dient der Erkennung und Behandlung von Dysplasien, die tertiäre Prävention der Therapie des Karzinoms. Hier besteht das Ziel in der Vermeidung von Rezidiven und Metastasen. Die Massnahmen zur sekundären Prävention zur Erkennung zervikaler, vulvärer und analer Krebsvorstufen umfassen neben der Erhebung einer dysplasiespezifischen Anamnese – unter anderem zur Erfassung von Risikofaktoren – die Entnahme von zytologischen Abstrichen (nur Zervix und Anus) und den HPV-Test (nur Zervix) als Basisvorsorge. Kolpo-, Vulvo- und Anoskopie sowie bioptische Abklärung gehören zu den erweiterten Untersuchungen. Die Behandlung der diagnostizierten Krebsvorstufe gehört ebenfalls zur sekundären Prävention.
Zervixkarzinom-Screenning
Allgemeines Die Einführung des Zervixkarzinom-Screenings mittels zytologischer Untersuchungen von zervikal abgestrichenem Zellmaterial (Pap-Test) in den späten 1960er-Jahren hat zu einer drastischen Abnahme der Inzidenz und Mortalität des Zervixkarzinoms geführt. In der Schweiz erfolgt ein sogenanntes opportunistisches Screening, das heisst auf Wunsch der Frau oder auf Empfehlung des Arztes. Viele Staaten kennen im Unterschied dazu ein organisiertes Screening, hierbei werden die Frauen behördlich zum Screening eingeladen. Aus einer deutschen Studie ist bekannt,
6 GYNÄKOLOGIE 1/2020
SCHWERPUNKT
Tabelle 1:
Anzahl der Neuerkrankungen von Zervix-, Vulvaund Analkarzinomen in der Schweiz (2)
Krebslokalisation Neuerkrankungen, Fälle
Zervix 254
Vulva ca. 260
Anus 128♀ (60♂)
dass über 90% der Zervixkarzinompatientinnen nie oder nur unregelmässig eine Vorsorgeuntersuchung in Anspruch genommen haben (4). Die «Nichtteilnahme» am Screening gilt damit als wichtiger Risikofaktor für die Entstehung eines Zervixkarzinoms, was die Bedeutung regelmässiger Vorsorgeuntersuchungen unterstreicht. Auffälligkeiten in der Screeninguntersuchung können auf eine Krebsvorstufe oder gar Krebs hinweisen. Weitere Abklärungen wie Kolposkopie, Biopsien, aber auch Konisationen sind einerseits zur Sicherung der Diagnose, andererseits zur Behandlung einer Dysplasie als direkte Konsequenz des Screeningresultates notwendig. Beinahe alle dysplastischen Veränderungen am Gebärmutterhals werden durch eine persistierende Infektion mit Hochrisiko-HPV induziert. Diese heilt gerade in jungen Jahren meistens spontan ab, was zu einer Regression der Dysplasie führt. Der natürliche Verlauf der HPV-Infektion sollte bei der Festlegung des Prozederes bei Dysplasiepatientinnen mitberücksichtigt werden: neben der psychosozialen Belastung und der Auslösung von Ängsten birgt das Zervixkarzinom-Screening in der Tat ein gewisses Risiko überflüssiger Abklärungen sowie Übertherapien mit dem bekannten erhöhten Frühgeburtlichkeitsrisiko nach Konisation. Diese gehen letztlich mit unnötigen Kosten für das Gesundheitssystem einher.
Dysplasiespezifische Anamnese Sexualverhalten (früher Sexualkontakt, multiple Partner/-innen), Nikotinkonsum, Geburtenzahl, Einsatz von Ovulationshemmern, Immunsuppression und Vorhandensein anderer sexuell übertragbarer Krankheiten bestimmen mit, ob eine HPV-Infektion ohne weitere Folgen abheilt oder – über die Entwicklung einer in der Ausprägung im Verlauf zunehmenden Dysplasie – schliesslich zum Zervixkarzinom führt. Es lohnt sich daher, die Anamnese im Zusammenhang mit der Vorsorgeuntersuchung entsprechend fokussiert zu erheben.
Zervixkarzinom-Screening in der Schweiz In der Schweiz kann das Screening zytologisch (PapTest) oder – ab dem 30. Lebensjahr – HPV-basiert erfolgten, obschon die Kosten für das HPV-basierte Screening zurzeit von der Grundversicherung nicht übernommen werden. Die aktuell gültigen, von der Schweizerischen Gesellschaft für Gynäkologie und
Geburtshilfe empfohlenen Screeningmodalitäten sind in Tabelle 2 zusammengefasst (5).
Zytologisches Screening Das Resultat des Pap-Abstrichs wird unter anderem durch die Entnahmebedingungen und durch die Interobservervariabilität beeinflusst, wobei Letztere bei leichtgradigen Veränderungen umso ausgeprägter ausfällt (6). Die Sensitivität des Pap-Tests wird mit 70%, die Spezifität mit 95% angegeben (7). Bei glandulären Läsionen ist von einer insgesamt noch tieferen Sensitivität auszugehen (8).
HPV-basiertes Screening Der HPV-Test zu Screeningzwecken vermag in randomisierten Studien die Inzidenz des Zervixkarzinoms weiter zu senken, einen Effekt auf die Mortalität konnte bisher nicht gezeigt werden (9). Die Sensitivität des HPV-Tests ist mit 94% im Vergleich zum PapTest höher. Allerdings führt das HPV-basierte Screening aufgrund der etwas niedrigeren Spezifität von 90%, im Vergleich zum Pap-Test, zu mehr vermeidbaren Abklärungen (10). Für Regionen, die wie die Schweiz ein opportunistisches Screening kennen, wurde zudem das sogenannte Lost-to-Follow-up von HPV-positiven Frauen als Problem beschrieben (11). Eine zwar vertretbare und aus Kostengründen (HPVTest um ein Vielfaches teurer als Pap-Test) zu befürwortende Ausdehnung der Screeningintervalle auf beispielsweise alle 5 oder mehr Jahre bei einem HPVbasierten Screening würde im opportunistischen System möglicherweise dazu führen, dass sich Frauen gerade bei negativem HPV-Test in falscher Sicherheit wiegen und unregelmässiger oder nicht mehr zum Screening erscheinen. Damit bliebe – wie oben erwähnt – einer der wichtigsten Risikofaktoren für die Entstehung eines Zervixkarzinoms erhalten oder würde gar generiert. Auf der anderen Seite beschränkt sich die Vorsorgeuntersuchung in der gynäkologischen Praxis in unseren Regionen erfreulicherweise nicht «nur» auf die Zervixkarzinomvorsorge. Durch die Notwendigkeit der präventiven Untersuchung der Brust oder durch die nicht zu vernachlässigende Relevanz der Beratung hinsichtlich allgemeiner und spezifischer Themen zur Erhaltung und
Abkürzungen
AIN ASCUS ASC-H HPV HRA HSIL LSIL MSM VIN
Anale intraepitheliale Neoplasie Atypical squamous cells of undetermined significance Atypical squamous cells cannot exclude HSIL Humanes Papillomavirus High resolution anoscopy High grade squamous intraepithelial lesion Low grade squamous intraepithelial lesion Männer, die Sex mit Männern haben Vulväre intraepitheliale Neoplasie
GYNÄKOLOGIE 1/2020
7
SCHWERPUNKT
Tabelle 2:
Screeningmodalitäten gemäss Empfehlungen der SGGG (5)
Alter der Frau < 21 Jahre 21 bis 29-Jährige 30 bis 70-Jährige > 70 Jahre
Zustand nach HPV-Impfung Zustand nach Gebärmutterentfernung
Modalitäten Kein Screening Zytologisches Screening alle 3 Jahre Zytologisches Screening alle 3 Jahre oder HPV-Screening alle 3 Jahre Es ist zu beachten, dass aktuell das HPV-Screening von der Grundversicherung nicht bezahlt wird In der Regel Ende des Screenings Voraussetzungen: I Mindestens 3 unauffällige zytologische Abstriche in den letzten 10 Jahren oder I Zwei negative HPV-Tests innerhalb von 3 Jahren I Noch nie Krebsvorstufen im analen oder genitalen Bereich gehabt I Keine Risikofaktoren wie wechselnde Partner/-innen, Immunabwehrschwäche
(HIV, Zustand nach Transplantation, usw.) Gleiches Screening wie bei Nichtgeimpften Voraussetzungen, die für ein Ende des Screenings erfüllt sein müssen: I Die Operation erfolgte nicht unter Erhalt des Gebärmutterhalses I Keine Krebsvorstufen im analen oder genitalen Bereich gehabt I Negativer HPV-Test I Keine Immunabwehrschwäche (HIV, Zustand nach Transplantation usw.)
Förderung der Gesundheit dürfte der wichtige Kontakt in vernünftigen zeitlichen Abständen zwischen Ärztin und Frau erhalten bleiben.
«Vulvakarzinom-Screening»
Allgemeines Die Inzidenz der Vulvakarzinom-Krebsvorstufen (VIN) ist seit den 1970er-Jahren um etwa 400% gestiegen. Rund 85% der vulvären Krebsvorstufen (VIN) werden durch High-Risk-HPV-Infektionen verursacht (am häufigsten finden sich die Typen 16 und 18). Bei den invasiven Karzinomen der Vulva ist die Assoziation mit HPV mit etwa 40% geringer (am häufigsten werden hier die Typen 16 und 33 detektiert) als bei den Vorstufen, weshalb die HPV-Impfung im Zusammenhang der Primärprävention auch unter dem Aspekt der
Vermeidung der vulvären (und analen, s.u.) Neoplasien evaluiert werden sollte (12). Besonders die HPVassoziierten vulvären Läsionen treten in 50% der Fälle multifokal auf und betreffen mit abnehmender Häufigkeit Labia majora, Klitoris, Labia minora, Perineum, Periurethralregion und die Ausführungsgänge der Bartholin-Drüsen. Nicht HPV-assoziierte Vorstufen (differenzierte VIN) und Karzinome betreffen vorwiegend die ältere Frau und basieren auf chronisch entzündlichen Hauterkrankungen. Der Lichen sclerosus gilt als klassisches Beispiel dafür. Ein spezifisches Screening zur Detektion des Vulvakarzinoms und seiner Vorstufen ist nicht vorgesehen, weshalb die Untersuchung der Vulva als obligater Bestandteil der gynäkologischen Krebsfrüherkennungsuntersuchung gilt.
8 GYNÄKOLOGIE 1/2020
SCHWERPUNKT
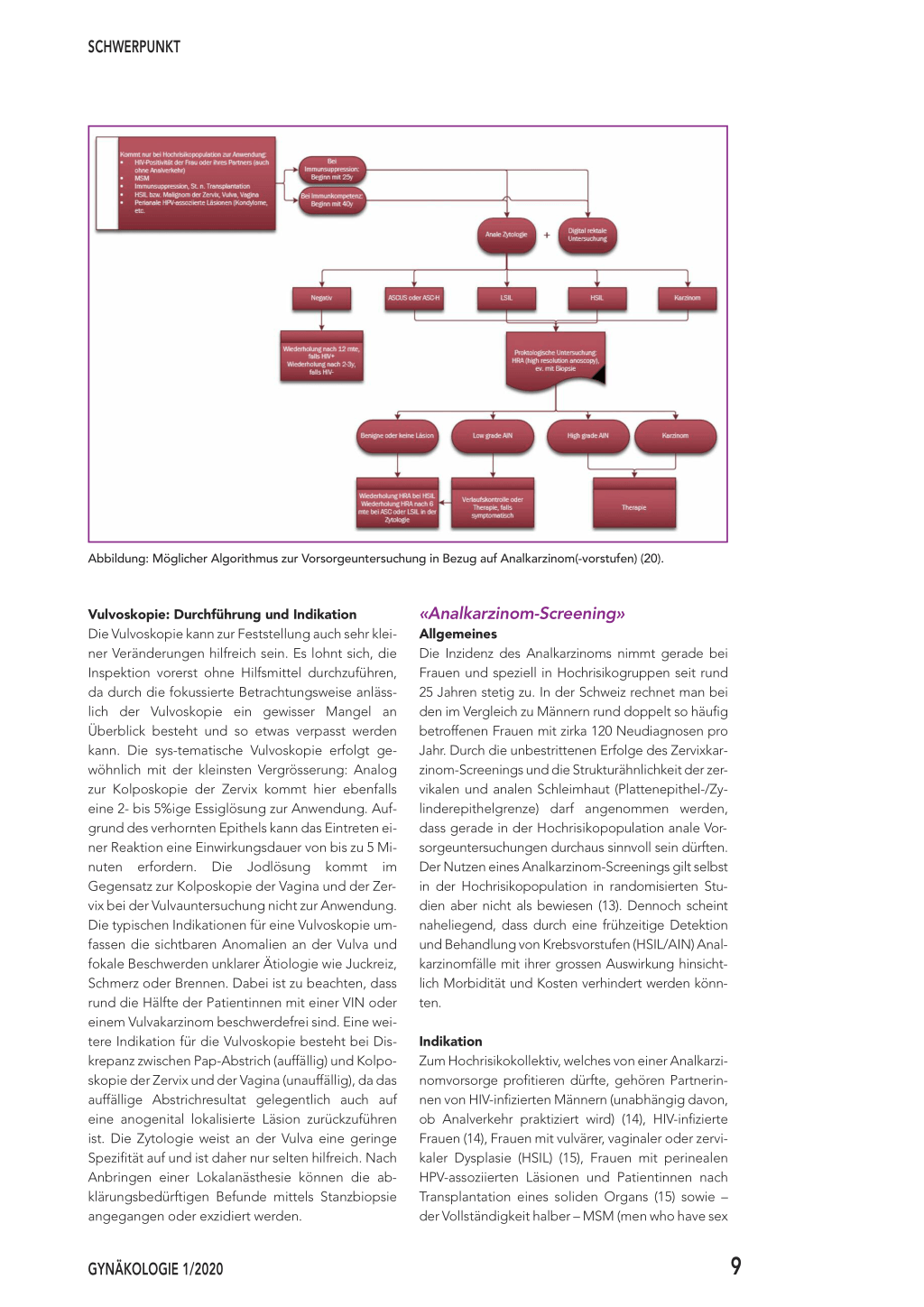
Abbildung: Möglicher Algorithmus zur Vorsorgeuntersuchung in Bezug auf Analkarzinom(-vorstufen) (20).
Vulvoskopie: Durchführung und Indikation Die Vulvoskopie kann zur Feststellung auch sehr kleiner Veränderungen hilfreich sein. Es lohnt sich, die Inspektion vorerst ohne Hilfsmittel durchzuführen, da durch die fokussierte Betrachtungsweise anlässlich der Vulvoskopie ein gewisser Mangel an Überblick besteht und so etwas verpasst werden kann. Die sys-tematische Vulvoskopie erfolgt gewöhnlich mit der kleinsten Vergrösserung: Analog zur Kolposkopie der Zervix kommt hier ebenfalls eine 2- bis 5%ige Essiglösung zur Anwendung. Aufgrund des verhornten Epithels kann das Eintreten einer Reaktion eine Einwirkungsdauer von bis zu 5 Minuten erfordern. Die Jodlösung kommt im Gegensatz zur Kolposkopie der Vagina und der Zervix bei der Vulvauntersuchung nicht zur Anwendung. Die typischen Indikationen für eine Vulvoskopie umfassen die sichtbaren Anomalien an der Vulva und fokale Beschwerden unklarer Ätiologie wie Juckreiz, Schmerz oder Brennen. Dabei ist zu beachten, dass rund die Hälfte der Patientinnen mit einer VIN oder einem Vulvakarzinom beschwerdefrei sind. Eine weitere Indikation für die Vulvoskopie besteht bei Diskrepanz zwischen Pap-Abstrich (auffällig) und Kolposkopie der Zervix und der Vagina (unauffällig), da das auffällige Abstrichresultat gelegentlich auch auf eine anogenital lokalisierte Läsion zurückzuführen ist. Die Zytologie weist an der Vulva eine geringe Spezifität auf und ist daher nur selten hilfreich. Nach Anbringen einer Lokalanästhesie können die abklärungsbedürftigen Befunde mittels Stanzbiopsie angegangen oder exzidiert werden.
«Analkarzinom-Screening»
Allgemeines Die Inzidenz des Analkarzinoms nimmt gerade bei Frauen und speziell in Hochrisikogruppen seit rund 25 Jahren stetig zu. In der Schweiz rechnet man bei den im Vergleich zu Männern rund doppelt so häufig betroffenen Frauen mit zirka 120 Neudiagnosen pro Jahr. Durch die unbestrittenen Erfolge des Zervixkarzinom-Screenings und die Strukturähnlichkeit der zervikalen und analen Schleimhaut (Plattenepithel-/Zylinderepithelgrenze) darf angenommen werden, dass gerade in der Hochrisikopopulation anale Vorsorgeuntersuchungen durchaus sinnvoll sein dürften. Der Nutzen eines Analkarzinom-Screenings gilt selbst in der Hochrisikopopulation in randomisierten Studien aber nicht als bewiesen (13). Dennoch scheint naheliegend, dass durch eine frühzeitige Detektion und Behandlung von Krebsvorstufen (HSIL/AIN) Analkarzinomfälle mit ihrer grossen Auswirkung hinsichtlich Morbidität und Kosten verhindert werden könnten.
Indikation Zum Hochrisikokollektiv, welches von einer Analkarzinomvorsorge profitieren dürfte, gehören Partnerinnen von HIV-infizierten Männern (unabhängig davon, ob Analverkehr praktiziert wird) (14), HIV-infizierte Frauen (14), Frauen mit vulvärer, vaginaler oder zervikaler Dysplasie (HSIL) (15), Frauen mit perinealen HPV-assoziierten Läsionen und Patientinnen nach Transplantation eines soliden Organs (15) sowie – der Vollständigkeit halber – MSM (men who have sex
GYNÄKOLOGIE 1/2020
9
SCHWERPUNKT
with men) (16). Da unter 25-jährige immunkompromittierte Patientinnen und unter 40-jährige immunkompetente Risikopatientinnen ein sehr tiefes Risiko für Analkarzinome aufweisen, sollte der Beginn der Vorsorgeuntersuchungen entsprechend angepasst werden.
Inhalt der Vorsorgeuntersuchung Die Vorsorgeuntersuchungen bestehen aus Zytologieentnahmen aus dem Analkanal als erstem Schritt, danach folgt die digital rektale Untersuchung. Die Möglichkeit einer HRA (high-resolution anoscopy) sollte gegeben sein: Analog zur Differenzialkolposkopie der Zervix beinhaltet die HRA die Verwendung einer 2- bis 5%igen Essiglösung und Jod. Die Sensitivität der analen Zytologie (ASCUS, ASC-H, LSIL, HSIL) ist mit 50 bis 81% mit derjenigen der Zervixzytologie (klassischer Pap-Test) vergleichbar (17). Ob mit einem Ko-Testing (zusätzliche HPV-Typisierung) die Aussagekraft der Vorsorgeuntersuchung verbessert werden kann, ist nicht abschliessend geklärt (18). Da in einer älteren Studie im Kollektiv der MSM die weiteren Abklärungen selbst bei sehr leichten zytologischen Alterationen (z. B. ASCUS) eine homogene Verteilung aller Dysplasiegrade ergeben haben (19), sollte bei zytologischen Auffälligkeiten in der Analzytologie unabhängig von ihrer Ausprägung eine HRA empfohlen werden. Ein möglicher Algorithmus zur Vorsorgeuntersuchung in Bezug auf Analkarzinom(-vorstufen) findet sich in obiger Abbildung (20).
Zusammenfassung
Der Nutzen des Zervixkarzinom-Screenings gilt als etabliert, Risikopatientinnen könnten auch von einem erweiterten Screening von Vulva und/oder Anus profitieren. Beim Zervixkarzinom wird das Screening in der Schweiz zwischen dem 21. und dem 70. Lebensjahr empfohlen. In der Regel erfolgt dies zytologiebasiert alle 3 Jahre oder – alternativ ab dem 30. Lebensjahr – durch HPV-Testung. Die HPV-Testung zu Screeningzwecken wird zurzeit noch nicht von der Krankenkasse vergütet. Ein eigentliches «Vulvakarzinom-Screening» ist nicht vorgesehen. Patientinnen mit inspektorischen Auffälligkeiten, Diskrepanz zwischen Pap-Test und Kolposkopie von Zervix/Vagina sowie bei Symptomen sollten eine Vulvoskopie erhalten. Die Zytologie der Vulva weist eine geringe Sensitivität auf und hat in der Vulvadiagnostik kaum einen Stellenwert. Die Jodprobe kommt bei der Vulva nicht zum Einsatz. Ein eigentliches «Analkarzinom-Screening» ist nicht vorgesehen. Hochrisikopatientinnen – darunter zählen
Frauen mit Immunsuppression, HIV-Positivität des
Partners, HSIL im unteren Genitaltrakt, aber auch mit
perinealen HPV-assoziierten Läsionen (z. B. Kondy-
lome) – könnten von einem Screening profitieren. Da
selbst leichtgradige zytologische Auffälligkeiten eine
hochgradige anale Dysplasie nicht ausschliessen,
sollte bei diesen Befunden in der Hochrisikosituation
grosszügig eine HRA indiziert werden.
I
Dr. med. Gian-Piero Ghisu (Korrespondenzadresse) E-Mail: gian-piero.ghisu@usz.ch
Prof. Dr. med. Daniel Fink
Klinik für Gynäkologie UniversitätsSpital Zürich 8091 Zürich
Interessenkonflikte: keine.
Quellen: 1. Krebsliga: Krebs in der Schweiz: wichtige Zahlen, Stand Dezember 2018. 2. Günthert A.: Das Vulvakarzinom. Schweizer Zeitschrift für Onkologie 2013; 04: 6–9. 3. WHO: EPHO5 (essential public health operation): Disease prevention, including early detection of illness. 4. Marquardt K et al.: Persistent Carcinoma in Cervical Cancer Screening: NonParticipation Is the Most Significant Cause. Acta Cytologica 2011; 55: 433–437. 5. SGGG-Expertenbrief Nr. 50: Empfehlungen für die Gebärmutterhalskrebsvorsorge. 03/2018. 6. Stoler MH, Schiffman M.: Atypical Squamous Cells of Undetermined Significance-Low-grade Squamous Intraepithelial Lesion Triage Study (ALTS) Group. Interobserver reproducibility of cervical cytologic and histologic interpretations: realistic estimates from the ASCUS-LSIL Triage Study. JAMA 2001; 285: 1500. 7. Reem AM et al.: Systematic reviews and meta-analyses of the accuracy of HPV tests, visual inspection with acetic acid, cytology, and colposcopy. Intern J Gynecol Obstet 2016; 132: 259–265. 8. Sasieni P, Castanon A, Cuzick J.: Screening and adenocarcinoma of the cervix. Int J Cancer 2009; 125(3): 525. 9. Ogilvie GS et al.: Effect of Screening With Primary Cervical HPV Testing vs Cytology Testing on High-grade Cervical Intraepithelial Neoplasia at 48 Months: The HPV FOCAL Randomized Clinical Trial. JAMA 2018; 3; 320(1): 43–52. 10. Melnikow J et al.: Screening for Cervical Cancer With High-Risk Human Papillomavirus Testing. Updated Evidence Report and Systematic Review for the US Preventive Services Task Force. JAMA 2018; 320(7): 687–705. 11. Louvanto K.: HPV testing with cytology triage for cervical cancer screening in routine practice. Am J Obstet Gynecol 2014; 210(5): 473. 12. S3-Leitlinie Vulvakarzinom, 2015. HPV-Managementforum (HPV-MF), Paul-Ehrlich-Gesellschaft für Chemotherapie e.V. (PEG). S3 Leitlinie – Impfprävention HPVassoziierter Neoplasien, AWMF Registernummer 082/002. 2013. 13. Chiao EY et al.: Screening HIV-infected individuals for anal cancer precursor lesions: a systematic review. Clin Infect Dis 2006; 43: 223. 14. Gaisa M, Sigel K, Hand J, Goldstone S.: High rates of anal dysplasia in HIV-infected men who have sex with men, women, and heterosexual men. AIDS 2014; 28: 215. 15. Scholefield JH, Sonnex C, Talbot IC, et al.: Anal and cervical intraepithelial neoplasia: possible parallel. Lancet 1989; 2: 765– 16. Schofield AM, Sadler L, Nelson L, et al.: A prospective study of anal cancer screening in HIV-positive and negative MSM. AIDS 2016; 30: 1375. 17. Nathan M et al.: Performance of anal cytology in a clinical setting when measured against histology and high-resolution anoscopy findings. AIDS 2010; 24: 373. 18. Burgos J et al.: The role of oncogenic human papillomavirus determination for diagnosis of high-grade anal intraepithelial neoplasia in HIV-infected MSM. AIDS 2017; 31: 2227. 19. Palefsky JM et al.: Anal cytology as a screening tool for anal squamous intraepithelial lesions. J Acquir Immune Defic Syndr Hum Retrovirol 1997; 14: 415. 20. Mod. Park IU, Palefsky JM.: Evaluation and Management of Anal Intraepithelial Neoplasia in HIV-Negative and HIV-Positive Men Who Have Sex with Men. Curr Infect Dis Rep 2010; 12(2): 126–133.
10 GYNÄKOLOGIE 1/2020