Transkript
SCHWERPUNKT
Perimenopausale Blutungsstörungen
Ursachen, Diagnostik, Therapie
Die Perimenopause beschreibt den Zeitraum zwischen der Prämenopause und dem ersten Jahr nach der Menopause. Deshalb lassen sich perimenopausale Blutungsstörungen nicht exakt von denjenigen in der Prämenopause und der Postmenopause abgrenzen. Deswegen bezieht der folgende Beitrag die Diagnostik und die Therapie von prä- und postmenopausalen Blutungsstörungen (1) mit ein.
PETRA STUTE, MICHAEL VON WOLFF
In der Bewertung der Ursache, der Diagnostik und der Therapie von Blutungsstörungen muss grundsätzlich zunächst unterschieden werden, ob sich diese während der Prä-/Peri- oder der Postmenopause ereignen. Insbesondere in der Postmenopause sind verschiedene Ursachen zu unterscheiden. Diese sind im Kasten definiert und in ihrer Häufigkeit zusammengestellt. In Tabelle 1 sind häufige Ursachen prämenopausaler, perimenopausaler und postmenopausaler Blutungen dargestellt.
Diagnostik
Blutungsstörung in der Prä-/Perimenopause Das diagnostische Vorgehen bei akuter und chronischer Blutungsstörung unterscheidet sich im Wesentlichen in der Detailliertheit der Labordiagnostik. Für eine rasche Therapie der akuten Blutung ist beispielsweise eine Hormondiagnostik nicht unbedingt erforderlich. Um aber ein akutes Blutungsrezidiv oder eine chronische Blutung zu vermeiden, muss die Ursache der Blutung bekannt sein, um entweder kausal oder präventiv symptomatisch behandeln zu können. Die nachfolgend beschriebene Diagnostik soll möglichst viele Aspekte der Blutungsstörung berücksichtigen. Wenn die Ursache gefunden wurde, dann werden einige der genannten weiteren diagnostischen Schritte überflüssig sein.
Kasten:
Definitionen und Häufigkeiten
I Abnorme uterine Blutung (AUB):
Jede uterine Blutung, die nicht auf den normierten Menstruationszyklus in
der Prä-/Perimenopause zurückzuführen ist.
I Postmenopausale Blutung:
Jede uterine Spontanblutung nach der Menopause
(jährliche Inzidenz ca. 10%, vor allem in der frühen Postmenopause)
Die Grundlage einer jeden Diagnostik sind die Anamnese und die körperliche und gynäkologische Untersuchung, gefolgt von der Labordiagnostik und der Beurteilung des Endometriums.
Labordiagnostik Hierzu gehören: I Schwangerschaftstest I Nativpräparat und mikrobiologischer Abstrich der
Portio bei Verdacht auf Zervizitis (Trichomonas vaginalis, Chlamydia trachomatis, Neisseria gonorrhea) I zytologischer Abstrich der Portio, gegebenenfalls Biopsie I Hormonstatus: FSH, Östradiol (E2), Progesteron (> 3 ng/ml = Ovulation hat stattgefunden), TSH, Prolaktin, Gesamttestosteron. Gegebenenfalls weiterführende Labordiagnostik je nach Anamnese: I Hämoglobin, Hämatokrit, gegebenenfalls Ferritin und CRP I Gerinnungsstatus: Thrombozytenzahl und zusätzlich bei Verdacht auf Gerinnungsstörung aPTT, PT, Faktor VIII, Willebrand-Faktor-Antigen und Aktivität, Blutungszeit beziehungsweise Thrombozytenfunktion I Blutgruppe I Transaminasen (ASAT, ALAT) I Kreatinin I Urinteststreifen (Ausschluss einer Proteinurie).
Beurteilung des Endometriums Das Endometriumkarzinom muss bei einer Blutungsstörung, insbesondere in der Postmenopause, immer berücksichtigt werden. Ein generelles Screening von asymptomatischen Frauen ohne Risikofaktoren wird zurzeit nicht emp-
12 GYNÄKOLOGIE 5/2014
SCHWERPUNKT
Tabelle 1:
Häufige Ursachen von Blutungsstörungen in Abhängigkeit vom Alter
Prämenopause (reproduktive Phase) (reife HypothalamusHypophysen-Ovar-Achse) Alter: ca. 20 bis 40 Jahre Anovulation Schwangerschaft Malignom Polyp Myom Adenomyosis rupturierte Ovarialzyste Ovarialtorsion Infektion endokrine Störung Gerinnungsstörung Medikamente
Perimenopause (instabile HypothalamusHypophysen-Ovar-Achse)
Alter: ca. 40 J. bis Menopause Anovulation Polyp Myom Adenomyosis Malignom
Postmenopause (stabile HypothalamusHypophysen-Ovar-Achse)
Atrophie Malignom Hormontherapie
fohlen. Möglicherweise ist eine gezielte Früherkennungsuntersuchung mit Vaginalsonografie und Endometriumbiopsie von Risikopatientinnen sinnvoll (2). In folgenden Situationen sollte eine Endometriumpathologie ausgeschlossen werden: I Blutungsstörung bei Frauen > 40 Jahre I Blutungsstörung bei Frauen < 40 Jahre und mit
Risikofaktoren (z.B. chronische Anovulation, Adipositas, Östrogen- oder Tamoxifen-Therapie, Diabetes mellitus, anamnestisch Endometriumhyperplasie, positive Eigen- oder Familienanamnese für Endometrium-, Mamma-, Ovar- oder Kolonkarzinom) I Blutungsstörung mit fehlendem Ansprechen auf eine Pharmakotherapie I Frauen mit intaktem Uterus, die eine Östrogenmonotherapie erhalten (diese ist kontraindiziert!) I Nachweis von atypischen Drüsenzellen beim zytologischen Abstrich der Portio I Nachweis von Endometriumzellen beim zytologischen Abstrich der Portio bei Frauen > 40 Jahre. Zur Beurteilung des Endometriums stehen nicht invasive und invasive Methoden zur Verfügung:
Nicht invasive Methoden Im Vordergrund der nicht invasiven Methoden steht die Vaginalsonografie. Hierbei wird die doppelte Endometriumdicke im anterioposterioren Sagittalschnitt von Basalis zu Basalis bestimmt, ohne dass eventuelle Flüssigkeitsansammlungen im Cavum uteri miteinberechnet werden. Eine weitere Voraussetzung für die Beurteilung ist, dass das Endometrium homogen ist; jede fokale Läsion muss bei symptomatischen Frauen histologisch abgeklärt werden. Eine Sonografie sollte möglichst vom 4. bis 6. Zyklustag (ZT) durchgeführt werden. In der Proliferations-
phase beträgt die normale doppelte Endometriumdicke etwa 4 bis 8 mm, in der Sekretionsphase etwa 8 bis 14 mm (3). Diese Grenzwerte sind jedoch nicht standardisiert!
Invasive Methoden Hierzu stehen die Endometriumbiopsie und klassisch die fraktionierte Abrasio in Kombination mit einer Hysteroskopie (HSK) zur Verfügung (4). Die Endometriumbiopsie mit Pipelle® wird der konventionellen Operation aufgrund der einfachen Handhabung und der relativ hohen Detektionsrate (99,6% für das postmenopausale und 91% für das prämenopausale Endometriumkarzinom) vielerorts vorgezogen. Die Endometriumbiopsie ist besonders zuverlässig, wenn mindestens die Hälfte des Endometriums vom Karzinom betroffen ist. Diesem «Restzweifel» kann man begegnen, indem zusätzliche histologische Untersuchungen (Re-Pipelle® oder besser HSK + fraktionierte Abrasio) beispielsweise bei persistierender, abnormer uteriner Blutung (AUB) trotz «benignem» Erstbefund durchgeführt werden. Je nach Studie sind 5 bis 15% der Gewebeproben jedoch unzureichend beziehungsweise nicht aussagekräftig. In dieser Situation oder bei persistierender Blutung, Zervikalstenose, anderer geplanter Operation und bei Wunsch der Patientin sollte ebenfalls eine klassische operative Abklärung erfolgen.
Blutungsstörung in der Postmenopause Die Diagnostik der postmenopausalen Blutung entspricht derjenigen der Blutungsstörung in der Prä-/ Perimenopause. Für die Beurteilung des Endometriums ist die Frage zentral, ob eine Hormontherapie durchgeführt wird oder nicht.
GYNÄKOLOGIE 5/2014
13
SCHWERPUNKT
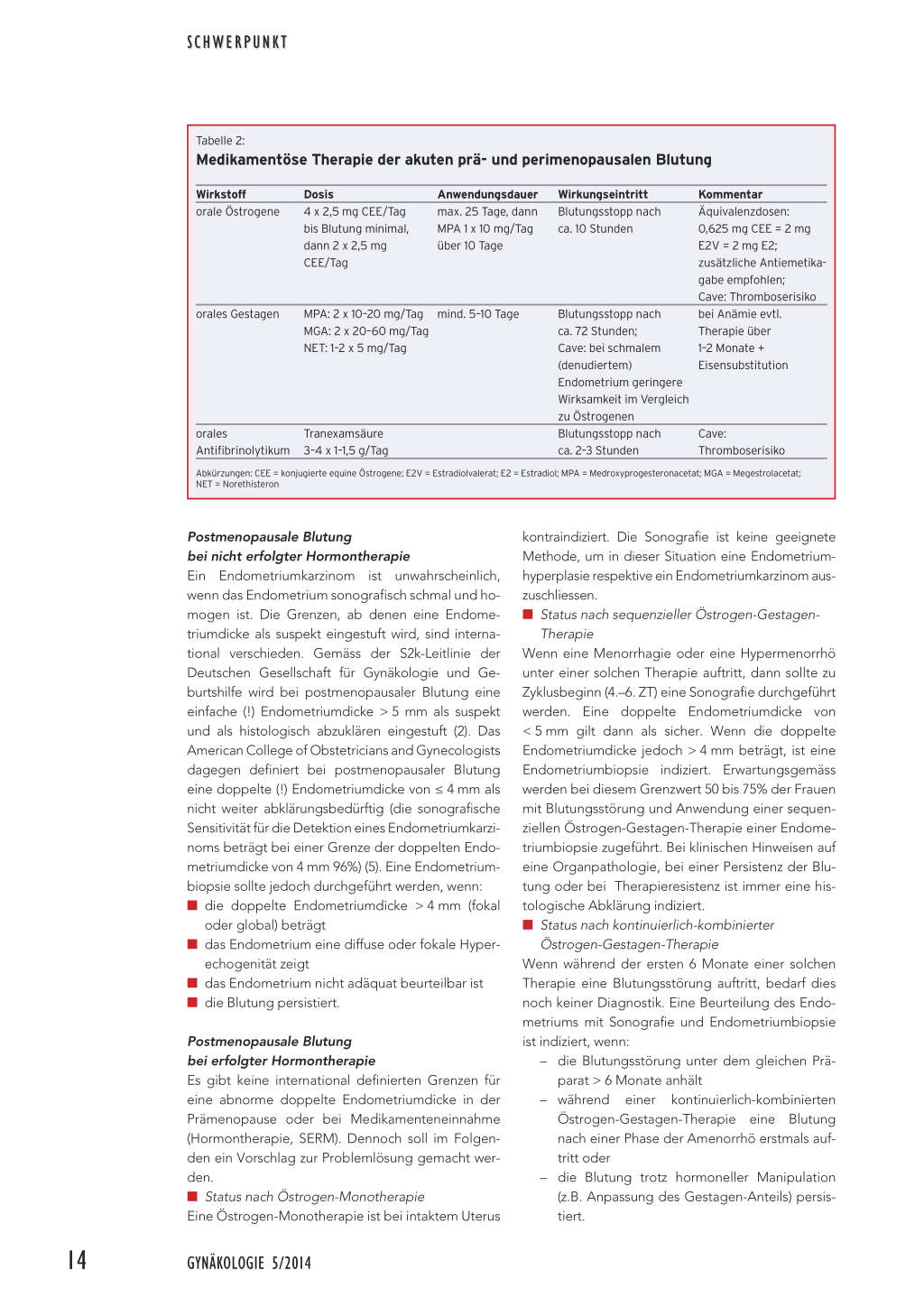
Tabelle 2:
Medikamentöse Therapie der akuten prä- und perimenopausalen Blutung
Wirkstoff orale Östrogene
Dosis 4 x 2,5 mg CEE/Tag bis Blutung minimal, dann 2 x 2,5 mg CEE/Tag
Anwendungsdauer max. 25 Tage, dann MPA 1 x 10 mg/Tag über 10 Tage
orales Gestagen
MPA: 2 x 10–20 mg/Tag mind. 5–10 Tage MGA: 2 x 20–60 mg/Tag NET: 1–2 x 5 mg/Tag
orales
Tranexamsäure
Antifibrinolytikum 3–4 x 1–1,5 g/Tag
Wirkungseintritt
Kommentar
Blutungsstopp nach
Äquivalenzdosen:
ca. 10 Stunden
0,625 mg CEE = 2 mg
E2V = 2 mg E2;
zusätzliche Antiemetika-
gabe empfohlen;
Cave: Thromboserisiko
Blutungsstopp nach
bei Anämie evtl.
ca. 72 Stunden;
Therapie über
Cave: bei schmalem
1–2 Monate +
(denudiertem)
Eisensubstitution
Endometrium geringere
Wirksamkeit im Vergleich
zu Östrogenen
Blutungsstopp nach
Cave:
ca. 2–3 Stunden
Thromboserisiko
Abkürzungen: CEE = konjugierte equine Östrogene; E2V = Estradiolvalerat; E2 = Estradiol; MPA = Medroxyprogesteronacetat; MGA = Megestrolacetat; NET = Norethisteron
Postmenopausale Blutung bei nicht erfolgter Hormontherapie Ein Endometriumkarzinom ist unwahrscheinlich, wenn das Endometrium sonografisch schmal und homogen ist. Die Grenzen, ab denen eine Endometriumdicke als suspekt eingestuft wird, sind international verschieden. Gemäss der S2k-Leitlinie der Deutschen Gesellschaft für Gynäkologie und Geburtshilfe wird bei postmenopausaler Blutung eine einfache (!) Endometriumdicke > 5 mm als suspekt und als histologisch abzuklären eingestuft (2). Das American College of Obstetricians and Gynecologists dagegen definiert bei postmenopausaler Blutung eine doppelte (!) Endometriumdicke von ≤ 4 mm als nicht weiter abklärungsbedürftig (die sonografische Sensitivität für die Detektion eines Endometriumkarzinoms beträgt bei einer Grenze der doppelten Endometriumdicke von 4 mm 96%) (5). Eine Endometriumbiopsie sollte jedoch durchgeführt werden, wenn: I die doppelte Endometriumdicke > 4 mm (fokal
oder global) beträgt I das Endometrium eine diffuse oder fokale Hyper-
echogenität zeigt I das Endometrium nicht adäquat beurteilbar ist I die Blutung persistiert.
Postmenopausale Blutung bei erfolgter Hormontherapie Es gibt keine international definierten Grenzen für eine abnorme doppelte Endometriumdicke in der Prämenopause oder bei Medikamenteneinnahme (Hormontherapie, SERM). Dennoch soll im Folgenden ein Vorschlag zur Problemlösung gemacht werden. I Status nach Östrogen-Monotherapie Eine Östrogen-Monotherapie ist bei intaktem Uterus
kontraindiziert. Die Sonografie ist keine geeignete Methode, um in dieser Situation eine Endometriumhyperplasie respektive ein Endometriumkarzinom auszuschliessen. I Status nach sequenzieller Östrogen-Gestagen-
Therapie Wenn eine Menorrhagie oder eine Hypermenorrhö unter einer solchen Therapie auftritt, dann sollte zu Zyklusbeginn (4.–6. ZT) eine Sonografie durchgeführt werden. Eine doppelte Endometriumdicke von < 5 mm gilt dann als sicher. Wenn die doppelte Endometriumdicke jedoch > 4 mm beträgt, ist eine Endometriumbiopsie indiziert. Erwartungsgemäss werden bei diesem Grenzwert 50 bis 75% der Frauen mit Blutungsstörung und Anwendung einer sequenziellen Östrogen-Gestagen-Therapie einer Endometriumbiopsie zugeführt. Bei klinischen Hinweisen auf eine Organpathologie, bei einer Persistenz der Blutung oder bei Therapieresistenz ist immer eine histologische Abklärung indiziert. I Status nach kontinuierlich-kombinierter
Östrogen-Gestagen-Therapie Wenn während der ersten 6 Monate einer solchen Therapie eine Blutungsstörung auftritt, bedarf dies noch keiner Diagnostik. Eine Beurteilung des Endometriums mit Sonografie und Endometriumbiopsie ist indiziert, wenn:
– die Blutungsstörung unter dem gleichen Präparat > 6 Monate anhält
– während einer kontinuierlich-kombinierten Östrogen-Gestagen-Therapie eine Blutung nach einer Phase der Amenorrhö erstmals auftritt oder
– die Blutung trotz hormoneller Manipulation (z.B. Anpassung des Gestagen-Anteils) persistiert.
14 GYNÄKOLOGIE 5/2014
SCHWERPUNKT
Therapie
Akute Blutung Entscheidend für die Therapiewahl bei akuter Blutung ist die hämodynamische Stabilität der Patientin. Die hämodynamisch instabile Patientin erfordert gegebenenfalls eine Transfusion und ein operatives, ursachenadaptiertes Vorgehen. Im Folgenden soll nur auf die hämodynamisch stabile Patientin eingegangen werden. In diesem Fall ist die hormonale Therapie die Therapie der ersten Wahl (Tabelle 2). Die Behandlungsstrategie ist bei einer perimenopausalen Patientin ähnlich derjenigen bei einer prämenopausalen. Allerdings sollte bei perimenopausalen Frauen das höhere Thromboserisiko (Tabelle 3) berücksichtigt werden, Östrogene sollten eher transkutan und weniger oral gegeben und zudem sollte kein Ethinylöstradiol verabreicht werden. Bei hohem Thromboserisiko ist die hormonale Therapie mit Östrogenen kontraindiziert. Bei kontraindizierter Östrogen-Therapie ist eine Gestagen-Monotherapie oder das operative Vorgehen mit Hysteroskopie und Endometriumablation zu erwägen. Die Endometriumablation ist einer Kürettage oder einer Embolisation der Arteria uterina vorzuziehen.
Ethinylestradiol enthaltende kombinierte orale Kontrazeptiva, Pflaster, Ring) im klassischen Regime (21/7) oder Langzyklus (3–4 x 21/7) (Reduktion des Blutverlustes um 40%) (8). Die medikamentöse Therapie in der second line besteht aus: I Antifibrinolytika (9, 10) – Tranexamsäure 3–4 x 1,0–1,5 g/Tag vom 1. bis
zum 5. ZT (Reduktion des Blutverlustes um 35–60%) I oralen Gestagenen vom 15. bis zum 26. ZT oder jeweils vom 1. bis zum 12. Tag des Kalendermonats (nur bei Anovulation sinnvoll) (11) – Medroxyprogesteronacetat: 5–10 mg/Tag – Norethisteronacetat: 1–2 x 5 mg/Tag – Duphaston 1–2 x 10 mg/Tag – mikronisiertes Progesteron 200–300 mg/Tag I GnRHa plus «add back»-Hormontherapie I Desmopressin (dDAVP) ab 1. ZT bei WillebrandJürgens-Syndrom.
Operative Therapie Die operativen Therapieoptionen umfassen Endometriumablation und -resektion sowie Hysterektomie (12, 13).
Chronische Blutung in der Prä-/Perimenopause Das Therapieziel bei chronischer Blutung in der Prämenopause sind die (Wieder-)Herstellung regelmässiger Zyklen und die Prävention der Endometriumhyperplasie respektive des Endometriumkarzinoms. Je nach Ursache gelingt das mit: I einer Behandlung der zugrunde liegenden Er-
krankung I einer Pharmakotherapie oder I einer Operation. Die im Folgenden dargestellten Therapieoptionen gelten für Frauen ohne Nachweis einer organischen Ursache der Blutungsstörung. Auf die Therapie einer Brachy- und/oder einer Hypomenorrhö wird nicht eingegangen.
Chronische Hypermenorrhö und/oder Menorrhagie (abnormes Blutvolumen) Die medikamentöse Therapie in der first line besteht aus: I Hormonspirale Levonorgestrel-IUD (Reduktion
des Blutverlustes um 75–95%) (6) I nichtsteroidalen Antirheumatika vom 1. bis zum
5. ZT beziehungsweise bis Blutungsende (Reduktion des Blutverlustes um 20–40%) (7) – Mefenaminsäure 3 x 500 mg/Tag – Naproxen 2 x 500 mg am 1. ZT, dann 250–
500 mg/Tag – Ibuprofen 3 x 400 mg/Tag I (Zurückhaltung in der Perimenopause): kombinierter hormonaler Kontrazeption (30–35 µg
Bei Oligo- und Polymenorrhö (Störung der Menstruationsfrequenz) I ovulatorische Oligomenorrhö: keine Therapie er-
forderlich I ovulatorische Polymenorrhö: keine Therapie er-
forderlich (Ausnahme: Anämie, Beeinträchtigung der Lebensqualität) I anovulatorische Oligo- und Polymenorrhö: – orale Gestagene vom 15. bis zum 26. ZT:
G Medroxyprogesteronacetat: 5–10 mg/Tag G Norethisteronacetat: 1–2 x 5 mg/Tag G Duphaston 1–2 x 10 mg/Tag G mikronisiertes Progesteron 200–300 mg/Tag
Tabelle 3:
Hereditäre und erworbene Thrombophilie
Hereditäre Thrombophilie Faktor-5-Leiden-Mutation
Prothrombin-Genmutation Protein-S-Mangel Protein-C-Mangel Antithrombin-III-Mangel Dysfibrinogenämie (selten)
Erworbene Thrombophilie aktuelle/vorangehende venöse Thromboembolie Malignom liegender zentraler Venenkatheter grosse Operation Trauma, Immobilisation Herzinfarkt, Apoplex Anti-Phospholipid-Antikörper-Syndrom myeloproliferative Erkrankung paroxysmale nächtliche Hämoglobinurie chronisch-entzündliche Darmerkrankung nephrotisches Syndrom Alter > 35 Jahre und Nikotinabusus
GYNÄKOLOGIE 5/2014
15
SCHWERPUNKT
– Östrogen-Gestagen-Präparat vom 15. bis zum 26. ZT, wenn keine ausreichende endometriale Östrogenwirkung in der ersten Zyklushälfte vermutet wird
– (Zurückhaltung in der Perimenopause): kombinierte hormonale Kontrazeptiva.
Postmenopausale Blutung Bei Frauen ohne erfolgter Hormontherapie Wenn eine Organpathologie ausgeschlossen wurde, ist eine Therapie nicht zwingend indiziert.
Bei Frauen mit erfolgter Hormontherapie Wenn eine Organpathologie ausgeschlossen wurde, kann das Hormonpräparat wie folgt gewechselt werden: I bei sequenzieller Östrogen-Gestagen-Therapie:
Therapieversuch mit Anheben der GestagenDosis und/oder Wechsel des Gestagen-Typs (19Nortestosteronabkömmling), Einlage eines Levenorgestrel-IUD oder operatives Vorgehen (Endometriumablation, Hysterektomie) I bei kontinuierlich kombinierter Östrogen-Gestagen-Therapie: Therapieversuch mit Anheben der Gestagendosis und/oder Wechsel des Gestagentyps (19-Nortestosteronabkömmling) oder Senken der Östrogendosis, Wechsel zu einer sequenziellen Östrogen-Gestagen-Therapie, Einlage eines Levonorgestrel-IUD oder operatives Vorgehen (Endometriumablation, Hysterektomie). I
Prof. Dr. med. Michael von Wolff (Korrespondenzadresse) E-Mail: Michael.vonWolff@insel.ch
und PD Dr. med. Petra Stute
Beide: Abteilung für Gynäkologische Endokrinologie und Reproduktionsmedizin Universitätsfrauenklinik Inselspital Bern 3010 Bern
Merkpunkte
I Bei einer peri- und einer postmenopausalen Blutungsstörung muss als Ursache immer ein Malignom in Betracht gezogen werden.
I Bei einer akuten Blutung in der Perimenopause, die keine operative Intervention erfordert, kann nach histologischer Endometriumbeurteilung ein endokriner Therapieversuch mit Östrogenen, gefolgt von Gestagenen, erwogen werden.
I Eine Therapie der chronischen perimenopausalen Blutung erfolgt nach histologischer Endometriumbeurteilung primär mit Levonorgestrel-IUD, nichtsteroidalen Antirheumatika oder sekundär mit Tranexamsäure, Gestagenen usw.
I Die Diagnostik und Therapie der postmenopausalen Blutung ist abhängig davon, ob und welche Hormone verabreicht werden.
Quellen: 1. von Wolff M., Stute P. (Hrsg.; Autoren): Blutungsstörungen. In: Gynäkologische Endokrinologie und Reproduktionsmedizin – Praxisbuch. 1. Auflage. Schattauer Verlage. Stuttgart 2013. 2 Interdisziplinäre Leitlinie der Deutschen Krebsgesellschaft e.V. (DKG) und der Deutschen Gesellschaft für Gynäkologie und Geburtshilfe (DGGG): Diagnostik und Therapie des Endometriumkarzinoms. AWMF-Leitlinien-Register Nr. 032/034, Entwicklungsstufe: 2k, 2008 (z.Z. in Überarbeitung). 3. Ass. Profs Gynecol & Obstet: APGO educational series on women’s health issues: Clinical management of abnormal uterine bleeding. Mai 2002. 4. Dijkhuizen FP, Mol BW, Brölmann HA, Heintz AP.: The accuracy of endometrial sampling in the diagnosis of patients with endometrial carcinoma and hyperplasia: a meta-analysis. Cancer 2000;15; 89: 1765–72. 5. Americ. Coll. Obstet & Gynecol (ACOG).: The role of transvaginal ultrasonography in the evaluation of postmenopausal bleeding. ACOG Committee Opinion No. 440. Obstet Gynecol 2009; 114: 409. 6. Lethaby AE, Cooke I, Rees M.: Progesterone or progestogen-releasing intrauterine systems for heavy menstrual bleeding. Cochrane Database Syst Rev 2005; CD002126. 7. Lethaby A, Augood C, Duckitt K, Farquhar C.: Nonsteroidal anti-inflammatory drugs for heavy menstrual bleeding. Cochrane Database Syst Rev 2007; CD000400. 8. Farquhar C, Brown J.: Oral contraceptive pill for heavy menstrual bleeding. Cochrane Database Syst Rev 2009; CD000154. 9. Lethaby A, Farquhar C, Cooke I.: Antifibrinolytics for heavy menstrual bleeding. Cochrane Database Syst Rev 2000; CD000249. 10. Lumsden MA, Wedisinghe L.: Tranexamic acid therapy for heavy menstrual bleeding. Expert Opin Pharmacother 2011; 12: 2089–95. 11. Lethaby A, Irvine G, Cameron I.: Cyclical progestogens for heavy menstrual bleeding. Cochrane Database Syst Rev 2008; CD001016. 12. Lethaby A, Hickey M, Garry R, Penninx J.: Endometrial resection / ablation techniques for heavy menstrual bleeding. Cochrane Database Syst Rev 2009; CD001501. 13. Middleton LJ, Champaneria R, Daniels JP, et al.: Hysterectomy, endometrial destruction, and levonorgestrel releasing intrauterine system (Mirena) for heavy menstrual bleeding: systematic review and meta-analysis of data from individual patients. BMJ 2010; 341:c3929.
Interessenkonflikte: keine.
16 GYNÄKOLOGIE 5/2014