Transkript
SCHWERPUNKT
Kontrazeption in der Perimenopause
Bewährte und neuere Methoden
Bei der Wahl der Kontrazeptionsmethode in der Perimenopause sollten deren Wirkungen auf altersbedingte Komorbiditäten sowie erhöhte thromboembolische und kardiovaskuläre Risiken berücksichtigt werden. Teilweise tragen Benefits von Kontrazeptiva aber auch dazu bei, perimenopausale Symptome zu reduzieren. Im Folgenden werden seit Langem bewährte sowie neuere geeignete (und weniger geeignete) Methoden hinsichtlich der aktuellen Studienlage beschrieben.
GABRIELE S. MERKI-FELD
Die Perimenopause ist die Lebensphase, in der die Ovarialfunktion langsam zum Erliegen kommt. Sie dauert im Mittel vier Jahre und geht mit Veränderungen einher, die die Psyche, das vegetative System und den Zyklus betreffen. Trotz deutlich erniedrigter Fertilität ist in diesen Jahren weiterhin eine Schwangerschaftsverhütung erforderlich, zumal es in der Regel nicht vorhersehbar ist, wann im Einzelfall die Postmenopause erreicht wird.
Physiologie der Perimenopause
Der Beginn der Perimenopause ist durch das Eintreten variabler Zykluslängen und eine Verkürzung der Zyklusdauer (mittlere Zyklusdauer 25–26 Tage statt 28–29 Tage) charakterisiert (1). Während der Perimenopause kann die Zykluslänge von 14 bis zu 50 Tagen variieren. Etwa 20% der Frauen erleben in dieser Zeit gar keine Zyklusveränderungen. Bereits vor den Zyklusveränderungen können erste Symptome wie Hitzewallungen, Schlafstörungen, Kopfschmerzen, Konzentrationsstörungen und Brustspannen auftreten. In einer britischen Kohortenstudie gaben 30% der Frauen in dieser Lebensphase ernsthafte vasomotorische Symptome an (2). Diese gehen in der Regel 1 bis 3 Jahre nach der Menopause wieder zurück. Die STRAW-Klassifikation der WHO definiert die verschiedenen Phasen der Perimenopause und der frühen Postmenopause (3): Im Mittel dauert die Perimenopause 4 Jahre, darin eingeschlossen ist das Jahr nach der letzten Menstruationsblutung. Die Fertilität in der Perimenopause ist deutlich reduziert. Die Estradiolspiegel sind bis kurz vor der Menopause eher erhöht als erniedrigt. Die Knochendichte nimmt bereits in den Jahren vor der Menopause ab (4). Mehrere Studien deuten dar-
auf hin, dass der Verlust an Knochendichte eher mit dem Anstieg der FSH-Spiegel (Stimulation der Osteoklasten) als mit fallenden Östradiolspiegeln zusammenhängt (5, 6). Die Perimenopause ist mit dem Auftreten des Metabolischen Syndroms assoziiert und deshalb ein Risikoalter für die Entwicklung einer koronaren Herzerkrankung (7). Obwohl kein direkter Zusammenhang zwischen Hypertonie und Perimenopause besteht, ist aufgrund der hohen Inzidenz einer Hypertonie in diesem Alter eine regelmässige Kontrolle des Blutdrucks sinnvoll. Allgemeine Präventionsmassnahmen in der Perimenopause umfassen die Kontrolle von Blutdruck, Schilddrüsenfunktion, Vitamin-D-Spiegel und Nüchternlipiden. Viele Frauen berichten in dieser Lebensphase über zunehmende Vergesslichkeit und Konzentrationsstörungen (8). Auch wenn diese Symptome in speziellen Tests kaum verifizierbar sind, so verursachen sie doch einen nicht unerheblichen Leidensdruck (9). Das Risiko, an einer schwereren Depression zu erkranken, verdoppelt sich in der Perimenopause und ist in der Postmenopause etwa um das Vierfache erhöht (9).
Kontrazeption in der Perimenopause
Die Wahrscheinlichkeit, in einer Partnerschaft mit regelmässigem Geschlechtsverkehr schwanger zu werden, liegt im Alter von 40 bis 44 Jahren bei etwa 30% und im Alter von 45 bis 49 Jahren bei 10% (10). Trotz erniedrigter Fertilität und langjähriger Verhütungserfahrung treten 8 bis 10% der unerwünschten Schwangerschaften in der Schweiz bei Frauen in der Altersgruppe der über 40-Jährigen auf.
GYNÄKOLOGIE 5/2014
23
SCHWERPUNKT
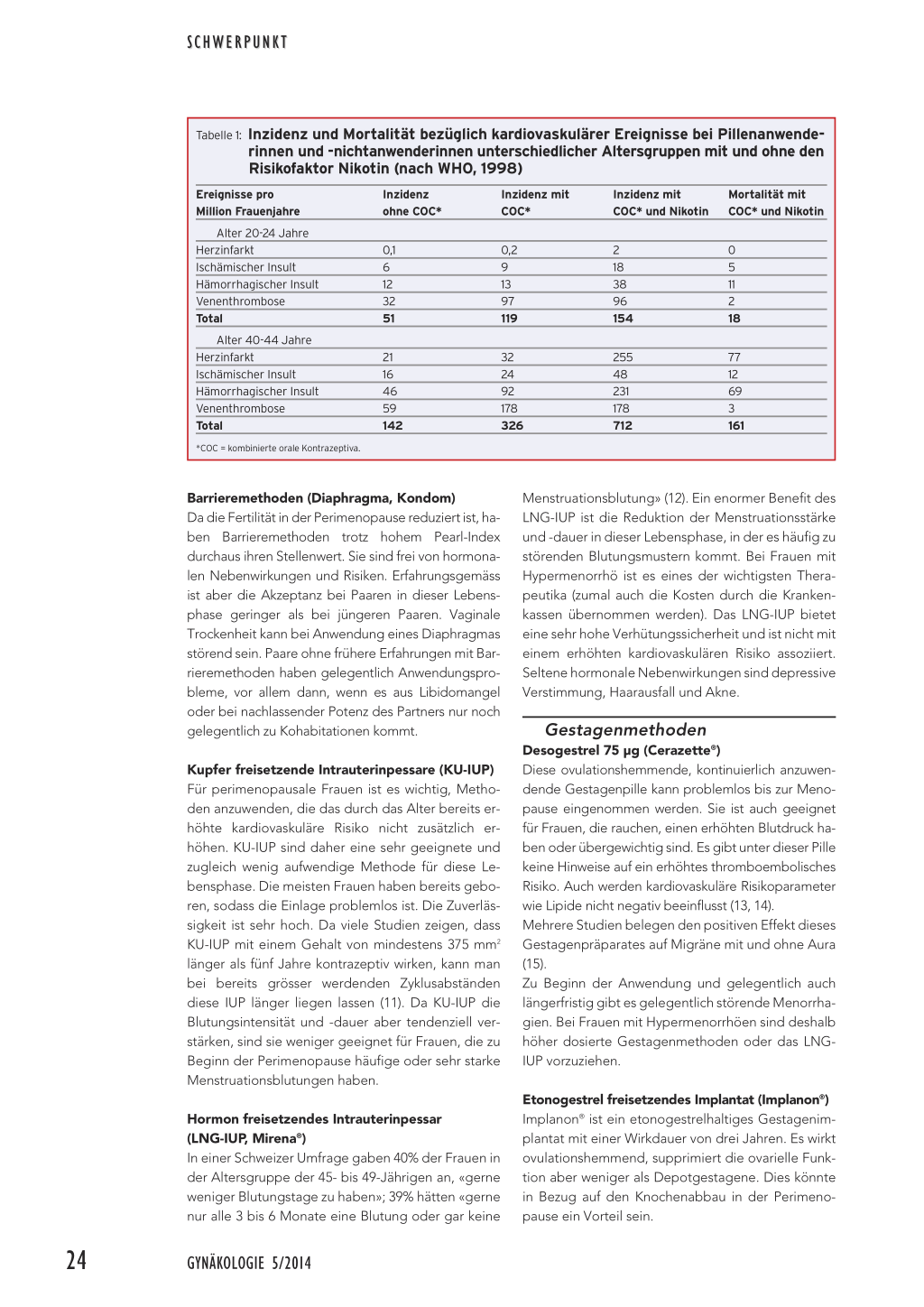
Tabelle 1: Inzidenz und Mortalität bezüglich kardiovaskulärer Ereignisse bei Pillenanwenderinnen und -nichtanwenderinnen unterschiedlicher Altersgruppen mit und ohne den Risikofaktor Nikotin (nach WHO, 1998)
Ereignisse pro Million Frauenjahre
Alter 20-24 Jahre Herzinfarkt Ischämischer Insult Hämorrhagischer Insult Venenthrombose Total
Alter 40-44 Jahre Herzinfarkt Ischämischer Insult Hämorrhagischer Insult Venenthrombose Total
Inzidenz ohne COC*
0,1 6 12 32 51
21 16 46 59 142
Inzidenz mit COC*
0,2 9 13 97 119
32 24 92 178 326
Inzidenz mit
Mortalität mit
COC* und Nikotin COC* und Nikotin
20 18 5 38 11 96 2 154 18
255 77 48 12 231 69 178 3 712 161
*COC = kombinierte orale Kontrazeptiva.
Barrieremethoden (Diaphragma, Kondom) Da die Fertilität in der Perimenopause reduziert ist, haben Barrieremethoden trotz hohem Pearl-Index durchaus ihren Stellenwert. Sie sind frei von hormonalen Nebenwirkungen und Risiken. Erfahrungsgemäss ist aber die Akzeptanz bei Paaren in dieser Lebensphase geringer als bei jüngeren Paaren. Vaginale Trockenheit kann bei Anwendung eines Diaphragmas störend sein. Paare ohne frühere Erfahrungen mit Barrieremethoden haben gelegentlich Anwendungsprobleme, vor allem dann, wenn es aus Libidomangel oder bei nachlassender Potenz des Partners nur noch gelegentlich zu Kohabitationen kommt.
Kupfer freisetzende Intrauterinpessare (KU-IUP) Für perimenopausale Frauen ist es wichtig, Methoden anzuwenden, die das durch das Alter bereits erhöhte kardiovaskuläre Risiko nicht zusätzlich erhöhen. KU-IUP sind daher eine sehr geeignete und zugleich wenig aufwendige Methode für diese Lebensphase. Die meisten Frauen haben bereits geboren, sodass die Einlage problemlos ist. Die Zuverlässigkeit ist sehr hoch. Da viele Studien zeigen, dass KU-IUP mit einem Gehalt von mindestens 375 mm2 länger als fünf Jahre kontrazeptiv wirken, kann man bei bereits grösser werdenden Zyklusabständen diese IUP länger liegen lassen (11). Da KU-IUP die Blutungsintensität und -dauer aber tendenziell verstärken, sind sie weniger geeignet für Frauen, die zu Beginn der Perimenopause häufige oder sehr starke Menstruationsblutungen haben.
Hormon freisetzendes Intrauterinpessar (LNG-IUP, Mirena®) In einer Schweizer Umfrage gaben 40% der Frauen in der Altersgruppe der 45- bis 49-Jährigen an, «gerne weniger Blutungstage zu haben»; 39% hätten «gerne nur alle 3 bis 6 Monate eine Blutung oder gar keine
Menstruationsblutung» (12). Ein enormer Benefit des LNG-IUP ist die Reduktion der Menstruationsstärke und -dauer in dieser Lebensphase, in der es häufig zu störenden Blutungsmustern kommt. Bei Frauen mit Hypermenorrhö ist es eines der wichtigsten Therapeutika (zumal auch die Kosten durch die Krankenkassen übernommen werden). Das LNG-IUP bietet eine sehr hohe Verhütungssicherheit und ist nicht mit einem erhöhten kardiovaskulären Risiko assoziiert. Seltene hormonale Nebenwirkungen sind depressive Verstimmung, Haarausfall und Akne.
Gestagenmethoden
Desogestrel 75 µg (Cerazette®) Diese ovulationshemmende, kontinuierlich anzuwendende Gestagenpille kann problemlos bis zur Menopause eingenommen werden. Sie ist auch geeignet für Frauen, die rauchen, einen erhöhten Blutdruck haben oder übergewichtig sind. Es gibt unter dieser Pille keine Hinweise auf ein erhöhtes thromboembolisches Risiko. Auch werden kardiovaskuläre Risikoparameter wie Lipide nicht negativ beeinflusst (13, 14). Mehrere Studien belegen den positiven Effekt dieses Gestagenpräparates auf Migräne mit und ohne Aura (15). Zu Beginn der Anwendung und gelegentlich auch längerfristig gibt es gelegentlich störende Menorrhagien. Bei Frauen mit Hypermenorrhöen sind deshalb höher dosierte Gestagenmethoden oder das LNGIUP vorzuziehen.
Etonogestrel freisetzendes Implantat (Implanon®) Implanon® ist ein etonogestrelhaltiges Gestagenimplantat mit einer Wirkdauer von drei Jahren. Es wirkt ovulationshemmend, supprimiert die ovarielle Funktion aber weniger als Depotgestagene. Dies könnte in Bezug auf den Knochenabbau in der Perimenopause ein Vorteil sein.
24 GYNÄKOLOGIE 5/2014
SCHWERPUNKT
Tabelle 2:
Abklärungen, die vor der Verschreibung kombinierter oraler Kontrazeptiva erforderlich sind, um das kardiovaskuläre Risiko der Patientin einschätzen zu können:
I Alter
I Rauchen (Nikotinabusus)
I Blutdruckkontrolle
I Eigen- oder Familienanmnese:
– thromboembolische Erkrankungen
– Herzinfarkt
– zerebraler Insult
– Lungenembolie
– Migräne
I Lipidstatus bei Alter > 35 Jahre
I Gewicht/BMI
Zum andern ist die Frequenz von Menorrhagien unter der Implantatanwendung vergleichsweise hoch; es kommt aber nicht, wie bei Depot-Medroxyprogesteronazetat, mit längerer Anwendungsdauer bei den meisten Frauen zur Amenorrhö. Bestehen dysfunktionelle Blutungen in der Perimenopause, ist das Implantat daher nur bedingt geeignet. Studien belegen die geringen metabolischen Effekte auf Lipide und kardiovaskuläre Risikoparameter (16). Das Implantat kann daher für Frauen in der Perimenopause zur Anwendung empfohlen werden.
Depot-Medroxyprogesteronacetat (Depo Provera®, Sayana®) Parenteral applizierte Depotgestagene hemmen die Ovulation. Sie sind in der Perimenopause eine Alternative für Frauen, die orale Gestagene oder Intrauterinpessare ablehnen. Irreguläre Blutungen in den ersten Monaten der Anwendung sind häufig, aber durch die vorübergehende orale oder transdermale Applikation natürlicher Östrogene gut therapierbar. Unter Anwendung von Depot-Medroxyprogesteronazetat 150 mg (DMPA) entwickelt sich bei 50% der Frauen nach einem Jahr eine Amenorrhö. Verstärkte oder verlängerte Menstruationsblutungen in der Perimenopause sowie ein Status bei Uterus myomatosus lassen sich gut mit Depotgestagenen therapieren. Hinsichtlich der Anwendbarkeit bei Frauen mit kardiovaskulären Risiken interessiert die Frage nach dem Einfluss von DMPA auf die Lipidfraktionen. Die hierzu vorliegenden Daten sind widersprüchlich. Einerseits wurden nicht signifikante Anstiege der Triglyzeride und des HDL beschrieben, andererseits wurde ein Abfall des HDL um 15% beschrieben (17). Es ist daher sinnvoll, bei Risikopatientinnen unter DMPA Lipidkontrollen durchzuführen. Die leichte Verschlechterung der Glukosetoleranz durch DMPA hat keine klinische Relevanz. Dagegen reichen, wie auch bei anderen Gestagenmethoden, die im Bereich der frühen Follikelreifungsphase liegenden Östradiolspiegel wahrscheinlich nicht aus, um den
physiologischen Knochenverlust in der Perimenopause zu verhindern. Langzeitanwenderinnen von DMPA verlieren weniger an Knochendichte in der frühen Menopause (18).
Kombinierte hormonale Kontrazeptiva Sowohl das kardiovaskuläre als auch das thromboembolische Risiko steigen mit dem Alter. Zudem bestehen bei vielen Frauen in der Perimenopause arterielle kardiovaskuläre Risikofaktoren wie Hypertonie, Rauchen, Übergewicht oder Hyperlipidämien. Über die Jahre führen diese Faktoren zur Verengung arterieller Gefässe und prädisponieren zu kardiovaskulären Ereignissen. Diese sind mit einer höheren Mortalität als thromboembolische Ereignisse assoziiert. Die (geringeren) Gefässwandveränderungen einer jungen Raucherin können durchaus das Verschreiben eines Kombinationspräparates erlauben, wogegen dies für eine 40-jährige Raucherin nicht mehr akzeptabel ist: Die Inzidenz kardiovaskulärer Erkrankungen bei 40- bis 44-jährigen Frauen ist mit 45/100 000 Frauenjahren (FJ) siebenmal höher als bei 20- bis 24-jährigen Frauen. Gleichzeitig ist auch die Mortalität an kardiovaskulären Erkrankungen in der Klasse der 35bis 44-Jährigen (9,2/100 000 FJ) etwa achtmal grösser als in der Altersklasse der 15- bis 24-Jährigen. Sie verdoppelt sich zusätzlich, wenn 40- bis 44-jährige Frauen orale Kontrazeptiva einnehmen (19). Auch wenn die absoluten Zahlen für diese Ereignisse niedrig sind, so bleibt doch zu bedenken, dass sie junge Frauen treffen und vermeidbar wären, wenn eine andere Kontrazeptionsmethode gewählt worden wäre. Die MICA-Studie und WHO-Daten zeigen, dass das Herzinfarktrisiko unter hormonaler Kontrazeption signifikant durch die Blutdruckkontrolle vor Verschreibung gesenkt werden kann. Das Risiko für eine Venenthrombose unter kombinierter Antikonzeption ist bei Frauen im Alter über 45 Jahre um das 6- bis 10-Fache erhöht im Vergleich zu jungen Frauen (20, 21). Das Thromboserisiko ist unter Anwendung nicht oraler Kombinationspräparate (Patch, Vaginalring) genauso gross. Verhütungspräparate mit natürlichen Östrogenen sind nach heutigem Wissen nicht mit geringeren Risiken verbunden. Auch wenn es durchaus Surrogatparameter gibt, die vielversprechend sind, gilt es hier, die epidemiologischen Daten abzuwarten. Die mit den Kombinationspräparaten assoziierten Risiken lassen sich auch nicht durch Reduktion der Ethinylestradioldosis von 30 µg auf 20 µg senken. Benefits der Anwendung von Kombinationspräparaten in der Perimenopause sind die Verhinderung des beginnenden Knochenabbaus, der positive Effekt auf perimenopausale Beschwerden und die oft geschätzte Zyklusregulation. Diese Benefits können teilweise aber auch durch andere therapeutische Massnahmen erreicht werden.
26 GYNÄKOLOGIE 5/2014
SCHWERPUNKT
Notfallkontrazeption Als Notfallkontrazeption stehen heute in der Schweiz folgende Methoden zur Verfügung: 1. Levonorgestrel (LNG) 1,5 mg Norlevo® 2. Ulipristalacetat (UPA) 30 mg EllaOne® 3. kupferhaltige Intrauterinpessare. Die Notfallkontrazeption ist keine Verhütungsmethode, kann aber in der Perimenopause beim Versagen von Barrieremethoden ergänzend angewandt werden. Natürlich stehen beide Methoden auch bei ungeschütztem Verkehr aus anderen Gründen zur Verfügung. UPA ist etwas effizienter als LNG. Zieht man in Betracht, dass die Fertilität in dieser Lebensphase doch recht reduziert ist, hat die notfallmässige Einlage eines IUP nur einen Stellenwert für Frauen, die längerfristig auf diese Art verhüten möchten.
Tubensterilisation Die Tubensterilisation respektive die Vasektomie beim Mann werden in Grossbritannien von 40% der über 40 Jahre alten Paare angewandt. Nur selten tritt in diesem Alter nach abgeschlossener Familienplanung noch einmal der Wunsch nach einer Schwangerschaft auf. Sind bereits perimenopausale Symptome vorhanden, ist zu diskutieren, ob der Aufwand für diese Verhütungsmethode noch gerechtfertigt ist. Die breite Anwendung der Sterilisation wird in einigen europäischen Ländern dadurch limitiert, dass die Kosten für den Eingriff nicht von der Krankenkasse übernommen werden. Kulturelle und religiöse Gründe sind weitere Ursachen für die Ablehnung dieser Verhütungsmethode. Vorteile der Sterilisation sind die hohe kontrazeptive Sicherheit und die Möglichkeit der Anwendung bei Frauen mit kardiovaskulären Risikofaktoren. Störende perimenopausale Symptome und der Verlust an Knochendichte werden durch diese Methode nicht beeinflusst.
Vasektomie Die Vasektomie ist eine in der Schweiz weniger verbreitete Verhütungsmethode. Sie hat ihren Stellenwert eher vor der Perimenopause, also in der Lebensphase der Frau, in der die Familienplanung bereits
Merkpunkte
I Die in der Perimenopause reduzierte Fertilität er-
laubt die Anwendung von Barrieremethoden zur Kon-
trazeption, auch bei stark negativem Kinderwunsch.
I Operative Methoden sollten eher früher durchge-
führt werden.
I Von kombinierten hormonalen Kontrazeptiva wird
nicht nur wegen des Risikos für eine Venenthrombose,
sondern auch wegen des altersbedingt stark erhöh-
ten Risikos für arteriellen Gefässverschluss abgeraten.
I Alternativen sind Intrauterinpessare oder Gestagene
in Form von Pillen, Implantaten oder Depot-
injektionen.
abgeschlossen ist, aber die Fertilität der Partner noch hoch ist. Die Kosten werden in der Schweiz nicht von der Krankenkasse übernommen. Die gewünschte Azoospermie nach Durchtrennung der Samenleiter tritt erst nach 2 bis 3 Monaten oder später ein. Ein Vorteil gegenüber der operativen Unterbindung der Frau sind die geringen Operationsrisiken, da der Samenleiter gut zugänglich ist. Nur selten treten Komplikationen auf (Infektionen 0,2–1,5%, postoperative Blutung 4–22%, chronische Schmerzen 1–14%) (22). I
PD Dr. med. Gabriele Susanne Merki-Feld Leiterin Kontrazeption und Adoleszenz Klinik für Reproduktions-Endokrinologie UniversitätsSpital Zürich 8091 Zürich E-Mail: gabriele.merki@usz.ch
Quellen: 1. Hale GE, Robertson DM, Burger HG.: The perimenopausal woman: endocrinology and management. J Ster Biochem Molecul Biol. 2014; 142: 121–31. 2. Mishra GD, Dobson AJ.: Using longitudinal profiles to characterize women’s symptoms through midlife: results from a large prospective study. Menopause. 2012; 19: 549–55. 3. Harlow SD, Gass M, Hall JE, et al.: Executive summary of the Stages of Reproductive Aging Workshop + 10: addressing the unfinished agenda of staging reproductive aging. Fertil steril 2012; 97: 843–51. 4. Seifert-Klauss V, Fillenberg S, Schneider H, et al.: Bone loss in premenopausal, perimenopausal and postmenopausal women: results of a prospective observational study over 9 years. Climacteric: J Intern Menopause Soc. 2012; 15: 433–40. 5. Cannon JG, Kraj B, Sloan G.: Follicle-stimulating hormone promotes RANK expression on human monocytes. Cytokine. 2011; 53: 141–44. 6. Iqbal J, Blair HC, Zallone A, Sun L, Zaidi M.: Further evidence that FSH causes bone loss independently of low estrogen. Endocrine. 2012; 41: 171–75. 7. Janssen I, Powell LH, Crawford S, et al.: Menopause and the metabolic syndrome: the Study of Women’s Health Across the Nation. Arch intern med. 2008; 168: 1568–575. 8. Harlow SD, Gass M, Hall JE, et al.: Executive summary of the Stages of Reproductive Aging Workshop + 10: addressing the unfinished agenda of staging reproductive aging. Journal clin endocrin metabol. 2012; 97: 1159–168. 9. Weber MT, Maki PM, McDermott MP.: Cognition and mood in perimenopause: a systematic review and meta-analysis. J Ster Biochem Molecul Biol. 2014; 142: 90–98. 10. Klein J, Sauer MV.: Assessing fertility in women of advanced reproductive age. American journal of obstetrics and gynecology. 2001; 185: 758–70. 11. Wu JP, Pickle S.: Extended use of the intrauterine device: a literature review and recommendations for clinical practice. Contraception. 2014; 89: 495–503. 12. Merki-Feld GS, Breitschmid N, Seifert B, Kreft M.: A survey on Swiss women’s preferred menstrual/withdrawal bleeding pattern over different phases of reproductive life and with use of hormonal contraception. Europ J Contrac & Reprod Health Care. 2014; 19: 266–75. 13. Barkfeldt J, Virkkunen A, Dieben T.: The effects of two progestogen-only pills containing either desogestrel (75 microg/day) or levonorgestrel (30 microg/day) on lipid metabolism. Contraception. 2001; 64: 295–99. 14. Lidegaard O, Nielsen LH, Skovlund CW, Skjeldestad FE, Lokkegaard E.: Risk of venous thromboembolism from use of oral contraceptives containing different progestogens and oestrogen doses: Danish cohort study, 2001–9. BMJ. 2011; 343: d6423. 15. Merki-Feld GS, Imthurn B, Langner R, Sandor PS, Gantenbein AR.: Headache frequency and intensity in female migraineurs using desogestrel-only contraception: a retrospective pilot diary study. Cephalalgia. 2013; 33: 340–46. 16. Merki-Feld GS, Imthurn B, Seifert B.: Effects of the progestagen-only contraceptive implant Implanon on cardiovascular risk factors. Clin Endocrinol (Oxf). 2008; 68: 355–60. 17. Enk L, Landgren BM, Lindberg UB, Silfverstolpe G, Crona N.: A prospective, one-year study on the effects of two long acting injectable contraceptives (depotmedroxyprogesterone acetate and norethisterone oenanthate) on serum and lipoprotein lipids. Horm Metab Res. 1992; 24: 85–89. 18. Kaunitz AM, Arias R, McClung M.: Bone density recovery after depot medroxyprogesterone acetate injectable contraception use. Contraception. 2008; 77: 67–76. 19. Consensus conference on combination oral contraceptives and cardiovascular disease. Fertil Steril. 1999; 71: 1S–6S. 20. van Hylckama Vlieg A, Helmerhorst FM et al.: The venous thrombotic risk of oral contraceptives, effects of oestrogen dose and progestogen type: results of the MEGA case-control study. BMJ. 2009; 339: b2921. 21. Combined Hormonal Contraceptives (CHCs) and the Risk of Cardiovascular Disease Endpoints. CHC-CVD final report 111022v2. 2011. 22. Dohle GR, Diemer T, Kopa Z, et al.: European Association of Urology guidelines on vasectomy. European urology. 2012; 61: 159–163.
Interessenkonflikte: Die Autorin hat als Referentin und Adviser für Bayer, MSD und HRA Pharma gearbeitet. In Zusammenhang mit diesem Artikel sind keine Gelder von den Firmen geflossen.
GYNÄKOLOGIE 5/2014
27