Transkript
SCHWERPUNKT
Operative Therapie bei Blutungsstörungen
Management bei symptomatischen Myomen, Polypen und dysfunktionalen Blutungen
Ein Viertel aller Frauen leiden in ihrem Leben unter abnormen uterinen Blutungen (1). Damit stellen Blutungsstörungen eines der häufigsten Probleme in der gynäkologischen Praxis dar. Eine systematische Diagnostik, das Wissen um die Erfolgschancen der verschiedenen Therapien und das informative Gespräch sind Voraussetzung, eine individuelle Therapie anbieten zu können.
BERNHARD FELLMANN-FISCHER
Diagnostik
In der Anamnese von Blutungsstörungen sollte immer an eine Schwangerschaft gedacht werden, im Zweifelsfall ist diese auszuschliessen. Bei der Zyklusanamnese ist unter anderem auf die Dysmenorrhö als indirektes Zeichen für die Adenomyose zu achten. Kinderwunsch und Familienplanung müssen bekannt sein. Risikofaktoren für das Endometriumkarzinom sind zu erfassen. In der Familienanamnese ist neben Tumorleiden auf Blutungsneigungen und Blutgerinnungstörungen zu achten. Hämoglobin und gegebenenfalls Ferritin geben Auskunft über den chronischen Blutverlust. Auch bei der Untersuchung hilft ein systematisches Vorgehen. Blutungsursachen des äusseren Genitale, der Vagina und der Portio sind auszuschliessen und ein aktueller zytologischer Abstrich sollte vorliegen. Nach der Palpation folgt die Transvaginalsonografie, mit der Frage nach intrauterinen Raumforderungen und der Höhe des Endometriums. Zum Ausschluss von Ovarialtumoren sind hierbei auch immer die Adnexen zu dokumentieren. Die Entnahme von Endometriumgewebe (z.B. mit «Pipelle de Cornier») wird vor einer Endometriumablation und einer Hysterektomie empfohlen (2).
Myome
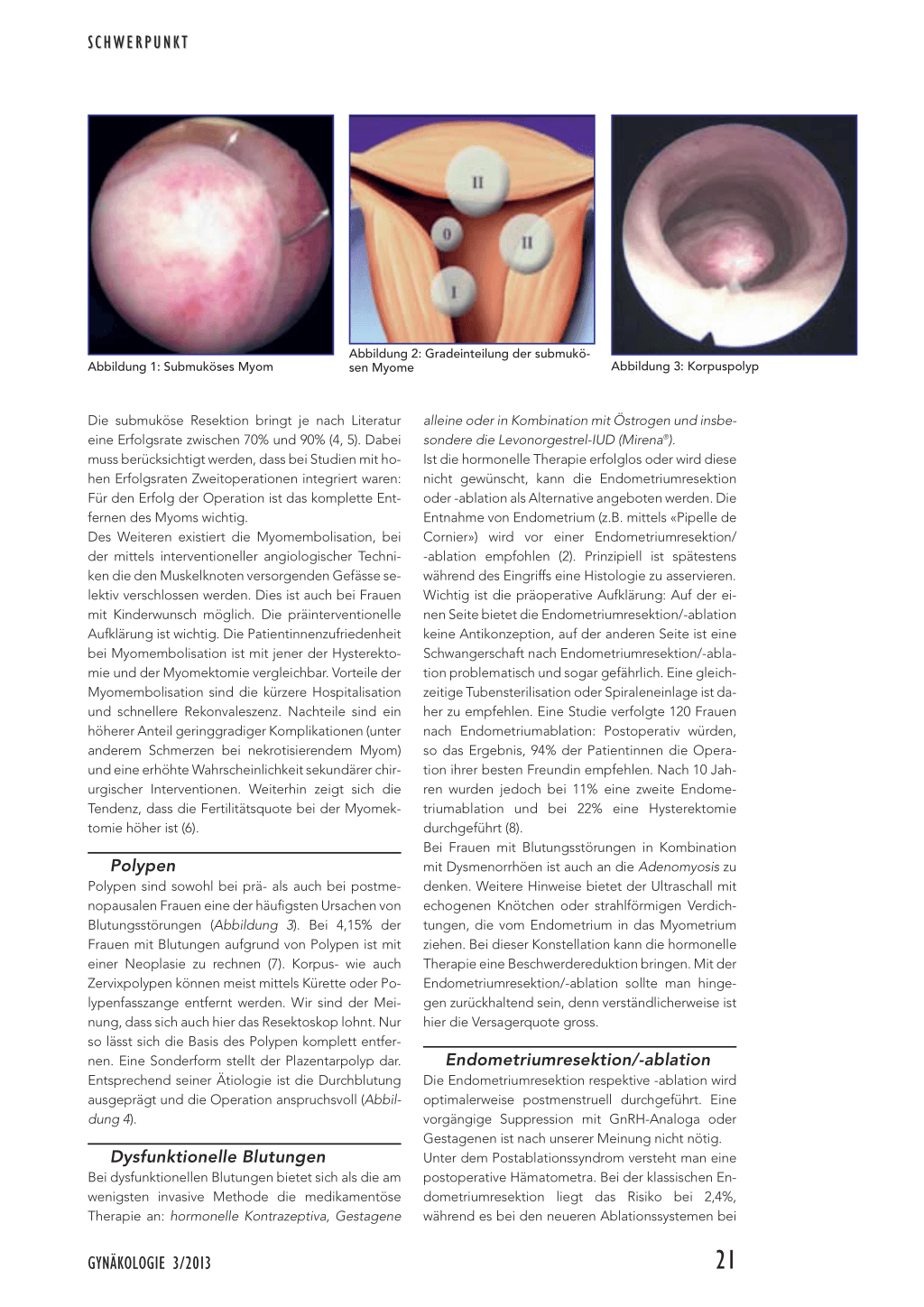
Uterusmyome sind bei Frauen die häufigsten Unterbauchtumore. 20% von ihnen liegen submukös (3) (Abbildung 1). Indikationen zur hysteroskopischen Resektion von submukösen Myomen sind neben therapieresistenten Blutungen Infertilität sowie primäre und sekundäre Sterilität. Zu beachten ist, dass bei multiplen Myomen die Resektion eines submukösen Myoms häufig keine oder nur eine temporäre Be-
schwerdereduktion bringt. Die präoperative sonografische Abklärung ist wichtig. Ein Sicherheitsabstand von mindestens 5 mm zwischen Myomkapsel und Serosa sollte vorhanden sein. Bei Myomen, die grösser sind als 5 cm, bietet sich zur Grössenreduktion der Einsatz von GnRH-Analoga an. Die Patientin ist präoperativ darüber aufzuklären, dass eventuell mehrere Eingriffe bis zur kompletten Entfernung nötig sind. Im Gegensatz zur monopolaren Resektion, bei der eine hypoosmolare Lösung verwendet wird, wird bei der bipolaren Resektion ein isoosmolares Spülmedium benutzt. Bei voraussichtlich längerer Operationszeit senkt die Anwendung eines bipolaren Resektoskopes das Risiko eines transuterinen Resektionssyndroms (TUR-Syndrom). Unter dem TUR-Syndrom versteht man Elektrolytverschiebungen aufgrund intravaskulär eingeschwemmten Spülmediums.
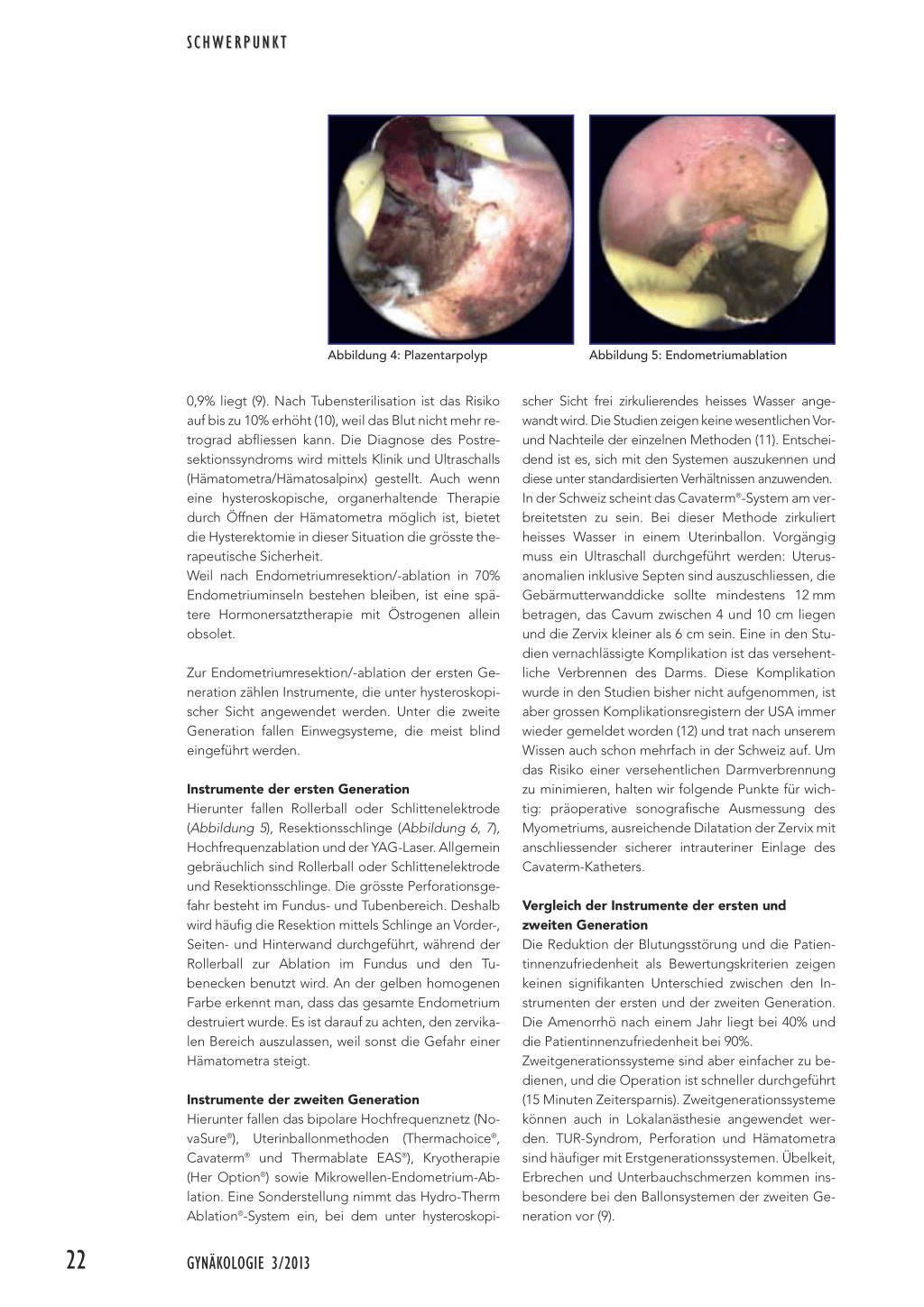
Submuköse Myome werden in drei Grade eingeteilt (Abbildung 2). Damit ein Myom durch den Zervikalkanal entfernt werden kann, muss insbesondere bei Grad-0-Myomen darauf geachtet werden, dass dieses vor Absetzen zerkleinert wird. Bei vorhandenem Kinderwunsch ist der möglichst gute Erhalt des Endometriums wichtig. Grad-II-Myome können operativ anspruchsvoll sein und bieten ein nicht unerhebliches Perforationsrisiko. Uterotonika können helfen, indem sie durch Kontraktion des Myometriums das Myom in die Gebärmutterhöhle drücken. Während der Resektion orientiert man sich an der Myomkapsel, die eine Resektionsstufe bildet. Kommt es zur Uterusperforation mit der elektrischen Schlinge, ist die Laparoskopie respektive Laparotomie zum Ausschluss einer Darmverletzung unumgänglich.
20 GYNÄKOLOGIE 3/2013
SCHWERPUNKT
Abbildung 1: Submuköses Myom
Abbildung 2: Gradeinteilung der submukö-
sen Myome
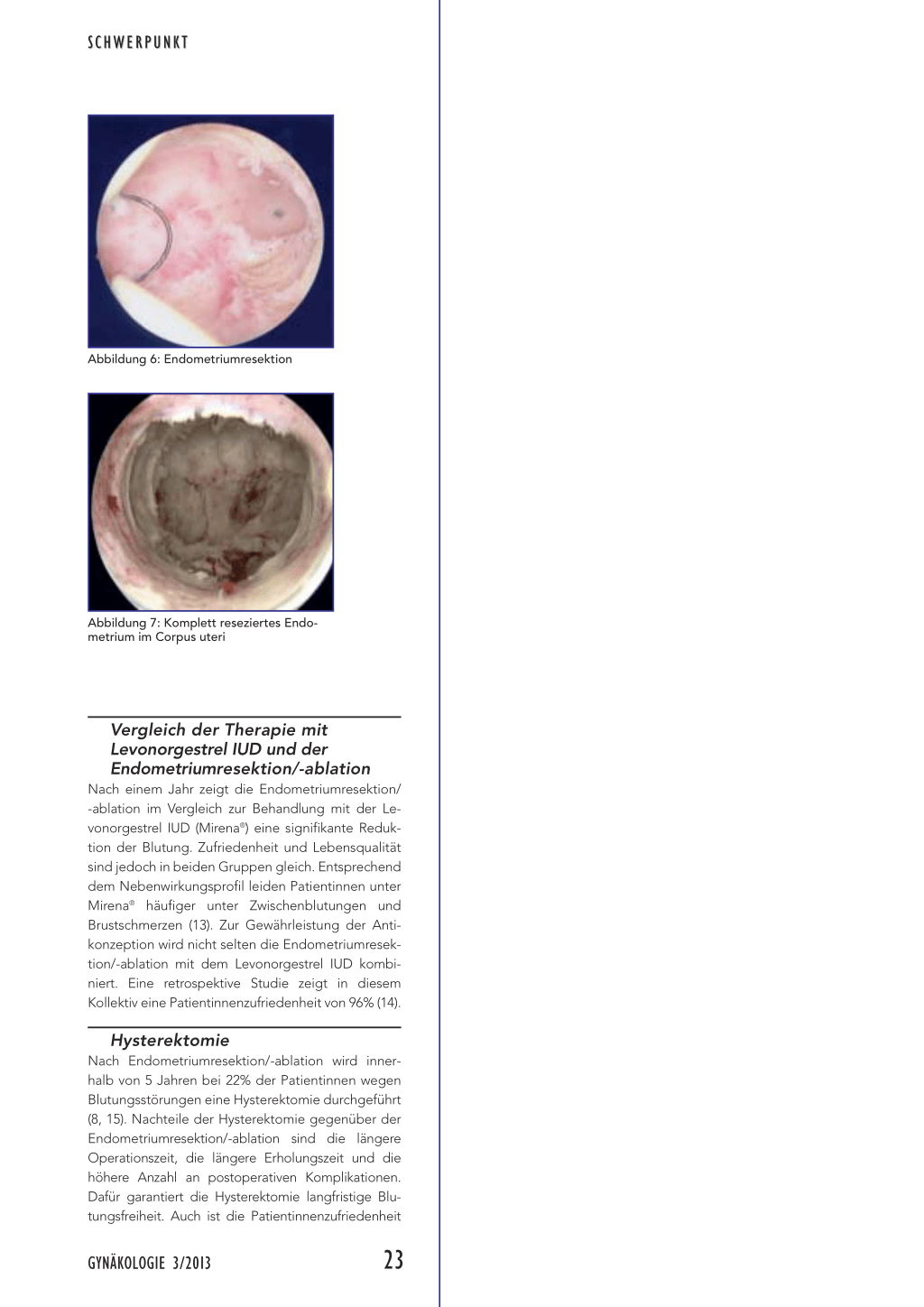
Abbildung 3: Korpuspolyp
Die submuköse Resektion bringt je nach Literatur eine Erfolgsrate zwischen 70% und 90% (4, 5). Dabei muss berücksichtigt werden, dass bei Studien mit hohen Erfolgsraten Zweitoperationen integriert waren: Für den Erfolg der Operation ist das komplette Entfernen des Myoms wichtig. Des Weiteren existiert die Myomembolisation, bei der mittels interventioneller angiologischer Techniken die den Muskelknoten versorgenden Gefässe selektiv verschlossen werden. Dies ist auch bei Frauen mit Kinderwunsch möglich. Die präinterventionelle Aufklärung ist wichtig. Die Patientinnenzufriedenheit bei Myomembolisation ist mit jener der Hysterektomie und der Myomektomie vergleichbar. Vorteile der Myomembolisation sind die kürzere Hospitalisation und schnellere Rekonvaleszenz. Nachteile sind ein höherer Anteil geringgradiger Komplikationen (unter anderem Schmerzen bei nekrotisierendem Myom) und eine erhöhte Wahrscheinlichkeit sekundärer chirurgischer Interventionen. Weiterhin zeigt sich die Tendenz, dass die Fertilitätsquote bei der Myomektomie höher ist (6).
Polypen
Polypen sind sowohl bei prä- als auch bei postmenopausalen Frauen eine der häufigsten Ursachen von Blutungsstörungen (Abbildung 3). Bei 4,15% der Frauen mit Blutungen aufgrund von Polypen ist mit einer Neoplasie zu rechnen (7). Korpus- wie auch Zervixpolypen können meist mittels Kürette oder Polypenfasszange entfernt werden. Wir sind der Meinung, dass sich auch hier das Resektoskop lohnt. Nur so lässt sich die Basis des Polypen komplett entfernen. Eine Sonderform stellt der Plazentarpolyp dar. Entsprechend seiner Ätiologie ist die Durchblutung ausgeprägt und die Operation anspruchsvoll (Abbildung 4).
Dysfunktionelle Blutungen
Bei dysfunktionellen Blutungen bietet sich als die am wenigsten invasive Methode die medikamentöse Therapie an: hormonelle Kontrazeptiva, Gestagene
alleine oder in Kombination mit Östrogen und insbesondere die Levonorgestrel-IUD (Mirena®). Ist die hormonelle Therapie erfolglos oder wird diese nicht gewünscht, kann die Endometriumresektion oder -ablation als Alternative angeboten werden. Die Entnahme von Endometrium (z.B. mittels «Pipelle de Cornier») wird vor einer Endometriumresektion/ -ablation empfohlen (2). Prinzipiell ist spätestens während des Eingriffs eine Histologie zu asservieren. Wichtig ist die präoperative Aufklärung: Auf der einen Seite bietet die Endometriumresektion/-ablation keine Antikonzeption, auf der anderen Seite ist eine Schwangerschaft nach Endometriumresektion/-ablation problematisch und sogar gefährlich. Eine gleichzeitige Tubensterilisation oder Spiraleneinlage ist daher zu empfehlen. Eine Studie verfolgte 120 Frauen nach Endometriumablation: Postoperativ würden, so das Ergebnis, 94% der Patientinnen die Operation ihrer besten Freundin empfehlen. Nach 10 Jahren wurden jedoch bei 11% eine zweite Endometriumablation und bei 22% eine Hysterektomie durchgeführt (8). Bei Frauen mit Blutungsstörungen in Kombination mit Dysmenorrhöen ist auch an die Adenomyosis zu denken. Weitere Hinweise bietet der Ultraschall mit echogenen Knötchen oder strahlförmigen Verdichtungen, die vom Endometrium in das Myometrium ziehen. Bei dieser Konstellation kann die hormonelle Therapie eine Beschwerdereduktion bringen. Mit der Endometriumresektion/-ablation sollte man hingegen zurückhaltend sein, denn verständlicherweise ist hier die Versagerquote gross.
Endometriumresektion/-ablation
Die Endometriumresektion respektive -ablation wird optimalerweise postmenstruell durchgeführt. Eine vorgängige Suppression mit GnRH-Analoga oder Gestagenen ist nach unserer Meinung nicht nötig. Unter dem Postablationssyndrom versteht man eine postoperative Hämatometra. Bei der klassischen Endometriumresektion liegt das Risiko bei 2,4%, während es bei den neueren Ablationssystemen bei
GYNÄKOLOGIE 3/2013
21
SCHWERPUNKT
Abbildung 4: Plazentarpolyp
Abbildung 5: Endometriumablation
0,9% liegt (9). Nach Tubensterilisation ist das Risiko auf bis zu 10% erhöht (10), weil das Blut nicht mehr retrograd abfliessen kann. Die Diagnose des Postresektionssyndroms wird mittels Klinik und Ultraschalls (Hämatometra/Hämatosalpinx) gestellt. Auch wenn eine hysteroskopische, organerhaltende Therapie durch Öffnen der Hämatometra möglich ist, bietet die Hysterektomie in dieser Situation die grösste therapeutische Sicherheit. Weil nach Endometriumresektion/-ablation in 70% Endometriuminseln bestehen bleiben, ist eine spätere Hormonersatztherapie mit Östrogenen allein obsolet.
Zur Endometriumresektion/-ablation der ersten Generation zählen Instrumente, die unter hysteroskopischer Sicht angewendet werden. Unter die zweite Generation fallen Einwegsysteme, die meist blind eingeführt werden.
Instrumente der ersten Generation Hierunter fallen Rollerball oder Schlittenelektrode (Abbildung 5), Resektionsschlinge (Abbildung 6, 7), Hochfrequenzablation und der YAG-Laser. Allgemein gebräuchlich sind Rollerball oder Schlittenelektrode und Resektionsschlinge. Die grösste Perforationsgefahr besteht im Fundus- und Tubenbereich. Deshalb wird häufig die Resektion mittels Schlinge an Vorder-, Seiten- und Hinterwand durchgeführt, während der Rollerball zur Ablation im Fundus und den Tubenecken benutzt wird. An der gelben homogenen Farbe erkennt man, dass das gesamte Endometrium destruiert wurde. Es ist darauf zu achten, den zervikalen Bereich auszulassen, weil sonst die Gefahr einer Hämatometra steigt.
Instrumente der zweiten Generation Hierunter fallen das bipolare Hochfrequenznetz (NovaSure®), Uterinballonmethoden (Thermachoice®, Cavaterm® und Thermablate EAS®), Kryotherapie (Her Option®) sowie Mikrowellen-Endometrium-Ablation. Eine Sonderstellung nimmt das Hydro-Therm Ablation®-System ein, bei dem unter hysteroskopi-
scher Sicht frei zirkulierendes heisses Wasser angewandt wird. Die Studien zeigen keine wesentlichen Vorund Nachteile der einzelnen Methoden (11). Entscheidend ist es, sich mit den Systemen auszukennen und diese unter standardisierten Verhältnissen anzuwenden. In der Schweiz scheint das Cavaterm®-System am verbreitetsten zu sein. Bei dieser Methode zirkuliert heisses Wasser in einem Uterinballon. Vorgängig muss ein Ultraschall durchgeführt werden: Uterusanomalien inklusive Septen sind auszuschliessen, die Gebärmutterwanddicke sollte mindestens 12 mm betragen, das Cavum zwischen 4 und 10 cm liegen und die Zervix kleiner als 6 cm sein. Eine in den Studien vernachlässigte Komplikation ist das versehentliche Verbrennen des Darms. Diese Komplikation wurde in den Studien bisher nicht aufgenommen, ist aber grossen Komplikationsregistern der USA immer wieder gemeldet worden (12) und trat nach unserem Wissen auch schon mehrfach in der Schweiz auf. Um das Risiko einer versehentlichen Darmverbrennung zu minimieren, halten wir folgende Punkte für wichtig: präoperative sonografische Ausmessung des Myometriums, ausreichende Dilatation der Zervix mit anschliessender sicherer intrauteriner Einlage des Cavaterm-Katheters.
Vergleich der Instrumente der ersten und zweiten Generation Die Reduktion der Blutungsstörung und die Patientinnenzufriedenheit als Bewertungskriterien zeigen keinen signifikanten Unterschied zwischen den Instrumenten der ersten und der zweiten Generation. Die Amenorrhö nach einem Jahr liegt bei 40% und die Patientinnenzufriedenheit bei 90%. Zweitgenerationssysteme sind aber einfacher zu bedienen, und die Operation ist schneller durchgeführt (15 Minuten Zeitersparnis). Zweitgenerationssysteme können auch in Lokalanästhesie angewendet werden. TUR-Syndrom, Perforation und Hämatometra sind häufiger mit Erstgenerationssystemen. Übelkeit, Erbrechen und Unterbauchschmerzen kommen insbesondere bei den Ballonsystemen der zweiten Generation vor (9).
22 GYNÄKOLOGIE 3/2013
SCHWERPUNKT
Abbildung 6: Endometriumresektion
Abbildung 7: Komplett reseziertes Endometrium im Corpus uteri
Vergleich der Therapie mit Levonorgestrel IUD und der Endometriumresektion/-ablation
Nach einem Jahr zeigt die Endometriumresektion/ -ablation im Vergleich zur Behandlung mit der Levonorgestrel IUD (Mirena®) eine signifikante Reduktion der Blutung. Zufriedenheit und Lebensqualität sind jedoch in beiden Gruppen gleich. Entsprechend dem Nebenwirkungsprofil leiden Patientinnen unter Mirena® häufiger unter Zwischenblutungen und Brustschmerzen (13). Zur Gewährleistung der Antikonzeption wird nicht selten die Endometriumresektion/-ablation mit dem Levonorgestrel IUD kombiniert. Eine retrospektive Studie zeigt in diesem Kollektiv eine Patientinnenzufriedenheit von 96% (14).
Hysterektomie
Nach Endometriumresektion/-ablation wird innerhalb von 5 Jahren bei 22% der Patientinnen wegen Blutungsstörungen eine Hysterektomie durchgeführt (8, 15). Nachteile der Hysterektomie gegenüber der Endometriumresektion/-ablation sind die längere Operationszeit, die längere Erholungszeit und die höhere Anzahl an postoperativen Komplikationen. Dafür garantiert die Hysterektomie langfristige Blutungsfreiheit. Auch ist die Patientinnenzufriedenheit
GYNÄKOLOGIE 3/2013
23
SCHWERPUNKT
2 Jahre postoperativ nach Hysterektomie signifikant grösser, diese Signifikanz ist jedoch nach 4 Jahren nicht mehr nachweisbar. Die initialen Kosten der Hysterektomie sind zwar grösser, bei der langfristigen Kostenberechung muss jedoch das relativ hohe Risiko einer zweiten Operation berücksichtigt werden (16). Nach Hysterektomie tritt im Durchschnitt die Menopause 1,9 bis 3,7 Jahre früher ein. Die gleichen Studien zeigen auch, dass nach zusätzlicher einseitiger Ovarektomie die Menopause 4,4 Jahre früher eintritt, als wenn man beide Ovarien belässt (17, 18). Immer wieder diskutiert wird der Einfluss der Hysterektomie auf die Sexualität, die Inkontinenz und den Beckenboden. Nach wie vor ist die Studienlage diesbezüglich kontrovers (19–21).
Für Frauen, die eine sichere permanente Blutungsfreiheit wünschen und bereit sind, die etwas erhöhten Risiken in Kauf zu nehmen, bietet die Hysterektomie eine gute Alternative. Entscheidend ist die richtige Operationstechnik.
Technik der Hysterektomie Ein Vergleich von laparoskopischer mit abdominaler Hysterektomie zeigt, dass die laparoskopische Hysterektomie weniger Blutverlust sowie eine kürzere Hospitalisation aufweist und eine schnellere Rückkehr zur normalen Tätigkeit ermöglicht, allerdings mit längerer Operationszeit und mehr urogenitalen Verletzungen einhergeht. Wird die laparoskopische Hysterektomie mit der vaginalen Hysterektomie verglichen, zeigt sich, dass bei der vaginalen Hysterektomie die Operationszeit kürzer ist und weniger urogenitale Verletzungen auftreten (22). Vorteil der laparoskopischen und abdominalen Hysterektomie ist die Möglichkeit, gleichzeitig intraabdominale Pathologien zu beurteilen. Daraus lässt sich die Schlussfolgerung ziehen, dass, wenn durchführbar und keine weiteren intrabdominalen Pathologien zu erwarten sind, der vaginale Zugang zu bevorzugen ist. Weil der abdominale Zugang am invasivsten und kosmetisch ungünstigsten ist, kann der laparoskopische Zugang helfen, den abdominalen zu vermeiden. Die immer wieder erwähnte erhöhte Quote von urogenitalen Verletzungen bei der laparoskopischen Hysterektomie führen wir auf eine inadäquate Operationstechnik zurück. Hohl und Kollegen konnten nachweisen, dass bei einer standardisierten Operationstechnik mit konsequentem Einsatz eines Uterusmanipulators mit Portiokappe, welcher die Harnleiter wegschiebt, urogenitale Verletzungen nicht vermehrt auftreten (23). Es stellt sich die Frage, ob bei der Hysterektomie eine elektive Adnexektomie durchgeführt werden sollte: Würden alle Frauen, die älter als 40 Jahre sind, bei einer Hysterektomie gleichzeitig elektiv adnexektomiert, könnte das Ovarialkarzinom um 5,2%
Merkpunkte
■ Organische Ursachen wie Polypen und submuköse Myome können oft mittels operativer Hysteroskopie therapiert werden.
■ Bei dysfunktionellen Blutungen steht die hormonelle Therapie an erster Stelle, ist diese frustran oder nicht gewünscht, kann die Endometriumablation als Alternative angeboten werden.
■ Die Hysterektomie sollte nicht nur als Ultima Ratio gesehen werden; stimmt die individuelle Indikation, bietet sie eine hohe und langfristige Patientinnenzufriedenheit.
gesenkt werden. Des Weiteren ist es möglich, dass sich bei Belassen der Ovarien im weiteren Leben der Patientin operationsbedürftige Befunde zeigen, sodass in 0,3 bis 13% eine Reoperation an den Ovarien stattfindet (24). Diesen Überlegungen steht der Verlust der endokrinen Ovarialfunktion entgegen (25). Auch bei postmenopausalen Patientinnen haben die Ovarien im Rahmen der Androgenbildung eine endokrine Bedeutung (26). Diese Androgenbildung hat eine immer wieder diskutierte Bedeutung für die Sexualität (27). Die elektive Adnexektomie sehen wir deshalb erst ab dem 60. Lebensjahr indiziert. Vorher muss individuell entschieden werden: Familiäres Risiko (z.B. BRCA-Mutation?), vermutete Schwierigkeiten bei einer erneuten Operation (z.B. Verwachsungen?) sowie der Wunsch der Patientin. Ähnliche Überlegungen gelten für die elektive Salpingektomie. Damit kann dem Tubenkarzinom und wahrscheinlich teilweise dem Ovarialkarzinom vorgebeugt werden, und auch eine Reoperation wegen Saktosalpinx wird verhindert. Nachteil der Salpingektomie ist, dass möglicherweise die Durchblutung des Ovars vermindert wird, was potenziell zu einer verfrühten Menopause führt. Bei dem Vergleich der suprazervikalen versus totale Hysterektomie zeigen sich nicht nur gleiche Resultate bezüglich Sexualität und Lebensqualität der Frauen, sondern auch gleiche Ergebnisse bezüglich Inkontinenzquote und Senkungsproblematik sowie gleiche Resultate bezüglich Schmerzen und Hospitalisationszeit. Bei der suprazervikalen Hysterektomie ist die Operationszeit verkürzt (in dem Kollektiv war ein grosser Laparotomieanteil), der Blutverlust verringert, und es trat seltener Fieber auf. Als nachteilig haben sich – in 7 bis 20% – auftretende zyklische Blutungen gezeigt. In 2 bis 5% musste sekundär die Zervix entfernt werden (28). Nach unserer Meinung ist der einzige Vorteil der suprazervikalen Hysterektomie die bessere Verankerungsmöglichkeit einer allfälligen Sakrozervikopexie bei Vaginalstumpfdeszensus.
24 GYNÄKOLOGIE 3/2013
SCHWERPUNKT
Zusammenfassung
Eine individuelle Therapie bei uterinen Blutungs-
störungen setzt voraus:
■ Systematik bei Anamnese und Diagnostik
■ Angebot der verschiedenen Therapieoptionen
■ Wissen um die Erfolgschancen, Risiken und Ne-
benwirkungen der Therapieoptionen
■ das einfühlsame, aufklärende Gespräch.
■
Dr. med. Bernhard Fellmann-Fischer Universitätsfrauenklinik Inselspital Bern 3010 Bern E-Mail: Bernhard.Fellmann-Fischer@insel.ch
Quellen:
1. Shapley M, Jordan K, Croft PR. : An epidemiological survey of symptoms of menstrual loss in the community. Br J Gen Prac 2004; 54: 359.
2. ACOG Practice Bulletin No81: Endometrial Ablation. Obstet Gynecol 2007; 109: 1233.
3. Buttram VC Jr, Reiter RC: Uterine leiomyomata: etiology, symptomatology, and management. Fertil Steril. 1981; 36(4): 433.
4. Polena V, Mergui JL, Perrot N, et al.: Long-term results of hysteroscopic myomectomy in 235 patients. EUR J Obstet Gynecol Reprod Biol 2007; 130: 232.
5. Varma R, Soneja H, Clark TJ, Gupta JK.: Hysteroscopic myomectomy for menorrhagia using Versascope bipolar system: efficacy and prognostic factors at a minimum of one year follow up. Eur J Obstet Gynecol Reprod Biol. 2009 Feb; 142(2): 154–59.
6. Gupta J K et al.: Uterine artery embolisation for symptomatic uterine fibroids, Cochrane database 2012.
7. Lee SC, Kaunitz AM, Sanchez-Ramos L, Rhatigan RM.: The oncogenic potential of endometrial polyps: a systematic review and meta-analysis. Obstet Gynecol. 2010; 116(5): 1197.
8. Fürst SN, Philipsen T, Joergensen JC.: Ten-year follow-up of endometrial ablation. Acta Obstet Gynecol Scand. 2007; 86(3): 334–38.
9. Lethaby A, Hickey M, Garry R, Pennix J.: Endometrial resection/ablation techniques for heavy menstrual bleeding. Cochrane Database 2009: CD001501.
10. McCausland AM, McCausland VM.: Frequency of symptomatic cornual hematometra and postablation tubal sterilization syndrome after total rollerball endometrial ablation: a 10-year follow-up. Am J Obstet Gynecol. 2002; 186(6): 1274.
11. Zarek S, Sharp H.: Global Endometrium Ablation Devices. Clin Obstet Gynecol. 2008 Mar; 51(1): 167–75.
12. Gurtcheff SE, Sharp HT.: Complications associated with global endometrial ablation: the utility of the MAUDE database. Obstet Gynecol. 2003 Dec; 102(6): 1278–82.
13. Lethaby AE, Cooke I, Rees M.: Progesterone or progestogen-releasing intrauterine systems for heavy menstrual bleeding. Cochrane Database Syst Rev. 2005 Oct 19; (4): CD002126.
14. Vaughan D, Byrne PJ.: An evaluation of the simultaneous use of the levonorgestrel-releasing intrauterine device (LNG-IUS, Mirena®) combined with endometrial ablation in the management of menorrhagia. Obstet Gynaecol. 2012 May; 32(4): 372–74.
15. Longinotti MK, Jacobson GF, Hung YY, Learman LA.: Probability of hysterectomy after endometrial ablation. Obstet Gynecol. 2008 Dec; 112(6): 1214–20.
16. Lethaby A, Shepperd S, Farquhar C, Cooke I.: Endometrial resection and ablation versus hysterectomy for heavy menstrual bleeding. Cochrane Database 2009.
17. Farquhar CM, Sadler L, Harvey SA, Stewart AW.: The association of hysterectomy and menopause: a prospective cohort study. Brit J Obst Gyn 2005; 112(7): 956–62.
18. Moorman PG, Myers ER, et al.: Effect of hysterectomy with ovarian preservation on ovarian function. Obstet Gynecol. 2011; 118(6): 1271.
19. Rhodes JC, Kjerulff KH, et al.: Hysterectomy and sexual functioning. JAMA. 1999; 282(20): 1934.
20. Altman D, Granath F, Cnattingius S, Falconer C.: Hysterectomy and risk of stress-urinary-incontinence surgery: nationwide cohort study. Lancet. 2007; 370(9597): 1494–99.
21. Altman D, Falconer C, Cnattingius S, Granath F.: Pelvic organ prolapse surgery following hysterectomy on benign indications. Am J Obstet Gynecol. 2008; 198(5): 572.
22. Nieboer TE et al.: Surgical approach to hysterectomy for benign, gynaecological disease (Review). The Cochrane Library 2009; Issue 2.
23. Hohl M.: Hysterektomie Update. Frauenheilkunde aktuell 2008; 3, 4–20.
24. Morse AN, et al.: The risk of hydrosalpinx formation and adnexectomy following tubal ligation and subsequent hysterectomy: a historical cohort study. Am J Obstet Gynecol. 2006; 194(5): 1273–76.
25. Lethaby A et al.: Total versus subtotal hysterectomy for benign gynaecological conditions (Review). The Cochrane Library 2009; Issue 2.
26. Adel A et al.: Perimenopausal androgen decline after ooporectomy does not influence sexuality or psychological well-being, Fertility and Sterility 2005; 83(4), 1021–28.
27. Pauls RN et al.: Impact of gynecological surgery on female sexual function. Int. Urogynaecol. Int. J. Impot. Res. 2010; 10: 105–14.
28. Lethaby A et al.: Total versus subtotal hysterectomy for benign gynaecological conditions (Review). The Cochrane Library 2009; Issue 2.
GYNÄKOLOGIE 3/2013
25