Transkript
SCHWERPUNKT
Sexuell übertragbare Virusinfektionen
Herpes genitalis, Condylomata acuminata, HIV-Infektion, Hepatitis C und B
Zu den sexuell übertragbaren Geschlechtskrankheiten (sexually transmitted diseases; STD) zählen mehr als 20 Infektionskrankheiten, welche durch Viren, Bakterien, Pilze und auch Parasiten während des Geschlechtsverkehrs übertragen werden. Krankheitsverlauf, Ansteckungsfähigkeit sowie Therapie und Prävention sind jeweils sehr unterschiedlich. Im Folgenden werden die vier häufigsten viral verursachten STD beschrieben.
SABINE BRUCKERT, SEVERIN LÄUCHLI
Herpes simplex genitalis
Der Herpes genitalis ist eine weitverbreitete Virusinfektion, die mit dem Herpes labialis («Fieberbläschen» an den Lippen) nahe verwandt ist. Herpes simplex genitalis kann durch HSV 1 oder 2 verursacht werden. Häufiger sind jedoch Infektionen mit HSV 2, die mit schwereren Manifestationen und häufigeren Rezidiven verbunden sind. Bei Frauen kommt es meist zu schmerzhaften vaginalen und vulvären Hautveränderungen. Bei Männern sind Eichel, Vorhaut und Penisschaft betroffen. Klinisch imponiert die Infektion 3 bis 7 Tage nach Ansteckung in kleinen, oft stark juckenden, zum Teil auch schmerzhaften kleinen Bläschen mit klarer Flüssigkeit auf gerötetem Grund. Die klare Flüssigkeit der Bläschen enthält einen hohen Gehalt an Herpesviren und ist somit hoch ansteckend. Ausserdem können Lymphknotenschwellungen und fieberhafte Allgemeinerscheinungen auftreten. Häufig werden auch atypische klinische Manifestationen beobachtet, beispielsweise lokalisierte Erytheme oder Erosionen im Genitalbereich. Unbehandelt nehmen Häufigkeit und Schwere der genitalen Episoden mit der Zeit ab, bei etwa einem Drittel der Patienten geschieht dies jedoch nicht. Das Virus kann direkt in der Bläschenflüssigkeit oder indirekt im Blut nachgewiesen werden. Die Ansteckung erfolgt meistens durch Kontakt mit Bläschen. Zu beachten ist, dass sehr häufig auch in der asymptomatischen Phase ein «Virusshedding» und somit Infektionen stattfinden können: Etwa 70% der Infektionen finden während der asymptomatischen Phase statt.
Therapieoptionen Therapeutisch werden routinemässig Aciclovir (Zovirax® und Generika), Valaciclovir (Valtrex® und Generika) und Famciclovir (Famvir®) eingesetzt (Tabelle 1). Aciclovir ist am besten studiert, muss aber aufgrund der Halbwertszeit stets in mehreren täglichen Gaben verabreicht werden, weshalb es nur noch in Ausnahmesituationen (z.B. bei besonders ausgeprägtem Verlauf) eingesetzt wird. Dabei ist zu beachten, dass die Medikamente innerhalb von 72 Stunden nach Ausbruch der Infektion verabreicht werden sollten. Die Therapie verkürzt die Krankheitsdauer, hemmt die Virenverbreitung und lindert die Symptome. Die Wirkung von topischem Aciclovir als Creme zur Behandlung von primärem oder rezidivierendem genitalem Herpes simplex variiert in Studien und besteht bestenfalls in einer minimalen Verkürzung der Krankheitsdauer. Die Experten der Centers for Disease Control and Prevention (CDC) raten deshalb davon ab. Eine suppressive Langzeittherapie ist meist nicht nötig. Zu diskutieren ist diese bei mehr als 12 Episoden von Herpesrezidiven pro Jahr oder wenn der Krankheitsausbruch mit/bei einem Erythema exsudativum multiforme verbunden ist (Tabelle 2).
Condylomata acuminata
Condylomata acuminata (auch «spitze Kondylome» oder «Feigwarzen» genannt) sind die häufigsten benignen Tumoren des äusseren Genitoanalbereiches. Sie werden durch humane Papillomaviren (HPV) ausgelöst. In der mehr als 90 verschiedene Genotypen umfassenden Familie der humanen Papillomaviren können über 50 Typen zu Infektionen im Genitoanal-
GYNÄKOLOGIE 4/2012
23
SCHWERPUNKT
Tabelle 1:
Primäre Herpes-simplex-genitalis-Episode: Therapie
Virostatikum Aciclovir
Valaciclovir Famciclovir
Dosierung 400 mg, dreimal täglich, 7 bis 10 Tage 200 mg, fünfmal täglich, 7 bis 10 Tage 1 g, zweimal täglich, 7 bis 10 Tage 250 mg, dreimal täglich, 5 bis 10 Tage
Evidenzlevel V I I I
Tabelle 2:
Rezidivierte Herpes-simplex-genitalis-Episode: Therapie
Virostatikum Aciclovir
Valaciclovir Famciclovir
Dosierung 200 mg, fünfmal täglich, 5 bis 10 Tage 400 mg, dreimal täglich, 5 Tage 400 mg, dreimal täglich, 5 bis 10 Tage 800 mg, zweimal täglich, 5 Tage 800 mg, dreimal täglich, 2 Tage 500 mg, zweimal täglich, 3 Tage 1 g, zweimal täglich, 5 bis 10 Tage 1 g, einmal täglich, 5 Tage 125 mg, zweimal täglich, 5 Tage 500 mg, zweimal täglich, 5 bis 10 Tage (HIV-positive Patienten) 1 g, zweimal 1 Tag
Evidenzlevel I V V II II I II I I II I
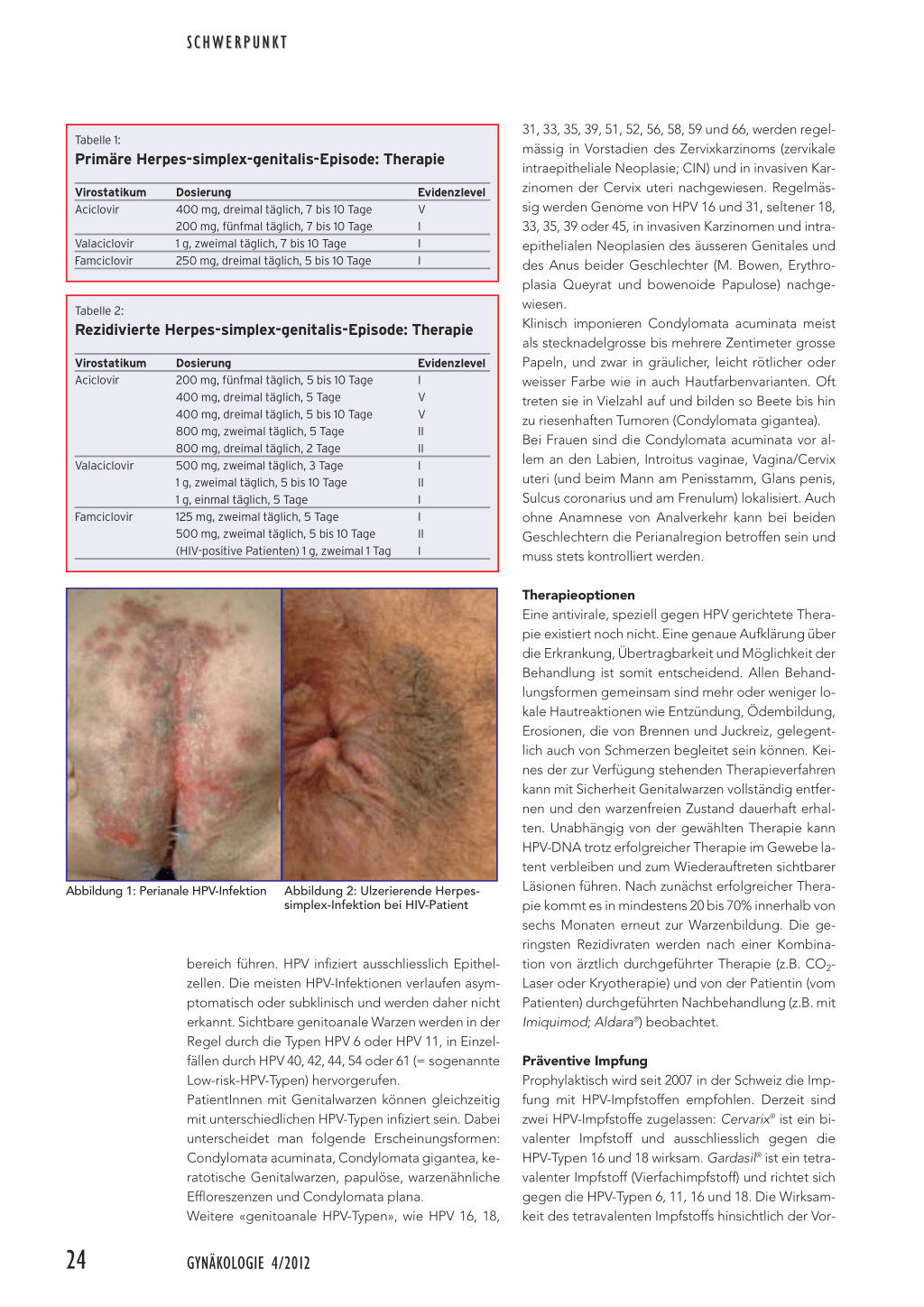
31, 33, 35, 39, 51, 52, 56, 58, 59 und 66, werden regelmässig in Vorstadien des Zervixkarzinoms (zervikale intraepitheliale Neoplasie; CIN) und in invasiven Karzinomen der Cervix uteri nachgewiesen. Regelmässig werden Genome von HPV 16 und 31, seltener 18, 33, 35, 39 oder 45, in invasiven Karzinomen und intraepithelialen Neoplasien des äusseren Genitales und des Anus beider Geschlechter (M. Bowen, Erythroplasia Queyrat und bowenoide Papulose) nachgewiesen. Klinisch imponieren Condylomata acuminata meist als stecknadelgrosse bis mehrere Zentimeter grosse Papeln, und zwar in gräulicher, leicht rötlicher oder weisser Farbe wie in auch Hautfarbenvarianten. Oft treten sie in Vielzahl auf und bilden so Beete bis hin zu riesenhaften Tumoren (Condylomata gigantea). Bei Frauen sind die Condylomata acuminata vor allem an den Labien, Introitus vaginae, Vagina/Cervix uteri (und beim Mann am Penisstamm, Glans penis, Sulcus coronarius und am Frenulum) lokalisiert. Auch ohne Anamnese von Analverkehr kann bei beiden Geschlechtern die Perianalregion betroffen sein und muss stets kontrolliert werden.
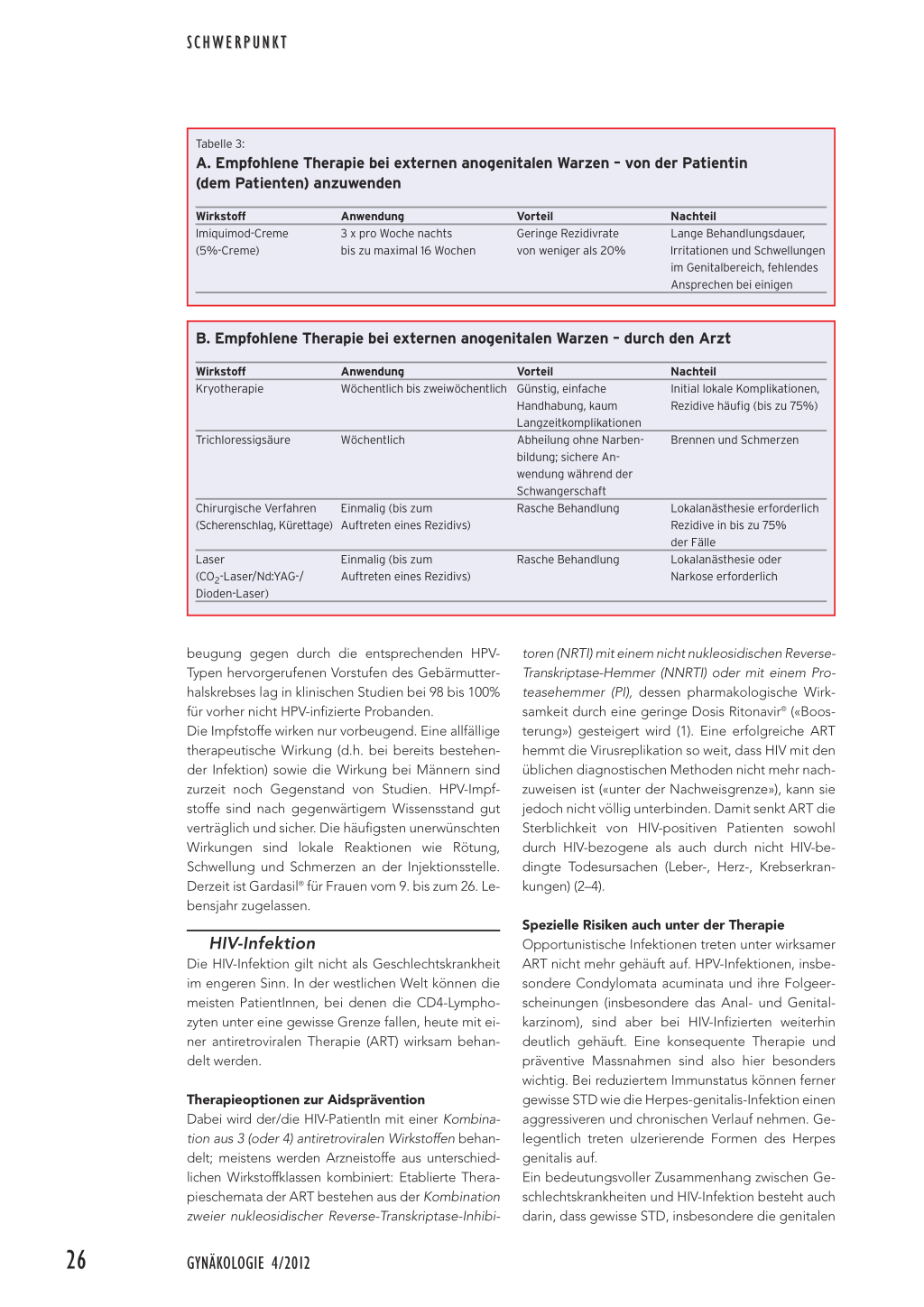
Abbildung 1: Perianale HPV-Infektion Abbildung 2: Ulzerierende Herpessimplex-Infektion bei HIV-Patient
bereich führen. HPV infiziert ausschliesslich Epithelzellen. Die meisten HPV-Infektionen verlaufen asymptomatisch oder subklinisch und werden daher nicht erkannt. Sichtbare genitoanale Warzen werden in der Regel durch die Typen HPV 6 oder HPV 11, in Einzelfällen durch HPV 40, 42, 44, 54 oder 61 (= sogenannte Low-risk-HPV-Typen) hervorgerufen. PatientInnen mit Genitalwarzen können gleichzeitig mit unterschiedlichen HPV-Typen infiziert sein. Dabei unterscheidet man folgende Erscheinungsformen: Condylomata acuminata, Condylomata gigantea, keratotische Genitalwarzen, papulöse, warzenähnliche Effloreszenzen und Condylomata plana. Weitere «genitoanale HPV-Typen», wie HPV 16, 18,
Therapieoptionen Eine antivirale, speziell gegen HPV gerichtete Therapie existiert noch nicht. Eine genaue Aufklärung über die Erkrankung, Übertragbarkeit und Möglichkeit der Behandlung ist somit entscheidend. Allen Behandlungsformen gemeinsam sind mehr oder weniger lokale Hautreaktionen wie Entzündung, Ödembildung, Erosionen, die von Brennen und Juckreiz, gelegentlich auch von Schmerzen begleitet sein können. Keines der zur Verfügung stehenden Therapieverfahren kann mit Sicherheit Genitalwarzen vollständig entfernen und den warzenfreien Zustand dauerhaft erhalten. Unabhängig von der gewählten Therapie kann HPV-DNA trotz erfolgreicher Therapie im Gewebe latent verbleiben und zum Wiederauftreten sichtbarer Läsionen führen. Nach zunächst erfolgreicher Therapie kommt es in mindestens 20 bis 70% innerhalb von sechs Monaten erneut zur Warzenbildung. Die geringsten Rezidivraten werden nach einer Kombination von ärztlich durchgeführter Therapie (z.B. CO2Laser oder Kryotherapie) und von der Patientin (vom Patienten) durchgeführten Nachbehandlung (z.B. mit Imiquimod; Aldara®) beobachtet.
Präventive Impfung Prophylaktisch wird seit 2007 in der Schweiz die Impfung mit HPV-Impfstoffen empfohlen. Derzeit sind zwei HPV-Impfstoffe zugelassen: Cervarix® ist ein bivalenter Impfstoff und ausschliesslich gegen die HPV-Typen 16 und 18 wirksam. Gardasil® ist ein tetravalenter Impfstoff (Vierfachimpfstoff) und richtet sich gegen die HPV-Typen 6, 11, 16 und 18. Die Wirksamkeit des tetravalenten Impfstoffs hinsichtlich der Vor-
24 GYNÄKOLOGIE 4/2012
SCHWERPUNKT
Tabelle 3:
A. Empfohlene Therapie bei externen anogenitalen Warzen – von der Patientin (dem Patienten) anzuwenden
Wirkstoff Imiquimod-Creme (5%-Creme)
Anwendung 3 x pro Woche nachts bis zu maximal 16 Wochen
Vorteil Geringe Rezidivrate von weniger als 20%
Nachteil Lange Behandlungsdauer, Irritationen und Schwellungen im Genitalbereich, fehlendes Ansprechen bei einigen
B. Empfohlene Therapie bei externen anogenitalen Warzen – durch den Arzt
Wirkstoff
Anwendung
Vorteil
Kryotherapie
Wöchentlich bis zweiwöchentlich Günstig, einfache
Handhabung, kaum
Langzeitkomplikationen
Trichloressigsäure
Wöchentlich
Abheilung ohne Narben-
bildung; sichere An-
wendung während der
Schwangerschaft
Chirurgische Verfahren Einmalig (bis zum
Rasche Behandlung
(Scherenschlag, Kürettage) Auftreten eines Rezidivs)
Laser
(CO2-Laser/Nd:YAG-/ Dioden-Laser)
Einmalig (bis zum Auftreten eines Rezidivs)
Rasche Behandlung
Nachteil Initial lokale Komplikationen, Rezidive häufig (bis zu 75%)
Brennen und Schmerzen
Lokalanästhesie erforderlich Rezidive in bis zu 75% der Fälle Lokalanästhesie oder Narkose erforderlich
beugung gegen durch die entsprechenden HPVTypen hervorgerufenen Vorstufen des Gebärmutterhalskrebses lag in klinischen Studien bei 98 bis 100% für vorher nicht HPV-infizierte Probanden. Die Impfstoffe wirken nur vorbeugend. Eine allfällige therapeutische Wirkung (d.h. bei bereits bestehender Infektion) sowie die Wirkung bei Männern sind zurzeit noch Gegenstand von Studien. HPV-Impfstoffe sind nach gegenwärtigem Wissensstand gut verträglich und sicher. Die häufigsten unerwünschten Wirkungen sind lokale Reaktionen wie Rötung, Schwellung und Schmerzen an der Injektionsstelle. Derzeit ist Gardasil® für Frauen vom 9. bis zum 26. Lebensjahr zugelassen.
HIV-Infektion
Die HIV-Infektion gilt nicht als Geschlechtskrankheit im engeren Sinn. In der westlichen Welt können die meisten PatientInnen, bei denen die CD4-Lymphozyten unter eine gewisse Grenze fallen, heute mit einer antiretroviralen Therapie (ART) wirksam behandelt werden.
Therapieoptionen zur Aidsprävention Dabei wird der/die HIV-PatientIn mit einer Kombination aus 3 (oder 4) antiretroviralen Wirkstoffen behandelt; meistens werden Arzneistoffe aus unterschiedlichen Wirkstoffklassen kombiniert: Etablierte Therapieschemata der ART bestehen aus der Kombination zweier nukleosidischer Reverse-Transkriptase-Inhibi-
toren (NRTI) mit einem nicht nukleosidischen ReverseTranskriptase-Hemmer (NNRTI) oder mit einem Proteasehemmer (PI), dessen pharmakologische Wirksamkeit durch eine geringe Dosis Ritonavir® («Boosterung») gesteigert wird (1). Eine erfolgreiche ART hemmt die Virusreplikation so weit, dass HIV mit den üblichen diagnostischen Methoden nicht mehr nachzuweisen ist («unter der Nachweisgrenze»), kann sie jedoch nicht völlig unterbinden. Damit senkt ART die Sterblichkeit von HIV-positiven Patienten sowohl durch HIV-bezogene als auch durch nicht HIV-bedingte Todesursachen (Leber-, Herz-, Krebserkrankungen) (2–4).
Spezielle Risiken auch unter der Therapie Opportunistische Infektionen treten unter wirksamer ART nicht mehr gehäuft auf. HPV-Infektionen, insbesondere Condylomata acuminata und ihre Folgeerscheinungen (insbesondere das Anal- und Genitalkarzinom), sind aber bei HIV-Infizierten weiterhin deutlich gehäuft. Eine konsequente Therapie und präventive Massnahmen sind also hier besonders wichtig. Bei reduziertem Immunstatus können ferner gewisse STD wie die Herpes-genitalis-Infektion einen aggressiveren und chronischen Verlauf nehmen. Gelegentlich treten ulzerierende Formen des Herpes genitalis auf. Ein bedeutungsvoller Zusammenhang zwischen Geschlechtskrankheiten und HIV-Infektion besteht auch darin, dass gewisse STD, insbesondere die genitalen
26 GYNÄKOLOGIE 4/2012
SCHWERPUNKT
Ulzera, durch eine Schädigung der Barrierefunktion der Haut die Übertragung des HI-Virus erleichtern. Der Prävention und Behandlung von STD kommt also auch im Rahmen der HIV-Prävention eine grosse Bedeutung zu.
Hepatitis B und C
Von den Hepatitisviren sind vor allem das Hepatitisvirus B und das Hepatitisvirus C sexuell übertragbar. Schutzimpfungen existieren zur Hepatitis-A- und Hepatitis-B-Prävention, jedoch nicht gegen Hepatitis C. Die Diagnose erfolgt durch Nachweis virusspezifischer Antikörper gegen Struktur- und Nichtstrukturproteine mittels Enzymimmunoassays und Immunoblots sowie durch Nachweis von Teilen des Virusgenoms mittels Polymerase-Kettenreaktion (RT-PCR). Liegt ein sicherer positiver Antikörpertest und ein im Abstand von mindestens drei Monaten mehrfach negativer PCR-Nachweis vor, so kann von einer vorangegangenen und nun ausgeheilten Infektion ausgegangen werden.
Symptome und Krankheitsverläufe Der Krankheitsverlauf der verschiedenen Hepatitisvirusinfektionen ist jeweils sehr unterschiedlich.
Hepatitis C So sind bei der Hepatitis-C-Infektion die Erstmanifestationen ähnlich einer Grippesymptomatik, es zeigen sich also Müdigkeit, Abgeschlagenheit, Appetitlosigkeit, Gelenkschmerzen; im weiteren Verlauf wird auch ein Druck- oder Spannungsgefühl im rechten Oberbauch beschrieben. In einigen Fällen kommt es zum Ikterus. In mehr als 70% der Fälle entwickelt sich eine chronische Hepatitis C. Aufgrund der hohen Virusvariabilität und der (wahrscheinlich) spezifischen Unterdrückung einer ausreichenden T-Zell-Antwort kommt es zu einer ständigen Vermehrung des Virus und damit zu dieser chronischen Infektion. Bei unbehandelter Erkrankung entwickelt sich bei etwa einem Viertel der Infizierten eine Leberzirrhose, was im weiteren Verlauf ein erhöhtes Risiko für ein Leberzellkarzinom bedeuten kann.
HBsAg und dem Auftauchen von anti-HBs (Serokon-
version) gilt die Ansteckungsgefahr als überwunden.
Jedoch kann es auch – in seltenen Fällen – zu einem
schweren Verlauf mit Enzephalopathie kommen. Hier
wird eine Therapie mit einem Nukleosidanalogon
(z.B. Lamivudin) empfohlen. Im schwersten Fall
kommt es bei zirka 1% der symptomatischen Verläufe
zum lebensbedrohlichen Verlauf (in Stunden bis we-
nigen Tagen), der sogenannten fulminanten Hepati-
tis. In diesem Fall gelten das rasche Verschwinden
des HBsAg und eine Schrumpfung der Leber als
ungünstige Zeichen; eine medikamentöse Therapie
und intensivmedizinische Betreuung mit der Mög-
lichkeit einer Lebertransplantation sind geboten. Die
Verabreichung von Interferon ist bei jeder Form der
akuten Hepatitis B kontraindiziert.
Die chronische Hepatitis B kommt in 5 bis 10% der
Fälle vor und ist definiert durch die Persistenz der
entsprechenden viralen Marker. Bei zirka 25% der In-
fizierten ist ein progredienter Krankheitsverlauf zu
beobachten – im Verlauf mit Leberzirrhose und/oder
Leberzellkarzinom.
■
Dr. med. Sabine Bruckert (Korrespondenzadresse) Klinik für Dermatologie UniversitätsSpital Zürich 8091 Zürich E-Mail: sabine.bruckert@usz.ch
Dr. med. Severin Läuchli Klinik für Dermatologie UniversitätsSpital Zürich 8091 Zürich
Quellen:
1. Choo QL et al.: Isolation of a cDNA clone derived from a blood-borne non-A, non-B viral hepatitis genome. Science 1989; 244(4902): 359–62. PMID: 2523562
2. Fujioka S, et al.: Prevalence of hepatitis B and C virus markers in outpatients of Mongolian general hospitals. Kansenshogaku Zasshi 1998; 72: 5–11.
3. Seger G.: Drogen und Hepatitis C: Neue Konzepte der Prävention gesucht. Dtsch Arztebl 2004; 101 (27): A 1929.
4. Armstrong GL et al.: The prevalence of hepatitis C virus infection in the United States. 1999 through 2002. Ann Intern Med. 2006; 144(10): 705–14.
Hepatitis B Bei der Hepatitis-B-Infektion ist ebenfalls eine akute Erkrankung von einer chronischen zu unterscheiden. So verlaufen zirka zwei Drittel der akuten Hepatitis-BInfektionskrankheiten asymptomatisch. Bei einem Viertel der Betroffenen treten dagegen klassische Hepatitiszeichen wie Ikterus, dunkler Urin, Gliederschmerzen sowie gastrointestinale Symptome auf. Oft wird somit eine akute Hepatitis-B-Infektion zufällig entdeckt. In der Regel heilt eine unkomplizierte akute Hepatitis B nach 2 bis 6 Wochen klinisch aus, der Nachweis von Antikörpern gegen das HBsAg (anti-HBs) zeigt dies an. Mit dem Verschwinden des
GYNÄKOLOGIE 4/2012
27