Transkript
Schweizerische Arbeitsgemeinschaft für Kinder- und Jugendgynäkologie (GYNEA) Groupement Suisse de Gynécologie de l’enfant et de l’adolescente (GYNEA)
Nouvelle pratique vaccinale de l’enfant et de l’adolescente
La vaccination contre l’hépatite B et les infections des HPV
Après celui de l’hépatite B, le vaccin contre les HPV (Human Papilloma Virus) est le deuxième disponible contre le cancer. Dorénavant on peut éviter ces maladies sexuellement transmissibles, et leur possible dégénération cancéreurse. Ainsi la vaccination contre ces deux maladies s’adresse principalement aux préadolescents (11 à 16 ans) avant le début de leur activité sexuelle. Si le vaccin contre l’hépatite B est recommandé aux filles et aux garçons, la vaccination contre les HPV s’adresse uniquement aux filles, puisque c’est chez les femmes que le fardeau de la maladie est bien documenté.
ALESSANDRO DIANA
Naturellement, la vaccination contre ces maladies ne va aucunement éluder l’indication de l’utilisation du préservatif ni du dépistage des lésions précancéreuses du col de l’utérus. Ces vaccins préviennent l’infection (vaccins préventifs) mais ne guérissent pas les lésions cancéreuses engendrées par l’infection.
Hépatite B
En Suisse, 0,3% de la population générale et jusqu’à 0,5% des femmes enceintes (1 sur 20) testées présente un AgHBs positif (1). On estime à 2000 les personnes présentant une infection chronique due au virus de l’hépatite B. La persistance de l’antigène HBs (AgHBs) de plus de six mois définit l’état de «maladie chronique» (2).
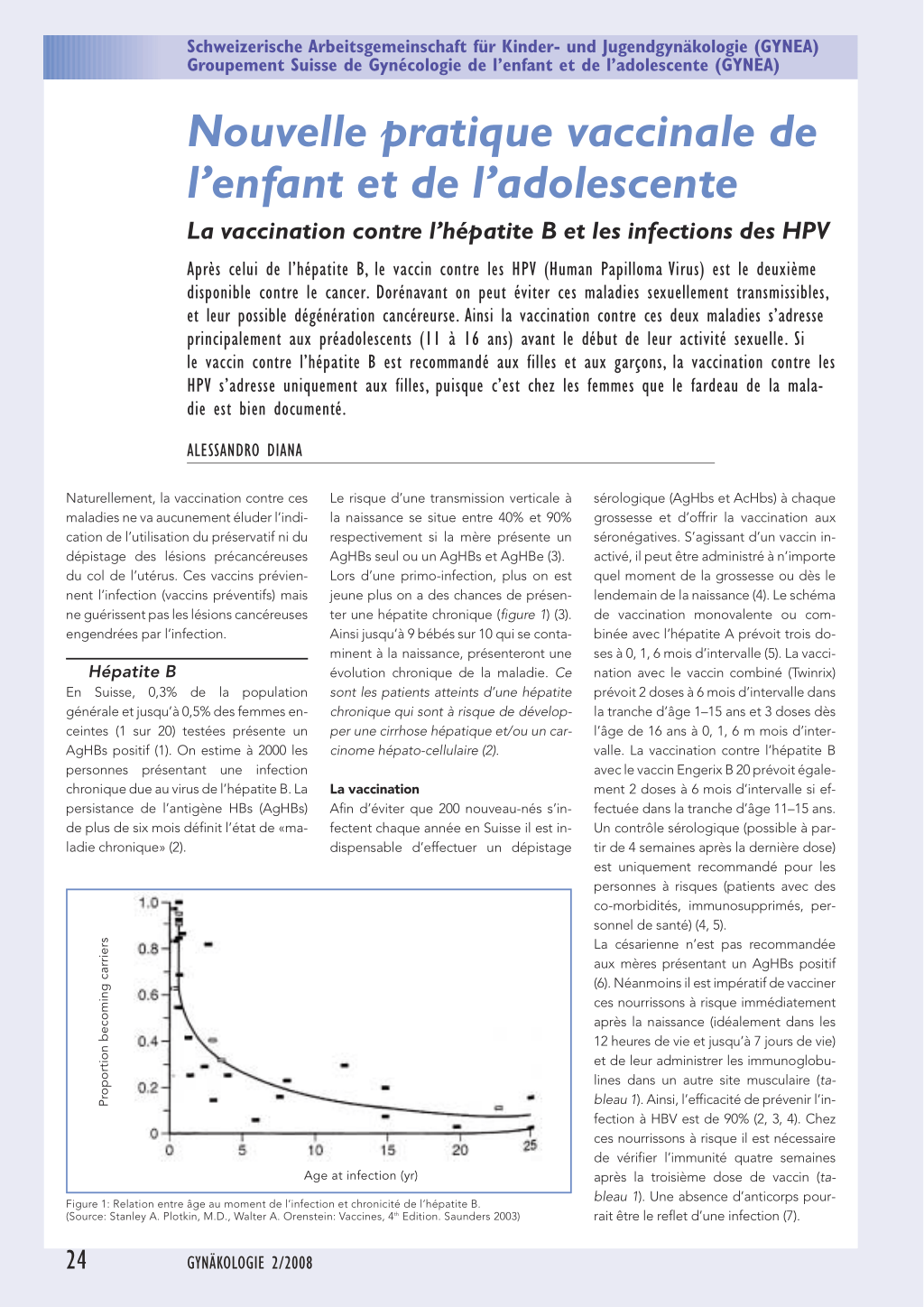
Le risque d’une transmission verticale à la naissance se situe entre 40% et 90% respectivement si la mère présente un AgHBs seul ou un AgHBs et AgHBe (3). Lors d’une primo-infection, plus on est jeune plus on a des chances de présenter une hépatite chronique (figure 1) (3). Ainsi jusqu’à 9 bébés sur 10 qui se contaminent à la naissance, présenteront une évolution chronique de la maladie. Ce sont les patients atteints d’une hépatite chronique qui sont à risque de développer une cirrhose hépatique et/ou un carcinome hépato-cellulaire (2).
La vaccination Afin d’éviter que 200 nouveau-nés s’infectent chaque année en Suisse il est indispensable d’effectuer un dépistage
Proportion becoming carriers
Age at infection (yr)
Figure 1: Relation entre âge au moment de l’infection et chronicité de l’hépatite B. (Source: Stanley A. Plotkin, M.D., Walter A. Orenstein: Vaccines, 4th Edition. Saunders 2003)
sérologique (AgHbs et AcHbs) à chaque grossesse et d’offrir la vaccination aux séronégatives. S’agissant d’un vaccin inactivé, il peut être administré à n’importe quel moment de la grossesse ou dès le lendemain de la naissance (4). Le schéma de vaccination monovalente ou combinée avec l’hépatite A prévoit trois doses à 0, 1, 6 mois d’intervalle (5). La vaccination avec le vaccin combiné (Twinrix) prévoit 2 doses à 6 mois d’intervalle dans la tranche d’âge 1–15 ans et 3 doses dès l’âge de 16 ans à 0, 1, 6 m mois d’intervalle. La vaccination contre l’hépatite B avec le vaccin Engerix B 20 prévoit également 2 doses à 6 mois d’intervalle si effectuée dans la tranche d’âge 11–15 ans. Un contrôle sérologique (possible à partir de 4 semaines après la dernière dose) est uniquement recommandé pour les personnes à risques (patients avec des co-morbidités, immunosupprimés, personnel de santé) (4, 5). La césarienne n’est pas recommandée aux mères présentant un AgHBs positif (6). Néanmoins il est impératif de vacciner ces nourrissons à risque immédiatement après la naissance (idéalement dans les 12 heures de vie et jusqu’à 7 jours de vie) et de leur administrer les immunoglobulines dans un autre site musculaire (tableau 1). Ainsi, l’efficacité de prévenir l’infection à HBV est de 90% (2, 3, 4). Chez ces nourrissons à risque il est nécessaire de vérifier l’immunité quatre semaines après la troisième dose de vaccin (tableau 1). Une absence d’anticorps pourrait être le reflet d’une infection (7).
24 GYNÄKOLOGIE 2/2008
Schweizerische Arbeitsgemeinschaft für Kinder- und Jugendgynäkologie (GYNEA) Groupement Suisse de Gynécologie de l’enfant et de l’adolescente (GYNEA)
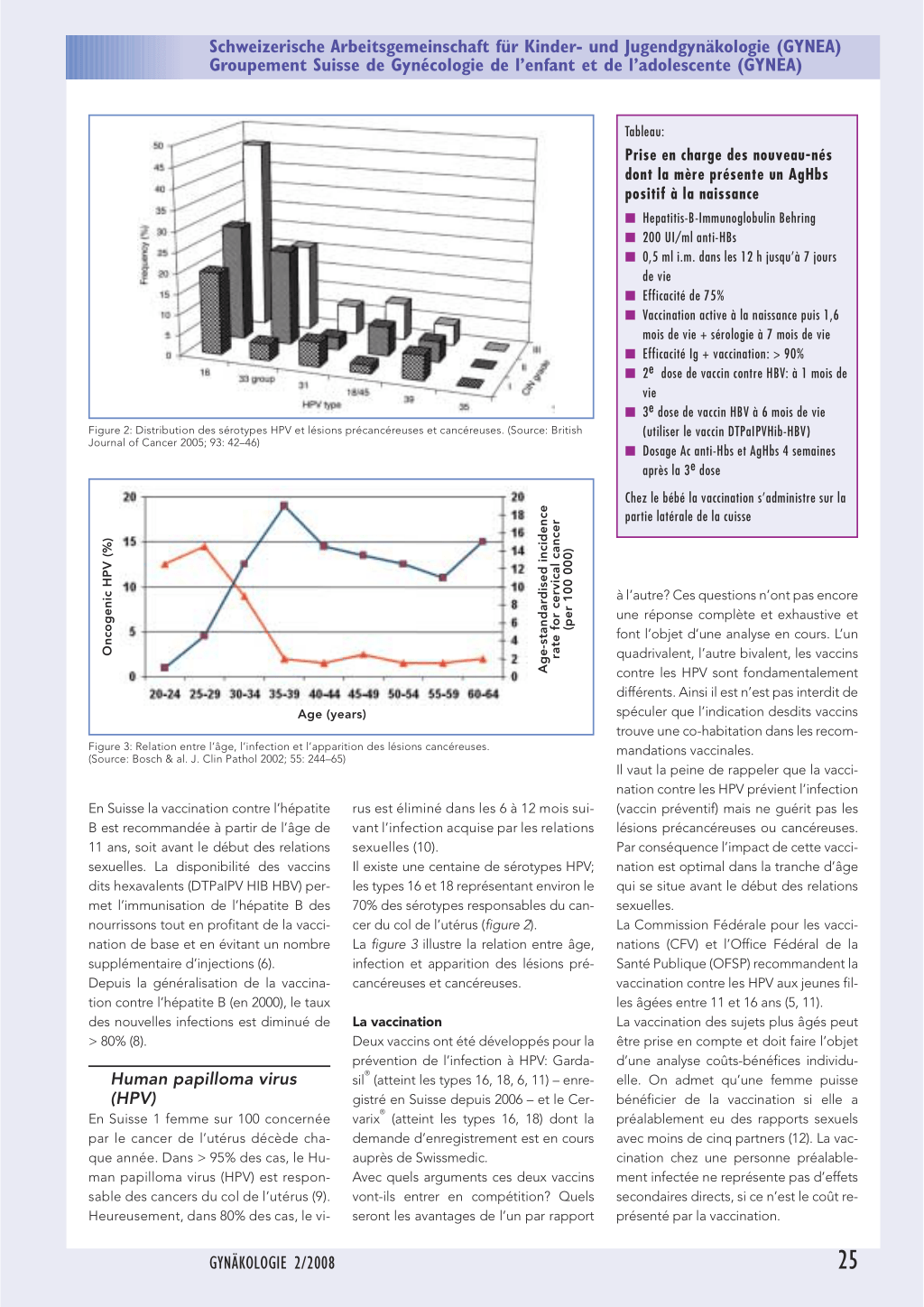
Figure 2: Distribution des sérotypes HPV et lésions précancéreuses et cancéreuses. (Source: British Journal of Cancer 2005; 93: 42–46)
Tableau:
Prise en charge des nouveau-nés dont la mère présente un AgHbs positif à la naissance
■ Hepatitis-B-Immunoglobulin Behring ■ 200 UI/ml anti-HBs ■ 0,5 ml i.m. dans les 12 h jusqu’à 7 jours
de vie ■ Efficacité de 75% ■ Vaccination active à la naissance puis 1,6
mois de vie + sérologie à 7 mois de vie ■ Efficacité Ig + vaccination: > 90% ■ 2e dose de vaccin contre HBV: à 1 mois de
vie ■ 3e dose de vaccin HBV à 6 mois de vie
(utiliser le vaccin DTPaIPVHib-HBV) ■ Dosage Ac anti-Hbs et AgHbs 4 semaines
après la 3e dose
Chez le bébé la vaccination s’administre sur la partie latérale de la cuisse
Oncogenic HPV (%) Age-standardised incidence
rate for cervical cancer (per 100 000)
Age (years)
Figure 3: Relation entre l’âge, l’infection et l’apparition des lésions cancéreuses. (Source: Bosch & al. J. Clin Pathol 2002; 55: 244–65)
En Suisse la vaccination contre l’hépatite B est recommandée à partir de l’âge de 11 ans, soit avant le début des relations sexuelles. La disponibilité des vaccins dits hexavalents (DTPaIPV HIB HBV) permet l’immunisation de l’hépatite B des nourrissons tout en profitant de la vaccination de base et en évitant un nombre supplémentaire d’injections (6). Depuis la généralisation de la vaccination contre l’hépatite B (en 2000), le taux des nouvelles infections est diminué de > 80% (8).
Human papilloma virus (HPV)
En Suisse 1 femme sur 100 concernée par le cancer de l’utérus décède chaque année. Dans > 95% des cas, le Human papilloma virus (HPV) est responsable des cancers du col de l’utérus (9). Heureusement, dans 80% des cas, le vi-
rus est éliminé dans les 6 à 12 mois suivant l’infection acquise par les relations sexuelles (10). Il existe une centaine de sérotypes HPV; les types 16 et 18 représentant environ le 70% des sérotypes responsables du cancer du col de l’utérus (figure 2). La figure 3 illustre la relation entre âge, infection et apparition des lésions précancéreuses et cancéreuses.
La vaccination Deux vaccins ont été développés pour la prévention de l’infection à HPV: Gardasil® (atteint les types 16, 18, 6, 11) – enregistré en Suisse depuis 2006 – et le Cervarix® (atteint les types 16, 18) dont la demande d’enregistrement est en cours auprès de Swissmedic. Avec quels arguments ces deux vaccins vont-ils entrer en compétition? Quels seront les avantages de l’un par rapport
à l’autre? Ces questions n’ont pas encore une réponse complète et exhaustive et font l’objet d’une analyse en cours. L’un quadrivalent, l’autre bivalent, les vaccins contre les HPV sont fondamentalement différents. Ainsi il est n’est pas interdit de spéculer que l’indication desdits vaccins trouve une co-habitation dans les recommandations vaccinales. Il vaut la peine de rappeler que la vaccination contre les HPV prévient l’infection (vaccin préventif) mais ne guérit pas les lésions précancéreuses ou cancéreuses. Par conséquence l’impact de cette vaccination est optimal dans la tranche d’âge qui se situe avant le début des relations sexuelles. La Commission Fédérale pour les vaccinations (CFV) et l’Office Fédéral de la Santé Publique (OFSP) recommandent la vaccination contre les HPV aux jeunes filles âgées entre 11 et 16 ans (5, 11). La vaccination des sujets plus âgés peut être prise en compte et doit faire l’objet d’une analyse coûts-bénéfices individuelle. On admet qu’une femme puisse bénéficier de la vaccination si elle a préalablement eu des rapports sexuels avec moins de cinq partners (12). La vaccination chez une personne préalablement infectée ne représente pas d’effets secondaires directs, si ce n’est le coût représenté par la vaccination.
GYNÄKOLOGIE 2/2008
25
Schweizerische Arbeitsgemeinschaft für Kinder- und Jugendgynäkologie (GYNEA) Groupement Suisse de Gynécologie de l’enfant et de l’adolescente (GYNEA)
La CFV n’a pas édicté de recommanda-
tion pour la vaccination contre les HPV
chez les hommes. L’absence de données
exhaustives sur le fardeau de la maladie
et d’efficacité chez l’homme justifie cette
abstention.
■
Dr méd. Alessandro Diana Médecin-chef Service de Pédiatrie Clinique des Grangettes 7, chemin des grangettes 1224 Chêne-Bougeries et Médecin associé Maladies infectieuses pédiatriques Hôpitaux universitaires de Genève (HUG) 1224 Genève E-Mail: alessandro.diana@hcuge.ch
Bibliographie:
1. Bundesamt für Gesundheit. BAG 1997. Empfehlungen zur Hepatitis-B-Impfung, Supplementum II, Stand Dezember 1997.
2. Steven CE, et al.: Vertical transmission of hepatitis B antigen in Taiwan. N Engl J Med 1975; 292: 771–774.
3. Beasley RP, et al.: Prevention of perinatally transmitted hepatitis B virus infections with hepatitis B immune globulin and hepatitis B vaccine. Lancet 1983; 2: 1099–1102.
4. General Recommendations on Immunization. Recommendations of the Advisory Committee on Immunization Practices (ACIP). MMRW. December 1, 2006/55 (RR15); 1–48.
5. http://www.infovac.ch/index2.php?option= com_docman&task=docget&Itemid=201&id=342
6. Recommandations pour la prévention de la transmission mère-enfant de l’hépatite B. Office Fédéral de la Santé Publique. Commission fédérale pour les vaccinations. Complément aux «Directives et recommandations no 2 : Recommandations pour la vaccination contre l’hépatite» Mai 2007.
7. Tan KL, et al.: Immunogenicity of recombinant yeast-derived hepatitis B vaccine in nonresponders to perinatal immunization. JAMA 1994; 271: 859–61.
8. World Health Organization: Expanded Programme on Immunization – global advisory group. Part I. Wkly Epidemiol Rec 1992; 3: 11–16 World Health Organization. Global progress toward universal childhood hepatitis B vaccination, 2003. Wkly
Epidemiol Rec 2003; 42: 366–70. 9. Bosch et al.: Prevalence of human papillomavirus in cervical cancer: a worldwide perspective. J Natl Cancer Inst. 1995: 87(11): 796–802. 10. Munoz et al.: Epidemiology Classification of Human Papillomavirus Types Associated with Cervical Cancer. NEJM 2003; 348: 518–27. 11. Directives et recommandations de vaccination contre les papillomavirus humains (2007) http:// www.infovac.ch/index2.php?option=com_docman &task=docget&Itemid=161&id=357 12. Myers ER, et al.: Mathematical model for the natural history of human papillomavirus infection and cervical carcinogenesis. Am J Epidemiol 2000; 151(12): 1158–1171.
Pour plus d’information sur ces vaccins et la vaccination en général, le personnel médical et le public peuvent consulter le site d’Infovac: www.infovac.ch