Transkript
KONGRESSTICKER
AAD 2017
Jahrestreffen der American Academy of Dermatology (AAD)
Neue Antikörper und Small Molecules revolutionieren die dermatologische Therapie
Der 75. Kongress der American Academy of Dermatology (AAD) zog 18 800 Teilnehmer aus 111 Ländern in seinen Bann – die vierthöchste Besucherzahl in seiner Geschichte. Besonders beliebt waren wie in jedem Jahr die Late-Breaking Clinical trials: Nur 48 von 180 eingereichten Studien schafften es, hier aufgenommen zu werden. Im Folgenden eine Synopse der interessantesten Studien.
Anteil Patienten in Prozent
Topisches small molecule überzeugt bei leichter Psoriasis
«Es gibt einen bisher nicht erfüllbaren Bedarf für eine lokale Behandlung, die besser wirkt und vertragen wird als die heute bestehenden Optionen für Patienten mit leichter bis moderater Psoriasis. Diese Lücke kann Benvitimod füllen», war die Bilanz von Dr. Jianzhong Zhang aus Peking (China), bei der Vorstellung seiner Studie: Der neue, nichtsteroidale Wirkstoff in Cremezubereitung war bei Patienten mit leichter bis moderater Plaquepsoriasis nicht nur gegenüber Plazebo überlegen, sondern auch der Behandlung mit einer Calcipotriol-Salbe. In der randomisierten, multizentrischen Phase-III-Studie wurde 1-prozentige Benvitimod-Creme sowohl gegenüber Calcipotriol 0,005 Prozent als auch gegenüber Plazebo geprüft. Die Untersuchung bestand in einer Behandlung über 12 Wochen, an die sich eine offene Follow-up-Phase von 48 Wochen anschloss. Alle 686 erwachsenen Teilnehmer litten seit
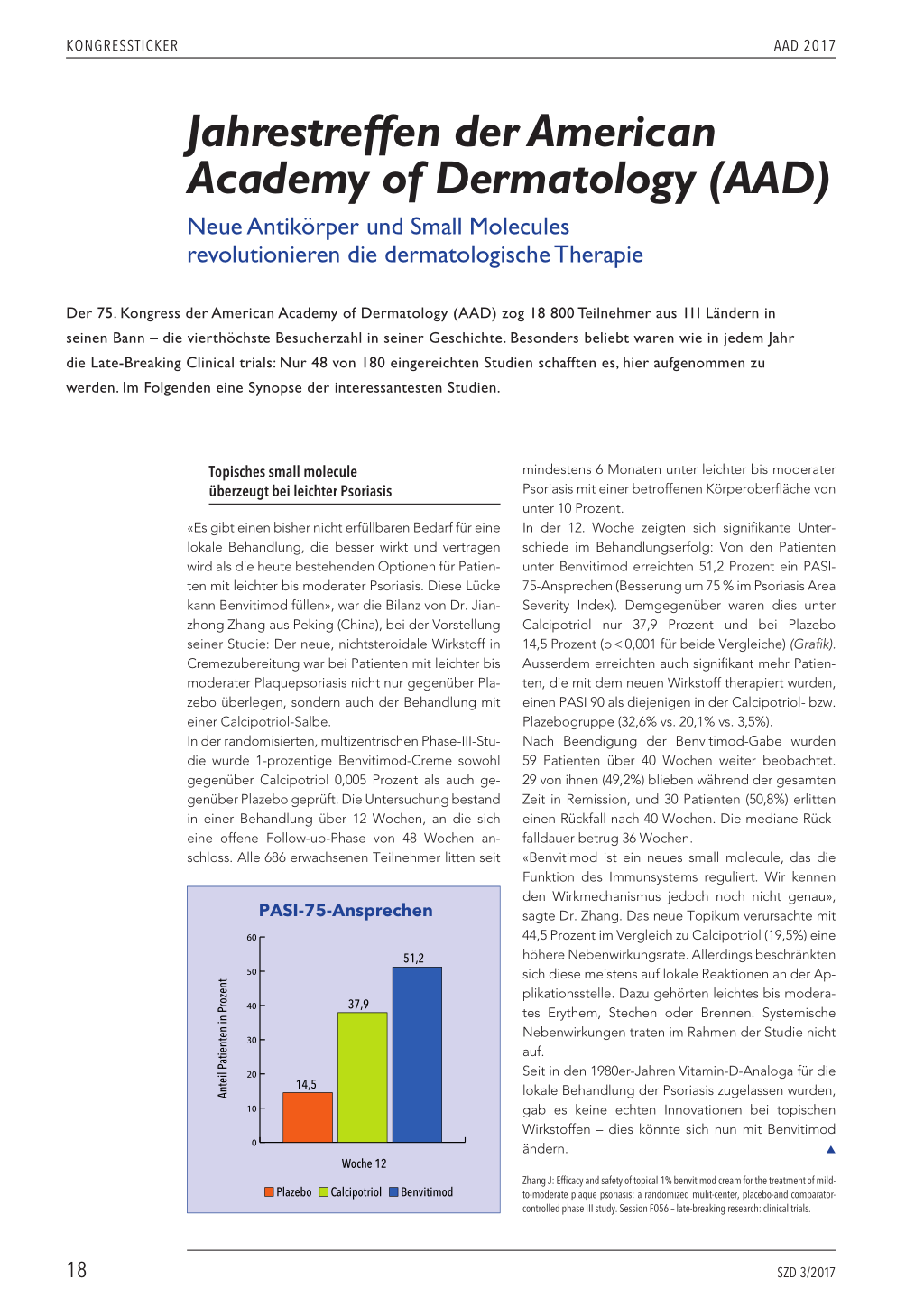
PASI-75-Ansprechen
60
51,2
50
40 37,9
30
20 14,5
10
0
Woche 12
Q Plazebo Q Calcipotriol Q Benvitimod
mindestens 6 Monaten unter leichter bis moderater
Psoriasis mit einer betroffenen Körperoberfläche von
unter 10 Prozent.
In der 12. Woche zeigten sich signifikante Unter-
schiede im Behandlungserfolg: Von den Patienten
unter Benvitimod erreichten 51,2 Prozent ein PASI-
75-Ansprechen (Besserung um 75 % im Psoriasis Area
Severity Index). Demgegenüber waren dies unter
Calcipotriol nur 37,9 Prozent und bei Plazebo
14,5 Prozent (p < 0,001 für beide Vergleiche) (Grafik). Ausserdem erreichten auch signifikant mehr Patien- ten, die mit dem neuen Wirkstoff therapiert wurden, einen PASI 90 als diejenigen in der Calcipotriol- bzw. Plazebogruppe (32,6% vs. 20,1% vs. 3,5%). Nach Beendigung der Benvitimod-Gabe wurden 59 Patienten über 40 Wochen weiter beobachtet. 29 von ihnen (49,2%) blieben während der gesamten Zeit in Remission, und 30 Patienten (50,8%) erlitten einen Rückfall nach 40 Wochen. Die mediane Rück- falldauer betrug 36 Wochen. «Benvitimod ist ein neues small molecule, das die Funktion des Immunsystems reguliert. Wir kennen den Wirkmechanismus jedoch noch nicht genau», sagte Dr. Zhang. Das neue Topikum verursachte mit 44,5 Prozent im Vergleich zu Calcipotriol (19,5%) eine höhere Nebenwirkungsrate. Allerdings beschränkten sich diese meistens auf lokale Reaktionen an der Ap- plikationsstelle. Dazu gehörten leichtes bis modera- tes Erythem, Stechen oder Brennen. Systemische Nebenwirkungen traten im Rahmen der Studie nicht auf. Seit in den 1980er-Jahren Vitamin-D-Analoga für die lokale Behandlung der Psoriasis zugelassen wurden, gab es keine echten Innovationen bei topischen Wirkstoffen – dies könnte sich nun mit Benvitimod ändern. L Zhang J: Efficacy and safety of topical 1% benvitimod cream for the treatment of mildto-moderate plaque psoriasis: a randomized mulit-center, placebo-and comparatorcontrolled phase III study. Session F056 – late-breaking research: clinical trials. 18 SZD 3/2017 KONGRESSTICKER AAD 2017 Zweiter IL-17-Blocker besteht Feuerprobe gegen Ustekinumab «Ob neue Medikamente wirklich besser sind, lässt sich nur in direkten Vergleichsstudien feststellen», sagte Prof. Kristian Reich aus Hamburg (D) bei der Vorstellung der IXORA-S-Studie. Er wies darauf hin, dass der Vergleich mit Ustekinumab, einem Biologikum der zweiten Generation, eine grössere Herausforderung für einen neuen Wirkstoff darstellt als der mit Etanercept. Ixekizumab, nach Secukinumab der zweite IL-17-Blocker, hat diese Bewährungsprobe in der IXORA-S-Studie bestanden. Zur Therapie der moderaten bis schweren Psoriasis war der IL-12/IL-23-Antikörper Ustekinumab nicht nur bezüglich des primären, sondern auch im Hinblick auf diverse sekundäre Endpunkte nach 24 Wochen überlegen. Der primäre Endpunkt der Studie war definiert als Prozentsatz der Patienten, die nach 24 Wochen mit PASI 90 ansprachen, was einer fast symptomfreien Haut gleichzusetzen ist. Dies gelang bei 83 Prozent der Psoriatiker, die mit Ixekizumab behandelt wurden, verglichen mit 59 Prozent unter Ustekinumab (p < 0,001). «Diese Studie sagt eine Menge über die Ansprechmuster aus; bei PASI 75 besteht wenig Unterschied zwischen den Wirkstoffen, aber eine Differenz von mehr als 24 Prozent bei PASI 90 nach so einer kurzen Behandlungszeit ist wirklich relevant», erklärte Reich. Darüber hinaus erreichten 50 Prozent der Patienten im «static Physician’s Global Assessment» (sPGA) eine ekzemfreie Haut. Dies ist laut Reich ein enormer Effekt. In der Studie wurden 136 Psoriatiker einer Therapie mit Ixekizumab zugeordnet. Diese bestand in einer Ausgangsdosis von 160 mg und nachfolgend 80 mg alle 2 Wochen für 12 Wochen sowie anschliessend 80 mg alle 4 Wochen. Die restlichen 166 Patienten wurden mit Ustekinumab (45/90 mg) behandelt. Bei den Nebenwirkungen zeigten sich insgesamt keine signifikanten Unterschiede zwischen den Gruppen. Schwere Nebenwirkungen traten bei fünf (3%) der Teilnehmer in der Ustekinumab-Gruppe und drei (2,2%) der Ixekizumab-Patienten auf (p = 0,735). Ein Ustekinumab- und zwei Ixekizumab-Patienten brachen die Studie wegen Nebenwirkungen ab. Behandlungsassoziierte Nebenwirkungen traten bei 75 Prozent der Patienten mit Ustekinumab auf und 70 Prozent derer, die Ixekizumab bekommen hatten (p = 0,299). Reich kündigte an, dass die IxekizumabPatienten an einer Verlängerungsstudie über 52 Wochen teilnehmen werden. Ixekizumab war auch bezüglich der Lebensqualität überlegen. Gemessen wurde diese mit dem DLQUI (Dermatology Life Quality Index). «In diesem Fragebogen gibt es auch Fragen, die gar nichts mit einem PASI 100 zu tun haben, wie zum Beispiel eine Frage danach, ob die Therapie den Patienten stört», gab Reich an. «Auch im DLQUI konnten wir einen klaren Vorteil für Ixekizumab feststellen», erklärte Reich. Im vorigen Jahr erwies sich der IL-17-Blocker Secuki- numab in der CLEAR-Studie Ustekinumab überle- gen. Im Gegensatz zu der CLEAR-Studie wurden in die IXORA-S-Studie nur Patienten mit einer Zweit- linienindikation eingeschlossen. L Reich K: Efficacy and safety of ixekizumab compared to ustekinumab after 24 weeks of treatment in patients with moderate-to-severe plaque psoriasis: results from IXORA-S, a randomized head-to-head trial. Session F056 – late-breaking research. Secukinumab: Die meisten Patienten erreichen einen erneuten Behandlungserfolg nach einer Therapiepause Psoriasispatienten erreichen die besten Abheilungsraten bei kontinuierlicher Therapie. Allerdings kommt es immer wieder zu Therapiepausen, zum Beispiel aufgrund von Operationen, Infektionen oder Urlaub. Die präsentierten Daten der Verlängerungsphase der ERASURE- und FIXTURE-Studie bestätigen nun: Kommt es während einer Behandlungsunterbrechung zu einem Wiederaufflammen der Psoriasis, so wird bei erneuter Behandlung mit dem Anti-IL-17 Secukinumab (300 mg) bei 94 Prozent der Patienten nach 16 Wochen erneuter Behandlung wieder ein PASI-75Ansprechen erreicht. Im selben Zeitraum wiesen 79 Prozent der vorherigen PASI-90-Responder (n = 117, s. Grafik) wieder ein PASI-90-Ansprechen und 67 Prozent der bis dato PASI- 100-Responder (n = 67) erneut ein PASI 100-Ansprechen auf. Die Daten stammen von 136 Patienten, die in zwei Jahren einen Rückfall erlitten. Die mediane Zeit bis zum Rückfall nach Absetzen von Secukinumab betrug 28 Wochen. Zudem war das Sicherheitsprofil weiterhin günstig und konsistent mit dem der vorherigen Phase-III-Studien. Wiederansprechen nach Therapiepause durchgezogene Linie: PASI 75; gestrichelte Linie: PASI 90 95,8 78,8 Bei erneuter Behandlung erreicht ein Grossteil der PASI-90Responder wieder ein PASI-90-Ansprechen. Grund für diesen grossen Erfolg bei erneuter Be- handlung mit Secukinumab ist vermutlich die auch in Studien dokumentierte sehr geringe Immunogenität von Secukinumab. L Blauvelt A et al.: Secukinumab retreatment shows rapid recapture of treatment response: an analysis of a phase 3 extension trial in psoriasis. Poster Nr. 4879.. SZD 3/2017 19 KONGRESSTICKER AAD 2017 Spezifische IL-23-Blockade wirksamer als Ustekinumab Die NAVIGATE-Studie untersuchte die Wirksamkeit und Verträglichkeit des IL-23-Hemmers Guselkumab bei Patienten, die nach einer 16-wöchigen Behand- lung mit Ustekinumab nicht ausreichend auf diese Behandlung ansprachen (Investigator’s Global Assess- ment (IGA) ≥ 2). Patienten, die auf Guselkumab um- gestellt wurden, wiesen in den Wochen 28 bis 40 im Vergleich zu Patienten, die weiterhin Ustekinumab erhielten, ein signifikant verbessertes Hautbild auf: Sie hatten doppelt so viele Arztbesuche, bei denen sie einen IGA-Score von 0 oder 1 (d.h. eine nahezu ab- geheilte Haut) sowie eine IGA-Verbesserung von mindestens 2 Punkten nach der 16. Woche erreich- ten. (1,5 Arztbesuche bei Therapie mit Guselkumab im Vergleich zu 0,7 mit Ustekinumab; p < 0,001). Guselkumab war nicht nur beim vorgenannten primären Studienendpunkt, sondern auch bei den wichtigsten sekundären Endpunkten im Vergleich zu Ustekinumab überlegen: Ein signifikanter Unter- schied zeigte sich zum Beispiel auch bei der Anzahl der Besuche, bei denen Patienten zwischen Woche 28 und 40 ein PASI-90-Ansprechen beziehungsweise einen IGA-Wert von 0 erreichten, sowie beim Anteil von Patienten, die einen IGA-Wert von 0 oder 1 mit einer Verbesserung in Woche 28 von mindestens 2 Punkten gegenüber Woche 16 erreichten (p ≤ 0,001 für alle Parameter). Die Überlegenheit blieb langfris- tig erhalten: In Woche 52 erreichte ein signifikant höherer Anteil von Patienten in der Guselkumab- Gruppe im Vergleich zu Ustekinumab einen IGA- Wert von 0 oder 1 und eine Verbesserung von min- destens 2 Punkten gegenüber Woche 16 (p ≤ 0,001 für alle Parameter). L Langley RG et al.: Efficacy of switching from ustekinumab to guselkumab in patients with moderate-to-severe plaque psoriasis: results from the NAVIGATE study. Poster Nr. 4915. Jodhaltiges Gel hilft gegen Dellwarzen Povidon-Jod ist ein breit wirksames Biozid, das Mikroorganismen einschliesslich Bakterien, Viren, Hefen, andere Pilze und Protozoen abtötet. Dimethylsulfoxid fungiert als Vehikel, das die perkutane Aufnahme von Povidon-Jod erleichtert. Ein Gel mit der Kombination dieser Inhaltsstoffe zeigte in einer Pilotstudie eine starke Wirksamkeit bei Molluscum contagiosum. 12 Patienten wurden mit dem neuen Gel zweimal täglich für einen Zeitraum von 4 Wochen behandelt. Alle 12 hatten eine entweder vollständige oder teilweise Besserung. Von insgesamt 115 Läsionen, die behandelt wurden, zeigten 103 (90%) nach 8 Wochen eine vollständige Abheilung. Das Gel war relativ gut verträglich, als einzige Nebenwirkung tra- ten leichte Hautirritation und eine Trockenheit auf. «Diese neue Kombination war ausserordentlich er- folgreich, es wurde bislang in der Literatur noch nie über so hohe Abheilungsraten bei Molluscum conta- giosum berichtet», erklärte Dr. Kara Capriotti aus Bryn Mawr (Pennsylvania/USA). Weitere, breiter an- gelegte Studien werden jetzt folgen. L Capriotti K: Molluscum contagiosum treated with dilute povidone-iodine. Session F073 – late-breaking research: procedural dermatology. Dupilumab mit TCS effektiv bei schwerer AD «Atopische Dermatitis ist die neue Psoriasis: Wir ha- ben endlich neue Medikamente, die hervorragende Ergebnisse zeigen», sagte Prof. Andrew Blauvelt aus Portland (Oregon/USA), während seiner Präsentation der CHRONOS-Studie. Die Untersuchung verglich eine Kombination von Dupilumab mit topischen Steroiden (TCS) versus Plazebo und TCS bei mode- rater bis schwerer atopischer Dermatitis (AD). Dabei erreichte die Kombinationstherapie mit Dupi- lumab signifikant bessere Behandlungsergebnisse. Blauvelt und seine Kollegen nahmen 740 Patienten in die Studie auf. 60 Prozent waren männlich, und das mittlere Alter betrug 34 Jahre. Die Studienteilneh- mer wurden drei verschiedenen Gruppen zugeord- net: Therapiert wurde entweder wöchentlich oder zweiwöchentlich mit 300 mg Dupilumab plus TCS, oder Plazebo plus TCS. Primärer Studienendpunkt war ein Scorewert von 0/1 im Investigator‘s Global Assessment, was einer (fast) ekzemfreien Haut ent- spricht und mindestens einer Verbesserung von 2 Punkten im Vergleich zum Ausgangsbefund. Nach 16 Wochen erreichten 39 Prozent beider Dupilumab- Gruppen den primären Endpunkt, im Vergleich zu 12 Prozent der Plazebogruppe (p < 0.0001). Dieses positive Resultat konnten 36 bis 40 Prozent der Dupi- lumab-Patienten über 52 Wochen aufrechterhalten. Das waren deutlich mehr als in der Plazebogruppe (13%, p < 0,0001). Darüber hinaus zeigte sich die Be- handlung mit Dupilumab auch bei einigen sekun- dären Endpunkten, wie zum Beispiel dem EASI (Eczema Area and Severity Index) 75 überlegen. Der Wirkstoff hatte zudem einen positiven Einfluss auf den Pruritus – das Symptom, das AD-Patienten am meisten beeinträchtigt. Schon im vorigen Jahr stellte Dupilumab in den SOLO-Studien seine überlegene Wirkung im Ver- gleich zu Plazebo in der Monotherapie unter Beweis, die den Ausschlag für die im März 2017 erteilte FDA- Zulassung gab. L Blauvelt A: Long-Term Management of Moderate-to-Severe Atopic Dermatitis with Dupilumab up to 1 year With Concomitant Topical Corticosteroids: a Randomized, Placebo-Controlled Phase 3 Trial (CHRONOS). Session F056 – late-breaking research. Maria Schiepeck 20 SZD 3/2017