Transkript
FORTBILDUNG
Hyposensibilisierung bei allergischer Rhinokonjunktivitis
Subkutan oder sublingual – SCIT oder SLIT?
Hyposensibilisierungen sind nicht mehr nur mit
subkutanen Spritzen durchführbar. Die sublin-
guale Immuntherapie hat sich bereits als Alter-
native gut bewährt. Weitere Alternativen werden
derzeit intensiv erforscht. Über neue Möglich-
keiten der Allergenapplikation im Rahmen der
spezifischen Immuntherapie orientierten Exper-
ten an der Tagung DDG KOMPAKT 2012 in
Berlin.
Letztes Jahr konnte das 100-Jahr-Jubiläum der spezifischen Immuntherapie (SIT) gefeiert werden. Den britischen Allergologen Noon und Freeman war es 1911 gelungen, erstmals mit Gräserpollenextrakt eine spezifische Hyposensibilisierung durchzuführen. Als einzige kausale Therapie IgE-vermittelter allergischer Sensibilisierungen ist die SIT für die klinische Praxis von grosser Bedeutung. Neben der subkutanen Immuntherapie (SCIT) konnte sich neuerdings als Alternative auch die sublinguale Immuntherapie (SLIT) etablieren (1). Zurzeit erprobt die Forschung darüber hinaus noch weitere alternative Wege für die Allergenapplikation wie die vestibuläre, die epikutane und die intranodale (intralymphatische) Verabreichung, wie Prof. Dr. Natalija Novak, Klinik für Dermatologie und Allergologie, Universität Bonn, berichtete.
Auf dem Weg zur Lolli-Immuntherapie?
Die orale Allergenapplikation im Bereich der sublingualen Mukosa hat sich als effektiv und gut verträglich erwiesen (2). Die Wahl der sublingualen Region für die Immuntherapie beruht auf der historisch gewachsenen Bevorzugung dieses Mundhöhlenbereichs für die Medikamentenverabreichung in der inneren Medizin. Die geringere Epitheldicke erhöht sublingual die Medikamentenresorption. Neben dem sublingualen Bereich gibt es aber in der Mundhöhle noch andere Regionen, die zur Allergenapplikation genutzt werden könnten. Die Mundhöhle ist ein immunologisch privilegierter Raum, wo Toleranz gegenüber bakteriellen Kommensalen und gegenüber Nahrungsmittelproteinen herrscht. Viele Zellen der Mundhöhlenschleimhaut sind mit antiinflammatorischen Eigenschaften ausgestattet (2). Die protolerogenen Eigenschaften der lokalen antigen-
präsentierenden Zellen (z.B. der dendritischen Zellen) spielen in der Mundschleimhaut eine zentrale Rolle. Bei der Suche nach der für die Immuntherapie am besten geeigneten Mundhöhlenregion ist das Zahlenverhältnis der «guten» Zellen (dendritische Zellen = LangerhansZellen) zu den «bösen» Zellen (Mastzellen) aufschlussreich (Tabelle 1). Bei der Immuntherapie sollen die «guten» Zellen angesprochen werden. Die «bösen» Zellen, welche die Nebenwirkungen der SIT hervorrufen, sollen dagegen möglichst in Ruhe gelassen werden. Es hat sich herausgestellt, dass das Verhältnis «guter» zu «bösen» Zellen in der Sublingualregion viel schlechter ist als in anderen Mundhöhlenregionen, besonders als im Vestibulum oris (hinter der Lippe).
Mukosadicke
Sublingualregion +
Anzahl von Langerhans-Zellen («gute» Zellen) in der Mundschleimhaut
++
Anzahl der Mastzellen
(«böse» Zellen)
+++
Vestibulum oris ++
+++ ++
(nach Prof. Dr. Natalija Novak)
Tabelle 1: Die Schleimhaut des Vestibulums ist besonders gut für die Immuntherapie geeignet, weil sie viele «gute» und nur wenige «böse» Zellen enthält.
Wenn Patienten bei sublingualer Allergenapplikation über sehr starke lokale Nebenwirkungen berichten, empfiehlt Natalija Novak statt der sublingualen die vestibuläre Applikation. Dadurch könne die Nebenwirkungsrate deutlich reduziert werden, sagte sie. Durch Wechsel des Applikationsareals konnte in einer kleinen Pilotstudie die Nebenwirkungsrate mit vestibulärer Verabreichung reduziert und die Effektivität der Immuntherapie erhöht werden, so die Referentin. Damit das Allergen den richtigen Ort erreicht, könnte in Zukunft – besonders bei jungen Patienten – der SIT-Lolli Einzug in die Immuntherapie halten. Entsprechend den unterschiedlichen darin enthaltenen Allergenen könnte der SIT-Lutscher in verschiedenen Farben angeboten werden.
10 [medicos] Nr. 2•2012
Hyposensibilisierung bei allergischer Rhinokonjunktivitis
Weitere Alternativen, die derzeit erforscht werden, sind die epikutane allergenspezifische Immuntherapie (EPIT) mittels Hautpflaster und die intralymphatische Immuntherapie (ILIT). Das Allergen kann unter Ultraschallkontrolle direkt in subkutane Lymphknoten injiziert werden. Die Anzahl benötigter Applikationen und die kumulative Allergendosis können dadurch wesentlich reduziert werden. Bei Gräserpollenallergikern wurde klinisch gezeigt, dass mit ILIT derselbe Effekt erreicht werden kann wie mit SCIT, wie die Referentin sagte.
Verdrängt die SLIT die SCIT?
Es gebe gute Argumente, die SCIT nicht zugunsten der SLIT zu verlassen, sagte Prof. Dr. Randolf Brehler, Klinik für Hautkrankheiten, Universitätsklinikum, Münster. Dass die Wirkung der Immuntherapie dosisabhängig ist, gilt sowohl für die SCIT als auch für die SLIT. Für die SCIT lautet die Empfehlung, während der Erhaltungstherapie etwa 5 bis 20 Mikrogramm des Majorallergens pro Injektion zu verabreichen. Der Referent machte darauf aufmerksam, dass SLIT-Gräserpollenpräparate oftmals unterdosiert seien. In den aktualisierten Cochrane-Metaanalysen erreichten die Effektstärken der SLIT nicht den gleichen Grad der Wirksamkeit wie die der SCIT (Tabelle 2). Klinische Studien belegen die Wirksamkeit der SCIT für viele verschiedene Allergene, während die Wirksamkeit der SLIT nur für Graspollenextrakte ausreichend belegt sei. Ob die Patienten, die ihre SLIT-Tabletten selbst einnehmen können, das Allergen auch wirklich applizieren, ist bei der SLIT nur schwer überprüfbar. Insgesamt vertrat Randolf Brehler die Ansicht, dass noch mehr Studien nötig seien, um für verschiedene Präparate die Gleichwertigkeit der SLIT zu zeigen.
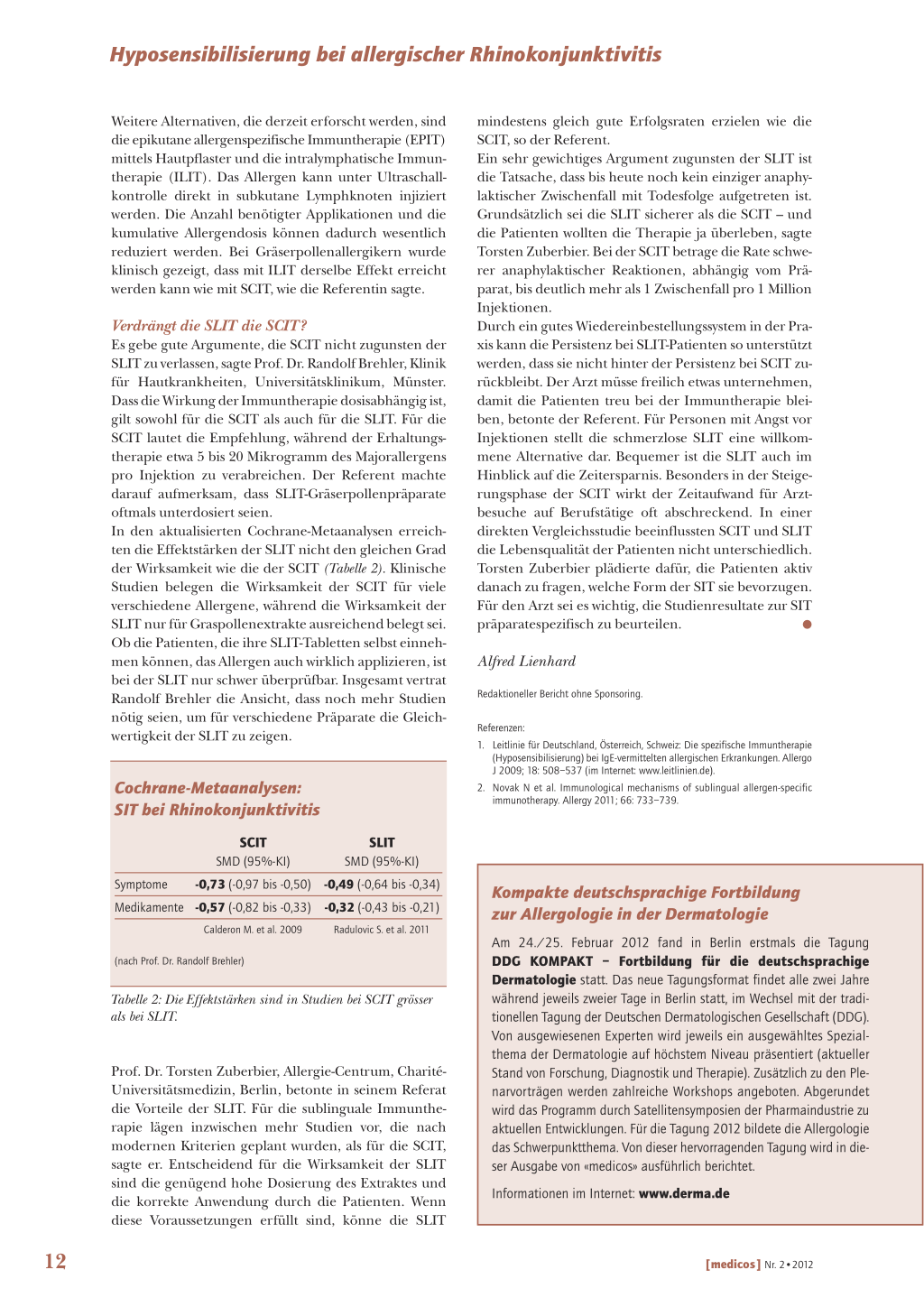
Cochrane-Metaanalysen: SIT bei Rhinokonjunktivitis
SCIT SMD (95%-KI)
SLIT SMD (95%-KI)
Symptome -0,73 (-0,97 bis -0,50) -0,49 (-0,64 bis -0,34)
Medikamente -0,57 (-0,82 bis -0,33) -0,32 (-0,43 bis -0,21)
Calderon M. et al. 2009
Radulovic S. et al. 2011
(nach Prof. Dr. Randolf Brehler)
Tabelle 2: Die Effektstärken sind in Studien bei SCIT grösser als bei SLIT.
Prof. Dr. Torsten Zuberbier, Allergie-Centrum, CharitéUniversitätsmedizin, Berlin, betonte in seinem Referat die Vorteile der SLIT. Für die sublinguale Immuntherapie lägen inzwischen mehr Studien vor, die nach modernen Kriterien geplant wurden, als für die SCIT, sagte er. Entscheidend für die Wirksamkeit der SLIT sind die genügend hohe Dosierung des Extraktes und die korrekte Anwendung durch die Patienten. Wenn diese Voraussetzungen erfüllt sind, könne die SLIT
mindestens gleich gute Erfolgsraten erzielen wie die
SCIT, so der Referent.
Ein sehr gewichtiges Argument zugunsten der SLIT ist
die Tatsache, dass bis heute noch kein einziger anaphy-
laktischer Zwischenfall mit Todesfolge aufgetreten ist.
Grundsätzlich sei die SLIT sicherer als die SCIT – und
die Patienten wollten die Therapie ja überleben, sagte
Torsten Zuberbier. Bei der SCIT betrage die Rate schwe-
rer anaphylaktischer Reaktionen, abhängig vom Prä-
parat, bis deutlich mehr als 1 Zwischenfall pro 1 Million
Injektionen.
Durch ein gutes Wiedereinbestellungssystem in der Pra-
xis kann die Persistenz bei SLIT-Patienten so unterstützt
werden, dass sie nicht hinter der Persistenz bei SCIT zu-
rückbleibt. Der Arzt müsse freilich etwas unternehmen,
damit die Patienten treu bei der Immuntherapie blei-
ben, betonte der Referent. Für Personen mit Angst vor
Injektionen stellt die schmerzlose SLIT eine willkom-
mene Alternative dar. Bequemer ist die SLIT auch im
Hinblick auf die Zeitersparnis. Besonders in der Steige-
rungsphase der SCIT wirkt der Zeitaufwand für Arzt-
besuche auf Berufstätige oft abschreckend. In einer
direkten Vergleichsstudie beeinflussten SCIT und SLIT
die Lebensqualität der Patienten nicht unterschiedlich.
Torsten Zuberbier plädierte dafür, die Patienten aktiv
danach zu fragen, welche Form der SIT sie bevorzugen.
Für den Arzt sei es wichtig, die Studienresultate zur SIT
präparatespezifisch zu beurteilen.
●
Alfred Lienhard
Redaktioneller Bericht ohne Sponsoring.
Referenzen:
1. Leitlinie für Deutschland, Österreich, Schweiz: Die spezifische Immuntherapie (Hyposensibilisierung) bei IgE-vermittelten allergischen Erkrankungen. Allergo J 2009; 18: 508–537 (im Internet: www.leitlinien.de).
2. Novak N et al. Immunological mechanisms of sublingual allergen-specific immunotherapy. Allergy 2011; 66: 733–739.
Kompakte deutschsprachige Fortbildung zur Allergologie in der Dermatologie
Am 24./25. Februar 2012 fand in Berlin erstmals die Tagung DDG KOMPAKT – Fortbildung für die deutschsprachige Dermatologie statt. Das neue Tagungsformat findet alle zwei Jahre während jeweils zweier Tage in Berlin statt, im Wechsel mit der traditionellen Tagung der Deutschen Dermatologischen Gesellschaft (DDG). Von ausgewiesenen Experten wird jeweils ein ausgewähltes Spezialthema der Dermatologie auf höchstem Niveau präsentiert (aktueller Stand von Forschung, Diagnostik und Therapie). Zusätzlich zu den Plenarvorträgen werden zahlreiche Workshops angeboten. Abgerundet wird das Programm durch Satellitensymposien der Pharmaindustrie zu aktuellen Entwicklungen. Für die Tagung 2012 bildete die Allergologie das Schwerpunktthema. Von dieser hervorragenden Tagung wird in dieser Ausgabe von «medicos» ausführlich berichtet.
Informationen im Internet: www.derma.de
12 [medicos] Nr. 2•2012