Transkript
HAUT UND SONNE
Diagnostik des malignen Melanoms
Hautkrebsvorsorge-Sprechstunde der Dermatologischen Klinik des Universitätsspitals Zürich
Von Ralph P. Braun, Isabel Kolm, Reinhard Dummer, Jürg Hafner, Lars French
Das maligne Melanom, auch «schwarzer Hautkrebs» genannt, gehört zu den bösartigen Tumoren und entsteht durch Entartung der melaninbildenden Zellen (Melanozyten). Es stellt bei Weitem nicht die häufigste Hautkrebsart dar, doch steigt die Inzidenz
dieses primär in fast 100 Prozent der Fälle an der Haut lokalisiert und somit einer einfachen klinischen Untersuchung zugänglich ist. Zu den verbreitetsten Untersuchungsmethoden zählen die klinische und die dermoskopische Untersuchung sowie die Ganzkörperübersichtsfotografie. Zudem existieren weitere bildgebende Verfahren, die ebenfalls kurz vorgestellt werden.
seit mehr als zwei Jahrzehnten deutlich schneller an Klinische Untersuchung
als bei anderen Tumoren. Es handelt sich um die
In den Sechziger- und Siebzigerjahren beruhte die klinische Diagnose des Melanoms auf Sym-
ptomen wie Blutung, Juckreiz oder Ulzeration.
bösartigste Form von Hautkrebs, denn das Melanom Zu jener Zeit erfolgte die Diagnose fast ausschliess-
kann Metastasen bilden und ist für über 90 Prozent
lich in sehr fortgeschrittenen Tumorstadien, was die Symptomatik erklärt. Zur Verbesserung der
der durch Hautkrebs verursachten Todesfälle verant-
Diagnosegenauigkeit haben diagnostische Hilfen wie die ABCD-Regel und das Zeichen des «häss-
wortlich. In der Schweiz werden etwa 1800 neue
lichen Entleins» (siehe weiter unten) massgeblich beigetragen. Als Grundregel gilt, dass die klinische
Melanomfälle pro Jahr diagnostiziert.
Untersuchung stets unter guten Beleuchtungsverhältnissen und am entkleideten Patienten er-
folgen sollte. Die Verwendung einer speziellen
Lupenleuchte mit 8- bis 10-facher Vergrösserung ist
Die Frühdiagnose ist beim Melanom besonders hierbei sehr hilfreich, da diese eine starke Ver-
wichtig. Erfolgt sie in einem frühen Stadium grösserung mit einer optimalen Ausleuchtung ver-
(Tumordicke nach Breslow unter 1 mm), liegt die bindet. Bei der klinischen Untersuchung ist es
Zehn-Jahres-Überlebensrate zwischen 90 und 97 Pro- sehr wichtig, systematisch vorzugehen, um nichts
zent. Wird die Diagnose jedoch in einem späteren zu übersehen. Besondere Sorgfalt sollte den Kör-
Stadium gestellt, liegt die Fünf-Jahres-Überlebens- perstellen gewidmet werden, die vom Patienten
rate nur noch bei 10 bis 15 Prozent (1, 2).
nicht selbst überwacht werden können, wie zum
Ein weiterer Grund für den hohen Stellenwert der Beispiel Fusssohlen, Zehenzwischenräume oder 6 Frühdiagnose beim Melanom ist die Tatsache, dass Retroaurikularregionen.
medicos 1/2009
HAUT UND SONNE
Differenzialdiagnose von pigmentierten Läsionen der Haut
Um die Schwierigkeiten in der Diagnostik von pigmentierten Läsionen der Haut besser zu verstehen, ist es wichtig, die verschiedenen Differenzialdiagnosen genau zu kennen. Hierzu zählt die Gruppe der Hauttumoren, zu welchen neben dem malignen Melanom auch die pigmentierten Basalzellkarzinome gehören. Innerhalb der Gruppe der Melanome unterscheidet man folgende Typen: das oberflächlich spreitende Melanom (SSM), das noduläre Melanom (NNM), das Lentigomaligna-Melanom (LMM), das akrolentiginöse Melanom (ALM) sowie das amelanotische Melanom. Unter Letzterem versteht man ein Melanom, welches nicht pigmentiert und daher sehr schwierig zu diagnostizieren ist. Des Weiteren ist die grosse Gruppe der pigmentierten melanozytären Nävi (Compo und Nävus, Junktionsnävus etc.) zu erwähnen sowie eine Gruppe von benignen Läsionen wie zum Beispiel die pigmentierten seborrhoischen Keratosen und vaskuläre Läsionen (Angiome, Angiokeratome). Die reine klinische Untersuchung mit dem blossen Auge hat eine eher geringe Sensitivität und Spezifizität. Für die Praxis bedeutet dies, dass viele gutartige Läsionen fälschlicherweise als Melanom diagnostiziert werden, was zu unnötigen chirurgischen Eingriffen führt. Zudem werden maligne Melanome eventuell nicht rechtzeitig als solche erkannt und die Diagnose erst in späteren Stadien gestellt. Die Diagnose eines Melanoms kann in einigen Fällen sehr schwierig sein, da diese gutartige Läsionen imitieren können. Glücklicherweise tritt dies sehr selten auf. Diese altbekannte Tatsache erklärt, warum es für das Melanom keine 100-prozentige Diagnosegenauigkeit geben kann. Eine Lösung für dieses Dilemma wäre, bei Risikopatienten systematisch alle Muttermale chirurgisch zu entfernen. Da die meisten Risikopatienten jedoch eine grosse Anzahl von Muttermalen aufweisen, wäre dies unrealistisch und in der Praxis für das Gesundheitssystem sehr kostspielig. Man weiss heute aufgrund von Erfahrungen aus den USA, als noch bis in den Achtzigerjahre systematische Nävektomien (Entfernung aller Muttermale) bei Risikopatienten durchgeführt worden sind, dass ein hoher Anteil dieser Patienten trotz chirurgischer Entfernung aller Muttermale im weiteren Verlauf ihres Lebens ein Melanom entwickelten. Dies kann dadurch erklärt werden, dass nur etwa 40 Prozent aller Melanome sich aus vorbestehenden Muttermalen entwickeln und 60 Prozent «de novo» in Haut ohne Male entstehen. Mittlerweile werden keine Nävektomien mehr durchgeführt.
ABCD-Regel
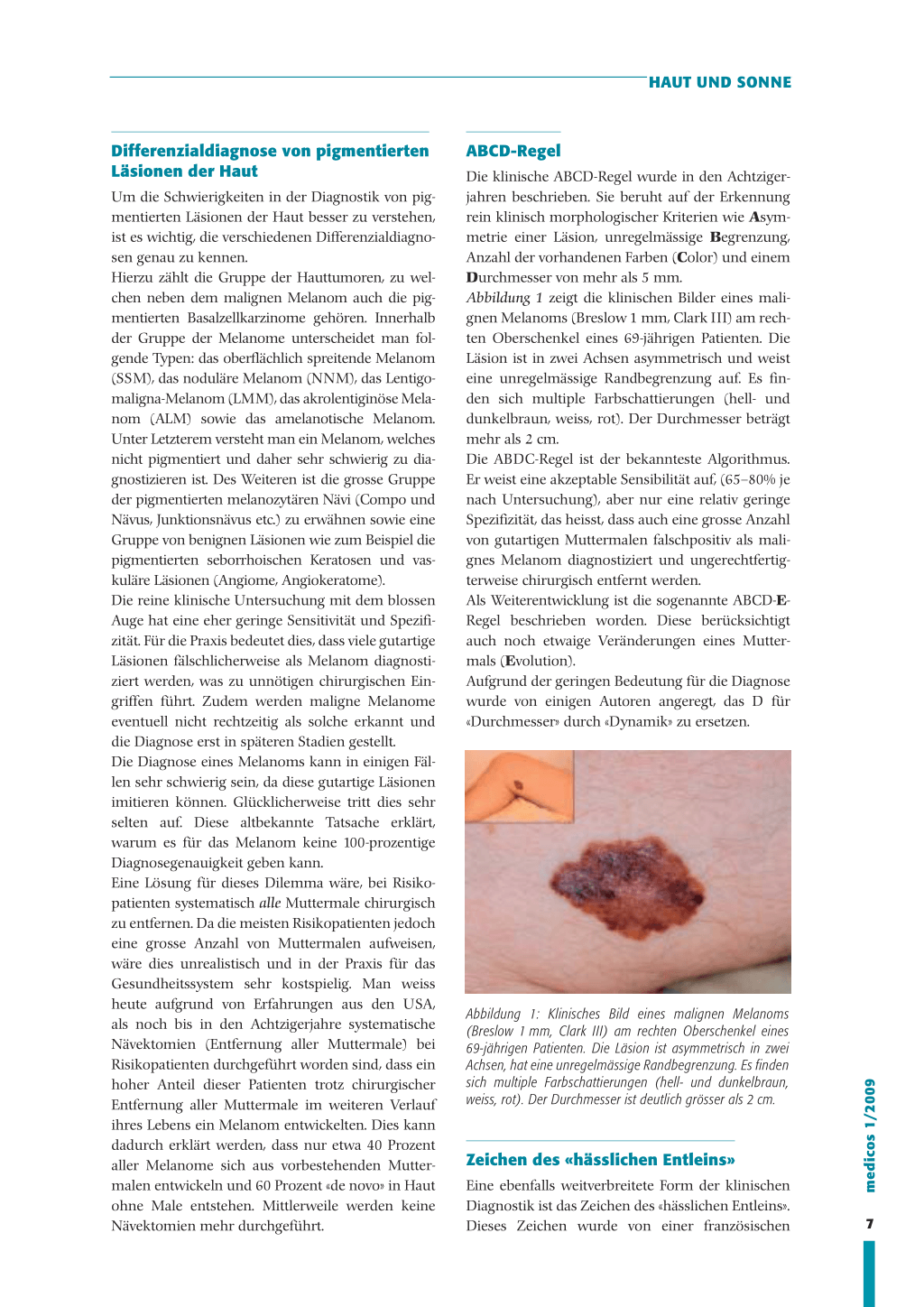
Die klinische ABCD-Regel wurde in den Achtzigerjahren beschrieben. Sie beruht auf der Erkennung rein klinisch morphologischer Kriterien wie Asymmetrie einer Läsion, unregelmässige Begrenzung, Anzahl der vorhandenen Farben (Color) und einem Durchmesser von mehr als 5 mm. Abbildung 1 zeigt die klinischen Bilder eines malignen Melanoms (Breslow 1 mm, Clark III) am rechten Oberschenkel eines 69-jährigen Patienten. Die Läsion ist in zwei Achsen asymmetrisch und weist eine unregelmässige Randbegrenzung auf. Es finden sich multiple Farbschattierungen (hell- und dunkelbraun, weiss, rot). Der Durchmesser beträgt mehr als 2 cm. Die ABDC-Regel ist der bekannteste Algorithmus. Er weist eine akzeptable Sensibilität auf, (65–80% je nach Untersuchung), aber nur eine relativ geringe Spezifizität, das heisst, dass auch eine grosse Anzahl von gutartigen Muttermalen falschpositiv als malignes Melanom diagnostiziert und ungerechtfertigterweise chirurgisch entfernt werden. Als Weiterentwicklung ist die sogenannte ABCD-ERegel beschrieben worden. Diese berücksichtigt auch noch etwaige Veränderungen eines Muttermals (Evolution). Aufgrund der geringen Bedeutung für die Diagnose wurde von einigen Autoren angeregt, das D für «Durchmesser» durch «Dynamik» zu ersetzen.
Abbildung 1: Klinisches Bild eines malignen Melanoms (Breslow 1 mm, Clark III) am rechten Oberschenkel eines 69-jährigen Patienten. Die Läsion ist asymmetrisch in zwei Achsen, hat eine unregelmässige Randbegrenzung. Es finden sich multiple Farbschattierungen (hell- und dunkelbraun, weiss, rot). Der Durchmesser ist deutlich grösser als 2 cm.
Zeichen des «hässlichen Entleins»
Eine ebenfalls weitverbreitete Form der klinischen Diagnostik ist das Zeichen des «hässlichen Entleins». Dieses Zeichen wurde von einer französischen
medicos 1/2009
7
HAUT UND SONNE
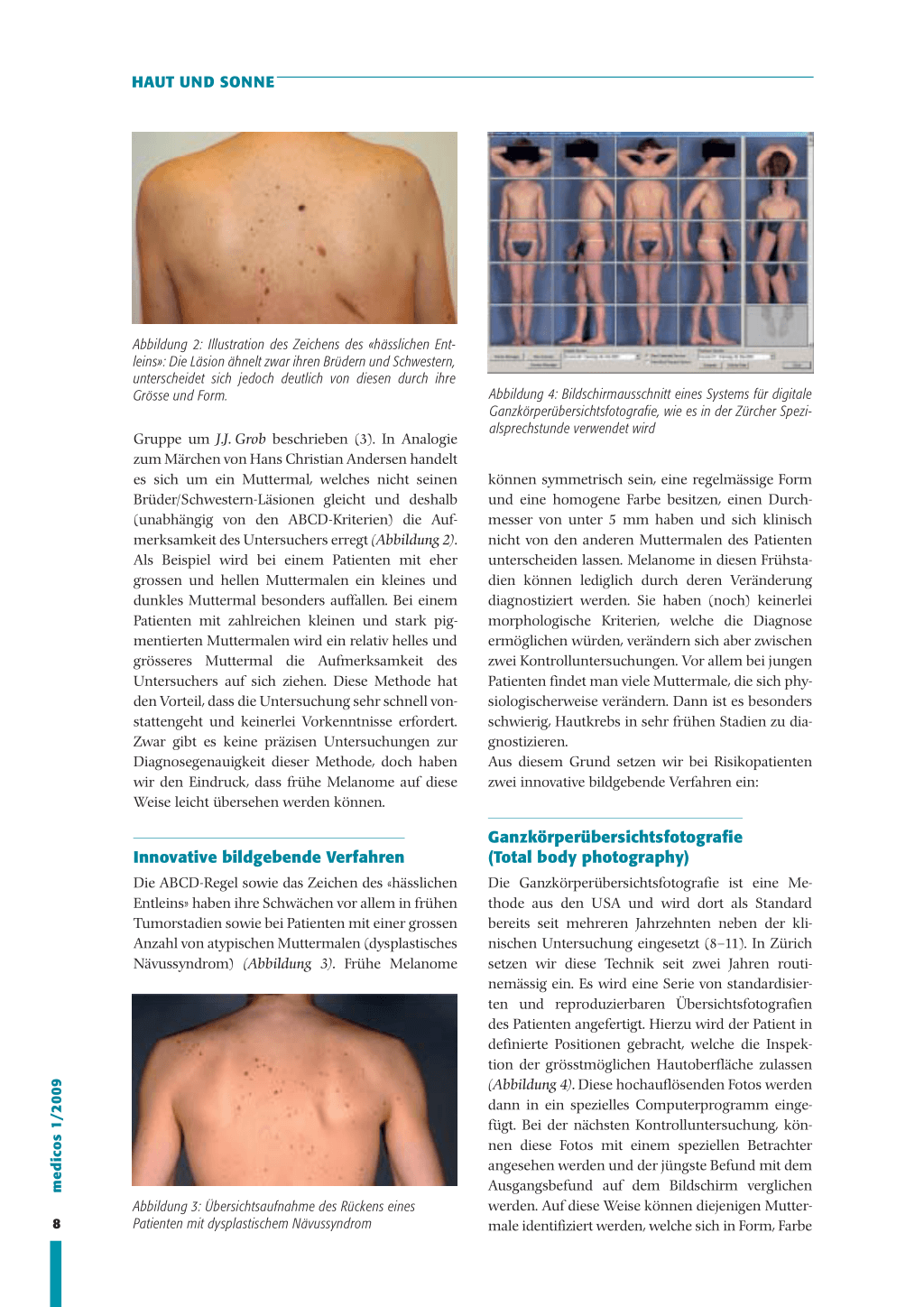
Abbildung 2: Illustration des Zeichens des «hässlichen Entleins»: Die Läsion ähnelt zwar ihren Brüdern und Schwestern, unterscheidet sich jedoch deutlich von diesen durch ihre Grösse und Form.
Gruppe um J.J. Grob beschrieben (3). In Analogie zum Märchen von Hans Christian Andersen handelt es sich um ein Muttermal, welches nicht seinen Brüder/Schwestern-Läsionen gleicht und deshalb (unabhängig von den ABCD-Kriterien) die Aufmerksamkeit des Untersuchers erregt (Abbildung 2). Als Beispiel wird bei einem Patienten mit eher grossen und hellen Muttermalen ein kleines und dunkles Muttermal besonders auffallen. Bei einem Patienten mit zahlreichen kleinen und stark pigmentierten Muttermalen wird ein relativ helles und grösseres Muttermal die Aufmerksamkeit des Untersuchers auf sich ziehen. Diese Methode hat den Vorteil, dass die Untersuchung sehr schnell vonstattengeht und keinerlei Vorkenntnisse erfordert. Zwar gibt es keine präzisen Untersuchungen zur Diagnosegenauigkeit dieser Methode, doch haben wir den Eindruck, dass frühe Melanome auf diese Weise leicht übersehen werden können.
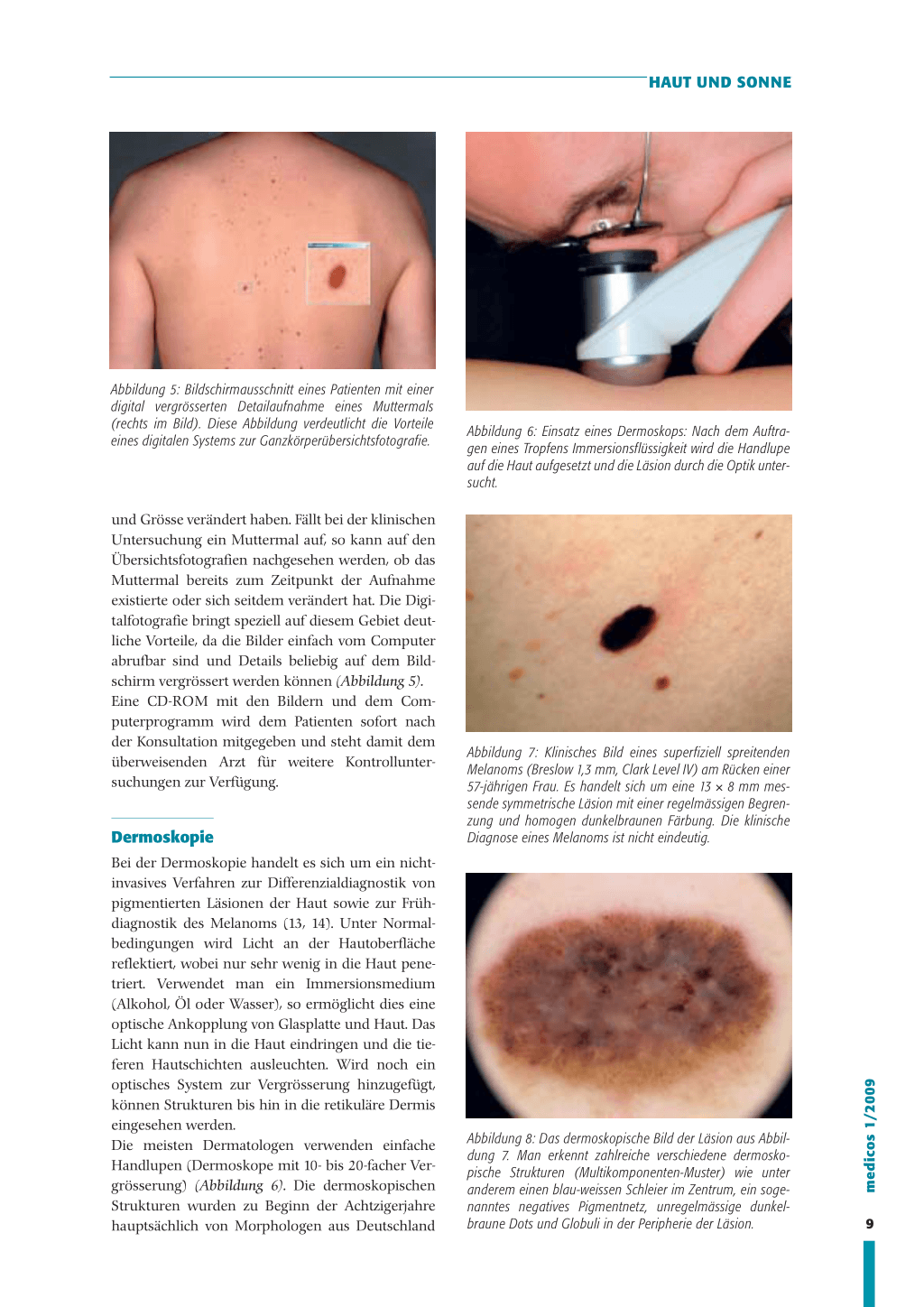
Abbildung 4: Bildschirmausschnitt eines Systems für digitale Ganzkörperübersichtsfotografie, wie es in der Zürcher Spezialsprechstunde verwendet wird
können symmetrisch sein, eine regelmässige Form und eine homogene Farbe besitzen, einen Durchmesser von unter 5 mm haben und sich klinisch nicht von den anderen Muttermalen des Patienten unterscheiden lassen. Melanome in diesen Frühstadien können lediglich durch deren Veränderung diagnostiziert werden. Sie haben (noch) keinerlei morphologische Kriterien, welche die Diagnose ermöglichen würden, verändern sich aber zwischen zwei Kontrolluntersuchungen. Vor allem bei jungen Patienten findet man viele Muttermale, die sich physiologischerweise verändern. Dann ist es besonders schwierig, Hautkrebs in sehr frühen Stadien zu diagnostizieren. Aus diesem Grund setzen wir bei Risikopatienten zwei innovative bildgebende Verfahren ein:
Innovative bildgebende Verfahren
Ganzkörperübersichtsfotografie (Total body photography)
Die ABCD-Regel sowie das Zeichen des «hässlichen Die Ganzkörperübersichtsfotografie ist eine Me-
Entleins» haben ihre Schwächen vor allem in frühen thode aus den USA und wird dort als Standard
Tumorstadien sowie bei Patienten mit einer grossen bereits seit mehreren Jahrzehnten neben der kli-
Anzahl von atypischen Muttermalen (dysplastisches nischen Untersuchung eingesetzt (8–11). In Zürich
Nävussyndrom) (Abbildung 3). Frühe Melanome setzen wir diese Technik seit zwei Jahren routi-
nemässig ein. Es wird eine Serie von standardisier-
ten und reproduzierbaren Übersichtsfotografien
des Patienten angefertigt. Hierzu wird der Patient in
definierte Positionen gebracht, welche die Inspek-
tion der grösstmöglichen Hautoberfläche zulassen
(Abbildung 4). Diese hochauflösenden Fotos werden
dann in ein spezielles Computerprogramm einge-
fügt. Bei der nächsten Kontrolluntersuchung, kön-
nen diese Fotos mit einem speziellen Betrachter
angesehen werden und der jüngste Befund mit dem
Ausgangsbefund auf dem Bildschirm verglichen
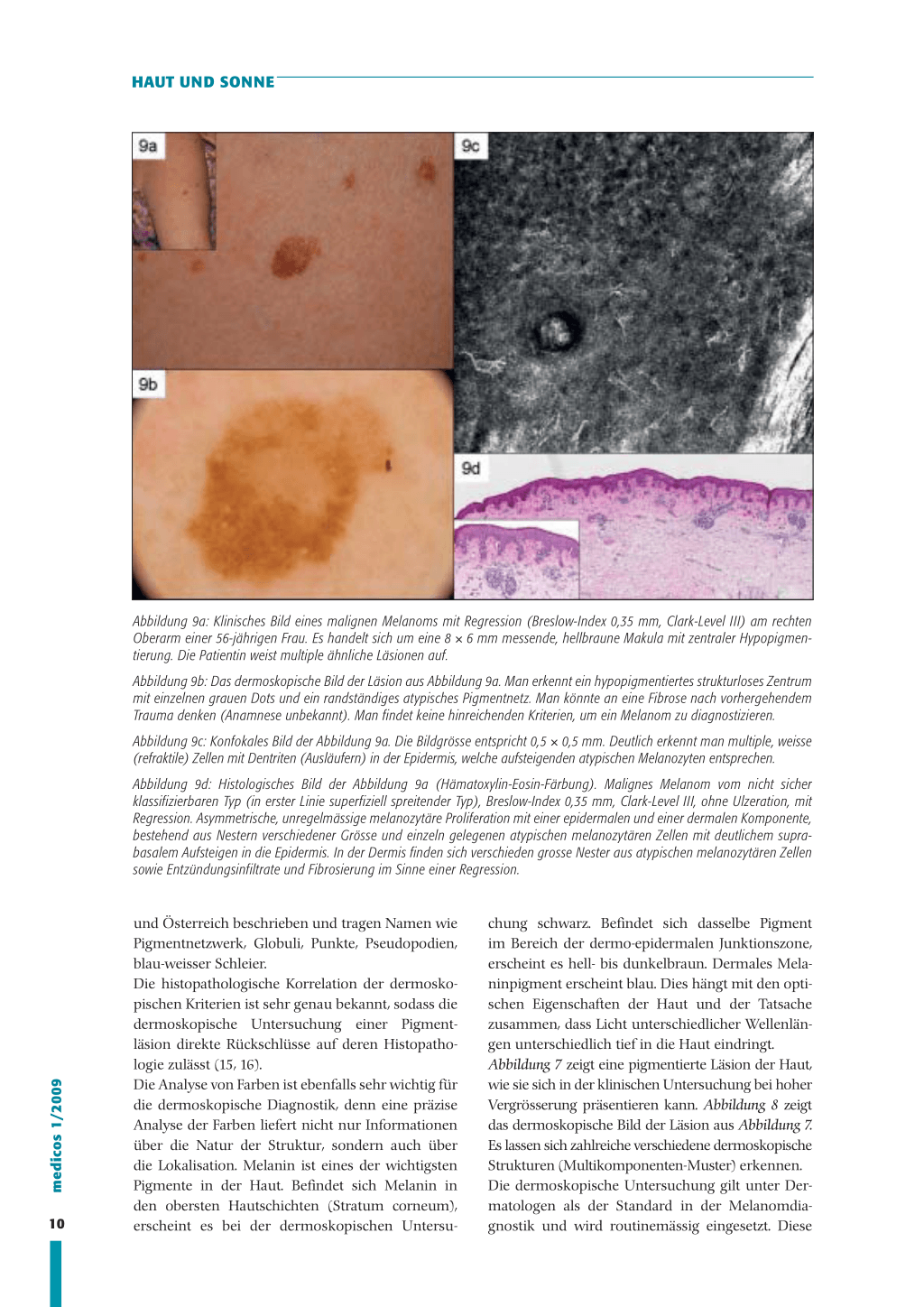
Abbildung 3: Übersichtsaufnahme des Rückens eines
werden. Auf diese Weise können diejenigen Mutter-
8 Patienten mit dysplastischem Nävussyndrom
male identifiziert werden, welche sich in Form, Farbe
medicos 1/2009
HAUT UND SONNE
Abbildung 5: Bildschirmausschnitt eines Patienten mit einer digital vergrösserten Detailaufnahme eines Muttermals (rechts im Bild). Diese Abbildung verdeutlicht die Vorteile eines digitalen Systems zur Ganzkörperübersichtsfotografie.
und Grösse verändert haben. Fällt bei der klinischen Untersuchung ein Muttermal auf, so kann auf den Übersichtsfotografien nachgesehen werden, ob das Muttermal bereits zum Zeitpunkt der Aufnahme existierte oder sich seitdem verändert hat. Die Digitalfotografie bringt speziell auf diesem Gebiet deutliche Vorteile, da die Bilder einfach vom Computer abrufbar sind und Details beliebig auf dem Bildschirm vergrössert werden können (Abbildung 5). Eine CD-ROM mit den Bildern und dem Computerprogramm wird dem Patienten sofort nach der Konsultation mitgegeben und steht damit dem überweisenden Arzt für weitere Kontrolluntersuchungen zur Verfügung.
Dermoskopie
Bei der Dermoskopie handelt es sich um ein nichtinvasives Verfahren zur Differenzialdiagnostik von pigmentierten Läsionen der Haut sowie zur Frühdiagnostik des Melanoms (13, 14). Unter Normalbedingungen wird Licht an der Hautoberfläche reflektiert, wobei nur sehr wenig in die Haut penetriert. Verwendet man ein Immersionsmedium (Alkohol, Öl oder Wasser), so ermöglicht dies eine optische Ankopplung von Glasplatte und Haut. Das Licht kann nun in die Haut eindringen und die tieferen Hautschichten ausleuchten. Wird noch ein optisches System zur Vergrösserung hinzugefügt, können Strukturen bis hin in die retikuläre Dermis eingesehen werden. Die meisten Dermatologen verwenden einfache Handlupen (Dermoskope mit 10- bis 20-facher Vergrösserung) (Abbildung 6). Die dermoskopischen Strukturen wurden zu Beginn der Achtzigerjahre hauptsächlich von Morphologen aus Deutschland
Abbildung 6: Einsatz eines Dermoskops: Nach dem Auftragen eines Tropfens Immersionsflüssigkeit wird die Handlupe auf die Haut aufgesetzt und die Läsion durch die Optik untersucht.
Abbildung 7: Klinisches Bild eines superfiziell spreitenden Melanoms (Breslow 1,3 mm, Clark Level IV) am Rücken einer 57-jährigen Frau. Es handelt sich um eine 13 × 8 mm messende symmetrische Läsion mit einer regelmässigen Begrenzung und homogen dunkelbraunen Färbung. Die klinische Diagnose eines Melanoms ist nicht eindeutig.
Abbildung 8: Das dermoskopische Bild der Läsion aus Abbildung 7. Man erkennt zahlreiche verschiedene dermoskopische Strukturen (Multikomponenten-Muster) wie unter anderem einen blau-weissen Schleier im Zentrum, ein sogenanntes negatives Pigmentnetz, unregelmässige dunkelbraune Dots und Globuli in der Peripherie der Läsion.
9
medicos 1/2009
HAUT UND SONNE
Abbildung 9a: Klinisches Bild eines malignen Melanoms mit Regression (Breslow-Index 0,35 mm, Clark-Level III) am rechten Oberarm einer 56-jährigen Frau. Es handelt sich um eine 8 × 6 mm messende, hellbraune Makula mit zentraler Hypopigmentierung. Die Patientin weist multiple ähnliche Läsionen auf.
Abbildung 9b: Das dermoskopische Bild der Läsion aus Abbildung 9a. Man erkennt ein hypopigmentiertes strukturloses Zentrum mit einzelnen grauen Dots und ein randständiges atypisches Pigmentnetz. Man könnte an eine Fibrose nach vorhergehendem Trauma denken (Anamnese unbekannt). Man findet keine hinreichenden Kriterien, um ein Melanom zu diagnostizieren.
Abbildung 9c: Konfokales Bild der Abbildung 9a. Die Bildgrösse entspricht 0,5 × 0,5 mm. Deutlich erkennt man multiple, weisse (refraktile) Zellen mit Dentriten (Ausläufern) in der Epidermis, welche aufsteigenden atypischen Melanozyten entsprechen.
Abbildung 9d: Histologisches Bild der Abbildung 9a (Hämatoxylin-Eosin-Färbung). Malignes Melanom vom nicht sicher klassifizierbaren Typ (in erster Linie superfiziell spreitender Typ), Breslow-Index 0,35 mm, Clark-Level III, ohne Ulzeration, mit Regression. Asymmetrische, unregelmässige melanozytäre Proliferation mit einer epidermalen und einer dermalen Komponente, bestehend aus Nestern verschiedener Grösse und einzeln gelegenen atypischen melanozytären Zellen mit deutlichem suprabasalem Aufsteigen in die Epidermis. In der Dermis finden sich verschieden grosse Nester aus atypischen melanozytären Zellen sowie Entzündungsinfiltrate und Fibrosierung im Sinne einer Regression.
und Österreich beschrieben und tragen Namen wie chung schwarz. Befindet sich dasselbe Pigment
Pigmentnetzwerk, Globuli, Punkte, Pseudopodien, im Bereich der dermo-epidermalen Junktionszone,
blau-weisser Schleier.
erscheint es hell- bis dunkelbraun. Dermales Mela-
Die histopathologische Korrelation der dermosko- ninpigment erscheint blau. Dies hängt mit den opti-
pischen Kriterien ist sehr genau bekannt, sodass die schen Eigenschaften der Haut und der Tatsache
dermoskopische Untersuchung einer Pigment- zusammen, dass Licht unterschiedlicher Wellenlän-
läsion direkte Rückschlüsse auf deren Histopatho- gen unterschiedlich tief in die Haut eindringt.
logie zulässt (15, 16).
Abbildung 7 zeigt eine pigmentierte Läsion der Haut,
medicos 1/2009
Die Analyse von Farben ist ebenfalls sehr wichtig für wie sie sich in der klinischen Untersuchung bei hoher
die dermoskopische Diagnostik, denn eine präzise Vergrösserung präsentieren kann. Abbildung 8 zeigt
Analyse der Farben liefert nicht nur Informationen das dermoskopische Bild der Läsion aus Abbildung 7.
über die Natur der Struktur, sondern auch über Es lassen sich zahlreiche verschiedene dermoskopische
die Lokalisation. Melanin ist eines der wichtigsten Strukturen (Multikomponenten-Muster) erkennen.
Pigmente in der Haut. Befindet sich Melanin in Die dermoskopische Untersuchung gilt unter Der-
den obersten Hautschichten (Stratum corneum), matologen als der Standard in der Melanomdia10 erscheint es bei der dermoskopischen Untersu- gnostik und wird routinemässig eingesetzt. Diese
HAUT UND SONNE
Methode erfordert spezifische Kenntnisse im Bereich der Histopathologie der Haut und ein grosses Mass an Erfahrung. Die Verwendung der Dermoskopie durch einen erfahrenen Untersucher führt zu einer grossen Zunahme der Diagnosegenauigkeit. Pehamberger et al. fanden in einer Studie zum oberflächlich spreitenden Melanom eine Zunahme der Diagnosegenauigkeit von 54 Prozent (klinische Untersuchung) auf 91 Prozent (dermoskopische Untersuchung).
«Optische Biopsie» (konfokale Mikroskopie)
Als eines von drei Zentren in Europa und als einzi-
ges Zentrum in der Schweiz setzen wir im Rahmen
der Hautkrebsvorsorge-Sprechstunde an der Der-
matologischen Klinik des Universitätsspitals Zürich
routinemässig die konfokale Mikroskopie (18, 19)
ein. Diese Technik erlaubt eine horizontale Beurtei-
lung einer Läsion bis in die Dermis, was ihr auch
den Spitznamen «optische Biopsie» verliehen hat. Sie
eignet sich hervorragend für die Diagnostik von ver-
dächtigen Pigmentläsionen, da man sehr deutlich
das Vorhandensein von atypischen Melanozyten in
der Epidermis («pagetoide melanozytäre Migra-
tion») oder architektonische Veränderungen der
Junktionszone erkennen kann (19). Die pagetoide
melanozytäre Migration ist typisch für das Mela-
nom. Die Abbildungen 9a und 9b zeigen eine kli-
nisch unauffällige, dermatoskopisch diskret ver-
dächtige melanozytäre Läsion, welche aber erst
mithilfe der konfokalen Mikroskopie als maligne
diagnostiziert werden konnte (pagetoide melano-
zytäre Migration, Abbildung 9c). Abbildung 9d zeigt
die Histologie derselben Läsion, in der ein regres-
sives Melanom bestätigt werden konnte.
Zusammenfassend kann gesagt werden, dass der
Frühdiagnose gerade beim Melanom eine sehr
wichtige Rolle zukommt, da zum einen die Haut
leicht untersucht werden kann und zum anderen
frühe Tumorstadien beim Melanom durch einen
einfachen chirurgischen Eingriff «geheilt» werden
können.
●
Literatur:
1. Balch C.M., Buzaid A.C., Soong S.J., Atkins M.B., Cascinelli N., Coit D.G. et al.: Final version of the American Joint Committee on Cancer staging system for cutaneous melanoma. J Clin Oncol 2001; 19(16): 3635–3648.
2. Balch C.M., Soong S.J., Gershenwald J.E., Thompson J.F., Reintgen D.S., Cascinelli N. et al.: Prognostic factors analysis of 17600 melanoma patients: validation of the American Joint Committee on Cancer melanoma staging system, J Clin Oncol 2001; 19(16): 3622–3634.
3. Grob J.J., Bonerandi J.J.: The «ugly duckling» sign: identification of the common characteristics of nevi in an individual as a basis for melanoma screening [letter; comment], Arch Dermatol 1998; 134(1): 103–104.
4. Seab J.A.: Dysplastic nevi and the dysplastic nevus syndrome, Dermatol Clin 1992; 10(1): 189–201.
5. Elder D.E., Green M.H., Guerry D., Kraemer K.H., Clark W.H.: The dysplastic nevus syndrome: our definition, Am J Dermatopathol 1982; 4(5): 455–460.
6. Elder D.E., Murphy G.F., Lavker R.L.: Wallace H. Clark, Jr., MD: a biography and annotated bibliography, Hum Pathol 1999; 30(5): 491–497.
7. English D.R., Menz J., Heenan P.J., Elder D.E., Watt J.D., Armstrong B.K.: The dysplastic naevus syndrome in patients with cutaneous malignant melanoma in Western Australia, Med J Aust 1986; 145(5): 194–198.
8. Kopf A.W., Salopek T.G., Slade J., Marghoob A.A., Bart R.S.: Techniques of cutaneous examination for the detection of skin cancer, Cancer 1995; 75(2 Suppl): 684–690.
9. Nehal K.S., Oliveria S.A., Marghoob A.A., Christos P.J., Dusza S., Tromberg J.S. et al.: Use of and beliefs about baseline photography in the management of patients with pigmented lesions: a survey of dermatology residency programmes in the United States, Melanoma Res 2002; 12(2): 161–167.
10. Slue W., Kopf A.W., Rivers J.K.: Total-body photographs of dysplastic nevi, Arch Dermatol 1988; 124(8): 1239–1243.
11. Slue W.E.: Total body photography for melanoma surveillance, N Y State J Med 1992; 92(11): 494–495.
12. Malvehy J., Puig S.: Follow-up of melanocytic skin lesions with digital totalbody photography and digital dermoscopy: a two-step method, Clin Dermatol 2002; 20(3): 297–304.
13. Braun R.P., Rabinovitz H., Oliviero M., Kopf A.W., Saurat J.H., Thomas L.: Dermatoscopie des lésions pigmentées, Ann Dermatol Venereol 2002; 129(2): 187–202.
14. Braun R.P., Saurat J.H., French LE.: Dermoscopy of pigmented lesions: a valuable tool in the diagnosis of melanoma, Swiss Med Wkly 2004; 134(7–8): 83–90.
15. Braun R.P., Kaya G., Masouye I., Krischer J., Saurat J.H.: Histopathologic correlation in dermoscopy: a micropunch technique, Arch Dermatol 2003; 139(3): 349–351.
16. Yadav S., Vossaert K.A., Kopf A.W., Silverman M., Grin-Jorgensen C.: Histopathologic correlates of structures seen on dermoscopy (epiluminescence microscopy), Am J Dermatopathol 1993; 15(4): 297–305.
17. Happe M., Freitag M., Stucker M., Altmeyer P., Hoffmann K. [High resolution 20 MHz ultrasound diagnosis in dermatology for noninvasive imaging of malignant melanomas], Z Arztl Fortbild Qualitatssich 1997; 91(4): 347–353.
18. Ruocco E., Argenziano G., Pellacani G., Seidenari S.: Noninvasive imaging of skin tumors. Dermatol Surg 2004; 30(2 Pt 2): 301–310.
19. Charles C.A., Marghoob A.A., Busam K.J., Clark-Loeser L., Halpern A.C.: Melanoma or pigmented basal cell carcinoma: a clinical-pathologic correlation with dermoscopy, in vivo confocal scanning laser microscopy, and routine histology, Skin Res Technol 2002; 8(4): 282–287.
Korrespondenzadresse: PD Dr. med. Ralph P. Braun Leitender Arzt Dermatologische Klinik, UniversitätsSpital Gloriastrasse 31 8091 Zürich Tel. 044-255 35 86, Fax 044-255 89 88 E-Mail: ralph.braun@usz.ch
Interessenkonflikte: keine
medicos 1/2009
11