Transkript
UEG-Week
Chronische Verstopfung
Tipps zur Abklärung und Behandlung
Chronische Verstopfung kann banale oder weniger banale Ursachen haben. Wie diese abgeklärt werden und wie eine chronische Verstopfung funktioneller Natur zu behandeln ist, war am Jahreskongress der United European Gastroenterology (UEG Week) in Wien zu hören.
Fotos: vh
Dr. Jordi Serra PD Dr. Viola Andresen
Obstipation ist eine subjektiv empfundene inkomplette oder zu seltene Defäkation. Bei chronischer Verstopfung sei die Ursachensuche sehr wichtig, betonte Dr. Jordi Serra, University Hospital Germans Trias i Pujol, Badalona (E). Eine ausführliche Anamnese umfasst die Symptome im Zeitverlauf, die Anzahl Darmbewegungen, Trigger, bereits ergriffene Massnahmen, Defäkationsmanöver wie auch Essund Stuhlgewohnheiten. Aktuell eingenommene Medikamente für andere Erkrankungen können als Nebenwirkung ebenfalls zu Verstopfung führen (1) (Tabelle 1). Auf Alarmsymptome wie Alter ab 50 Jahren, unbeabsichtigter Gewichtsverlust, Blut im Stuhl, Anämie, Fieber, starke Bauchschmerzen und kolorektale Tumoren in der Familie müsse ebenfalls geachtet werden, so Jordi weiter. Die klinische Untersuchung sollte eine neurologische Abklärung mit der Frage nach Parkinson und eine abdominale Untersuchung beinhalten. Mit einer Tastuntersuchung des Analkanals mit dem Finger lassen sich Hämorrhoiden, Rektozele, Impaktionen oder strukturelle Abnormitäten auf-
Tabelle 1:
Medikamentenklassen, die zu Verstopfung führen können
Analgetika
Anticholinergika
Antikonvulsiva Antihypertonika
Ionenaustauscherharze Kationen Chemotherapeutika Diverse
Quelle: mod. nach (1)
Opioide, nicht steroidale Entzündungshemmer (NSAID) z.B. trizyklische Antidepressiva, Antiparkinsonika, Antipsychotika
z.B. Kalziumkanalblocker, Diuretika, Betaagonisten Colestyramin, Colestipol z.B. Aluminium, Kalzium, Eisen, Wismut
z.B. Bariumsulfat, Kontrazeptiva, Alendronsäure
decken. Diese Tastuntersuchung empfiehlt Serra bei jedem Patienten mit chronischer Verstopfung durchzuführen.
Medikamentöse Massnahmen
Handelt es sich bei der Verstopfung um eine funktionelle Störung und führen Massnahmen wie mehr trinken, mehr Bewegung und mehr Nahrungsfasern zu keiner befriedigenden Besserung, ist der Einsatz von konventionellen Laxanzien die nächste Option (Tabelle 2). Die damit erwirkte Wasserretention führt im Darm zur Stuhlerweichung und regt die Darmtätigkeit an. Dazu führen zum Beispiel Quellstoffe wie beispielsweise Sterculia-Gummi oder Flohsamen. Osmotische Laxativa (verschiedene Salze wie z.B. Magnesium-, Natriumsulfat) wie auch isoosmotische Laxanzien (z.B. Macrogol) halten durch erhöhte Salzkonzentration ebenfalls Wasser im Darm zurück. Auch Zuckeralkohole wie Lactulose erhöhen den Wassergehalt im Darm. Die Vergärung im Darm führt zu einer Erhöhung des Säuregehalts und hält das Wasser zurück, was in einer Aufweichung des Stuhls resultiert. Die Verstopfung kann auch durch stimulierende Laxanzien wie die Klasse der Diphenole (Bisacodyl oder Natriumpicosulfat) und der Antrachinonderivate (z.B. Senna) aufgelöst werden. Diese regen die Sekretion von Elektrolyten und Wasser in das Darmlumen an und hemmen gleichzeitig deren Rückresorption aus dem Darm. Das bewirkt eine Volumenzunahme im Darm, was die Peristaltik anregt. Sekretagoga wie Lubiproston und Linaclotid regen die Sekretion ebenfalls an und hemmen die Rückresorption. Für sehr viele Patienten sei eine Therapie mit Macrogol sehr hilfreich, so PD Dr. Viola Andresen, Israelitisches Krankenhaus Hamburg (D). In einem systematischen Review zeigte sich für Macrogol mit und ohne Elektrolyte eine Verbesserung der wöchentlichen Stuhlfrequenz um nahezu das Doppelte, verglichen mit Plazebo und anderen Laxanzien wie Serotoninagonisten und Lactulose (2). Mögliche Nebenwirkungen wie Diarrhö, Blähungen und Abdominalkrämpfe können auftreten. Falls die Therapie nicht genügend anschlägt, kann das Prokinetikums Prucaloprid, ein Serotoninagonist, zum Einsatz kommen. Dieser erhöht die spontanen Darmbewegungen im Vergleich zu Plazebo ebenfalls signifikant, wie eine Metaanalyse zeigte (3). Meist transiente Nebenwirkungen wie Kopfschmerzen, Übelkeit und Diarrhö können dabei vor allem zu Therapiebeginn auftreten.
18 CongressSelection Gastroenterologie | Januar 2019
UEG-Week
Tabelle 2:
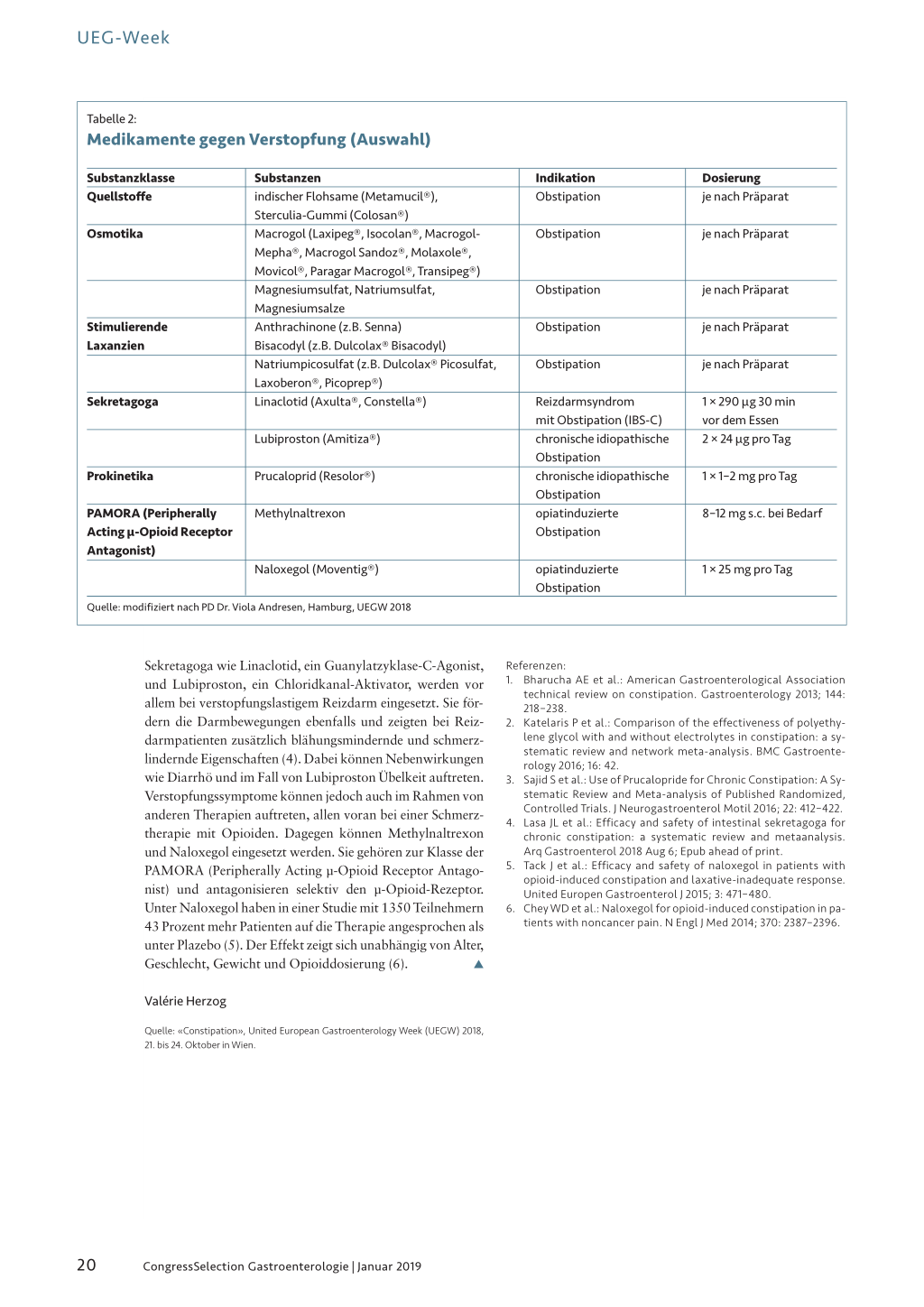
Medikamente gegen Verstopfung (Auswahl)
Substanzklasse Quellstoffe Osmotika
Stimulierende Laxanzien
Sekretagoga
Substanzen indischer Flohsame (Metamucil®), Sterculia-Gummi (Colosan®) Macrogol (Laxipeg®, Isocolan®, MacrogolMepha®, Macrogol Sandoz®, Molaxole®, Movicol®, Paragar Macrogol®, Transipeg®) Magnesiumsulfat, Natriumsulfat, Magnesiumsalze Anthrachinone (z.B. Senna) Bisacodyl (z.B. Dulcolax® Bisacodyl) Natriumpicosulfat (z.B. Dulcolax® Picosulfat, Laxoberon®, Picoprep®) Linaclotid (Axulta®, Constella®)
Lubiproston (Amitiza®)
Prokinetika
Prucaloprid (Resolor®)
PAMORA (Peripherally Acting µ-Opioid Receptor Antagonist)
Methylnaltrexon Naloxegol (Moventig®)
Quelle: modifiziert nach PD Dr. Viola Andresen, Hamburg, UEGW 2018
Indikation Obstipation
Obstipation
Dosierung je nach Präparat
je nach Präparat
Obstipation
Obstipation
Obstipation
Reizdarmsyndrom mit Obstipation (IBS-C) chronische idiopathische Obstipation chronische idiopathische Obstipation opiatinduzierte Obstipation
opiatinduzierte Obstipation
je nach Präparat je nach Präparat je nach Präparat 1 290 µg 30 min vor dem Essen 2 24 µg pro Tag 1 1–2 mg pro Tag 8–12 mg s.c. bei Bedarf
1 25 mg pro Tag
Sekretagoga wie Linaclotid, ein Guanylatzyklase-C-Agonist,
und Lubiproston, ein Chloridkanal-Aktivator, werden vor
allem bei verstopfungslastigem Reizdarm eingesetzt. Sie för-
dern die Darmbewegungen ebenfalls und zeigten bei Reiz-
darmpatienten zusätzlich blähungsmindernde und schmerz-
lindernde Eigenschaften (4). Dabei können Nebenwirkungen
wie Diarrhö und im Fall von Lubiproston Übelkeit auftreten.
Verstopfungssymptome können jedoch auch im Rahmen von
anderen Therapien auftreten, allen voran bei einer Schmerz-
therapie mit Opioiden. Dagegen können Methylnaltrexon
und Naloxegol eingesetzt werden. Sie gehören zur Klasse der
PAMORA (Peripherally Acting µ-Opioid Receptor Antago-
nist) und antagonisieren selektiv den µ-Opioid-Rezeptor.
Unter Naloxegol haben in einer Studie mit 1350 Teilnehmern
43 Prozent mehr Patienten auf die Therapie angesprochen als
unter Plazebo (5). Der Effekt zeigt sich unabhängig von Alter,
Geschlecht, Gewicht und Opioiddosierung (6).
L
Referenzen: 1. Bharucha AE et al.: American Gastroenterological Association
technical review on constipation. Gastroenterology 2013; 144: 218–238. 2. Katelaris P et al.: Comparison of the effectiveness of polyethylene glycol with and without electrolytes in constipation: a systematic review and network meta-analysis. BMC Gastroenterology 2016; 16: 42. 3. Sajid S et al.: Use of Prucalopride for Chronic Constipation: A Systematic Review and Meta-analysis of Published Randomized, Controlled Trials. J Neurogastroenterol Motil 2016; 22: 412–422. 4. Lasa JL et al.: Efficacy and safety of intestinal sekretagoga for chronic constipation: a systematic review and metaanalysis. Arq Gastroenterol 2018 Aug 6; Epub ahead of print. 5. Tack J et al.: Efficacy and safety of naloxegol in patients with opioid-induced constipation and laxative-inadequate response. United Europen Gastroenterol J 2015; 3: 471–480. 6. Chey WD et al.: Naloxegol for opioid-induced constipation in patients with noncancer pain. N Engl J Med 2014; 370: 2387–2396.
Valérie Herzog
Quelle: «Constipation», United European Gastroenterology Week (UEGW) 2018, 21. bis 24. Oktober in Wien.
20 CongressSelection Gastroenterologie | Januar 2019