Transkript
EASD
Albuminurie bedeutet Risiko für die Diabetikerniere
Fortschritte in Diagnostik und Therapie der diabetischen Nephropathie
Die diabetische Nierenerkrankung zählt zu den grossen, weitgehend ungelösten Problemen im Management des Diabetes mellitus. Intensive Forschung zur verbesserten und vor allem früheren Diagnostik sind im Gange, und neue Antidiabetika scheinen sich günstig auf die Entwicklung der Nephropathie auszuwirken.
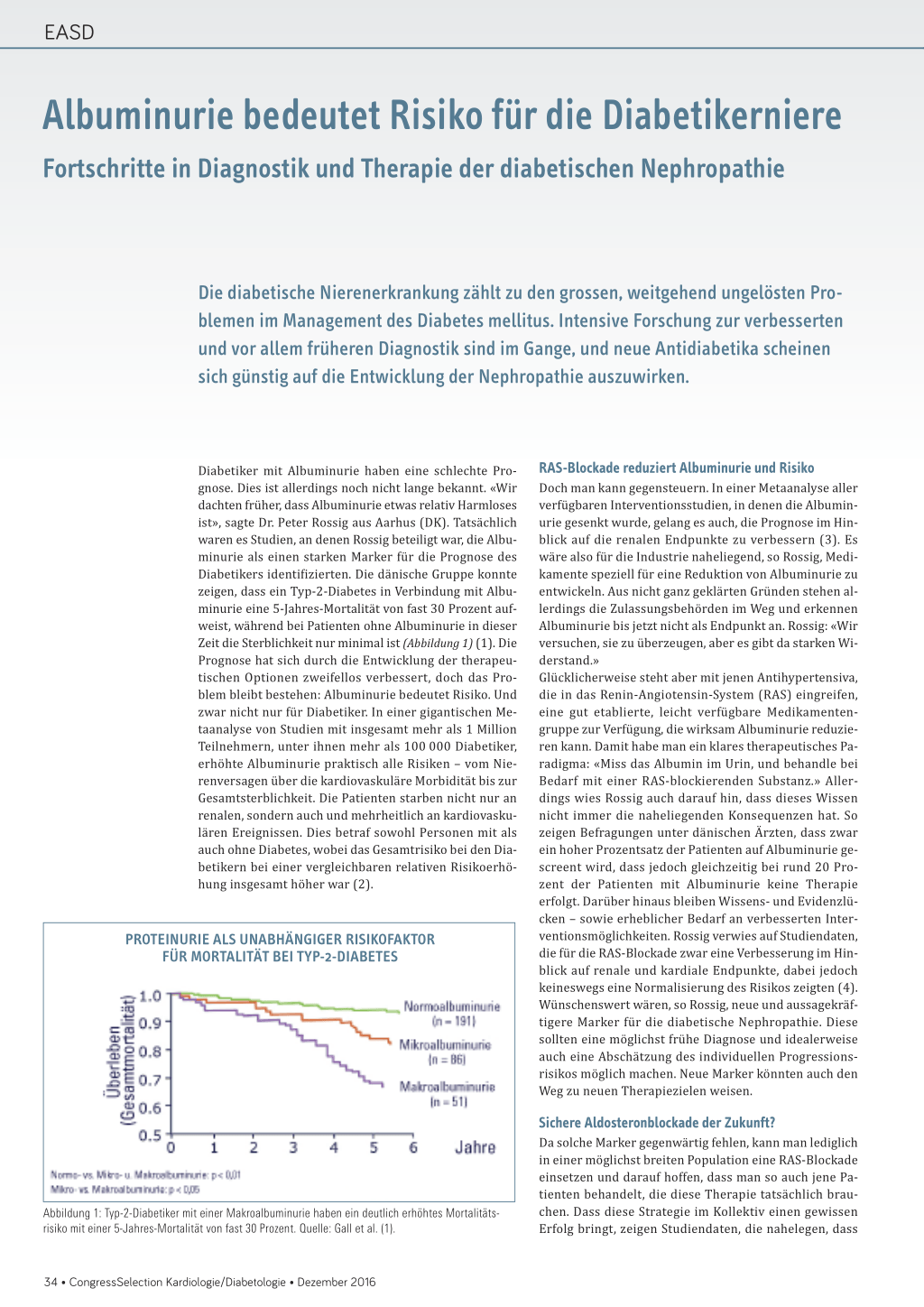
Diabetiker mit Albuminurie haben eine schlechte Prognose. Dies ist allerdings noch nicht lange bekannt. «Wir dachten früher, dass Albuminurie etwas relativ Harmloses ist», sagte Dr. Peter Rossig aus Aarhus (DK). Tatsächlich waren es Studien, an denen Rossig beteiligt war, die Albuminurie als einen starken Marker für die Prognose des Diabetikers identifizierten. Die dänische Gruppe konnte zeigen, dass ein Typ-2-Diabetes in Verbindung mit Albuminurie eine 5-Jahres-Mortalität von fast 30 Prozent aufweist, während bei Patienten ohne Albuminurie in dieser Zeit die Sterblichkeit nur minimal ist (Abbildung 1) (1). Die Prognose hat sich durch die Entwicklung der therapeutischen Optionen zweifellos verbessert, doch das Problem bleibt bestehen: Albuminurie bedeutet Risiko. Und zwar nicht nur für Diabetiker. In einer gigantischen Metaanalyse von Studien mit insgesamt mehr als 1 Million Teilnehmern, unter ihnen mehr als 100 000 Diabetiker, erhöhte Albuminurie praktisch alle Risiken – vom Nierenversagen über die kardiovaskuläre Morbidität bis zur Gesamtsterblichkeit. Die Patienten starben nicht nur an renalen, sondern auch und mehrheitlich an kardiovaskulären Ereignissen. Dies betraf sowohl Personen mit als auch ohne Diabetes, wobei das Gesamtrisiko bei den Diabetikern bei einer vergleichbaren relativen Risikoerhöhung insgesamt höher war (2).
PROTEINURIE ALS UNABHÄNGIGER RISIKOFAKTOR FÜR MORTALITÄT BEI TYP-2-DIABETES
RAS-Blockade reduziert Albuminurie und Risiko
Doch man kann gegensteuern. In einer Metaanalyse aller verfügbaren Interventionsstudien, in denen die Albuminurie gesenkt wurde, gelang es auch, die Prognose im Hinblick auf die renalen Endpunkte zu verbessern (3). Es wäre also für die Industrie naheliegend, so Rossig, Medikamente speziell für eine Reduktion von Albuminurie zu entwickeln. Aus nicht ganz geklärten Gründen stehen allerdings die Zulassungsbehörden im Weg und erkennen Albuminurie bis jetzt nicht als Endpunkt an. Rossig: «Wir versuchen, sie zu überzeugen, aber es gibt da starken Widerstand.» Glücklicherweise steht aber mit jenen Antihypertensiva, die in das Renin-Angiotensin-System (RAS) eingreifen, eine gut etablierte, leicht verfügbare Medikamentengruppe zur Verfügung, die wirksam Albuminurie reduzieren kann. Damit habe man ein klares therapeutisches Paradigma: «Miss das Albumin im Urin, und behandle bei Bedarf mit einer RAS-blockierenden Substanz.» Allerdings wies Rossig auch darauf hin, dass dieses Wissen nicht immer die naheliegenden Konsequenzen hat. So zeigen Befragungen unter dänischen Ärzten, dass zwar ein hoher Prozentsatz der Patienten auf Albuminurie gescreent wird, dass jedoch gleichzeitig bei rund 20 Prozent der Patienten mit Albuminurie keine Therapie erfolgt. Darüber hinaus bleiben Wissens- und Evidenzlücken – sowie erheblicher Bedarf an verbesserten Interventionsmöglichkeiten. Rossig verwies auf Studiendaten, die für die RAS-Blockade zwar eine Verbesserung im Hinblick auf renale und kardiale Endpunkte, dabei jedoch keineswegs eine Normalisierung des Risikos zeigten (4). Wünschenswert wären, so Rossig, neue und aussagekräftigere Marker für die diabetische Nephropathie. Diese sollten eine möglichst frühe Diagnose und idealerweise auch eine Abschätzung des individuellen Progressionsrisikos möglich machen. Neue Marker könnten auch den Weg zu neuen Therapiezielen weisen.
Abbildung 1: Typ-2-Diabetiker mit einer Makroalbuminurie haben ein deutlich erhöhtes Mortalitätsrisiko mit einer 5-Jahres-Mortalität von fast 30 Prozent. Quelle: Gall et al. (1).
Sichere Aldosteronblockade der Zukunft?
Da solche Marker gegenwärtig fehlen, kann man lediglich in einer möglichst breiten Population eine RAS-Blockade einsetzen und darauf hoffen, dass man so auch jene Patienten behandelt, die diese Therapie tatsächlich brauchen. Dass diese Strategie im Kollektiv einen gewissen Erfolg bringt, zeigen Studiendaten, die nahelegen, dass
34 • CongressSelection Kardiologie/Diabetologie • Dezember 2016
EASD
eine frühe RAS-Blockade bei Diabetikern die Entwicklung von Mikroalbuminurie verhindern kann. In einer Metaanalyse wurde ein günstiger Effekt dieser undifferenzierten Behandlungsstrategie gefunden (5). Auch eine aggressivere Blockade des RAS wurde versucht. Rossig: «Leider hat sich dieser Ansatz langfristig nicht bewährt. Ein Element fehlt allerdings noch in diesem Bild: Wir haben noch keine Langzeitdaten zur Aldosteronblockade. Aldosteron ist jedoch von hohem Interesse, da es Effekte auf das Endothel, das Herz, die Nieren und das Nervensystem hat.» Studiendaten zeigen, dass jene Patienten, bei denen es unter Therapie mit einem Angiotensin-II-Rezeptor-Blocker zu einem Anstieg von Aldosteron kommt, eine schlechtere Prognose und einen schnelleren Verlust der Nierenfunktion zeigen (6). Die Angst vor einem Entgleisen der Kaliumspiegel limitiert den Einsatz von Aldosteronblockern. Neue Substanzen, die den Kaliumspiegel nicht beeinflussen und damit sicherer sein sollen, sind in Entwicklung. Die verfügbaren Studiendaten sind vielversprechend. So gelang es, mit dem nicht steroidalen Mineralokortikoid-Rezeptor-Antagonisten Finerenon bei Patienten mit diabetischer Nephropathie die Albuminurie zu reduzieren (7). Zwei grosse klinische Studien mit renalen und kardialen Endpunkten laufen gegenwärtig.
Neue Marker, neue Mechanismen, neue Tests
Über die Albuminurie hinaus sind die Mechanismen der diabetischen Nephropathie in Diskussion. Untersucht wird beispielsweise, ob es sich tatsächlich vorwiegend um eine glomeruläre Pathologie handelt oder ob beziehungsweise wieweit der Tubulus involviert ist. Rossig: «Es ist bekannt, dass der Tubulus im Endstadium der Niereninsuffizienz eine wichtige Rolle spielt. Die Frage ist allerdings, ob das auch auf die frühen Stadien zutrifft.» Tatsächlich wurden bei manchen Patienten mit Typ-1Diabetes und Nephropathie Marker für eine Inflammation des Tubulus gefunden, die man sonst vor allem vom akuten Nierenversagen her kennt. Diese Marker erwiesen sich als starke Prädiktoren für Nierenversagen (8). Auch Vitamin D wird mit Nierenversagen und kardiovaskulären Endpunkten in Verbindung gebracht. Niedrige Vitamin-D-Spiegel sind bei Diabetikern mit erhöhter Mortalität assoziiert (9). In Interventionsstudien wurde ein günstiger Effekt auf die Albuminurie durch Supplementation gezeigt (10). Weiter ist Harnsäure von Interesse. Bei Typ-I-Diabetikern waren erhöhte Harnsäurespiegel mit einem erhöhten Risiko von Makroalbuminurie assoziiert (Abbildung 2) (11). Eine grosse klinische Studie, die die Wirkung von Allopurinol auf das renale Risiko von Typ-I-Diabetikern untersucht, wird gegenwärtig an mehr als 20 Zentren in Amerika und Europa durchgeführt. Aktuelle Untersuchungen gehen auch über klassische Risikofaktoren hinaus und bewegen sich in dem Bereich von Genomics, Epigenomics und Proteomics. Unter Proteomanalyse (Proteomics) versteht man die quantitative Analyse der zu einem bestimmten Zeitpunkt und unter determinierten Bedingungen in einer Zelle, in einem Organismus oder in einem bestimmten Kompartiment vorhandenen Proteine. Rossig: «Das ist ein teures Verfahren. Aber es hat das Potenzial, unser Verständnis der Pathophysiologie zu erweitern, Risikopatienten zu identifizieren und den Weg zu neuen therapeutischen Targets zu weisen.» Tatsächlich zeigt das Proteom im Urin von Patienten mit Mikro- oder Makroalbuminurie Auffälligkei-
HARNSÄURE ALS PRÄDIKTOR FÜR DIE ENTWICKLUNG EINER MAKROALBUMINURIE
Abbildung 2: Bei Typ-1-Diabetikern mit den höchsten Harnsäurewerten kommt es häufiger zur Entwicklung einer Makroalbuminurie. Quelle: Hovind et al. (11)
ten, und es gibt Hinweise, dass diese Auffälligkeiten bereits auftreten könnten, bevor Albumin im Harn messbar wird. Rossig: «Eine Veränderung der Kollagenfragmente ist eine der ersten nachweisbaren Auffälligkeiten.» Rossigs Gruppe konnte auch eine Normalisierung des Urinproteoms unter Therapie mit einem Sartan demonstrieren (12). In einer europaweiten Studie wird gegenwärtig untersucht, ob sich die Proteomanalyse als Basis für Risikostratifizierung und klinische Entscheidungen eignet.
Nephropathie: Nicht alle Antidiabetika sind gleich
Die klassischen Antidiabetika zeigen kaum Einfluss auf eine einmal eingetretene Albuminurie. Rossig: «Offenbar geht es nicht nur darum, den Blutzucker zu senken, sondern auch darum, wie man ihn senkt.» Eine Reihe neuer Substanzen dürfte nämlich sehr wohl Einfluss auf die Progression einer Albuminurie nehmen. Beispielsweise konnte mit dem GLP1-Rezeptor-Agonisten Liraglutid über 70 Tage eine Reduktion der Albuminurie um 20 Prozent erreicht werden (13). Von besonderem Interesse im Hinblick auf die Nierenfunktion sind die direkt an der Niere wirksamen SGLT2Inhibitoren. Diese Substanzen waren ursprünglich bei Niereninsuffizienz streng kontraindiziert, haben sich jedoch in den vergangenen Jahren zu neuen Hoffnungsträgern für Patienten mit diabetischer Nephropathie entwickelt. Es gibt Hinweise, dass SGLT2-Inhibitoren die problematische Hyperfiltration im Glomerulus des Diabetikers reduzieren (14). Rossig wies auf Post-hoc-Analysen aus den grossen klinischen Studien sowie auf kleinere, experimentelle Arbeiten hin. Eine grosse, klinische Endpunktstudie gebe es bis heute nicht.
Take Home Messa es
® Albuminurie ist ein bedeutender Risikomarker – nicht nur bei Diabetikern. ® Eine RAS-Blockade mit einem ACE-Hemmer oder einem Angiotensin-II-Rezeptor-
Blocker reduziert Albuminurie.
® Hyperurikämie ist ein Risikofaktor für diabetische Nephropathie. ® GLP1-Rezeptor-Agonisten und SGLT2-Inhibitoren dürften bei Patienten mit Nephro-
pathie Antidiabetika der Wahl werden.
® Grosse Endpunktstudien zur Therapie der diabetischen Nephropathie stehen noch
aus.
CongressSelection Kardiologie/Diabetologie • Dezember 2016 • 35
EASD
Allerdings wurden auch im Rahmen des EASD 2016 neue Studiendaten zur Wirkung der SGLT2-Inhibitoren auf die Niere präsentiert. So zeigte eine Post-hoc-Analyse von Phase-III-Daten zu Canagliflozin, dass es unter dem SGLT2-Inhibitor über 2 Jahre zu einer langsameren Abnahme der glomerulären Filtrationsrate kam als unter Therapie mit Glimepirid und dass dieser Effekt nicht mit verbesserter glykämischer Kontrolle erklärt werden konnte (15).
Reno Barth
Referenzen: 1. Gall MA et al.: Albuminuria and poor glycemic control predict mortality in NIDDM. Diabetes 1995; 44 (11): 1303–1309. 2. Fox CS et al.: Associations of kidney disease measures with mortality and end-stage renal disease in individuals with and without diabetes: a meta-analysis. Lancet 2012; 380 (9854): 1662–1673. 3. Lambers Heerspink HJ et al.: GFR decline and subsequent risk of established kidney outcomes: a meta-analysis of 37 randomized controlled trials. Am J Kidney Dis 2014; 64 (6): 860–866. 4. Brenner BM et al.: Effects of losartan on renal and cardiovascular outcomes in patients with type 2 diabetes and nephropathy. N Engl J Med 2001; 345 (12): 861–869. 5. Persson F et al.: Prevention of microalbuminuria using early intervention with renin-angiotensin system inhibitors in patients with type 2 diabetes: A systematic review. J Renin Angiotensin Aldosterone Syst 2016; 17(3). pii: 1470320316652047. 6. Schjoedt KJ et al.: Aldosterone escape during blockade of the reninangiotensin-aldosterone system in diabetic nephropathy is associated with enhanced decline in glomerular filtration rate. Diabetologia 2004; 47 (11): 1936–1939.
7. Bakris GL et al.: Effect of Finerenone on Albuminuria in Patients With Diabetic Nephropathy: A Randomized Clinical Trial. JAMA 2015; 314 (9): 884–894. 8. Nielsen SE et al.: Urinary liver-type fatty acid-binding protein predicts progression to nephropathy in type 1 diabetic patients. Diabetes Care 2010; 33 (6): 1320–1324. 9. Joergensen C et al.: Vitamin D levels and mortality in type 2 diabetes. Diabetes Care 2010; 33 (10): 2238–2243. 10. Joergensen C et al.: Vitamin D analogue therapy, cardiovascular risk and kidney function in people with Type 1 diabetes mellitus and diabetic nephropathy: a randomized trial. Diabet Med 2015; 32 (3): 374–381. 11. Hovind P et al.: Serum uric acid as a predictor for development of diabetic nephropathy in type 1 diabetes: an inception cohort study. Diabetes 2009; 58 (7): 1668–1671. 12. Andersen S et al.: Urinary proteome analysis enables assessment of renoprotective treatment in type 2 diabetic patients with microalbuminuria. BMC Nephrol 2010; 11: 29. 13. Von Scholten BJ et al.: Time course and mechanisms of the antihypertensive and renal effects of liraglutide treatment. Diabet Med 2015; 32 (3): 343–352. 14. Cherney DZ et al.: Renal hemodynamic effect of sodium-glucose cotransporter 2 inhibition in patients with type 1 diabetes mellitus. Circulation 2014; 129 (5): 587–597. 15. Heerspink HJL et al.: Canagliflozin slows progression of renal function decline independent of glycaemic effects. EASD 2016, Abstract 53.
Quelle: 31st Camillo Golgi Lecture im Rahmen der 52. Jahrestagung der European Association for the Study of Diabetes (EASD), 13. September 2016 in München.
KONGRESSNOTIZ
Plädoyer für mehr Ursachenforschung in der Diabetologie
Den «Diabetes Price for Excellence» der EASD und der Novo Nordisk Foundation erhielt in diesem Jahr Prof. Andrew Hattersley aus Exeter (GB). Damit wurde die Leistung des Wissenschaftlers bei der Erforschung genetischer Formen des Diabetes geehrt. In seinem Festvortrag betonte der Preisträger, wie wichtig die exakte Diabetesdiagnostik ist. Sein Fallbeispiel war die neue britische Premierministerin Theresa May. Als diese mit 56 Jahren einen Diabetes bekam, wurde sie über ein Jahr lang als «Typ-2-Diabetes» erfolglos mit oralen Antidiabetika therapiert, bevor die richtige Diagnose eines Typ-1-Diabetes gestellt wurde. Heute behandelt sich die Premierministerin mit einer intensivierten Insulintherapie mit 4 täglichen Injektionen. Diabetesantikörper helfen nicht durchgehend bei der Differenzialdiagnostik eines neu aufgetretenen Diabetes bei Erwachsenen und Älteren, die Inselzellantikörper schon gar nicht und auch nicht immer die GAD-Antikörper. Letztere hätten zwar eine Spezifität von 97 Prozent, aber eine Sensitivität von nur
66 Prozent. Auch genetische Risiko-Scores für Typ-1-Diabetes hätten eine zu starke Überlappung und seien unbrauchbar. Hierzu präsentierte Hattersley eine Statistik: Der Typ1-Diabetes tritt über alle der 6 geprüften Lebensdekaden in gleicher absoluter Häufigkeit auf. In einer weiteren Präsentation aus seinem Institut in Exeter wurden auf dem EADV-Kongress von Nicholas J. Thomas und Mitarbeitern die genetischen Daten aus der UK-Biobank im Detail vorgetragen (2). Diese zeigen, dass etwa die Hälfte aller Fälle von Typ-1-Diabetes erst nach dem 30. Lebensjahr auftritt. Deshalb sollten Ärzte bei einem neu aufgetretenen Diabetes bei Erwachsenen nicht immer automatisch in der Annahme eines Typ-2-Diabetes die Behandlung mit Metformin beginnen, warnte Hattersley. Die Daten aus der UK-Biobank unterstreichen Hattersleys Eingangssätze zu seinem Vortrag: «Die Priorität der Diabetologie und der Diabetologen liegt heute immer noch auf dem Gebiet der Therapie. Die Diagnostik findet viel zu wenig Beachtung.» Er verwies auf die Onkolo-
gie, in der die molekulargenetische Diagnostik
im Vergleich zur onkologischen Therapie
einen viel grösseren Teil ausmache als in der
Diabetologie. Hattersleys Postulat: «Diabeto-
logen sollten ihre Therapie nach der Ursache
und nicht nur nach der Blutzuckerhöhe aus-
richten.»
AZA
Quelle: Nach einem Blog von Prof. Helmut Schatz, Bochum (D), auf blog.endokrinologie.net
Referenzen: 1. Andrew Hattersley: Defining heterogeneity in diabetes to improve clinical care. Preisvortrag auf dem EASD-Kongress München, auf der 52. Jahrestagung der European Association for the Study of Diabetes (EASD), 14. September 2016 in München. 2. J. Thomas et al.: Classifying diabetes by type 1 genetic risk shows autoimmune diabetes cases are evenly distributed above and below 30 years of age. Vortrag OP 264 auf der 52. Jahrestagung der European Association for the Study of Diabetes (EASD), 16. September 2016 in München.
36 • CongressSelection Kardiologie/Diabetologie • Dezember 2016