Transkript
NEUE THERAPIEN
Mit Antikörpern gegen Tumoren
Immunonkologie als Hot Topic der Urologie
EAU
Krebstherapien scheitern langfristig oft an ihrer Toxizität und an Resistenzbildungen bei den behandelten Tumorentitäten. Das Wissen über die Prozesse der Krebsabwehr mithilfe des eigenen Immunsystems führte jedoch dazu, dass neue Wege in der Tumorbehandlung möglich werden; dieses neue Feld der Immunonkologie hat das Potenzial, die Uroonkologie zu revolutionieren.
Tagtäglich bilden sich im menschlichen Körper Tumorzellen – und dennoch entsteht daraus keine Krebserkrankung. Das Immunsystem erkennt entartete Zellen und zerstört sie, bevor sie Schaden anrichten können. Diese Aufgabe übernehmen die T-Zellen: Sie tragen Rezeptoren, die bestimmte Oberflächenproteine auf Körperzellen erkennen können. Dieses Primärsignal wird aber immer von einem Sekundärsignal begleitet: Ist die Zelle aus Sicht des Immunsystems in Ordnung, erhält die T-Zelle diese Information über ein Inhibitorsignal (Checkpoint-Inhibition), zum Beispiel über die PD-1/PD1-Loder die CTLA4/CTLA4-L-Interaktionen (1). Die Immunzelle wird dann inaktiv und verschont die betreffende Zielzelle. Auf der anderen Seite zum Beispiel vermittelt das CD40/ CD40L-System der T-Zelle ein aktivierendes Co-Signal, woraufhin diese die Zielzelle als Bedrohung abtötet. Tumorzellen nutzen solche Co-Signale, um sich vor der Zerstörung durch das Immunsystem zu schützen. Sie überexprimieren beispielsweise PD1-Ligand (PD1-L) und inaktivieren somit die patrouillierenden T-Zellen in ihrer Umgebung. Die Immunantwort bleibt aus, die Tumorzelle überlebt und kann proliferieren; ein Tumor entwickelt sich (Abbildung 1).
Potenziale der Immunonkologie – Tumorzellen sichtbar machen
Chirurgie, Bestrahlung sowie Chemo- und zielgerichtete («targeted») Therapien sind die typischen Behandlungsoptionen bei den meisten fortgeschrittenen Krebserkrankungen in der Urologie. Von diesen Behandlungen profitieren jedoch oftmals weniger als 20 Prozent der Patienten mit fortgeschrittenen soliden Tumorerkrankungen im Sinne einer längeren Überlebenszeit. Neue therapeutische Ansätze für fortgeschrittene Tumorerkrankungen müssen daher in erster Linie darauf zielen, das Langzeitüberleben und dabei auch die Lebensqualität der Patienten spürbar zu verbessern. Insbesondere die immunmodulatorischen Medikamente spielen wohl zukünftig in der Weiterentwicklung der Tumormedizin eine entscheidende Rolle. Während beispielsweise die Vakzinierung oder der adoptive T-Zell-Transfer schon sehr lange intensiv untersucht werden, waren es erst die Phase-III-Ergebnisse der Blockade des Checkpoint-Moleküls CTLA-4 durch Ipilimumab, die einen echten Durchbruch zeigten. Demnach kann das körpereigene Immunsystem selbst im fortgeschrittenen Stadium eines malignen Melanoms wieder in die Lage versetzt werden, eine anhaltende antitumorale Immunantwort aufzu-
Abbildung 1: Checkpoint-Inhibition zur Kontrolle der Immunantwort (Grafik: BMS)
bauen (Abbildung 1). Ipilimumab war 2011 die erste immunonkologische Substanz, die den Verlauf für Tumorpatienten verbesserte. Hinzu kam dann 2015 als erster PD1-Inhibitor Nivolumab, der derzeit für die Behandlung von Melanom und Lungenkarzinom eingesetzt werden darf. Doch auch in der Urologie liegt mittlerweile die EU-Zulassung von Nivolumab – für die Therapie des fortgeschrittenen klarzelligen Nierenzellkarzinoms – vor.
Fortsetzung der Erfolgsgeschichte beim fortgeschrittenen Nierenzellkarzinom
Die Zulassung für Nivolumab zur Behandlung des fortgeschrittenen Nierenzellkarzinoms gründet auf der Begutachtung der Phase-III-Studie CheckMate-025 (2). Darin wurde Nivolumab im Vergleich zu Everolimus bei Patienten mit fortgeschrittenem klarzelligem Nierenzellkarzinom (Abbildung 2) nach vorheriger Therapie mit einem Angiogeneseinhibitor untersucht. Primärer Endpunkt bei CheckMate-025 war das Gesamtüberleben (overall survival; OS). Es zeigte sich, dass mit Nivolumab behandelte Patienten eine mediane Gesamtüberlebenszeit von 25 Monaten hatten. Mit Everolimus waren es hingegen nur etwa 19,6 Monate (HR: 0,73; 98,5%-KI: 0,57–0,93; p = 0,0018) (2). Nivolumab ist damit auch die erste und einzige Anti-PD-1-Therapie, die in einer randomisierten Phase-III-Studie einen signifikanten Überlebensvorteil bei Nierenzellkarzinom erzielte. Darüber hinaus berichteten die mit Nivolumab behandelten Patienten über
CongressSelection Urologie • Mai 2016 • 5
EAU NEUE THERAPIEN
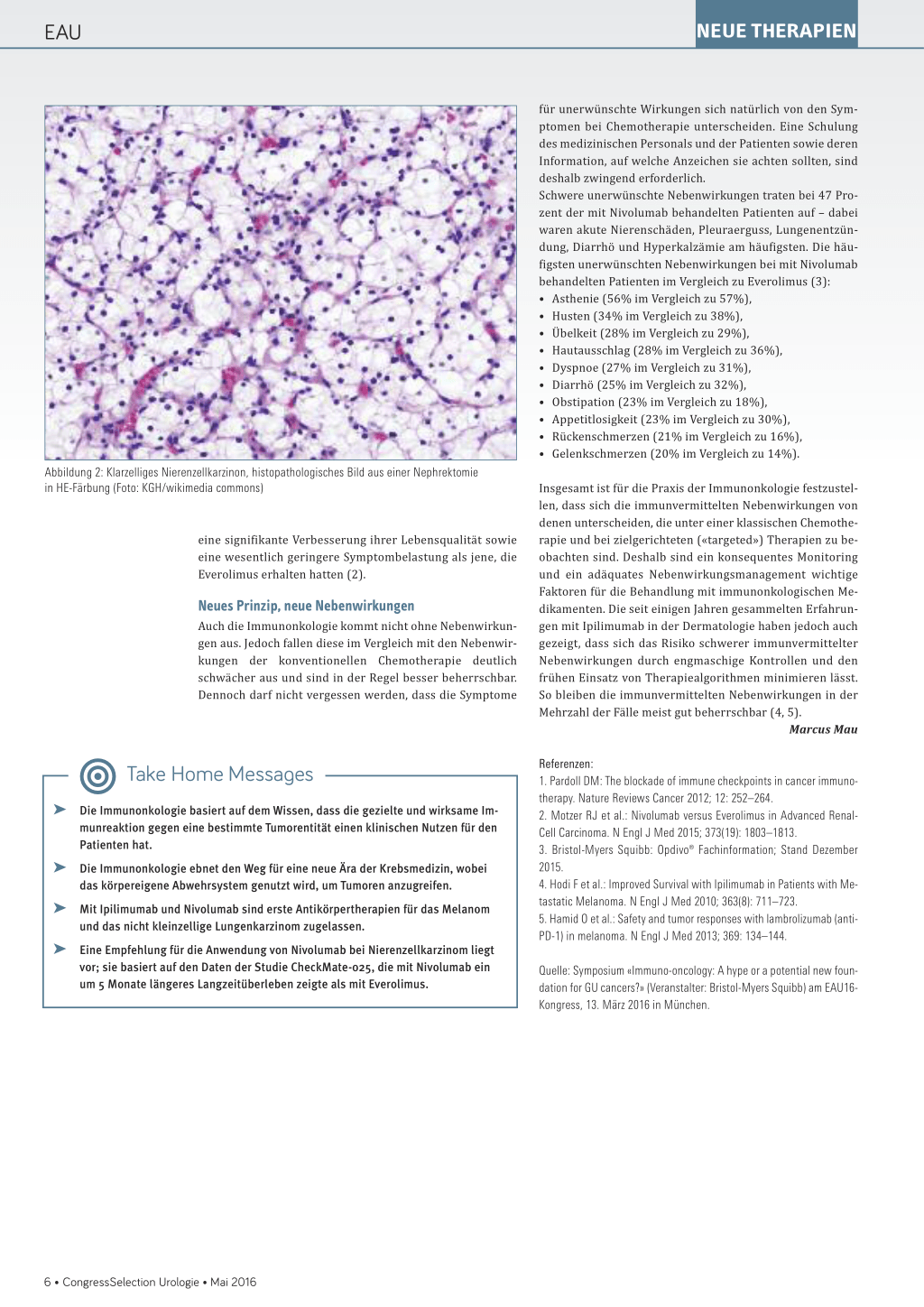
Abbildung 2: Klarzelliges Nierenzellkarzinon, histopathologisches Bild aus einer Nephrektomie in HE-Färbung (Foto: KGH/wikimedia commons)
eine signifikante Verbesserung ihrer Lebensqualität sowie eine wesentlich geringere Symptombelastung als jene, die Everolimus erhalten hatten (2).
Neues Prinzip, neue Nebenwirkungen
Auch die Immunonkologie kommt nicht ohne Nebenwirkungen aus. Jedoch fallen diese im Vergleich mit den Nebenwirkungen der konventionellen Chemotherapie deutlich schwächer aus und sind in der Regel besser beherrschbar. Dennoch darf nicht vergessen werden, dass die Symptome
für unerwünschte Wirkungen sich natürlich von den Symptomen bei Chemotherapie unterscheiden. Eine Schulung des medizinischen Personals und der Patienten sowie deren Information, auf welche Anzeichen sie achten sollten, sind deshalb zwingend erforderlich. Schwere unerwünschte Nebenwirkungen traten bei 47 Prozent der mit Nivolumab behandelten Patienten auf – dabei waren akute Nierenschäden, Pleuraerguss, Lungenentzündung, Diarrhö und Hyperkalzämie am häufigsten. Die häufigsten unerwünschten Nebenwirkungen bei mit Nivolumab behandelten Patienten im Vergleich zu Everolimus (3): • Asthenie (56% im Vergleich zu 57%), • Husten (34% im Vergleich zu 38%), • Übelkeit (28% im Vergleich zu 29%), • Hautausschlag (28% im Vergleich zu 36%), • Dyspnoe (27% im Vergleich zu 31%), • Diarrhö (25% im Vergleich zu 32%), • Obstipation (23% im Vergleich zu 18%), • Appetitlosigkeit (23% im Vergleich zu 30%), • Rückenschmerzen (21% im Vergleich zu 16%), • Gelenkschmerzen (20% im Vergleich zu 14%).
Insgesamt ist für die Praxis der Immunonkologie festzustellen, dass sich die immunvermittelten Nebenwirkungen von denen unterscheiden, die unter einer klassischen Chemotherapie und bei zielgerichteten («targeted») Therapien zu beobachten sind. Deshalb sind ein konsequentes Monitoring und ein adäquates Nebenwirkungsmanagement wichtige Faktoren für die Behandlung mit immunonkologischen Medikamenten. Die seit einigen Jahren gesammelten Erfahrungen mit Ipilimumab in der Dermatologie haben jedoch auch gezeigt, dass sich das Risiko schwerer immunvermittelter Nebenwirkungen durch engmaschige Kontrollen und den frühen Einsatz von Therapiealgorithmen minimieren lässt. So bleiben die immunvermittelten Nebenwirkungen in der Mehrzahl der Fälle meist gut beherrschbar (4, 5).
Marcus Mau
Take Home Messa es
® Die Immunonkologie basiert auf dem Wissen, dass die gezielte und wirksame Im-
munreaktion gegen eine bestimmte Tumorentität einen klinischen Nutzen für den Patienten hat.
® Die Immunonkologie ebnet den Weg für eine neue Ära der Krebsmedizin, wobei
das körpereigene Abwehrsystem genutzt wird, um Tumoren anzugreifen.
® Mit Ipilimumab und Nivolumab sind erste Antikörpertherapien für das Melanom
und das nicht kleinzellige Lungenkarzinom zugelassen.
® Eine Empfehlung für die Anwendung von Nivolumab bei Nierenzellkarzinom liegt
vor; sie basiert auf den Daten der Studie CheckMate-025, die mit Nivolumab ein um 5 Monate längeres Langzeitüberleben zeigte als mit Everolimus.
Referenzen: 1. Pardoll DM: The blockade of immune checkpoints in cancer immunotherapy. Nature Reviews Cancer 2012; 12: 252–264. 2. Motzer RJ et al.: Nivolumab versus Everolimus in Advanced RenalCell Carcinoma. N Engl J Med 2015; 373(19): 1803–1813. 3. Bristol-Myers Squibb: Opdivo® Fachinformation; Stand Dezember 2015. 4. Hodi F et al.: Improved Survival with Ipilimumab in Patients with Metastatic Melanoma. N Engl J Med 2010; 363(8): 711–723. 5. Hamid O et al.: Safety and tumor responses with lambrolizumab (antiPD-1) in melanoma. N Engl J Med 2013; 369: 134–144.
Quelle: Symposium «Immuno-oncology: A hype or a potential new foundation for GU cancers?» (Veranstalter: Bristol-Myers Squibb) am EAU16Kongress, 13. März 2016 in München.
6 • CongressSelection Urologie • Mai 2016