Transkript
STUDIE REFERIERT
Wie lange muss man Antibiotika tatsächlich einnehmen?
In den meisten Leitlinien wird empfohlen, orale Antibiotika über einen bestimmten Zeitraum einzunehmen, auch wenn die Beschwerden bereits abgeklungen sind. Mit dieser Massnahme sollen Rezidive und Resistenzen verhindert werden. Britische Wissenschaftler stellen diese Vorgehensweise nun infrage. Denn in Studien zeigte sich, dass bei einigen Indikationen mit kürzeren Behandlungszeiten ebenso gute klinische Heilungsraten erzielt werden können wie mit längeren. In einem Review systematischer Reviews kam ein amerikanisch-britisches Forscherteam zu ähnlichen Ergebnissen.
Family Practice
Antibiotika gehören zu den am häufigsten verschriebenen Medikamenten. Weltweit bereitet jedoch die Zunahme von Resistenzen Probleme. Zur Entwicklung von Antibiotikaresistenzen tragen viele Faktoren bei. Dazu gehören auch die Häufigkeit und die Dauer der Einnahme. Unnötige Anwendungen sollten daher nach Möglichkeit vermieden werden (1). Derzeit wird Patienten in Australien, Kanada, den USA und Europa geraten, alle verschriebenen Antibiotika einzunehmen, auch wenn die Symptome bereits vollständig abgeklungen sind. Diese Empfehlung beruht auf der Annahme, dass eine frühzeitige Beendigung der Behandlung die Entwicklung von Antibiotikaresistenzen fördert. «Diese Hypothese wurde bis anhin nicht wissenschaftlich belegt», bemängeln Martin Llewelyn von der Brighton
MERKSÄTZE
O Die Gefahr der kollateralen Selektion nimmt mit der Dauer der Antibiotikabehandlung zu.
O Bei einigen Indikationen können mit kürzeren Antibiotikabehandlungen ebenso gute klinische Heilungsraten erzielt werden wie mit einer längeren Therapie.
O Bei Infektionen mit «professionellen» Keimen ist die längere Standardbehandlung mit einer Kombination verschiedener Antibiotika erforderlich.
and Sussex Medical School (GB) und seine Arbeitsgruppe (1).
Gezielte und kollaterale Selektion
Bei der Anwendung von Antibiotika kann es zu jedem Zeitpunkt durch spontane genetische Mutationen zu einer «gezielten Selektion» resistenter Varianten des bekämpften Erregers kommen, die mit demselben Antibiotikum später nicht mehr beseitigt werden können. Dieser Mechanismus ist nach Einschätzung der Autoren jedoch nur bei wenigen «professionellen» Keimen wie den Erregern von Tuberkulose, Gonorrhö oder Typhus von Bedeutung. Diese Infektionen müssen ausreichend lang mit einer ausreichend dosierten Kombination verschiedener Antibiotika behandelt werden (1). Der überwiegende Anteil der Resistenzen entwickelt sich jedoch nicht aufgrund der «gezielten», sondern aufgrund einer «kollateralen Selektion» bei normalerweise harmlosen Spezies wie Escherichia coli und den ESKAPEOrganismen (Enterococcus faecium, Staphylococcus aureus, Klebsiella pneumoniae, Acitenobacter spp., Pseudomonas spp., Enterobacter spp.), die zur physiologischen Mikroflora des Menschen gehören und sich als «opportunistische» Pathogene verhalten können. Bei der Einnahme von Antibiotika – gleichgültig gegen welchen Erreger – werden antibiotikaempfindliche Spezies und Stämme dieser Kommensalflora durch resistente ersetzt. Je länger die Behandlung dauert, desto höher ist die Wahrscheinlichkeit der kollateralen Selektion.
Im Rahmen der kollateralen Resistenzentwicklung kommt es zudem leicht zur unkontrollierten Ausbreitung resistenter Bakterienstämme und -arten, denn sie werden vorwiegend unter asymptomatischen Trägern und weniger durch erkrankte Personen übertragen. Des Weiteren können viele der zur Resistenz beitragenden mutierten Gene an andere Stämme derselben Bakterienart oder an andere Bakterienarten weitergegeben werden. Dies trifft beispielsweise auf die Methicillinresistenz bei Staphylococcus aureus oder die Resistenz gegen Carbapeneme bei Klebsiella pneumoniae zu (1).
Kürzere Behandlung
oft ausreichend
Die Festlegung einer bestimmten indikationsbezogenen Behandlungsdauer beruht – neben der Hypothese der Resistenzentwicklung bei zu früher Beendigung – auch auf der Annahme, dass eine kürzere Behandlung mit ungünstigeren klinischen Ergebnissen verbunden sein könnte. Bei einigen Indikationen zeigte sich jetzt jedoch in Vergleichsstudien, dass mit einer kürzeren Einnahmedauer ähnliche klinische Heilungsraten erzielt werden können wie mit der längeren Standardbehandlung (Tabelle 1). Die einzige Ausnahme beobachteten Llewelyn und sein Team im Zusammenhang mit Otitis media. In einer Studie war eine kürzere Behandlung der Otitis media bei Kindern unter zwei Jahren mit einer geringeren klinischen Heilungsrate (66%) verbunden als eine Behandlung über 10 Tage (84%). Aber auch in diesem Fall bezogen sich die Unterschiede lediglich auf die Dauer der Symptomatik und nicht auf die Rezidivhäufigkeit oder die gezielte Selektion resistenter Erreger. Im Zusammenhang mit den opportunistischen Pathogenen der Kommensalflora zeigte sich in keiner klinischen Studie ein erhöhtes Resistenzrisiko bei kürzerer Behandlungsdauer (1).
Individuelle Behandlungsdauer
wünschenswert
Llewelyn und sein Team weisen in ihrer Analyse darauf hin, dass bei der üblichen indikationsspezifisch festgelegten Behandlungsdauer das unterschiedliche Ansprechen von Patienten auf dasselbe Antibiotikum nicht berücksichtigt wird. In Krankenhäusern kann mittlerweile
1138
ARS MEDICI 24 I 2017
STUDIE REFERIERT
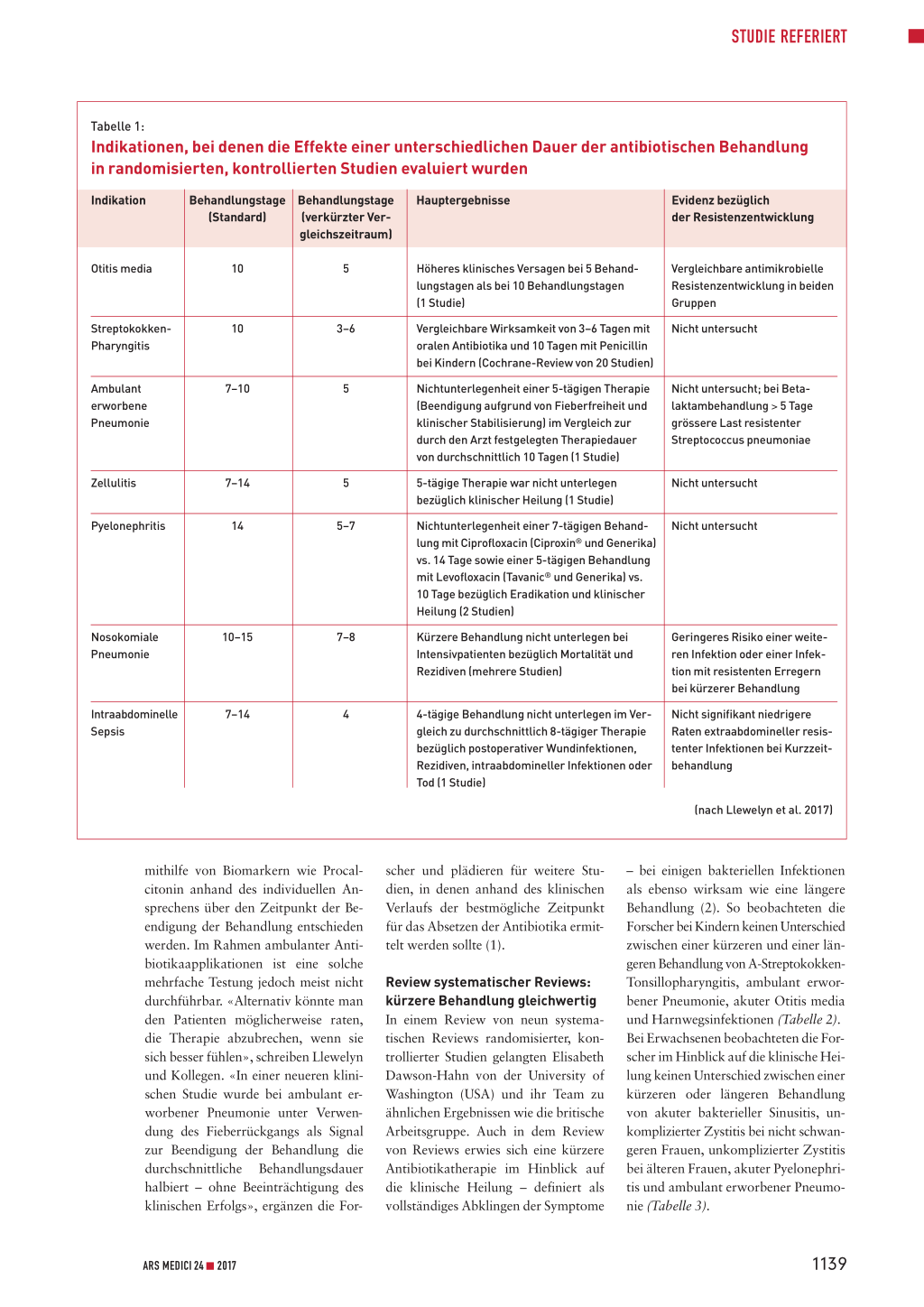
Tabelle 1:
Indikationen, bei denen die Effekte einer unterschiedlichen Dauer der antibiotischen Behandlung in randomisierten, kontrollierten Studien evaluiert wurden
Indikation
Behandlungstage Behandlungstage
(Standard)
(verkürzter Ver-
gleichszeitraum)
Hauptergebnisse
Evidenz bezüglich der Resistenzentwicklung
Otitis media
10
StreptokokkenPharyngitis
Ambulant erworbene Pneumonie
10 7–10
Zellulitis Pyelonephritis
7–14 14
Nosokomiale Pneumonie
10–15
Intraabdominelle Sepsis
7–14
5
Höheres klinisches Versagen bei 5 Behand-
Vergleichbare antimikrobielle
lungstagen als bei 10 Behandlungstagen
Resistenzentwicklung in beiden
(1 Studie)
Gruppen
3–6 Vergleichbare Wirksamkeit von 3–6 Tagen mit Nicht untersucht oralen Antibiotika und 10 Tagen mit Penicillin bei Kindern (Cochrane-Review von 20 Studien)
5 Nichtunterlegenheit einer 5-tägigen Therapie Nicht untersucht; bei Beta-
(Beendigung aufgrund von Fieberfreiheit und klinischer Stabilisierung) im Vergleich zur
laktambehandlung > 5 Tage grössere Last resistenter
durch den Arzt festgelegten Therapiedauer
Streptococcus pneumoniae
von durchschnittlich 10 Tagen (1 Studie)
5
5-tägige Therapie war nicht unterlegen
Nicht untersucht
bezüglich klinischer Heilung (1 Studie)
5–7 Nichtunterlegenheit einer 7-tägigen Behand- Nicht untersucht lung mit Ciprofloxacin (Ciproxin® und Generika) vs. 14 Tage sowie einer 5-tägigen Behandlung mit Levofloxacin (Tavanic® und Generika) vs. 10 Tage bezüglich Eradikation und klinischer Heilung (2 Studien)
7–8
Kürzere Behandlung nicht unterlegen bei
Geringeres Risiko einer weite-
Intensivpatienten bezüglich Mortalität und
ren Infektion oder einer Infek-
Rezidiven (mehrere Studien)
tion mit resistenten Erregern
bei kürzerer Behandlung
4 4-tägige Behandlung nicht unterlegen im Ver- Nicht signifikant niedrigere
gleich zu durchschnittlich 8-tägiger Therapie Raten extraabdomineller resis-
bezüglich postoperativer Wundinfektionen,
tenter Infektionen bei Kurzzeit-
Rezidiven, intraabdomineller Infektionen oder behandlung
Tod (1 Studie)
(nach Llewelyn et al. 2017)
mithilfe von Biomarkern wie Procalcitonin anhand des individuellen Ansprechens über den Zeitpunkt der Beendigung der Behandlung entschieden werden. Im Rahmen ambulanter Antibiotikaapplikationen ist eine solche mehrfache Testung jedoch meist nicht durchführbar. «Alternativ könnte man den Patienten möglicherweise raten, die Therapie abzubrechen, wenn sie sich besser fühlen», schreiben Llewelyn und Kollegen. «In einer neueren klinischen Studie wurde bei ambulant erworbener Pneumonie unter Verwendung des Fieberrückgangs als Signal zur Beendigung der Behandlung die durchschnittliche Behandlungsdauer halbiert – ohne Beeinträchtigung des klinischen Erfolgs», ergänzen die For-
scher und plädieren für weitere Studien, in denen anhand des klinischen Verlaufs der bestmögliche Zeitpunkt für das Absetzen der Antibiotika ermittelt werden sollte (1).
Review systematischer Reviews: kürzere Behandlung gleichwertig
In einem Review von neun systematischen Reviews randomisierter, kontrollierter Studien gelangten Elisabeth Dawson-Hahn von der University of Washington (USA) und ihr Team zu ähnlichen Ergebnissen wie die britische Arbeitsgruppe. Auch in dem Review von Reviews erwies sich eine kürzere Antibiotikatherapie im Hinblick auf die klinische Heilung – definiert als vollständiges Abklingen der Symptome
– bei einigen bakteriellen Infektionen als ebenso wirksam wie eine längere Behandlung (2). So beobachteten die Forscher bei Kindern keinen Unterschied zwischen einer kürzeren und einer längeren Behandlung von A-StreptokokkenTonsillopharyngitis, ambulant erworbener Pneumonie, akuter Otitis media und Harnwegsinfektionen (Tabelle 2). Bei Erwachsenen beobachteten die Forscher im Hinblick auf die klinische Heilung keinen Unterschied zwischen einer kürzeren oder längeren Behandlung von akuter bakterieller Sinusitis, unkomplizierter Zystitis bei nicht schwangeren Frauen, unkomplizierter Zystitis bei älteren Frauen, akuter Pyelonephritis und ambulant erworbener Pneumonie (Tabelle 3).
ARS MEDICI 24 I 2017
1139
STUDIE REFERIERT
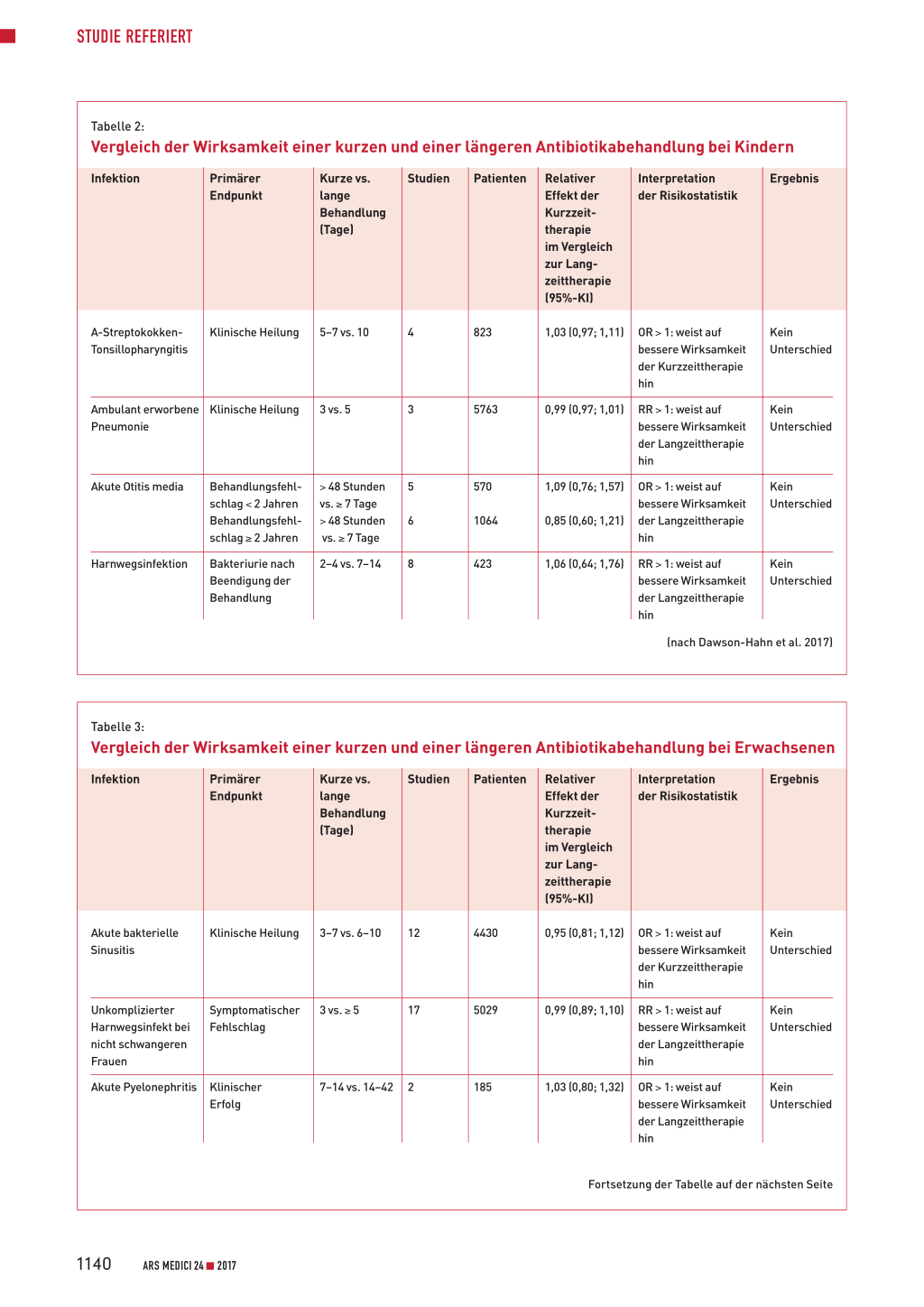
Tabelle 2:
Vergleich der Wirksamkeit einer kurzen und einer längeren Antibiotikabehandlung bei Kindern
Infektion
Primärer Endpunkt
Kurze vs. lange Behandlung (Tage)
Studien
Patienten
Relativer Effekt der Kurzzeittherapie im Vergleich zur Langzeittherapie (95%-KI)
Interpretation der Risikostatistik
Ergebnis
A-Streptokokken- Klinische Heilung 5–7 vs. 10 Tonsillopharyngitis
4
Ambulant erworbene Klinische Heilung 3 vs. 5 Pneumonie
3
Akute Otitis media Harnwegsinfektion
Behandlungsfehlschlag < 2 Jahren Behandlungsfehlschlag ≥ 2 Jahren > 48 Stunden vs. ≥ 7 Tage > 48 Stunden vs. ≥ 7 Tage
Bakteriurie nach Beendigung der Behandlung
2–4 vs. 7–14
5 6 8
823
5763
570 1064 423
1,03 (0,97; 1,11)
OR > 1: weist auf bessere Wirksamkeit der Kurzzeittherapie hin
Kein Unterschied
0,99 (0,97; 1,01)
RR > 1: weist auf bessere Wirksamkeit der Langzeittherapie hin
Kein Unterschied
1,09 (0,76; 1,57) 0,85 (0,60; 1,21)
OR > 1: weist auf bessere Wirksamkeit der Langzeittherapie hin
Kein Unterschied
1,06 (0,64; 1,76)
RR > 1: weist auf bessere Wirksamkeit der Langzeittherapie hin
Kein Unterschied
(nach Dawson-Hahn et al. 2017)
Tabelle 3:
Vergleich der Wirksamkeit einer kurzen und einer längeren Antibiotikabehandlung bei Erwachsenen
Infektion
Primärer Endpunkt
Kurze vs. lange Behandlung (Tage)
Studien
Patienten
Relativer Effekt der Kurzzeittherapie im Vergleich zur Langzeittherapie (95%-KI)
Interpretation der Risikostatistik
Ergebnis
Akute bakterielle Sinusitis
Klinische Heilung 3–7 vs. 6–10 12
Unkomplizierter Harnwegsinfekt bei nicht schwangeren Frauen
Symptomatischer Fehlschlag
3 vs. ≥ 5
17
Akute Pyelonephritis Klinischer Erfolg
7–14 vs. 14–42 2
4430 5029 185
0,95 (0,81; 1,12)
OR > 1: weist auf bessere Wirksamkeit der Kurzzeittherapie hin
0,99 (0,89; 1,10)
RR > 1: weist auf bessere Wirksamkeit der Langzeittherapie hin
1,03 (0,80; 1,32)
OR > 1: weist auf bessere Wirksamkeit der Langzeittherapie hin
Kein Unterschied
Kein Unterschied
Kein Unterschied
Fortsetzung der Tabelle auf der nächsten Seite
1140
ARS MEDICI 24 I 2017
STUDIE REFERIERT
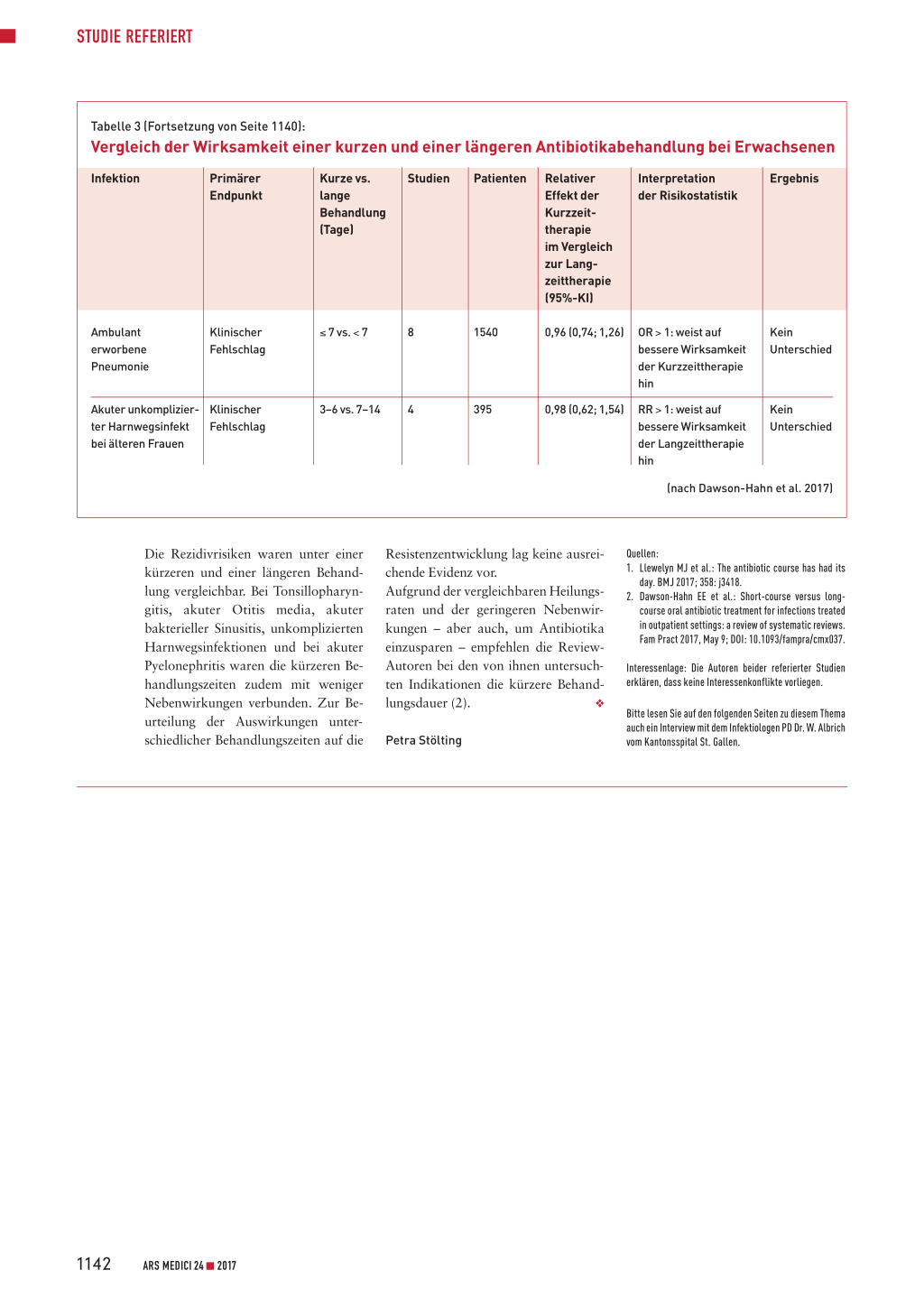
Tabelle 3 (Fortsetzung von Seite 1140):
Vergleich der Wirksamkeit einer kurzen und einer längeren Antibiotikabehandlung bei Erwachsenen
Infektion
Primärer Endpunkt
Kurze vs. lange Behandlung (Tage)
Studien
Patienten
Relativer Effekt der Kurzzeittherapie im Vergleich zur Langzeittherapie (95%-KI)
Interpretation der Risikostatistik
Ergebnis
Ambulant erworbene Pneumonie
Klinischer Fehlschlag
Akuter unkomplizier- Klinischer ter Harnwegsinfekt Fehlschlag bei älteren Frauen
≤ 7 vs. < 7 8 3–6 vs. 7–14 4 1540 395 0,96 (0,74; 1,26) OR > 1: weist auf bessere Wirksamkeit der Kurzzeittherapie hin
Kein Unterschied
0,98 (0,62; 1,54)
RR > 1: weist auf bessere Wirksamkeit der Langzeittherapie hin
Kein Unterschied
(nach Dawson-Hahn et al. 2017)
Die Rezidivrisiken waren unter einer kürzeren und einer längeren Behandlung vergleichbar. Bei Tonsillopharyngitis, akuter Otitis media, akuter bakterieller Sinusitis, unkomplizierten Harnwegsinfektionen und bei akuter Pyelonephritis waren die kürzeren Behandlungszeiten zudem mit weniger Nebenwirkungen verbunden. Zur Beurteilung der Auswirkungen unterschiedlicher Behandlungszeiten auf die
Resistenzentwicklung lag keine ausrei-
chende Evidenz vor.
Aufgrund der vergleichbaren Heilungs-
raten und der geringeren Nebenwir-
kungen – aber auch, um Antibiotika
einzusparen – empfehlen die Review-
Autoren bei den von ihnen untersuch-
ten Indikationen die kürzere Behand-
lungsdauer (2).
O
Petra Stölting
Quellen: 1. Llewelyn MJ et al.: The antibiotic course has had its
day. BMJ 2017; 358: j3418. 2. Dawson-Hahn EE et al.: Short-course versus long-
course oral antibiotic treatment for infections treated in outpatient settings: a review of systematic reviews. Fam Pract 2017, May 9; DOI: 10.1093/fampra/cmx037.
Interessenlage: Die Autoren beider referierter Studien erklären, dass keine Interessenkonflikte vorliegen.
Bitte lesen Sie auf den folgenden Seiten zu diesem Thema auch ein Interview mit dem Infektiologen PD Dr. W. Albrich vom Kantonsspital St. Gallen.
1142
ARS MEDICI 24 I 2017