Transkript
FORTBILDUNG
Management der chronischen Hepatitis B
Leitliniengemässe Diagnostik und Therapieoptionen
Nach einer Infektion mit dem Hepatitis-B-Virus (HBV)
kommt es bei bis zu 5 Prozent der Erwachsenen und bei
mehr als 90 Prozent der Neugeborenen zur Chronifizie-
rung der Erkrankung. Amerikanische Wissenschaftler
haben den aktuellen Wissensstand zum Verlauf, zur Dia-
gnose und zur Behandlung der chronischen Hepatitis B in
einem Review zusammengefasst.
British Medical Journal
Seit der Einführung einer Impfung gegen das Hepatitis-BVirus (HBV) im Jahr 1981 hat die Häufigkeit der Infektionen beträchtlich abgenommen. Dennoch leiden derzeit nach Schätzungen der Weltgesundheitsorganisation (WHO) weltweit etwa 240 Millionen Menschen unter einer chronischen Hepatitis B (CHB). Bei etwa 30 Prozent der Betroffenen entwickelt sich eine Leberzirrhose, und bei etwa 23 Prozent dieser Zirrhosepatienten kommt es innerhalb von 5 Jahren zur Dekompensation (Abbildung 1). Das Risiko für die Entwicklung hepatozellulärer Karzinome (HCC) ist bei Patienten mit CHB ebenfalls erhöht. Zu den Regionen mit hoher HBV-Prävalenz (> 7%) gehören China, Südostasien, Afrika, die Pazifikinseln, Teile des mittleren Ostens und das Amazonasbecken. Eine mittlere Verbreitungshäufigkeit (2–7%) wird in Zentral- und Südwestasien sowie in Ost- und Südeuropa, in Russland, in Zentralamerika und in Südamerika beobachtet. In den USA, in Westeuropa, in Australien und in Japan beträgt die HBVPrävalenz weniger als 2 Prozent. Nach Angaben der Schweizerischen Expertengruppe für virale Hepatitis (Swiss Experts in Viral Hepatitis, SEVHep) leben in der Schweiz etwa 24 000 Personen mit Hepatitis B.
MERKSÄTZE
O Eine antivirale Behandlung senkt das Risiko für die Entwicklung von Leberzirrhose und Leberkrebs.
O Für eine zeitlich begrenzte Therapie steht pegyliertes Interferon zur Verfügung.
O Die Langzeitbehandlung mit Nukleos(t)idanaloga kann eine Reversion der Fibrose und der Zirrhose bewirken.
Die Ansteckung durch kontaminiertes Blut oder andere Körperflüssigkeiten erfolgt vorwiegend über ungeschützten Geschlechtsverkehr. In Regionen mit hoher HBV-Prävalenz wird das Virus auch häufig perinatal übertragen.
Serologische Indikatoren
Die Hepatitis B wird durch verschiedene serologische Indikatoren charakterisiert: O Als primärer Marker einer HBV-Infektion gilt die Serum-
konzentration des Hepatitis-B-Oberflächenantigens (HBsAg). Die regelmässige Bestimmung des HBsAg-Spiegels ist zur Evaluierung des Erkrankungsverlaufs und des Behandlungserfolgs von Nutzen. O Der Hepatitis-B-Oberflächenantikörper (Anti-HBs) richtet sich gegen das HBsAg und gilt als ein Indikator für die Immunität gegenüber dem HBV. O Der gegen das intrazelluläre Kernantigen HBc-IgM gerichtete Hepatitis-B-Kern-Antikörper (Anti-HBc-IgM) weist auf eine akute Infektion hin. Der Anti-HBc-IgM-Spiegel kann aber auch während einer Exazerbation der CHB erhöht sein. O Der Hepatitis-B-Kern-Antikörper Anti-HBc-IgG bindet an das Kernatigen HBc-IgG und gilt als Marker der CHB. O Beim HBV-Be-Antigen (HBeAg) handelt es sich um ein sekretorisches Protein im Zusammenhang mit der Virusreplikation. An dieses Antigen bindet der HBe-Antikörper (Anti-HBe).
Klinischer Verlauf
Der Verlauf der HBV-Infektion kann in vier Stadien unterteilt werden. Nach der Ansteckung durchlaufen die Patienten zunächst eine Immuntoleranzphase. Dieser Zeitraum ist durch die Präsenz von HBeAg, hohe HBV-DNA-Serumspiegel (> 20 000 IU/ml), normale Alaninaminotranferase-(ALT-) und hohe HBsAG-Werte gekennzeichnet (Abbildung 2). Während der Immuntoleranzphase verhält sich das Virus nicht zytopathisch, und die Leberentzündung ist nur geringfügig ausgeprägt. Anschliessend versucht das Immunsystem, infizierte Hepatozyten über eine T-Zell-mediierte Immunreaktion zu eliminieren, was zur Apoptose der betroffenen Leberzellen führt. In dieser Immuneliminierungsphase steigt die ALT-Konzentration über die Normwerte an, die HBV-DNA-Spiegel schwanken, und es kommt zur Leberentzündung. Die Immunreaktion führt bei vielen Patienten zu einer HBeAg-Serokonversion (definiert als Verschwinden von HBeAg) und zur Entwicklung von Anti-HBe-Antikörpern.
158
ARS MEDICI 4 I 2016
FORTBILDUNG
Leberkrebs
Bei 4–6% der Patienten mit chronischer HBV-Infektion entwickelt sich ein HCC.
Akute Infektion
Y Bei < 90% der infizierten Kinder entwickelt sich eine CHB.
Y Bei > 5% der infizierten Erwachsenen entwickelt sich eine CHB.
Chronische Infektion
Leberzirrhose
Bei 30% der Patienten mit chronischer HBV-Infektion entwickelt sich eine Leberzirrhose.
Leberversagen (Dekompensation)
Bei 23% der Patienten mit einer Leberzirrhose kommt es innerhalb von 5 Jahren zur Dekompensation.
Lebertransplantation
Tod
Abbildung 1: Natürlicher Verlauf der Hepatitis B (CHB: chronische Hepatitis-B-Infektion; HBV: Hepatitis-B-Virus; HCC: hepatozelluläres Karzinom; nach Sundaram und Kowdley 2015)
HBV-DNA
HBV-DNA ALT HBeAg Anti-HBe
HBeAg
Anti-HBe
Diagnose und Evaluierung
Die Diagnose der Hepatitis B wird durch den Nachweis von HBsAg gestellt. Des Weiteren wird die Erkrankung anhand der Bestimmung der ALT-, der HBV-DNA- und der AntiHBc-IgG-Spiegel sowie durch die Evaluierung des HBeAgund des Leberzirrhosestatus charakterisiert. Ergänzend empfehlen Leitlinienexperten ein Screening im Hinblick auf Koinfektionen mit HIV (humanes Immundefizienzvirus) oder mit Hepatitis C.
Immuntoleranz gering
Immun-Clearence mittel/schwer
histologische Leberaktivität mittel/schwer
Inaktiver Carrier-Status
keine/gering
Abbildung 2: Phasen der Hepatitis-B-Virus-(HBV-)Infektion (HBeAg: HBV-Be-Antigen; Anti-HBe: HBe-Antikörper; DNA: Desoxyribonukleinsäure; ALT: Alaninaminotranferase; nach Sundaram und Kowdley 2015)
Der nachfolgende inaktive Trägerstatus ist durch eine HBsAg-Präsenz im Serum, eine HBeAg-Serokonversion, niedrige HBV-DNA-Serumkonzentrationen (< 2000 IU/ml) und ALT-Werte im Normbereich gekennzeichnet. In dieser Phase unbestimmter Dauer kommt es bei manchen Patienten auch zum Verschwinden von HBsAg.
HBeAg-negative chronische Hepatitis B
Nach der HBeAg-Serokonversion kommt es in einigen Fällen zur Reaktivierung des HBV und somit zu einer HBeAg-negativen CHB. Bei diesen Patienten besteht im Vergleich zur HBeAg-positiven Erkrankungsform ein doppelt so hohes Risiko für die Progression zur Zirrhose. Inaktive Träger und Patienten mit HBeAg-negativer Hepatitis B sollten sorgfältig voneinander unterschieden werden, weil Letztere von einer antiviralen Behandlung profitieren.
Behandlungsbeginn
Für Patienten mit dekompensierter Leberzirrhose empfehlen alle Leitlinien die Behandlung mit Nukleos(t)idanaloga. Im Hinblick auf den Behandlungsbeginn bei Patienten mit kompensierter Zirrhose sind die Fachgesellschaften unterschiedlicher Meinung. Während die europäische Leitlinie der EASL auch für alle Patienten mit kompensierter Leberzirrhose eine Behandlung empfiehlt, raten amerikanische Experten der AASLD und der APASL erst ab einer Viruslast von 2000 IU/ml zum Therapiebeginn (Tabelle 1). Für Patienten ohne Zirrhose in der Immuntoleranzphase und für inaktive Träger empfehlen die Leitlinienexperten eine Überwachung der ALT- und der HBV-RNA-Werte im Abstand von drei Monaten. Da bei inaktiven Trägern das Risiko für die Entwicklung eines HCC erhöht ist, sollte bei ihnen zusätzlich ein entsprechendes Monitoring durchgeführt werden. Bei allen anderen Patienten basiert die Entscheidung für einen Therapiebeginn auf dem HBeAg-Status, der ALTSerumkonzentration, der HBV-Last, dem Alter (< 40 vs. > 40 Jahre) und dem Stadium der Leberzirrhose. Bei Männern gilt eine ALT-Konzentration von 30 U/l und bei Frauen eine ALT-Konzentration von 19 U/l als obere Normgrenze.
Behandlungsstrategien
Das wichtigste Behandlungsziel besteht in der Verminderung der HBV-Last, weil diese eng mit dem Progressionsrisiko
ARS MEDICI 4 I 2016
159
FORTBILDUNG
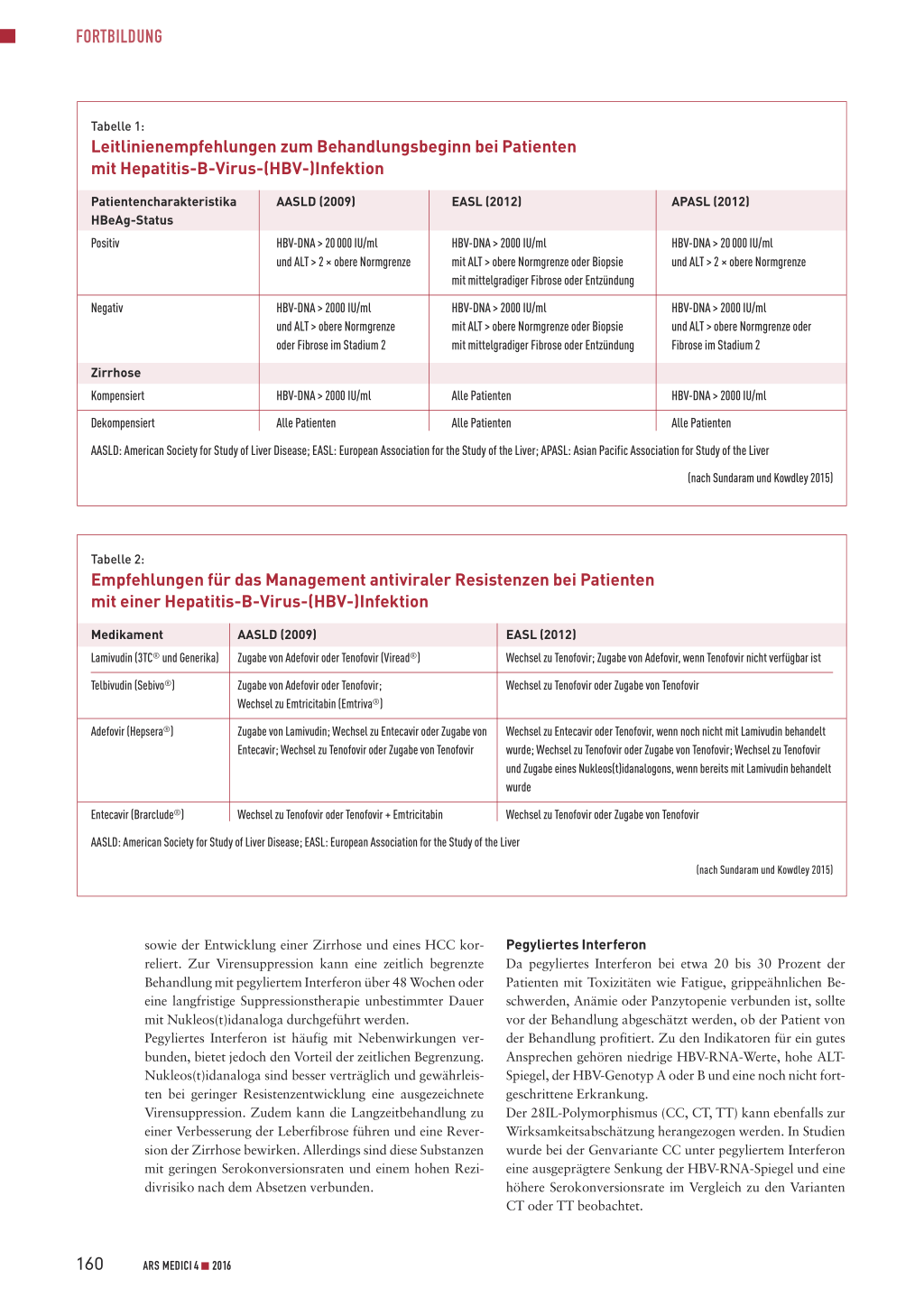
Tabelle 1:
Leitlinienempfehlungen zum Behandlungsbeginn bei Patienten mit Hepatitis-B-Virus-(HBV-)Infektion
Patientencharakteristika HBeAg-Status
Positiv
AASLD (2009)
HBV-DNA > 20 000 IU/ml und ALT > 2 × obere Normgrenze
EASL (2012)
HBV-DNA > 2000 IU/ml mit ALT > obere Normgrenze oder Biopsie mit mittelgradiger Fibrose oder Entzündung
APASL (2012)
HBV-DNA > 20 000 IU/ml und ALT > 2 × obere Normgrenze
Negativ
HBV-DNA > 2000 IU/ml und ALT > obere Normgrenze oder Fibrose im Stadium 2
HBV-DNA > 2000 IU/ml mit ALT > obere Normgrenze oder Biopsie mit mittelgradiger Fibrose oder Entzündung
HBV-DNA > 2000 IU/ml und ALT > obere Normgrenze oder Fibrose im Stadium 2
Zirrhose
Kompensiert
HBV-DNA > 2000 IU/ml
Alle Patienten
HBV-DNA > 2000 IU/ml
Dekompensiert
Alle Patienten
Alle Patienten
Alle Patienten
AASLD: American Society for Study of Liver Disease; EASL: European Association for the Study of the Liver; APASL: Asian Pacific Association for Study of the Liver
(nach Sundaram und Kowdley 2015)
Tabelle 2:
Empfehlungen für das Management antiviraler Resistenzen bei Patienten mit einer Hepatitis-B-Virus-(HBV-)Infektion
Medikament
AASLD (2009)
Lamivudin (3TC® und Generika) Zugabe von Adefovir oder Tenofovir (Viread®)
EASL (2012) Wechsel zu Tenofovir; Zugabe von Adefovir, wenn Tenofovir nicht verfügbar ist
Telbivudin (Sebivo®)
Zugabe von Adefovir oder Tenofovir; Wechsel zu Emtricitabin (Emtriva®)
Wechsel zu Tenofovir oder Zugabe von Tenofovir
Adefovir (Hepsera®)
Zugabe von Lamivudin; Wechsel zu Entecavir oder Zugabe von Entecavir; Wechsel zu Tenofovir oder Zugabe von Tenofovir
Wechsel zu Entecavir oder Tenofovir, wenn noch nicht mit Lamivudin behandelt wurde; Wechsel zu Tenofovir oder Zugabe von Tenofovir; Wechsel zu Tenofovir und Zugabe eines Nukleos(t)idanalogons, wenn bereits mit Lamivudin behandelt wurde
Entecavir (Brarclude®)
Wechsel zu Tenofovir oder Tenofovir + Emtricitabin
Wechsel zu Tenofovir oder Zugabe von Tenofovir
AASLD: American Society for Study of Liver Disease; EASL: European Association for the Study of the Liver
(nach Sundaram und Kowdley 2015)
sowie der Entwicklung einer Zirrhose und eines HCC korreliert. Zur Virensuppression kann eine zeitlich begrenzte Behandlung mit pegyliertem Interferon über 48 Wochen oder eine langfristige Suppressionstherapie unbestimmter Dauer mit Nukleos(t)idanaloga durchgeführt werden. Pegyliertes Interferon ist häufig mit Nebenwirkungen verbunden, bietet jedoch den Vorteil der zeitlichen Begrenzung. Nukleos(t)idanaloga sind besser verträglich und gewährleisten bei geringer Resistenzentwicklung eine ausgezeichnete Virensuppression. Zudem kann die Langzeitbehandlung zu einer Verbesserung der Leberfibrose führen und eine Reversion der Zirrhose bewirken. Allerdings sind diese Substanzen mit geringen Serokonversionsraten und einem hohen Rezidivrisiko nach dem Absetzen verbunden.
Pegyliertes Interferon
Da pegyliertes Interferon bei etwa 20 bis 30 Prozent der Patienten mit Toxizitäten wie Fatigue, grippeähnlichen Beschwerden, Anämie oder Panzytopenie verbunden ist, sollte vor der Behandlung abgeschätzt werden, ob der Patient von der Behandlung profitiert. Zu den Indikatoren für ein gutes Ansprechen gehören niedrige HBV-RNA-Werte, hohe ALTSpiegel, der HBV-Genotyp A oder B und eine noch nicht fortgeschrittene Erkrankung. Der 28IL-Polymorphismus (CC, CT, TT) kann ebenfalls zur Wirksamkeitsabschätzung herangezogen werden. In Studien wurde bei der Genvariante CC unter pegyliertem Interferon eine ausgeprägtere Senkung der HBV-RNA-Spiegel und eine höhere Serokonversionsrate im Vergleich zu den Varianten CT oder TT beobachtet.
160
ARS MEDICI 4 I 2016
FORTBILDUNG
In einer der grössten Studien zur Wirksamkeit von pegylierten Interferonen, an der 814 HBeAg-positive Patienten teilnahmen, war die Serokonversionsrate von HBeAg zu AntiHBeAg unter einer Monotherapie mit pegyliertem Interferon im Vergleich zu Lamivudin allein (32% vs. 19%; p < 0,001) oder einer Kombination beider Medikamente (27% vs. 19%; p = 0,02) signifikant höher. In anderen Studien war eine Kombination von pegyliertem Interferon mit Nukleos(t)idanaloga oder mit Ribavirin (Copegus®, Rebetol®) nicht mit besseren Ansprechraten verbunden als die Monotherapie mit pegyliertem Interferon. Pegyliertes Interferon sollte vorzeitig abgesetzt werden, wenn der HBV-DNA-Serumspiegel nicht unter 20 000 IU/ml abgesenkt werden kann oder wenn in Woche 12 oder 24 keine Reduzierung des HBsAg-Spiegels unter 1500 IU/ml erreicht wird. Nukleos(t)idanaloga Zur Behandlung der CHB stehen verschiedene Nukleos(t)idanaloga wie Lamivudin, Adefovir, Telbivudin, Entecavir und Tenofovir zur Verfügung. In internationalen Richtlinien werden für Patienten, die noch nicht mit dieser Substanzklasse behandelt wurden, jedoch nur Entecavir und Tenofovir als Erstlinientherapie empfohlen. Entecavir: In Zulassungsstudien erzielte Entecavir im Vergleich zu Lamivudin bei HBeAg-positiven und -negativen Patienten innerhalb von 48 Wochen eine signifikant bessere Wirksamkeit zur Absenkung der HBV-DNA-Spiegel unter die Nachweisgrenze und zur Normalisierung der ALT-Konzentration. In einer Beobachtungsstudie zeigte sich bei therapienaiven Patienten eine kumulative Wahrscheinlichkeit von 1,2 Prozent für eine Resistenzbildung gegenüber Entecavir. Bei lamivudinrefraktären Patienten wurde unter Entecavir eine kumulative Wahrscheinlichkeit von 51 Prozent für die Entwicklung resistenter Mutationen beobachtet. Tenofovir: In randomisierten kontrollierten Studien mit 846 HBeAg-positiven und 603 HBeAg-negativen Patienten wurden mit Tenofovir im Vergleich zu Adefovir bei einem signifikant höheren Patientenanteil eine Normalisierung der ALTWerte (68% vs. 54%; p = 0,03) und ein Verschwinden von HBsAg (3% vs. 0%; p = 0,02) erreicht. Zudem wurden in dieser Patientenkohorte auch nach 8 Jahren Langzeitbehandlung keine Resistenzmutationen beobachtet. Bei zu Behandlungsbeginn HBeAg-positiven Patienten kann 6 bis 12 Monate nach der Anti-HBe-Serokonversion ein Absetzen der Nukleos(t)idanaloga in Betracht gezogen werden. Bei zuvor HBeAg-negativer Erkrankungsform kann die Behandlung nach dem Verschwinden von HBsAg beendet werden. Antivirale Resistenzen Bei antiviralen Resistenzen sollte ein Medikament ohne Kreuzresistenz gegenüber der jeweiligen Mutation ausge- wählt werden. Bei Resistenzen gegen Lamivudin oder Adefo- vir ist ein Wechsel zu Tenofovir eine geeignete Option. Auch Entecavir hat sich bei Resistenzen gegen Adefovir als wirk- sam erwiesen (Tabelle 2). O Petra Stölting Quelle: Sundaram V, Kowdley K: Management of chronic hepatitis B infection. BMJ 2015; 351: h4263. Interessenkonflikte: Beide Autoren haben Gelder von verschiedenen Pharmaunternehmen erhalten. ARS MEDICI 4 I 2016 161