Transkript
FORTBILDUNG
Interstitielle Zystitis
Symptomatik, Diagnostik und Behandlungsoptionen des unterschätzten Leidens
Die interstitielle Zystitis ist eine schwere, die Lebensqualität einschränkende Krankheit. Oft dauert es Jahre, bis den Patientinnen die richtige Diagnose und auch die richtige Behandlung zukommt. Die Anamnese und die sorgfältige Abklärung von Patientinnen mit chronischen Schmerzen im Blasen-/Beckenbereich sind die Grundlage der Diagnose und Basis für die Einleitung der entsprechenden Therapie.
SONJA BRANDNER
schen Studien sind die Kosten höher als jene der Behandlung von Diabetikern, Asthmakranken oder Hypertonikern (2). Die Prävalenz ist aufgrund der Heterogenität des Krankheitsbildes und der Überlappung verschiedener Schmerzsyndrome schwierig abzuschätzen. Wahrscheinlich sind rund 1 Prozent der Frauen betroffen. PBS ist wahrscheinlich assoziiert mit anderen Schmerzsyndromen wie Reizdarm (IBS), Chronic Fatigue Syndrome und Fibromyalgie. In der Vorgeschichte findet man eine Anamnese von rezidivierenden Harnwegsinfekten, «Blasenprobleme» in der Kindheit sowie eine erhöhte Rate von sexuellem Missbrauch und physischer Gewalt (3).
Aufgrund der Diversität der Symptome ist der Begriff der interstitiellen Zystitis (IC) durch den Begriff «Painfull Bladder Syndrome» (PBS) abgelöst worden. Dies trägt der Vielfalt der Symptome und Erscheinungsformen der interstitiellen Zystitis besser Rechnung. Die Internationale Kontinenzgesellschaft (ICS) definiert in ihrer Terminologie das Bladder Pain Syndrome (im Folgenden IC/PBS genannt) wie folgt: «Painful bladder syndrome is the complaint of suprapubic pain related to bladder filling, accompanied by other symptoms such as increased daytime and nighttime frequency, in the absence of proven urinary infection or other obvious pathology» (1).
Problematisches Krankheitsbild Neben dem erheblichen Leidensdruck der Patientinnen verursachen die Betreuung und Behandlung der interstitiellen Zystitis immense Kosten. Nach Schätzungen aus amerikani-
Merksätze
O Bei Patientinnen mit Schmerzen im Becken, Drang und Pollakisurie immer an «Painful Bladder Syndrome» (PBS) denken!
O Keine rezidivierende Antibiotikatherapie ohne Keim- und Resistenznachweis im Katheterurin!
O Ein adäquates Schmerzmanagement steht am Anfang des individualisierten Therapieplanes.
O Konservative, nicht invasive Therapien vor irreversible Behandlungen stellen!
Ätiologie Die Pathogenese der IC basiert nach wie vor auf verschiedenen Hypothesen. Die meistbeachtete geht davon aus, dass am Anfang ein Schaden am Urothel respektive an der GAGSchicht (= Glykosamin-Glykan-Schicht) besteht. Durch erhöhte Permeabilität des Urothels werden verschiedene Inflammationsprozesse in Gang gesetzt. Diese führen zur Reizung der Schmerzfasern und zu einer immunologischen Antwort. Diese Prozesse erklären die progressive Blasenfunktionsstörung und den neuropathischen Schmerz. Des Weiteren wurde festgestellt, dass Patientinnen mit IC/PBS ähnlich anderen chronischen Schmerzpatientinnen eine zentrale Alteration des Schmerzempfindens aufweisen.
Klinik Das Leitsymptom ist der Schmerz, meist begleitet von Drang (84%) und Pollakisurie (92%). Dabei ist wegweisend, dass die Beschwerden in Zusammenhang mit der Blasenfüllung und -entleerung auftreten. Dysurie fehlt meistens. Patientinnen mit interstitieller Zystitis weisen selten eine funktionelle Blasenkapazität von über 150 ml auf. Miktionstagebuch und Schmerzkalender sind einfache und hilfreiche Instrumente, um sich im klinischen Alltag einen Überblick über die Symptomatik zu machen. Lebensqualitäts- oder spezielle Blasenschmerzfragebögen können dabei eingesetzt werden. Sie sind im englischen Sprachraum weitverbreitet, nicht alle sind in Deutsch validiert. Ein sehr bewährtes Instrument, unter anderem für die Beurteilung des Therapieerfolges, ist die Visual-Analog-Skala (VAS). Diese misst das subjektive Schmerzempfinden. Die Durchführung ist einfach, nicht zeitintensiv und gut verständlich auch für Patientinnen mit anderem Sprachhintergrund oder Analphabeten (Abbildung 1 und 2; Miktionskalender und VAS).
ARS MEDICI 18 I 2014
903
FORTBILDUNG
lose Hämaturie verursacht. Bei steriler Leukozyturie sollte eine TBC mittels Langzeitkultur ausgeschlossen werden (Tabelle 1). Die erweiterte Anamnese soll andere mögliche Ursachen der Blasenschmerzen eruieren. Bei zyklischen Blasenschmerzen, verbunden mit zyklischer Makrohämaturie, ist an eine vesikale Endometriose zu denken. Die radiogene oder diabetische Vesikopathie sind weitere Differenzialdiagnosen, die in die klinische Beurteilung miteinbezogen werden sollten.
Abbildung 1: Typischer Miktionskalender
Abbildung 2: Visual-Analog-Skala zur Erfassung der Schmerzintensität
Tabelle 1:
Basisdiagnostik
O Restharn O Schmerzmapping O grobkursorischer Neurostatus (Sensibilität Wurzeln S2–S4,
Bulbokavernosus- und Analreflex) O Urinsediment und -kultur (Einmalkatheter) O gynäkologische Untersuchung inkl. Transvaginalschall zum
Ausschluss pelviner Masse, Hernie, Deszensus O Beckenbodentesting (Hypertonus), Triggerpunkte
Diagnostik Die Anamnese und der Miktionskalender sind wegweisend. Differenzialdiagnostisch kommen verschiedene gynäkologische und nicht gynäkologische Ursachen der Schmerzen infrage, weshalb eine Minimaldiagnostik vor Therapiebeginn sinnvoll ist. Bei entsprechender Anamnese (Raucherinnen, Anillinexposition, Mikro-/Makrohämaturie) ist ein Blasenkarzinom auszuschliessen, wobei dieses meist eine schmerz-
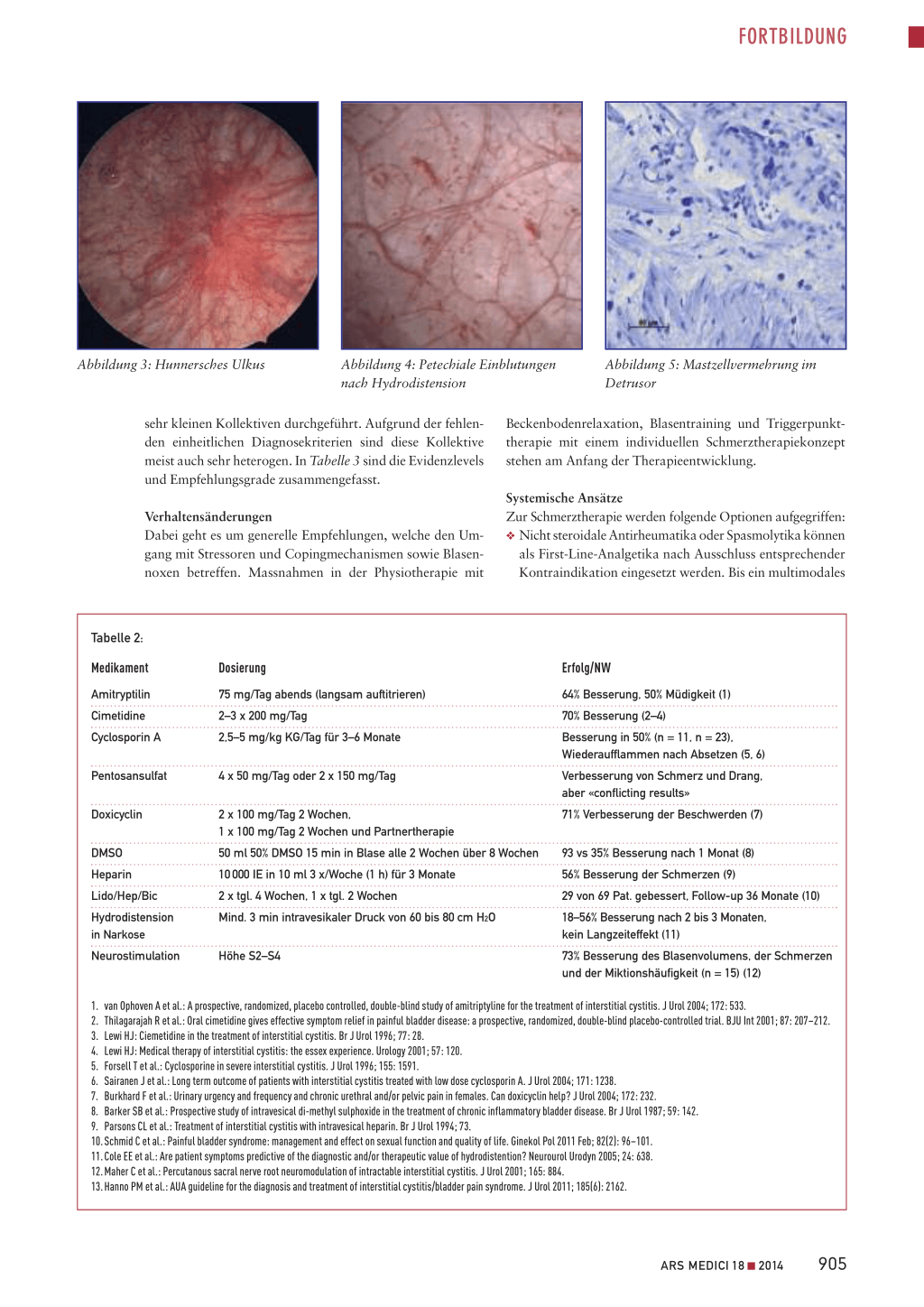
Die Rolle der Zystoskopie und der Urodynamik Primär dient die Zystoskopie dem Ausschluss intravesikaler Pathologien wie zum Beispiel Blasensteine oder Blasenkarzinome. Eine neuere Studie aus Asien hat ein leicht erhöhtes Risiko für Blasenkarzinome bei IC/PBS-Patientinnen gezeigt, weshalb die Zystoskopie bei therapieresistenten Patientinnen und bei Nachweis einer Mikrohämaturie sinnvoll erscheint. Zur Primärdiagnose einer interstitiellen Zystitis ist die Zystoskopie nur bedingt hilfreich. Typische Befunde bei der interstitiellen Zystitis sind petechiale Einblutungen (Abbildung 4) im Hydrodistensionstest oder Hunnersche Ulzera (Abbildung 3). Nicht alle Patientinnen mit Hunnerschen Läsionen/Petechien haben Symptome und umgekehrt. Somit bleibt der Stellenwert der Zystoskopie im Abklärungsschema dieser Patientinnen umstritten. In der muskeltiefen Biopsie kann typischerweise eine Mastzellvermehrung (> 28/mm2) nachgewiesen werden (Abbildung 5). Therapeutisch geben in einer Studie von Ottem 56 Prozent der Patientinnen eine Schmerzbesserung nach Hydrodistension an. Der Effekt hielt maximal zwei Monate an (4). Der Stellenwert der Urodynamik ist ebenfalls umstritten. Es gilt, die 12 bis 20 Prozent der Patientinnen mit einer Detrusorhyperaktivität herauszufiltern (5). Dieser Anteil der Betroffenen spricht auf Anticholinergika an. Im Endstadium der Erkrankung kann eine «Low-compliance-Blase» bestehen, was therapeutische Konsequenzen hat. Wir empfehlen bei therapieresistenten Patientinnen mit fehlender Erhöhung der Blasenkapazität nach Therapie, eine Urodynamik zum Ausschluss einer «Low-compliance-Blase» durchzuführen.
Therapieoptionen Im Grundsatz gilt, bei chronischen Krankheiten konservativen und reversiblen Therapieoptionen den Vorrang vor der Chirurgie zu geben. Die individualisierte Schmerztherapie stellt die Basis der Therapie dar. Ein interdisziplinäres und interprofessionelles Konzept ist insbesondere bei Assoziation mit anderen Krankheitsbildern sinnvoll (Rheumatologie, Gastroenterologie, Physiotherapie usw.). Die Therapiewahl muss individuell mit der Patientin zusammen erfolgen. Massgeschneiderte Therapien haben die grössten Erfolgsaussichten. Die möglichen negativen Effekte müssen sorgfältig gegen den zu erwarteten Nutzen abgewogen werden. Bei jedem Therapiebeginn oder -wechsel soll eine Standortbestimmung, zum Beispiel in Form der Erfassung der Symptomatik auf der VAS-Schmerzskala und mittels Miktionskalender, erfolgen, und mit dem gleichen Instrument soll der Therapieerfolg überprüft werden. Insgesamt ist die Datenlage betreffend die verschiedenen Therapieoptionen sehr dürftig. Die meisten Studien sind mit
904
ARS MEDICI 18 I 2014
FORTBILDUNG
Abbildung 3: Hunnersches Ulkus
Abbildung 4: Petechiale Einblutungen nach Hydrodistension
Abbildung 5: Mastzellvermehrung im Detrusor
sehr kleinen Kollektiven durchgeführt. Aufgrund der fehlenden einheitlichen Diagnosekriterien sind diese Kollektive meist auch sehr heterogen. In Tabelle 3 sind die Evidenzlevels und Empfehlungsgrade zusammengefasst.
Verhaltensänderungen Dabei geht es um generelle Empfehlungen, welche den Umgang mit Stressoren und Copingmechanismen sowie Blasennoxen betreffen. Massnahmen in der Physiotherapie mit
Beckenbodenrelaxation, Blasentraining und Triggerpunkttherapie mit einem individuellen Schmerztherapiekonzept stehen am Anfang der Therapieentwicklung.
Systemische Ansätze Zur Schmerztherapie werden folgende Optionen aufgegriffen: O Nicht steroidale Antirheumatika oder Spasmolytika können
als First-Line-Analgetika nach Ausschluss entsprechender Kontraindikation eingesetzt werden. Bis ein multimodales
Tabelle 2: Medikament Amitryptilin Cimetidine Cyclosporin A
Pentosansulfat
Doxicyclin
DMSO Heparin Lido/Hep/Bic Hydrodistension in Narkose Neurostimulation
Dosierung 75 mg/Tag abends (langsam auftitrieren) 2–3 x 200 mg/Tag 2,5–5 mg/kg KG/Tag für 3–6 Monate
4 x 50 mg/Tag oder 2 x 150 mg/Tag
2 x 100 mg/Tag 2 Wochen, 1 x 100 mg/Tag 2 Wochen und Partnertherapie 50 ml 50% DMSO 15 min in Blase alle 2 Wochen über 8 Wochen 10 000 IE in 10 ml 3 x/Woche (1 h) für 3 Monate 2 x tgl. 4 Wochen, 1 x tgl. 2 Wochen Mind. 3 min intravesikaler Druck von 60 bis 80 cm H2O
Höhe S2–S4
Erfolg/NW
64% Besserung, 50% Müdigkeit (1) 70% Besserung (2–4) Besserung in 50% (n = 11, n = 23), Wiederaufflammen nach Absetzen (5, 6) Verbesserung von Schmerz und Drang, aber «conflicting results» 71% Verbesserung der Beschwerden (7)
93 vs 35% Besserung nach 1 Monat (8) 56% Besserung der Schmerzen (9) 29 von 69 Pat. gebessert, Follow-up 36 Monate (10) 18–56% Besserung nach 2 bis 3 Monaten, kein Langzeiteffekt (11) 73% Besserung des Blasenvolumens, der Schmerzen und der Miktionshäufigkeit (n = 15) (12)
1. van Ophoven A et al.: A prospective, randomized, placebo controlled, double-blind study of amitriptyline for the treatment of interstitial cystitis. J Urol 2004; 172: 533. 2. Thilagarajah R et al.: Oral cimetidine gives effective symptom relief in painful bladder disease: a prospective, randomized, double-blind placebo-controlled trial. BJU Int 2001; 87: 207–212. 3. Lewi HJ: Ciemetidine in the treatment of interstitial cystitis. Br J Urol 1996; 77: 28. 4. Lewi HJ: Medical therapy of interstitial cystitis: the essex experience. Urology 2001; 57: 120. 5. Forsell T et al.: Cyclosporine in severe interstitial cystitis. J Urol 1996; 155: 1591. 6. Sairanen J et al.: Long term outcome of patients with interstitial cystitis treated with low dose cyclosporin A. J Urol 2004; 171: 1238. 7. Burkhard F et al.: Urinary urgency and frequency and chronic urethral and/or pelvic pain in females. Can doxicyclin help? J Urol 2004; 172: 232. 8. Barker SB et al.: Prospective study of intravesical di-methyl sulphoxide in the treatment of chronic inflammatory bladder disease. Br J Urol 1987; 59: 142. 9. Parsons CL et al.: Treatment of interstitial cystitis with intravesical heparin. Br J Urol 1994; 73. 10. Schmid C et al.: Painful bladder syndrome: management and effect on sexual function and quality of life. Ginekol Pol 2011 Feb; 82(2): 96–101. 11. Cole EE et al.: Are patient symptoms predictive of the diagnostic and/or therapeutic value of hydrodistention? Neurourol Urodyn 2005; 24: 638. 12. Maher C et al.: Percutanous sacral nerve root neuromodulation of intractable interstitial cystitis. J Urol 2001; 165: 884. 13. Hanno PM et al.: AUA guideline for the diagnosis and treatment of interstitial cystitis/bladder pain syndrome. J Urol 2011; 185(6): 2162.
ARS MEDICI 18 I 2014
905
FORTBILDUNG
Tabelle 3:
Evidenzlevels/Empfehlungsgrad
Therapieform Verhaltensänderung Physiotherapie Stressreduktion Diätetische Massnahmen DMSO-Instillation Lidocain Botox Neuromodulation Resektion Hunnersche Ulzera Zystektomie mit Neoblase
Evidenzlevel 3 3 4 4 2 2 4 3 3 3
Empfehlungsgrad C C C C B C D C C C
Erstlinienbehandlung
Stressmanagement, Beckenbodenrelaxation,
Blasentraining, Schmerzmanagement
Zweitlinienbehandlung
Oral: Amitryptyline (Cimetidine, Elmiron®) intravesikal: DMSO, Lido-Heparin-Bicarbonat
Drittlinienbehandlung Zystoskopie mit Hydrodistension und Behandlung von Hunnerschen Ulzera
Fünftlinienbehandlung Cyclosporin A
Botoxinjektion in Detrusor
Viertlinienbehandlung Neuromodulation
Sechstlinienbehandlung
Blasenaugmentation oder Zystektomie
Abbildung 6: Therapieschritte adaptiert nach AUA-Guidelines 2011 (Treatment Algorithm)
Therapiekonzept greift, sind oft auch potentere Schmerzmittel aus der Opiatgruppe nötig. Diese werden nach den üblichen WHO-Empfehlungen eingesetzt. O Um der neuropathischen Komponente gerecht zu werden, sind die Substanzen Gabapentin (Neurontin®) und Pregbalin (Lyrica®) vor allem bei assoziierter Fibromyalgie eine gute Option. Diese Substanzen sind bei Diabetikern zur Behandlung von neuropathischen Schmerzen gut untersucht. O Amitryptilin (Saroten® usw.): Diese Substanz gehört in die Klasse der trizyklischen (blasenwirksamen) Antidepressiva. Sie stabilisiert die Mastzellen, als SSRI unterdrückt sie das zentrale Schmerzempfinden und führt zu nächtlicher Sedation, mit der betaadrenergen Wirkung wird die Blasenfüllung optimiert. Hauptproblem bilden die Nebenwirkungen (Sedation, Übelkeit und Schwindel), welche des Öfteren zu frühzeitigem Absetzen der Medikation führen.
Ein vorsichtiges Eintitrieren mit Einnahme zur Nacht sowie Aufklärung und Motivation der Patientin erhöhen die Erfolgschancen. Weitere Ansätze in der systemischen Therapie: O Doxyzyklin: In ihrer Arbeit von 2004 konnten Burkhard und Kollegen (7 [Tabelle 2]) zeigen, dass 71 Prozent der Patientinnen mit Drang, Pollakisurie und urethralen/vesikalen Schmerzen von einer vierwöchigen Doxyzyklintherapie profitierten; dies betraf insbesondere Patientinnen mit einer zystoskopisch nachgewiesenen Trigonumleukoplakie. Die Fotosensibilisierung sowie Übelkeit sind oft limitierend und senken die Compliance. O Cimetidine als Mastzellstabilisator ist in der Schweiz nicht mehr erhältlich. O Cyclosporin A gilt in den neuen Guidelines der American Urological Association als Fifth-Line-Behandlung. Schwere Nebenwirkungen aufgrund der Immunsuppression und der Nierentoxizität rechtfertigen den Einsatz dieses nachgewiesenermassen effizienten Medikaments nur nach Ausschöpfen anderer Therapien. O Pentosansulfat (Elmiron®) ist eine gut untersuchte Substanz, welche die GAG-Schicht regeneriert. In den Studien zeigten sich aber auch in der Plazebogruppe gute Erfolge. Elmiron® ist in der Schweiz nicht zugelassen, und wir haben deshalb entsprechend wenig klinische Erfahrung mit dieser Substanz.
Intravesikale Therapien Die Instillationstherapie hat den Vorteil, dass systemische Effekte weitgehend vermieden werden können, und zwar bei guter Wirksamkeit der Medikamente am Ort des Geschehens. Das Erlernen des Selbstkatheterismus ist bei entsprechend einfühlsamer Instruktion meist kein Problem. O Di-Methyl-Sulfoxid-Instillation: DMSO wirkt muskelre-
laxierend, entzündungshemmend, schmerzlindernd sowie mastzellstabilisierend. Hauptnebenwirkung ist der vorübergehende unangenehme Knoblauchgeruch sowie gelegentlich eine lokale Irritation im Anschluss an die Instillation. Sie kann durch nachfolgende Lidocaininstillation behoben werden. DMSO ist keine Pflichtleistung der Krankenkasse und bedarf einer vorgängigen Kostengutsprache. O Heparin-Instillation: Heparin ähnelt dem GAG-Layer und kann diesen ersetzen (Hypothese). O Lidocain mit Bicarbonat-Instillation: Das Bicarbonat erhöht die Blasenwandpermeabilität und verlängert somit die Wirkung von Lidocain. In Kombination mit Heparin wird der Effekt auf den Schmerz nochmals verbessert (6). Lidocain allein hat nur einen sehr kurzfristigen Effekt (7). O Botoxinjektion in die Blasenwand: Im Gegensatz zur Injektion von Botulinumtoxin bei der Detrusorinstabilität ist bei IC/PBS die Datenlage sehr dürftig. Der fehlende Langzeiteffekt ist durch den Abbau des Botox am synaptischen Spalt ebenfalls nicht gegeben.
Invasive Therapien Bei therapieresistenter IC/PBS kommen ferner invasivere Therapiemethoden infrage. Dieser Schritt muss gut überlegt und mit der Patientin sowie im interdisziplinären Kontext besprochen sein.
906
ARS MEDICI 18 I 2014
FORTBILDUNG
Dazu gehören: O Fulguration von Hunnerschen Ulzera (8) oder Hydro-
distension (9) in Narkose können sinnvoll sein. O Sakrale Neurostimulation: Es sind ebenfalls nur kleine
Kollektive, aber mit erfreulichem Erfolg untersucht. Die Installation eines Neurostimulators ist ein aufwendiges und kostenintensives Verfahren. Nach initialer Testphase mit externen Elektroden kann der Neurostimulator analog einem Schrittmacher subkutan implantiert werden. O Zystektomie oder Blasenaugmentation: In ausgewählten Einzelfällen kann diese invasive Therapie die Lebensqualität der Patientin deutlich verbessern. Es zeigten sich gute Resultate bezüglich Schmerz und Blasenkapazität. Die Blasenaugmentation oder Zystektomie mit Neoblase muss sorgfältig evaluiert und überdacht werden. Sie kommt vor allem bei der fibrotisch bedingten kleinkapazitären Blase infrage.
Zusammenfassung Patientinnen mit IC/PBS weisen meist eine lange und beschwerliche Leidensgeschichte auf. Die sorgfältige und einfühlsame Evaluation von Beschwerden und des individuellen Leidensdrucks sind die Basis eines personifizierten Behandlungskonzeptes. Nach Ausschluss anderer schmerzverursachender Diagnosen ist ein Stufenschema – beginnend mit konservativen, nicht invasiven Therapien bis hin zur Zystektomie bei therapieresistenter kleinkapazitärer Blase –
Schritt für Schritt mit der Patientin zu gehen. Eine interdis-
ziplinäre, allenfalls auch psychosomatische Betreuung kann
sinnvoll sein (Abbildung 6).
O
Dr. med. Sonja Brandner
Frauenzimmer Bern – Gynäkologie und mehr
Monbijoustrasse 22, 3011 Bern
E-Mail: sonja.brandner@hin.ch
Quellen: 1. Abrams P et al.: The standardisation of terminology of lower urinary tract function.
Neurourology and urodynamics 2002; 21: 167–178. 2. Clemens JQ et al.: Costs of interstitial cystitis in a managed care population. Urology
2008; 71: 776–780. 3. Mayson BE et al.: The relationship between sexual abuse and interstitial cystitis. Curr
Urol Rep 2009; 10(6): 441–447. 4. Ottem DP et al.: What is the value of cystoscopy and hydrodistension for interstitial
cystitis? Urology 2005; 66: 494. 5. Kirkemo A et al.: Associations among urodynamic findings and symptoms in women
enrolled in the Interstitial Cystitis Data Base (ICDB) Study. Urology 1997; 49: 76. 6. Parsons CL.: Successful downregulation of bladder sensory nerves with combination
of heparin and alkalinized lidocaine in patients with interstitial cystitis. Urology 2005; 65: 45. 7. Nickel JC et al.: Intravesical alkalinized lidocaine (PSD597) offers sustained relief from symptoms of interstitial cystitis and painful bladder syndrome. BJU Int 2008; 103: 910. 8. Malloy TR et al.: Laser therapy for interstitial cystitis. Urol Clin North Am 1994; 21: 141. 9. Cole EE et al.: Are patient symptoms predictive of the diagnostic and/or therapeutic value of hydrodistention? Neurourol Urodyn 2005; 24: 638.
Erstpublikation in «Gynäkologie» 1/2014.