Transkript
Aktuelle Entwicklungen bei Impfungen
In den nächsten Jahren ist mit neuen Impfstoffen zu rechnen
BERICHT
12. Kongress für Infektionskrankheiten und Tropenmedizin (KIT 2014) Köln, 25. bis 28. Juni 2014 Symposium «Aktuelle Entwicklungen bei Impfungen»
In der Impfstoffentwicklung gibt es berechtigte Gründe zur Hoffnung: Gegen immer mehr Infektionen ist eine Impfung möglich. Und selbst bei Erkrankungen, gegen die bereits Impfstoffe zur Verfügung standen, konnte durch Einbeziehung von mehr Serotypen eine breitere Abdeckung und damit auch eine verbesserte Protektion erreicht werden. Einen Überblick über aktuelle Hoffnungsträger auf diesem Gebiet gab es beim diesjährigen Kongress für Infektionskrankheiten und Tropenmedizin auf einem von der Deutschen Gesellschaft für Tropenmedizin und Internationale Gesundheit e. V. ausgerichteten Symposium.
CAROLA WEISS
Um von diesen Fortschritten zu profitieren, muss man nicht in die Tropen reisen – auch hierzulande gibt es genügend Herausforderungen für die Impfstoffentwicklung. Hierzu erläuterte Prof. Dr. Mathias Pletz vom Universitätsklinikum Jena die aktuellen Entwicklungen bei der Prophylaxe von Pneumokokkeninfektionen.
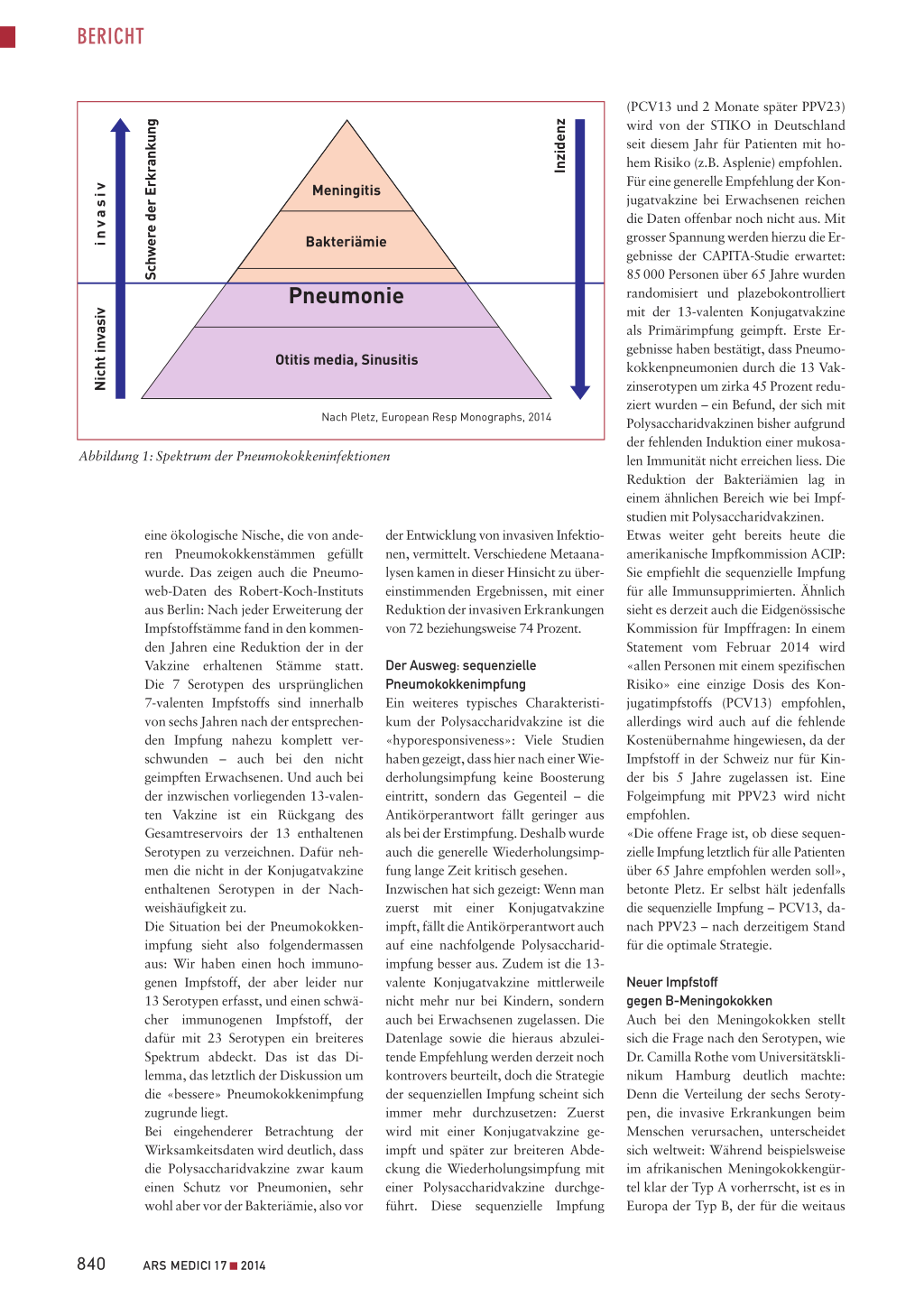
Pneumokokken und das Serotypendilemma Um die Studiendaten zu Pneumokokkenimpfungen zu verstehen, muss man zwischen nichtinvasiven und invasiven Infektionen unterscheiden (Abbildung 1). Während die nichtinvasiven Infektionen sehr häufig, aber harmlos sind, sind invasive Infektionen zwar sehr selten, aber mit einer hohen Letalität verbunden. Die wesentliche Krankheitslast wird reflektiert durch die ambulante Bronchopneumonie, die zu etwa 40 bis 60 Prozent von Pneumokokken verursacht wird; 15 Prozent der Pneumokokkenpneumonien nehmen einen invasiven Verlauf, definiert durch den Nachweis von Pneumokokken in der Blutkultur oder in anderen sonst sterilen Körperflüssigkeiten. Letale Verläufe findet man vor allem bei älteren Patienten. Die wesentliche Hürde in der Impfstoffentwicklung gegen pathogene Pneumokokken ist deren Polysaccharidkapsel, die sie vor Phagozytose schützt, denn Polysaccharide sind wenig immunogen. Von dieser Kapsel gibt es zudem 94 verschiedene Serotypen. Um die geringe Immunität zu überwinden und dennoch eine Immunantwort zu induzieren, werden bei der Pneumokokkenimpfung zwei unterschiedliche Strategien angewendet: Die ältere Strategie ist die Polysaccharidvakzine. Sie enthält 23 der 94 Serotypen. «Hier packt man einfach unheimlich viel Antigen in die Spritze, um überhaupt eine Immunantwort zu bekommen», erläuterte Pletz. Diese Vakzine konnte man allerdings bei Kindern überhaupt nicht einsetzen, weil das noch nicht ausgereifte Immunsystem der Kinder hierauf nicht reagierte. Deshalb hat man für den Einsatz bei Kindern eine Konjugatvakzine entwickelt. Bei dieser wird jedes verwendete Poly-
saccharidantigen mit einem hoch immunogegen Protein gekoppelt, also «konjugiert». Im Unterschied zum alleinigen Polysaccharid wird der so entstandene Molekülkomplex von B-Zellen internalisiert und den CD4Zellen präsentiert, was letztlich zu einer T-Zell-Antwort und auch zu einer mukosalen Immunität sowie zu einem immunologischen Gedächtnis führt. Die mukosale Immunität ist wichtig, um auch die asymptomatische Kolonisierung zu reduzieren. «Denn das Hauptreservoir von Pneumokokken sind nicht erkrankte, kolonisierte Kleinkinder», sagte Pletz. So sind in Kindertagesstätten etwa 80 Prozent der Kinder kolonisiert, «und wir wissen, dass die geimpften Kinder in der Lage sind, die Pneumokokken in ihrem Nasopharynx zu eradizieren. Dadurch legen wir quasi das Reservoir für die Pneumokokken trocken, und mit einer ausreichend hohen Impfrate bekommen wir Herdenprotektionseffekte.» Konjugatvakzine wurden ursprünglich als 7-valente, später als 10-valente und mittlerweile als 13-valente Vakzine angeboten. Daten aus den USA zeigen, dass es nach Einführung der 7-valenten Vakzine im Jahr 2000 innerhalb von zwei Jahren zu einem Rückgang der invasiven Pneumokokkeninfektionen um 80 Prozent kam. Aber auch bei den nicht geimpften über 65-Jährigen, also bei den Grosseltern der geimpften Generation, ergab sich eine Inzidenzreduktion von 37 Prozent, bei der Elterngeneration (18- bis 49-Jährige) von 40 Prozent. Das zeigt, dass hier über die Herdenprotektion tatsächlich auch ein Schutz für die Erwachsenen erreicht werden konnte. So weit die gute Nachricht – die schlechte: Es kam zum Replacement; durch die Eradikation der mit der Impfung abgedeckten Stämme entstand
ARS MEDICI 17 I 2014
839
BERICHT
invasiv
Schwere der Erkrankung
Nicht invasiv
Meningitis Bakteriämie
Pneumonie
Otitis media, Sinusitis
Nach Pletz, European Resp Monographs, 2014
Abbildung 1: Spektrum der Pneumokokkeninfektionen
eine ökologische Nische, die von anderen Pneumokokkenstämmen gefüllt wurde. Das zeigen auch die Pneumoweb-Daten des Robert-Koch-Instituts aus Berlin: Nach jeder Erweiterung der Impfstoffstämme fand in den kommenden Jahren eine Reduktion der in der Vakzine erhaltenen Stämme statt. Die 7 Serotypen des ursprünglichen 7-valenten Impfstoffs sind innerhalb von sechs Jahren nach der entsprechenden Impfung nahezu komplett verschwunden – auch bei den nicht geimpften Erwachsenen. Und auch bei der inzwischen vorliegenden 13-valenten Vakzine ist ein Rückgang des Gesamtreservoirs der 13 enthaltenen Serotypen zu verzeichnen. Dafür nehmen die nicht in der Konjugatvakzine enthaltenen Serotypen in der Nachweishäufigkeit zu. Die Situation bei der Pneumokokkenimpfung sieht also folgendermassen aus: Wir haben einen hoch immunogenen Impfstoff, der aber leider nur 13 Serotypen erfasst, und einen schwächer immunogenen Impfstoff, der dafür mit 23 Serotypen ein breiteres Spektrum abdeckt. Das ist das Dilemma, das letztlich der Diskussion um die «bessere» Pneumokokkenimpfung zugrunde liegt. Bei eingehenderer Betrachtung der Wirksamkeitsdaten wird deutlich, dass die Polysaccharidvakzine zwar kaum einen Schutz vor Pneumonien, sehr wohl aber vor der Bakteriämie, also vor
der Entwicklung von invasiven Infektionen, vermittelt. Verschiedene Metaanalysen kamen in dieser Hinsicht zu übereinstimmenden Ergebnissen, mit einer Reduktion der invasiven Erkrankungen von 72 beziehungsweise 74 Prozent.
Der Ausweg: sequenzielle Pneumokokkenimpfung Ein weiteres typisches Charakteristikum der Polysaccharidvakzine ist die «hyporesponsiveness»: Viele Studien haben gezeigt, dass hier nach einer Wiederholungsimpfung keine Boosterung eintritt, sondern das Gegenteil – die Antikörperantwort fällt geringer aus als bei der Erstimpfung. Deshalb wurde auch die generelle Wiederholungsimpfung lange Zeit kritisch gesehen. Inzwischen hat sich gezeigt: Wenn man zuerst mit einer Konjugatvakzine impft, fällt die Antikörperantwort auch auf eine nachfolgende Polysaccharidimpfung besser aus. Zudem ist die 13valente Konjugatvakzine mittlerweile nicht mehr nur bei Kindern, sondern auch bei Erwachsenen zugelassen. Die Datenlage sowie die hieraus abzuleitende Empfehlung werden derzeit noch kontrovers beurteilt, doch die Strategie der sequenziellen Impfung scheint sich immer mehr durchzusetzen: Zuerst wird mit einer Konjugatvakzine geimpft und später zur breiteren Abdeckung die Wiederholungsimpfung mit einer Polysaccharidvakzine durchgeführt. Diese sequenzielle Impfung
Inzidenz
(PCV13 und 2 Monate später PPV23) wird von der STIKO in Deutschland seit diesem Jahr für Patienten mit hohem Risiko (z.B. Asplenie) empfohlen. Für eine generelle Empfehlung der Konjugatvakzine bei Erwachsenen reichen die Daten offenbar noch nicht aus. Mit grosser Spannung werden hierzu die Ergebnisse der CAPITA-Studie erwartet: 85 000 Personen über 65 Jahre wurden randomisiert und plazebokontrolliert mit der 13-valenten Konjugatvakzine als Primärimpfung geimpft. Erste Ergebnisse haben bestätigt, dass Pneumokokkenpneumonien durch die 13 Vakzinserotypen um zirka 45 Prozent reduziert wurden – ein Befund, der sich mit Polysaccharidvakzinen bisher aufgrund der fehlenden Induktion einer mukosalen Immunität nicht erreichen liess. Die Reduktion der Bakteriämien lag in einem ähnlichen Bereich wie bei Impfstudien mit Polysaccharidvakzinen. Etwas weiter geht bereits heute die amerikanische Impfkommission ACIP: Sie empfiehlt die sequenzielle Impfung für alle Immunsupprimierten. Ähnlich sieht es derzeit auch die Eidgenössische Kommission für Impffragen: In einem Statement vom Februar 2014 wird «allen Personen mit einem spezifischen Risiko» eine einzige Dosis des Konjugatimpfstoffs (PCV13) empfohlen, allerdings wird auch auf die fehlende Kostenübernahme hingewiesen, da der Impfstoff in der Schweiz nur für Kinder bis 5 Jahre zugelassen ist. Eine Folgeimpfung mit PPV23 wird nicht empfohlen. «Die offene Frage ist, ob diese sequenzielle Impfung letztlich für alle Patienten über 65 Jahre empfohlen werden soll», betonte Pletz. Er selbst hält jedenfalls die sequenzielle Impfung – PCV13, danach PPV23 – nach derzeitigem Stand für die optimale Strategie.
Neuer Impfstoff gegen B-Meningokokken Auch bei den Meningokokken stellt sich die Frage nach den Serotypen, wie Dr. Camilla Rothe vom Universitätsklinikum Hamburg deutlich machte: Denn die Verteilung der sechs Serotypen, die invasive Erkrankungen beim Menschen verursachen, unterscheidet sich weltweit: Während beispielsweise im afrikanischen Meningokokkengürtel klar der Typ A vorherrscht, ist es in Europa der Typ B, der für die weitaus
840
ARS MEDICI 17 I 2014
BERICHT
2500000 2000000
2 204 516
1500000
1 451 083 1 279 668
1000000
925 896
500000 0
908 15 497
55–59 60–69
122 174
70–79
295 554
80–89
479 848
90–99
00–07
2008
2009
2010
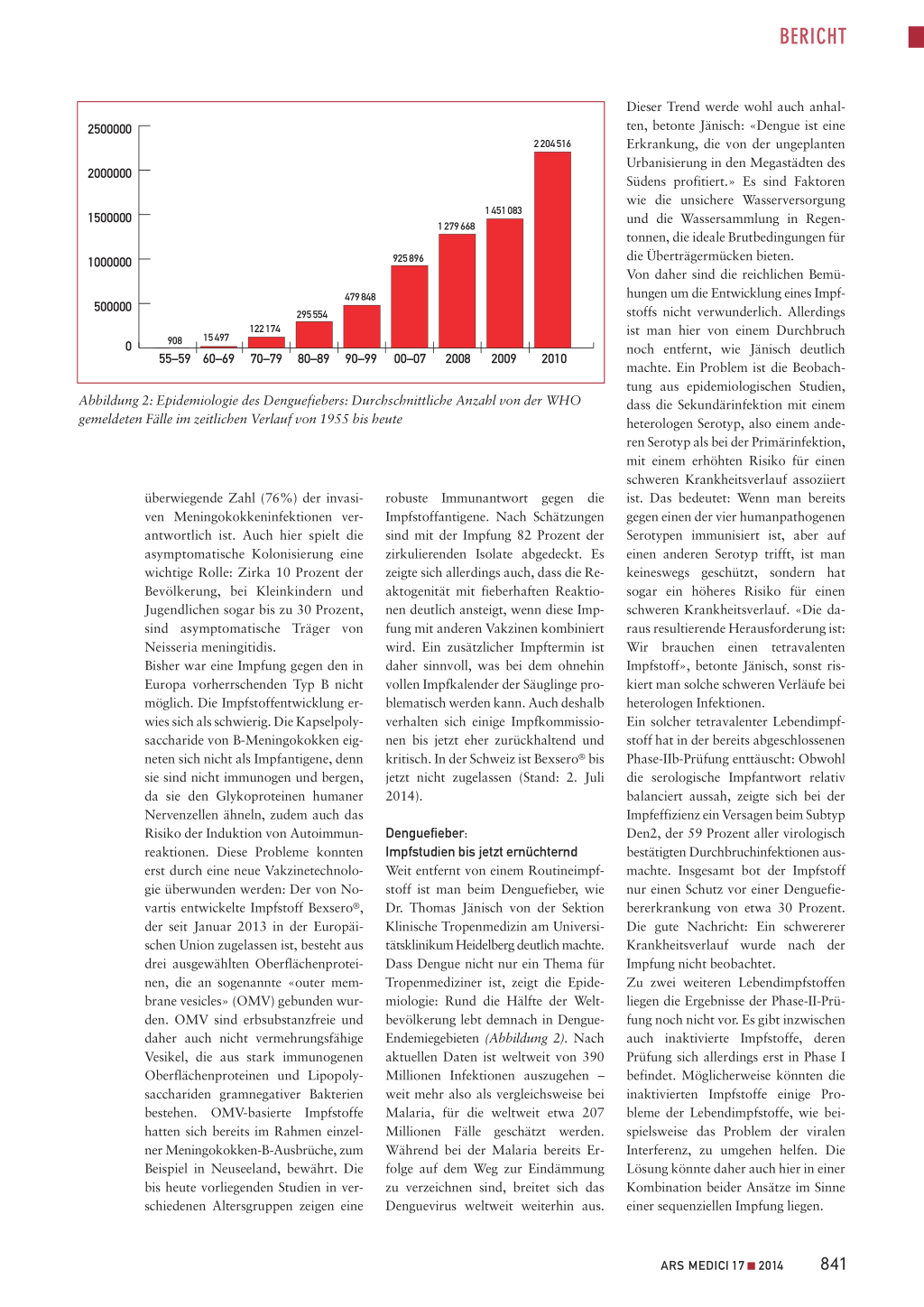
Abbildung 2: Epidemiologie des Denguefiebers: Durchschnittliche Anzahl von der WHO gemeldeten Fälle im zeitlichen Verlauf von 1955 bis heute
überwiegende Zahl (76%) der invasiven Meningokokkeninfektionen verantwortlich ist. Auch hier spielt die asymptomatische Kolonisierung eine wichtige Rolle: Zirka 10 Prozent der Bevölkerung, bei Kleinkindern und Jugendlichen sogar bis zu 30 Prozent, sind asymptomatische Träger von Neisseria meningitidis. Bisher war eine Impfung gegen den in Europa vorherrschenden Typ B nicht möglich. Die Impfstoffentwicklung erwies sich als schwierig. Die Kapselpolysaccharide von B-Meningokokken eigneten sich nicht als Impfantigene, denn sie sind nicht immunogen und bergen, da sie den Glykoproteinen humaner Nervenzellen ähneln, zudem auch das Risiko der Induktion von Autoimmunreaktionen. Diese Probleme konnten erst durch eine neue Vakzinetechnologie überwunden werden: Der von Novartis entwickelte Impfstoff Bexsero®, der seit Januar 2013 in der Europäischen Union zugelassen ist, besteht aus drei ausgewählten Oberflächenproteinen, die an sogenannte «outer membrane vesicles» (OMV) gebunden wurden. OMV sind erbsubstanzfreie und daher auch nicht vermehrungsfähige Vesikel, die aus stark immunogenen Oberflächenproteinen und Lipopolysacchariden gramnegativer Bakterien bestehen. OMV-basierte Impfstoffe hatten sich bereits im Rahmen einzelner Meningokokken-B-Ausbrüche, zum Beispiel in Neuseeland, bewährt. Die bis heute vorliegenden Studien in verschiedenen Altersgruppen zeigen eine
robuste Immunantwort gegen die Impfstoffantigene. Nach Schätzungen sind mit der Impfung 82 Prozent der zirkulierenden Isolate abgedeckt. Es zeigte sich allerdings auch, dass die Reaktogenität mit fieberhaften Reaktionen deutlich ansteigt, wenn diese Impfung mit anderen Vakzinen kombiniert wird. Ein zusätzlicher Impftermin ist daher sinnvoll, was bei dem ohnehin vollen Impfkalender der Säuglinge problematisch werden kann. Auch deshalb verhalten sich einige Impfkommissionen bis jetzt eher zurückhaltend und kritisch. In der Schweiz ist Bexsero® bis jetzt nicht zugelassen (Stand: 2. Juli 2014).
Denguefieber: Impfstudien bis jetzt ernüchternd Weit entfernt von einem Routineimpfstoff ist man beim Denguefieber, wie Dr. Thomas Jänisch von der Sektion Klinische Tropenmedizin am Universitätsklinikum Heidelberg deutlich machte. Dass Dengue nicht nur ein Thema für Tropenmediziner ist, zeigt die Epidemiologie: Rund die Hälfte der Weltbevölkerung lebt demnach in DengueEndemiegebieten (Abbildung 2). Nach aktuellen Daten ist weltweit von 390 Millionen Infektionen auszugehen – weit mehr also als vergleichsweise bei Malaria, für die weltweit etwa 207 Millionen Fälle geschätzt werden. Während bei der Malaria bereits Erfolge auf dem Weg zur Eindämmung zu verzeichnen sind, breitet sich das Denguevirus weltweit weiterhin aus.
Dieser Trend werde wohl auch anhalten, betonte Jänisch: «Dengue ist eine Erkrankung, die von der ungeplanten Urbanisierung in den Megastädten des Südens profitiert.» Es sind Faktoren wie die unsichere Wasserversorgung und die Wassersammlung in Regentonnen, die ideale Brutbedingungen für die Überträgermücken bieten. Von daher sind die reichlichen Bemühungen um die Entwicklung eines Impfstoffs nicht verwunderlich. Allerdings ist man hier von einem Durchbruch noch entfernt, wie Jänisch deutlich machte. Ein Problem ist die Beobachtung aus epidemiologischen Studien, dass die Sekundärinfektion mit einem heterologen Serotyp, also einem anderen Serotyp als bei der Primärinfektion, mit einem erhöhten Risiko für einen schweren Krankheitsverlauf assoziiert ist. Das bedeutet: Wenn man bereits gegen einen der vier humanpathogenen Serotypen immunisiert ist, aber auf einen anderen Serotyp trifft, ist man keineswegs geschützt, sondern hat sogar ein höheres Risiko für einen schweren Krankheitsverlauf. «Die daraus resultierende Herausforderung ist: Wir brauchen einen tetravalenten Impfstoff», betonte Jänisch, sonst riskiert man solche schweren Verläufe bei heterologen Infektionen. Ein solcher tetravalenter Lebendimpfstoff hat in der bereits abgeschlossenen Phase-IIb-Prüfung enttäuscht: Obwohl die serologische Impfantwort relativ balanciert aussah, zeigte sich bei der Impfeffizienz ein Versagen beim Subtyp Den2, der 59 Prozent aller virologisch bestätigten Durchbruchinfektionen ausmachte. Insgesamt bot der Impfstoff nur einen Schutz vor einer Denguefiebererkrankung von etwa 30 Prozent. Die gute Nachricht: Ein schwererer Krankheitsverlauf wurde nach der Impfung nicht beobachtet. Zu zwei weiteren Lebendimpfstoffen liegen die Ergebnisse der Phase-II-Prüfung noch nicht vor. Es gibt inzwischen auch inaktivierte Impfstoffe, deren Prüfung sich allerdings erst in Phase I befindet. Möglicherweise könnten die inaktivierten Impfstoffe einige Probleme der Lebendimpfstoffe, wie beispielsweise das Problem der viralen Interferenz, zu umgehen helfen. Die Lösung könnte daher auch hier in einer Kombination beider Ansätze im Sinne einer sequenziellen Impfung liegen.
ARS MEDICI 17 I 2014
841
BERICHT
Norovirusenteritis – Strategien gegen «das perfekte menschliche Pathogen» Das Norovirus ist «das perfekte menschliche Pathogen», betonte Prof. Dr. Hans-Dieter Nothdurft von der Abteilung für Infektions- und Tropenmedizin der Medizinischen Klinik Innenstadt in München: Es ist hoch kontagiös, relativ umweltstabil, wird zudem schnell und in enormen Mengen verbreitet und vermittelt darüber hinaus selbst nach einer natürlichen Infektion nur eine begrenzte Immunität. «Das ist eine grosse Herausforderung für eine Impfstoffentwicklung», so Nothdurft weiter. Doch aufgrund der epidemiologischen Bedeutung ist es sinnvoll, sich dieser Herausforderung zu stellen. Denn inzwischen gilt das Norovirus weltweit als eine führende Ursache der akuten Gastroenteritis. Es ist für etwa die Hälfte aller Gastroenteritisausbrüche verantwortlich. In Ländern mit Rotavirus-Impfprogrammen wurden
Noroviren zum wichtigsten enteritischen Pathogen bei Kindern und Jugendlichen. Gerade bei Kleinkindern wie auch bei älteren Menschen führt die Infektion zu hohen Hospitalisierungsraten, mit bis zu 200 000 Todesfällen pro Jahr bei Kindern unter 5 Jahren, hauptsächlich in Entwicklungsländern. Doch selbst in industrialisierten Ländern geht man von bis zu 5000 Todesfällen pro Jahr aus, so Nothdurft. In der Impfstoffentwicklung setzt man hier auf die VLP-Technologie: VLP (virus-like particles) sind Proteinkapseln aus viralen Proteinen, die sich selbst zu virusähnlichen Partikeln anordnen, ohne aber genetisches Material des Virus zu enthalten – damit haben sie einen potenziellen Sicherheitsvorteil gegenüber attenuierten Lebendimpfstoffen. Diese Technologie wurde bereits bei HPV-Impfstoffen erfolgreich umgesetzt und scheint gerade bei mukosalen Infektionskrankheiten Vorteile zu haben. Nach den Ergebnissen von
Phase-I-Studien handelt es sich auch
bei der Norovirus-VLP-Vakzine um ein
sicheres Produkt, mit dem in fast allen
Altersgruppen bereits nach der ersten
Dosis eine Immunogenität erzeugt wer-
den konnte. Es scheint, dass bei Infek-
tion zumindest der Schweregrad einer
Erkrankung, aber auch die Virusaus-
scheidung deutlich reduziert werden
können. Vor allem Letzteres könnte
einen günstigen Einfluss auf die welt-
weite Krankheitslast haben, betonte
Nothdurft. Wenn die weitere klinische
Prüfung diese ersten Daten bestätigt,
dann könnte dieser Impfstoff in etwa
drei Jahren zur Verfügung stehen, so
die Einschätzung des Referenten, der
allerdings davon ausgeht, dass der
Impfstoff nur eine zeitlich begrenzte
Immunantwort induzieren und, ähn-
lich der Grippeimpfung, häufige Wie-
derholungsimpfungen notwendig ma-
chen wird.
O
Carola Weiss
842
ARS MEDICI 17 I 2014