Transkript
FORTBILDUNG
Allergische Rhinitis und atopisches Ekzem
Bewährte und neue medikamentöse Therapiemöglichkeiten
Die allergische Rhinitis ist die häufigste Erkrankung des Immunsystems. Auch wenn die Symptome nicht lebensbedrohlich sind, beeinträchtigen sie die Lebensqualität der Betroffenen beträchtlich. Zudem ist die allergische Rhinitis häufig mit anderen Komorbiditäten assoziiert. Der folgende Beitrag befasst sich mit den aktuellen medikamentösen Therapiemöglichkeiten sowohl bei allergischer Rhinitis als auch beim häufig gleichzeitig auftretenden atopischen Ekzem.
LUDGER KLIMEK
Die allergische Rhinitis betrifft weltweit zirka 10 bis 20 Prozent der Bevölkerung (1). Sie beginnt oftmals bereits in der Kindheit und führt zu einer dauerhaften Beeinträchtigung der Lebensqualität. Typische Symptome der allergischen Rhinitis sind Rhinorrhö, nasale Obstruktion, Niesreiz und Pruritus sowie okulare Symptome. Patienten mit allergischer Rhinitis leiden häufig auch unter einem atopischen Ekzem, welches unter anderem auch zu Gehörgangsekzemen führen kann. Zu den Symptomen des Gehörgangsekzems zählen trockene Gehörgangshaut, Schuppenbildung und Pruritus (2). Heute stehen eine Reihe wirksamer Therapeutika zur Behandlung bei allergischer Rhinitis zur Verfügung. Allerdings sollte eine geeignete Therapie erst nach ärztlicher Diagnose erfolgen. Laut einer Umfrage diagnostizieren und behandeln
jedoch viele Betroffene ihre allergische Rhinitis selbst, ohne den Rat eines Arztes einzuholen. Zirka 20 Prozent der Betroffenen unterlassen sogar jegliche Therapie (3). Eine medikamentöse Behandlung bei allergischer Rhinitis ist häufig indiziert, wenn die Karenz der allergieauslösenden Stoffe nicht möglich ist. Eingesetzt werden heute hauptsächlich Mastzellstabilisatoren, Antihistaminika, Glukokortikoide, Leukotrienrezeptorantagonisten und Dekongestiva (Tabelle 1). Tritt begleitend ein atopisches Ekzem auf, sollte dieses mittels einer Stufentherapie behandelt werden (Tabelle 2). Neben der topischen Basistherapie sind insbesondere Glukokortikoide und Calcineurinhemmer vielversprechend (4). Bei einem Gehörgangsekzem wird die topische Applikation einer glukokortikoidhaltigen Fettsalbe als Prophylaxe empfohlen (2).
Mastzellstabilisatoren Cromoglicinsäure hat eine stabilisierende Wirkung auf die histaminproduzierenden Mastzellen, indem sie ihren Degranulationsprozess blockiert (5). Im Vergleich mit anderen pharmakologischen Substanzen, wie Antihistaminika und Glukokortikoiden, hat sie jedoch eine schwächere Wirkung. Auch bringt die bis zu viermal tägliche Anwendung zusätzliche Nachteile mit sich, sodass dieser Wirkstoff nur noch eine untergeordnete Rolle bei der Therapie der allergischen Rhinitis spielt (1). Zur Behandlung bei atopischem Ekzem wird die Therapie mit oralen Mastzellstabilisatoren nicht empfohlen, da sie keinen therapeutischen Effekt haben (4). Als Bestandteil von Cremes konnte allerdings gezeigt werden, dass Cromoglicinsäure den Pruritus günstig beeinflussen kann (6).
Merksätze
O Betroffene müssen besser diagnostiziert werden und eine ausreichende Nachsorge erhalten.
O Nasale Glukokortikoide stellen zurzeit die erste Wahl bei der Therapie der allergischen Rhinitis dar.
O Ein neues Nasenspray, welches die Gabe von Glukokortikoid und Antihistaminikum vereint, könnte in Zukunft eine Alternative zu den heutigen Therapieoptionen der allergischen Rhinitis darstellen.
O Beim atopischen Ekzem sind, neben der topischen Basistherapie, topische Glukokortikoide und Calcineurinhemmer die erste Wahl.
Antihistaminika Antihistaminika sind Wirkstoffe, welche die Histaminrezeptoren blockieren und somit die Freisetzung von Histamin abschwächen. Eine grosse Rolle spielen hierbei die H1-Antihistaminika, da diese die H1-Rezeptoren besetzen, welche hauptverantwortlich sind für die allergische Reaktion. Grundsätzlich unterscheidet man bei den H1-Antihistaminika Substanzen der ersten und zweiten Generation. Die erste Generation der H1-Antihistaminika weist eine ausgeprägte sedierende Wirkung auf, die sich negativ auf Leistungsfähigkeit und motorische Fähigkeiten auswirkt (7). H1-Antihistaminika der zweiten Generation können hingegen aufgrund ihres hydrophilen Charakters nur im verringerten Masse die Blut-Hirn-Schranke passieren und weisen dadurch nur geringe bis gar keine sedierenden Eigenschaften auf. Bei allergischer Rhinitis werden dementsprechend die Präparate der zweiten
108
ARS MEDICI 2 I 2014
FORTBILDUNG
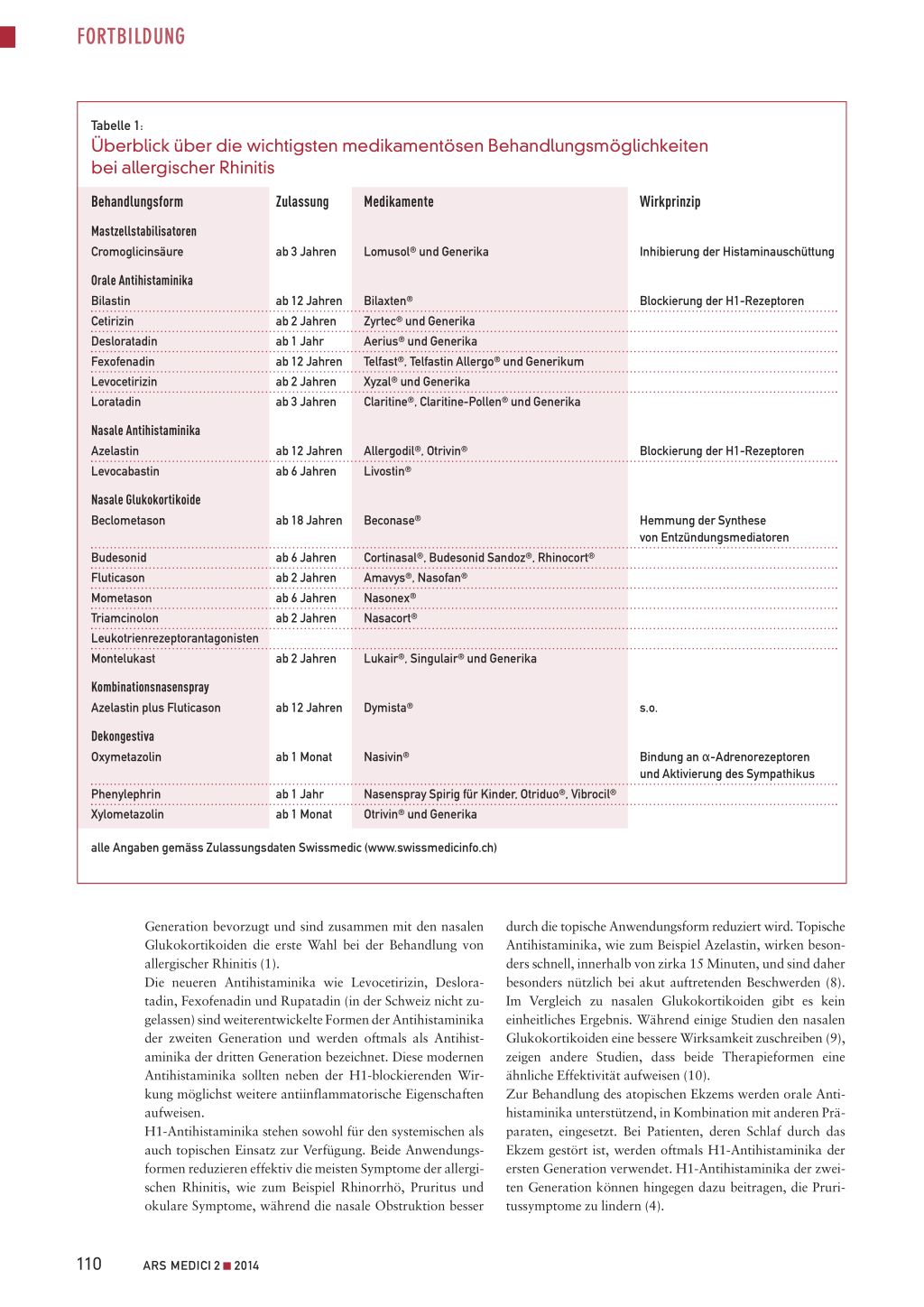
Tabelle 1:
Überblick über die wichtigsten medikamentösen Behandlungsmöglichkeiten bei allergischer Rhinitis
Behandlungsform
Mastzellstabilisatoren Cromoglicinsäure
Orale Antihistaminika Bilastin Cetirizin Desloratadin Fexofenadin Levocetirizin Loratadin
Nasale Antihistaminika Azelastin Levocabastin
Nasale Glukokortikoide Beclometason
Zulassung
ab 3 Jahren
ab 12 Jahren ab 2 Jahren ab 1 Jahr ab 12 Jahren ab 2 Jahren ab 3 Jahren
ab 12 Jahren ab 6 Jahren
ab 18 Jahren
Budesonid Fluticason Mometason Triamcinolon Leukotrienrezeptorantagonisten Montelukast
ab 6 Jahren ab 2 Jahren ab 6 Jahren ab 2 Jahren
ab 2 Jahren
Kombinationsnasenspray Azelastin plus Fluticason
ab 12 Jahren
Dekongestiva Oxymetazolin
ab 1 Monat
Phenylephrin Xylometazolin
ab 1 Jahr ab 1 Monat
Medikamente
Lomusol® und Generika
Bilaxten® Zyrtec® und Generika Aerius® und Generika Telfast®, Telfastin Allergo® und Generikum Xyzal® und Generika Claritine®, Claritine-Pollen® und Generika
Allergodil®, Otrivin® Livostin®
Beconase®
Cortinasal®, Budesonid Sandoz®, Rhinocort® Amavys®, Nasofan® Nasonex® Nasacort®
Lukair®, Singulair® und Generika
Dymista®
Nasivin®
Nasenspray Spirig für Kinder, Otriduo®, Vibrocil® Otrivin® und Generika
Wirkprinzip
Inhibierung der Histaminauschüttung Blockierung der H1-Rezeptoren
Blockierung der H1-Rezeptoren Hemmung der Synthese von Entzündungsmediatoren
s.o. Bindung an α-Adrenorezeptoren und Aktivierung des Sympathikus
alle Angaben gemäss Zulassungsdaten Swissmedic (www.swissmedicinfo.ch)
Generation bevorzugt und sind zusammen mit den nasalen Glukokortikoiden die erste Wahl bei der Behandlung von allergischer Rhinitis (1). Die neueren Antihistaminika wie Levocetirizin, Desloratadin, Fexofenadin und Rupatadin (in der Schweiz nicht zugelassen) sind weiterentwickelte Formen der Antihistaminika der zweiten Generation und werden oftmals als Antihistaminika der dritten Generation bezeichnet. Diese modernen Antihistaminika sollten neben der H1-blockierenden Wirkung möglichst weitere antiinflammatorische Eigenschaften aufweisen. H1-Antihistaminika stehen sowohl für den systemischen als auch topischen Einsatz zur Verfügung. Beide Anwendungsformen reduzieren effektiv die meisten Symptome der allergischen Rhinitis, wie zum Beispiel Rhinorrhö, Pruritus und okulare Symptome, während die nasale Obstruktion besser
durch die topische Anwendungsform reduziert wird. Topische Antihistaminika, wie zum Beispiel Azelastin, wirken besonders schnell, innerhalb von zirka 15 Minuten, und sind daher besonders nützlich bei akut auftretenden Beschwerden (8). Im Vergleich zu nasalen Glukokortikoiden gibt es kein einheitliches Ergebnis. Während einige Studien den nasalen Glukokortikoiden eine bessere Wirksamkeit zuschreiben (9), zeigen andere Studien, dass beide Therapieformen eine ähnliche Effektivität aufweisen (10). Zur Behandlung des atopischen Ekzems werden orale Antihistaminika unterstützend, in Kombination mit anderen Präparaten, eingesetzt. Bei Patienten, deren Schlaf durch das Ekzem gestört ist, werden oftmals H1-Antihistaminika der ersten Generation verwendet. H1-Antihistaminika der zweiten Generation können hingegen dazu beitragen, die Pruritussymptome zu lindern (4).
110 ARS MEDICI 2 I 2014
FORTBILDUNG
Tabelle 2:
Stufentherapie bei atopischem Ekzem
Stufe 1: trockene Haut
Therapie
topische Basistherapie, Hydratation der Haut, Emollienzien, Vermeidung oder Reduktion von Triggerfaktoren
Stufe 2: leichte Ekzeme
antipruroginöse und antiseptische Wirkstoffe, topische Glukokortikoide (Klasse 1–2) und/oder topische Calcineurinhemmer
Stufe 3: moderate Ekzeme
topische Glukokortikoide (Klasse 2–3) und/oder Calcineurinhemmer
Stufe 4: persistierende, schwer systemische Therapie
ausgeprägte Ekzeme
(z.B. Ciclosporin A)
nach (4)
Topische Glukokortikoide Nasale Glukokortikoide sind die erste Wahl bei allergischer Rhinitis, da sie alle nasalen Symptome wirksam unterdrücken (1). Die lokalen Nebenwirkungen beschränken sich meist auf Epistaxis, nasale Trockenheit, Irritationen im Rachenbereich und Kopfschmerzen. Systemische Nebenwirkungen, wie sie bei systemischer Gabe von Glukokortikoiden entstehen, treten hingegen nur selten auf, und eine Wachstumshemmung bei Kindern konnte bisher nur bei der Gabe von Beclometasondipropionat nachgewiesen werden (11). Trotzdem sollte bei langfristiger Gabe das Wachstum von Kindern regelmässig überprüft werden. Im Gegensatz zu Antihistaminika haben nasale Glukokortikoide eine spät eintretende Wirksamkeit von bis zu zwei bis drei Wochen. Die Therapie muss dementsprechend früh begonnen und regelmässig angewendet werden und sollte nicht «bei Bedarf» erfolgen. Bei der Behandlung des atopischen Ekzems zählen topische Glukokortikoide zu den wichtigsten antiinflammatorischen Substanzen. Sie werden je nach Wirkungsstärke in vier Klassen unterteilt. Im Normalfall reichen Glukokortikoide der Klassen 1 und 2 aus, und nur bei schwer ausgeprägten Ekzemen sollten auch höhere Stärkeklassen verschrieben werden. Diese potenteren Glukokortikoide sollten jedoch nur in Ausnahmefällen in Gesicht und Gehörgang angewandt werden. Zu den Nebenwirkungen zählen unter anderem Atrophie, Hautinfektionen und Striae distensae. Dementsprechend sollte die Therapie mit Glukokortikoiden nicht dauerhaft durchgeführt werden, sondern in Intervallen erfolgen (4).
Leukotrienrezeptorantagonisten Leukotriene führen zu einer starken Bronchokonstriktion, erhöhten Kapillarpermeabilität und vermehrten Sekretion der Schleimdrüsen (12). Leukotrienrezeptorantagonisten unterbinden diesen Vorgang, indem sie entweder den Rezeptor selbst blockieren (Montelukast, Zafirlukast) oder das Enzym 5-Lipoxygenase inhibieren (Zileuton [in der Schweiz nicht zugelassen]), welches an der Entstehung der Leukotriene beteiligt ist.
Leukotrienrezeptorantagonisten weisen eine ähnliche Effektivität wie orale H1-Antihistaminika auf (24). In Kombination mit einem oralen H1-Antihistaminikum haben sie eine höhere Wirksamkeit als orale H1-Antihistaminika allein, weshalb die Wirkstoffe zusammen eingesetzt werden sollten (13). Aufgrund der überlegenen Wirksamkeit der nasalen Glukokortikoide stellen Leukotrienrezeptorantagonisten bei allergischer Rhinitis jedoch nur die zweite Wahl dar. In Deutschland und der Schweiz ist zum heutigen Zeitpunkt nur der Wirkstoff Montelukast zur Behandlung der AR zugelassen. Beim atopischen Ekzem gibt es keine eindeutigen Beweise für einen Therapieerfolg von Montelukast. Während einige Studien dem Wirkstoff einen positiven Effekt zuschreiben (14), konnten andere Studien dies nicht belegen (15).
Dekongestiva (α-Sympathomimetika) Für die akute Behandlung bei allergischer Rhinitis werden ␣-Sympathomimetika eingesetzt, welche an ␣-Adrenorezeptoren binden und diese aktivieren. Die Folge ist eine Vasokonstriktion der nasalen Mukosa, die zu einer verringerten Inflammation und einem Abschwellen der Schleimhäute führt. Die Gabe der Substanzen kann sowohl topisch als auch systemisch erfolgen. Zu den Nebenwirkungen der systemischen Medikamente gehören Tachykardien, Unruhe, Schlaflosigkeit und Hypertonie (16). Bei der topischen Nutzung der Dekongestiva kann es zu nasaler Trockenheit und Niesreiz kommen. Eine langfristige Nutzung kann zudem zu einer Rhinitis medicamentosa führen. Die Therapie mit Dekongestiva sollte daher nicht länger als drei bis fünf Tage andauern (1).
Calcineurinhemmer Calcineurinhemmer werden zur Behandlung bei atopischem Ekzem angewandt. Sie inhibieren das Enzym Calcineurin, welches an der Immunzellaktivierung beteiligt ist. Calcineurinhemmer blockieren so die Ausschüttung inflammatorischer Zytokine. Die topischen Calcineurinhemmer Pimecrolimus (Elidel®) und Tacrolimus (Protopic®) sollten beim Gehörgangsekzem genutzt werden, wenn topische Glukokortikoide schlecht vertragen werden (2). Nur bei einer chronischen, therapieresistenten Form des atopischen Ekzems sollte die Gabe des systemischen Calcineurinhemmers Ciclosporin A erfolgen, da dieser ein starkes Nebenwirkungsprofil aufweist (4).
Allergenspezifische Immuntherapie Die allergenspezifische Immuntherapie (SIT) ist die einzige Form der Therapie, die nicht die Symptome bekämpft, sondern auf eine dauerhafte Toleranz gegenüber den Allergenen abzielt. Hierzu werden den Betroffenen in steigender Konzentration Allergene entweder unter die Haut injiziert (subkutane Immuntherapie: SCIT) oder mittels Tropfen über die Mundschleimhaut zugeführt (sublinguale Immuntherapie: SLIT). Die Anwendung erfolgt über einen langen Zeitraum (zirka 3 Jahre) und soll die Überempfindlichkeit gegenüber den Allergenen normalisieren. Die Erfolgsrate der beiden Therapieformen ist abhängig vom Allergen, insbesondere die Pollenallergie kann mithilfe der SIT gut behandelt werden (17). Neue Studien zur SCIT zeigen, dass diese Form der
112 ARS MEDICI 2 I 2014
FORTBILDUNG
Therapie bereits im ersten Jahr eine ähnlich hohe Effektivität bezüglich einer Symptomminderung aufweist wie die Pharmakotherapie (18). Die meisten Nebenwirkungen bei der SCIT sind Lokalreaktionen, wie Rötungen oder Schwellungen. Diese unerwünschten Reaktionen sind jedoch nur leicht bis mittelschwer und mithilfe der Gabe von Antihistaminika relativ leicht zu lindern (17). Das Auftreten eines anaphylaktischen Schocks kommt sehr viel seltener vor. Trotzdem sollte der Patient nach der Injektion noch mindestens 30 Minuten lang in der Praxis beobachtet werden, damit der Arzt gegebenenfalls Gegenmassnahmen einleiten kann (17). Bei der SLIT treten die meisten Nebenwirkungen ebenfalls lokal auf und sind vorwiegend milderer Ausprägung. Starke systemische Reaktionen treten in der Regel nicht auf (17). Für die Behandlung bei atopischem Ekzem könnte die SIT in der Zukunft ebenfalls eine Rolle spielen. So konnte gezeigt werden, dass diese Form der Therapie bei Patienten mit Hausstaubmilbenallergie wirksam war (19). Weitere klinische Studien sind jedoch notwendig, um den Nutzen der Therapie beim atopischen Ekzem zu belegen.
Neue Wirkprinzipien
Eine Weiterentwicklung und Verbesserung der heutigen
Therapieansätze ist notwendig, da trotz der zahlreichen The-
rapiemöglichkeiten bei vielen Betroffenen die Symptome
nicht ausreichend gelindert werden können. Studien zeigen,
dass etwa 40 Prozent der Patienten eine Kombinationsthera-
pie mit verschiedenen Präparaten anwenden (20, 21),
obwohl der zusätzliche Nutzen eines zweiten Präparates in
vielen Studien nicht belegt werden konnte (22, 23).
Demgegenüber konnte in einer Studie gezeigt werden, dass
die Kombination eines nasalen Glukokortikoids (Fluticason-
propionat) und eines nasalen Antihistaminikums (Azelastin)
eine höhere Wirksamkeit bezüglich der Linderung der Sym-
ptome hatte als die Gabe der einzelnen Wirkstoffe (24). Wäh-
rend bei der Studie von Ratner et al. zwei verschiedene
Nasensprays angewandt werden mussten, gibt es inzwischen
neuere Studien, welche die Nutzung der zwei Wirkstoffe in
einem gemeinsamen Nasenspray beschreiben (25–27). Die
ersten Studien zeigen, dass diese neue Rezeptur (Dymista®)
alle nasalen Symptome signifikant stärker lindert als die
Monotherapie mit nasalem Glukokortikoid oder Antihist-
aminikum (25–27). Darüber hinaus besserten sich die Sym-
ptome schneller als bei der Therapie mit den einzelnen Wirk-
stoffen (25). Dieser neuartige Ansatz könnte daher zukünftig
eine Alternative zu den heutigen Therapieoptionen der aller-
gischen Rhinitis werden.
O
Prof. Dr. med. Ludger Klimek Zentrum für Rhinologie und Allergologie D-65183 Wiesbaden E-Mail: ludger.klimek@allergiezentrum.org
Interessenkonflikte: Fachbeiträge und Studien für ALK-Abello (Denmark), Allergopharma (Germany), Artu-Biologicals (Netherlands), Bencard (Great Britain) Bionorica (Germany), Biomay (AustriaI), Boehringer Ingelheim (Germany), Cytos (Switzerland), Dr. Pfleger (Germany), HAL (Netherlands), Hartington (Spain), GSK (Great Britain), Leti (Spain), Lofarma (Italy), Novartis (Switzerland), MEDA (Germany), MSD (USA), Optima (Germany), Roxall (Germany).
Diese Arbeit erschien zuerst in «Der Allgemeinarzt» 10/2013. Die Übernahme erfolgt mit freundlicher Genehmigung von Verlag und Autor. Der Beitrag wurde von der Redaktion ARS MEDICI an die Verhältnisse in der Schweiz angepasst (Medikamente, Zulassungen und Literatur).
Literatur: 1. Brozek JL, Bousquet J, Baena-Cagnani CE et al.: Allergic Rhinitis and its Impact on Asthma
(ARIA) guidelines: 2010 revision. J Allergy Clin Immunol 2010; 126 (3): 466–476. 2. Kwok P: Äusseres Ohr. In: Strutz, J.; Mann, W. (Hrsg) Praxis der HNO-Heilkunde,
Kopf- und Halschirurgie. Georg Thieme Verlag, Stuttgart, 2009; S: 240–253. 3. Maurer M, Zuberbier T: Undertreatment of rhinitis symptoms in Europe: findings from a
cross-sectional questionnaire survey. Allergy 2007; 62 (9): 1057–1063. 4. Deutsche Dermatologische Gesellschaft, Deutsche Gesellschaft für Allergologie und
klinische Immunologie, Deutsche Gesellschaft für Kinder- und Jugendmedizin 2008; www.awmf.org; abgerufen am 11.01.2012. 5. Ratner PH, Ehrlich PM, Fineman SM et al.: Use of intranasal cromolyn sodium for allergic rhinitis. Mayo Clin Proc 2002; 77 (4): 350–354. 6. Edwards AM, Stevens MT, Church MK: The effects of topical sodium cromoglicate on itch and flare in human skin induced by intradermal histamine: a randomised double-blind vehicle controlled intra-subject design trial. BMC Res Notes 2011; 4 (1): 47. 7. Kay GG, Quig ME: Impact of sedating antihistamines on safety and productivity. Allergy Asthma Proc 2001; 22 (5): 281–283. 8. Newson-Smith G, Powell M, Baehre M et al.: A placebo controlled study comparing the efficacy of intranasal azelastine and beclomethasone in the treatment of seasonal allergic rhinitis. Eur Arch Otorhinolaryngol 1997; 254 (5): 236–241. 9. Yáñez A, Rodrigo GJ: Intranasal corticosteroids versus topical H1 receptor antagonists for the treatment of allergic rhinitis: a systematic review with meta-analysis. Ann Allergy Asthma Immunol. 2002; 89 (5): 479–484. 10. Kaliner MA, Berger WE, Ratner PH et al.: The efficacy of intranasal antihistamines in the treatment of allergic rhinitis. Ann Allergy Asthma Immunol 2011; 106 (2 Suppl): S6–S11 11. Skoner DP, Rachelefsky GS, Meltzer EO et al.: Detection of growth suppression in children during treatment with intranasal beclomethasone dipropionate. Pediatrics 2000; 105 (2): E23. 12. Samuelsson B: Leukotrienes: mediators of immediate hypersensitivity reactions and inflammation. Science 1983; 220 (4597): 568–575. 13. Rodrigo GJ, Yáñez A: The role of antileukotriene therapy in seasonal allergic rhinitis: a systematic review of randomized trials. Ann Allergy Asthma Immunol 2006; 96 (6): 779–786. 14. Yanase DJ, David-Bajar K: The leukotriene antagonist montelukast as a therapeutic agent for atopic dermatitis. J Am Acad Dermatol 2001; 44 (1): 89–93. 15. Friedmann PS, Palmer R, Tan E et al.: A double-blind, placebo-controlled trial of montelukast in adult atopic eczema. Clin Exp Allergy 2007; 37 (10): 1536–1540. 16. Interdisziplinäre Arbeitsgruppe «Allergische Rhinitis» der Sektion HNO: Allergische Rhinokonjunktivitis. Allergo J 2003; 12: 182–194. 17. Kleine-Tebbe J, Bufe A, Ebner C et al.: Die spezifische Immuntherapie (Hyposensibilisierung) bei IgE-vermittelten allergischen Erkrankungen. Allergo J 2009; 18: 508–537. 18. Matricardi PM, Kuna P, Panetta V et al.: Subcutaneous immunotherapy and pharmacotherapy in seasonal allergic rhinitis: a comparison based on meta-analyses. J Allergy Clin Immunol 2011; 128 (4): 791–799.e6. 19. Bussmann C, Bockenhoff A, Henke H et al.: Does allergen-specific immunotherapy represent a therapeutic option for patients with atopic dermatitis? J Allergy Clin Immunol 2006; 118 (6): 1292–1298. 20. Canonica GW, Bousquet J, Mullol J et al.: A survey of the burden of allergic rhinitis in Europe. Allergy 2007; 62 (Suppl 85): 17–25. 21. Dalal AA, Stanford R, Henry H et al.: Economic burden of rhinitis in managed care: a retrospective claims data analysis. Annals of Allergy, Asthma & Immunology 2008; 101 (1): 23–29. 22. Anolik R: Clinical benefits of combination treatment with mometasone furoate nasal spray and loratadine vs monotherapy with mometasone furoate in the treatment of seasonal allergic rhinitis. Ann Allergy Asthma Immunol 2008; 100 (3): 264–271. 23. Di Lorenzo G, Pacor ML, Pellitteri ME et al.: Randomized placebo-controlled trial comparing fluticasone aqueous nasal spray in mono-therapy, fluticasone plus cetirizine, fluticasone plus montelukast and cetirizine plus montelukast for seasonal allergic rhinitis. Clin Exp Allergy 2004; 34 (2): 259–267. 24. Ratner PH, Hampel F, van Bavel J et al.: Combination therapy with azelastine hydrochloride nasal spray and fluticasone propionate nasal spray in the treatment of patients with seasonal allergic rhinitis. Ann Allergy Asthma Immunol 2008; 100 (1): 74–81. 25. Carr W, Bernstein J, Lieberman P, et al. (2012) A novel intranasal therapy of azelastine with fluticasone for the treatment of allergic rhinitis. J Allergy Clin Immunol. 129 (5): 1282–1289.e10. 26. Hampel FC, Ratner PH, van Bavel J et al.: Double-blind, placebo-controlled study of azelastine and fluticasone in a single nasal spray delivery device. Ann Allergy Asthma Immunol 2010; 105 (2): 168–173. 27. Meltzer EO, LaForce C, Ratner P et al.: MP29-02 (a novel intranasal formulation of azelastine hydrochloride and fluticasone propionate) in the treatment of seasonal allergic rhinitis: a randomized, double-blind, placebo-controlled trial of efficacy and safety. Allergy Asthma Proc 2012; 33 (4): 324–332.
114 ARS MEDICI 2 I 2014