Transkript
FORTBILDUNG
Die akute Wundversorgung bei Kindern
Erstbeurteilung, Anästhesie, Wundreinigung und Wundverschluss
Die Versorgung von Wunden spielt in der Kindernotfallmedizin eine wichtige Rolle. Die Prinzipien hierfür sind beim Kind und Erwachsenen identisch, jedoch gilt es beim Kind, die Umstände, das Kind selbst, seine Ängste und die Ängste der Eltern einzuschätzen und in den Behandlungsplan mit einzubeziehen. Nicht selten hängt eine suffiziente Wundversorgung vor allem von der richtigen Einschätzung des Kindes ab.
ULRIKE SUBOTIC UND GEORG STAUBLI
Primäre Ziele der Wundversorgung sind die Wiederherstellung der normalen Funktion, die Schmerzbehandlung, die Reduktion des Infektionsrisikos und ein gutes kosmetisches Ergebnis. Sekundäres Ziel der Wundversorgung ist es, dem Kind, und gelegentlich auch den Eltern, die Angst vor der Behandlung zu nehmen. Dadurch werden die Kooperation des Kindes und damit die Möglichkeit der optimalen Wundexploration erreicht. Um das zu erreichen, ist eine ausreichende Analgesie bereits bei der Erstbeurteilung der Wunde notwendig. Auch an das Entdecken und Behandeln zusätzlicher Verletzungen sollte man denken.
Anatomie und Physiologie von Wunden Die Epidermis, Dermis, das Subkutangewebe und die Faszie sind die Schichten, die am häufigsten bei einer akuten Wunde
Merksätze
❖ Eine ausreichende Analgesie ist bereits für die Erstbeurteilung und die Wundreinigung notwendig.
❖ Vor allem bei tiefen Bisswunden sowie Bisswunden im Gesicht und an den Händen ist die prophylaktische Antibiotikagabe zu erwägen.
❖ Der Tetanusschutz ist immer zu prüfen. ❖ Basisanalgetika (z.B. Paracetamol, NSAR) nicht vergessen, damit
die Kinder auch nach dem Eingriff möglichst schmerzfrei sind. ❖ Die Rasur bis auf die Haut erhöht das Infektionsrisiko. Das Rasieren
der Augenbrauen ist obsolet, da diese entweder sehr langsam oder gar nicht nachwachsen.
verletzt sind. Reicht die Wunde bis in das Subkutangewebe, ist das Erfassen beziehungsweise der Ausschluss einer Verletzung von Gefässen und Nerven oder tieferen Strukturen wie Sehnen, Muskulatur oder Gelenken und Knochen notwendig. Die Wundheilung durchläuft vier Stadien (1): 1. Blutstillung: Nach initialer Verletzung erfolgt die Blutstil-
lung mittels Aktivierung der Thrombozytenaggregation, Fibrin und der Gerinnungskaskade. 2. Entzündung: Das Einwandern von Neutrophilen und Makrophagen führt zu einer lokalen Entzündungsreaktion, die eine Ausbreitung von Bakterien verhindert und die Wundheilung initiiert. 3. Proliferation: Während der Proliferationsphase wird der Weichteildefekt durch Granulationsgewebe und Matrix ersetzt und der Defekt verschlossen. 4. Reifung: Das Granulationsgewebe wird während der Reifung durch Umwandlung von Kollagen Typ III in Kollagen Typ I verstärkt und gewinnt an Stabilität und Integrität. Nach 3 Wochen beträgt die Zugfestigkeit 20 Prozent und nach 3 Monaten 60 Prozent (2).
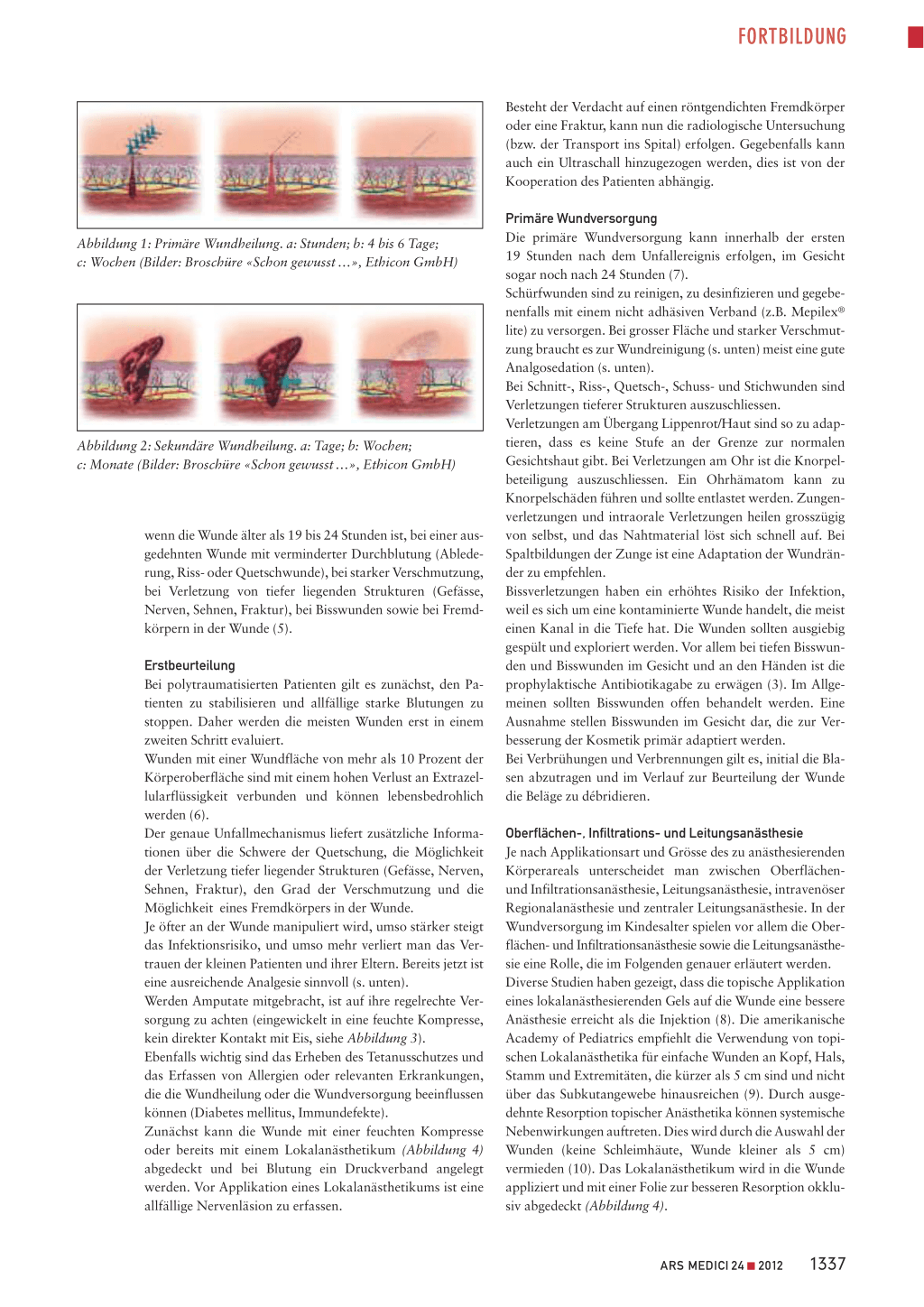
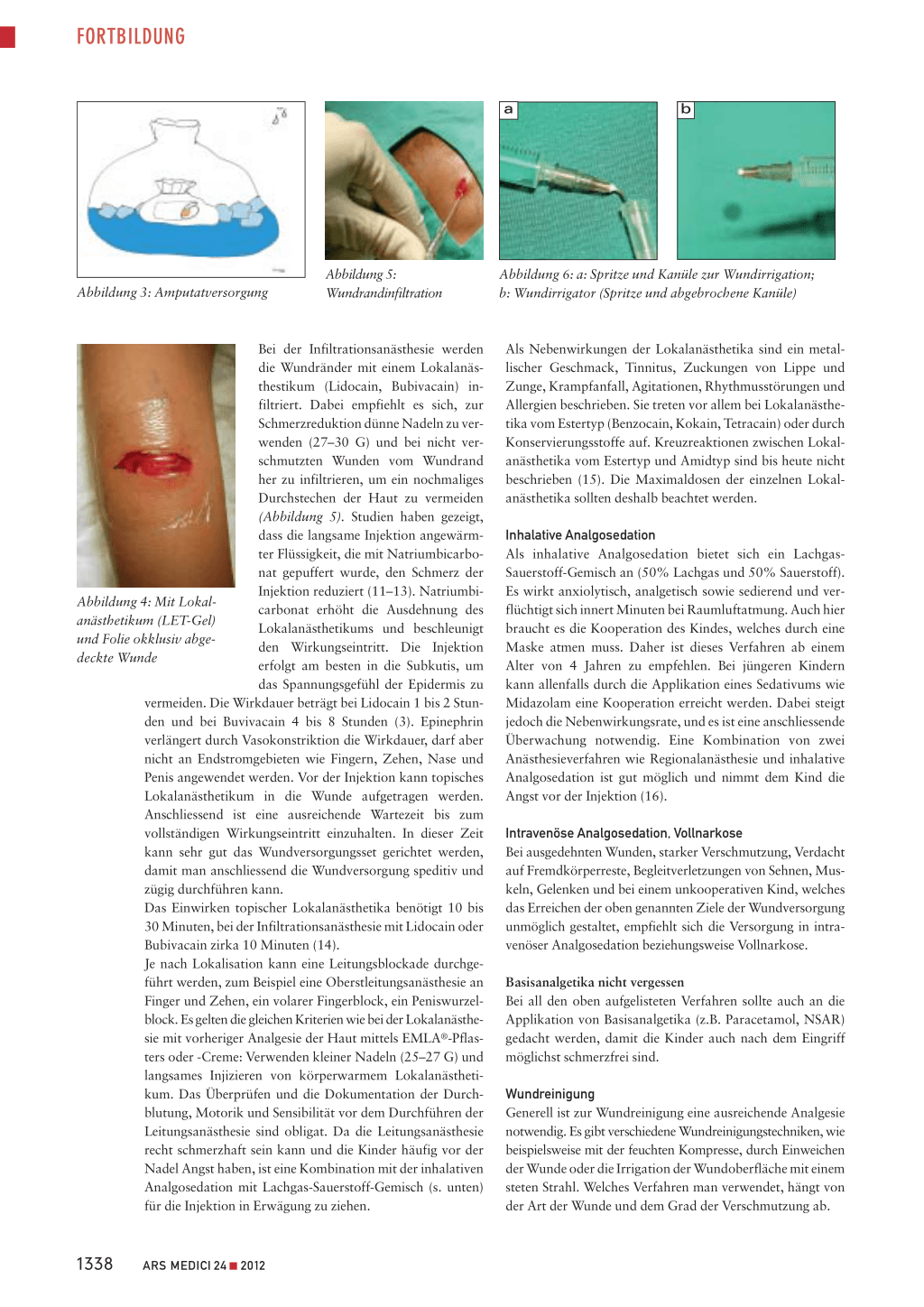
Voraussetzung für eine normale Wundheilung ist die ausreichende Blutversorgung. Entzündung, Infektion, Verschmutzung oder Nekrose verzögern beziehungsweise verhindern die adäquate Heilung. Das beste kosmetische Ergebnis wird bei einer primären Wundheilung erreicht. Hierunter versteht man den Wundverschluss mit Adaptation der Wundränder und Verschluss der Haut (Abbildung 1). Mitunter verzögert sich die Wundheilung, weil der Wundverschluss erst 3 bis 5 Tage nach dem Unfallereignis erfolgt, zum Beispiel bei verspäteter Vorstellung einer sauberen Wunde, bei primärer Versorgung einer Wundinfektion nach ausreichender Wundsäuberung oder nach Abwarten der Demarkierung bei initial nicht sicherer Durchblutung der Wundränder nach dem Débridement. Werden Wunden offen gelassen, kommt es zur sogenannten sekundären Wundheilung durch Kontraktion des Wundrandes (3) (Abbildung 2). Es gibt viele verschiedene Wundtypen, wie Prellungen, Quetschungen, Schürfwunden, Quetschwunden, Risswunden, Ablederungsverletzungen, Verbrühungen und Verbrennungen, Stich-, Schnitt- und Schusswunden sowie Pfählungsverletzungen und Bisswunden. Die meisten Wunden, vor allem bei kleinen Kindern, entstehen infolge Einwirkung stumpfer Gewalt am Kopf (4). Ein erhöhtes Infektionsrisiko besteht bei einer Verletzung über die Epidermis hinaus, bei Begleiterkrankungen wie Diabetes mellitus und Immunsuppression,
1336 ARS MEDICI 24 ■ 2012
FORTBILDUNG
Besteht der Verdacht auf einen röntgendichten Fremdkörper oder eine Fraktur, kann nun die radiologische Untersuchung (bzw. der Transport ins Spital) erfolgen. Gegebenfalls kann auch ein Ultraschall hinzugezogen werden, dies ist von der Kooperation des Patienten abhängig.
Abbildung 1: Primäre Wundheilung. a: Stunden; b: 4 bis 6 Tage; c: Wochen (Bilder: Broschüre «Schon gewusst …», Ethicon GmbH)
Abbildung 2: Sekundäre Wundheilung. a: Tage; b: Wochen; c: Monate (Bilder: Broschüre «Schon gewusst …», Ethicon GmbH)
wenn die Wunde älter als 19 bis 24 Stunden ist, bei einer ausgedehnten Wunde mit verminderter Durchblutung (Ablederung, Riss- oder Quetschwunde), bei starker Verschmutzung, bei Verletzung von tiefer liegenden Strukturen (Gefässe, Nerven, Sehnen, Fraktur), bei Bisswunden sowie bei Fremdkörpern in der Wunde (5).
Erstbeurteilung Bei polytraumatisierten Patienten gilt es zunächst, den Patienten zu stabilisieren und allfällige starke Blutungen zu stoppen. Daher werden die meisten Wunden erst in einem zweiten Schritt evaluiert. Wunden mit einer Wundfläche von mehr als 10 Prozent der Körperoberfläche sind mit einem hohen Verlust an Extrazellularflüssigkeit verbunden und können lebensbedrohlich werden (6). Der genaue Unfallmechanismus liefert zusätzliche Informationen über die Schwere der Quetschung, die Möglichkeit der Verletzung tiefer liegender Strukturen (Gefässe, Nerven, Sehnen, Fraktur), den Grad der Verschmutzung und die Möglichkeit eines Fremdkörpers in der Wunde. Je öfter an der Wunde manipuliert wird, umso stärker steigt das Infektionsrisiko, und umso mehr verliert man das Vertrauen der kleinen Patienten und ihrer Eltern. Bereits jetzt ist eine ausreichende Analgesie sinnvoll (s. unten). Werden Amputate mitgebracht, ist auf ihre regelrechte Versorgung zu achten (eingewickelt in eine feuchte Kompresse, kein direkter Kontakt mit Eis, siehe Abbildung 3). Ebenfalls wichtig sind das Erheben des Tetanusschutzes und das Erfassen von Allergien oder relevanten Erkrankungen, die die Wundheilung oder die Wundversorgung beeinflussen können (Diabetes mellitus, Immundefekte). Zunächst kann die Wunde mit einer feuchten Kompresse oder bereits mit einem Lokalanästhetikum (Abbildung 4) abgedeckt und bei Blutung ein Druckverband angelegt werden. Vor Applikation eines Lokalanästhetikums ist eine allfällige Nervenläsion zu erfassen.
Primäre Wundversorgung Die primäre Wundversorgung kann innerhalb der ersten 19 Stunden nach dem Unfallereignis erfolgen, im Gesicht sogar noch nach 24 Stunden (7). Schürfwunden sind zu reinigen, zu desinfizieren und gegebenenfalls mit einem nicht adhäsiven Verband (z.B. Mepilex® lite) zu versorgen. Bei grosser Fläche und starker Verschmutzung braucht es zur Wundreinigung (s. unten) meist eine gute Analgosedation (s. unten). Bei Schnitt-, Riss-, Quetsch-, Schuss- und Stichwunden sind Verletzungen tieferer Strukturen auszuschliessen. Verletzungen am Übergang Lippenrot/Haut sind so zu adaptieren, dass es keine Stufe an der Grenze zur normalen Gesichtshaut gibt. Bei Verletzungen am Ohr ist die Knorpelbeteiligung auszuschliessen. Ein Ohrhämatom kann zu Knorpelschäden führen und sollte entlastet werden. Zungenverletzungen und intraorale Verletzungen heilen grosszügig von selbst, und das Nahtmaterial löst sich schnell auf. Bei Spaltbildungen der Zunge ist eine Adaptation der Wundränder zu empfehlen. Bissverletzungen haben ein erhöhtes Risiko der Infektion, weil es sich um eine kontaminierte Wunde handelt, die meist einen Kanal in die Tiefe hat. Die Wunden sollten ausgiebig gespült und exploriert werden. Vor allem bei tiefen Bisswunden und Bisswunden im Gesicht und an den Händen ist die prophylaktische Antibiotikagabe zu erwägen (3). Im Allgemeinen sollten Bisswunden offen behandelt werden. Eine Ausnahme stellen Bisswunden im Gesicht dar, die zur Verbesserung der Kosmetik primär adaptiert werden. Bei Verbrühungen und Verbrennungen gilt es, initial die Blasen abzutragen und im Verlauf zur Beurteilung der Wunde die Beläge zu débridieren.
Oberflächen-, Infiltrations- und Leitungsanästhesie Je nach Applikationsart und Grösse des zu anästhesierenden Körperareals unterscheidet man zwischen Oberflächenund Infiltrationsanästhesie, Leitungsanästhesie, intravenöser Regionalanästhesie und zentraler Leitungsanästhesie. In der Wundversorgung im Kindesalter spielen vor allem die Oberflächen- und Infiltrationsanästhesie sowie die Leitungsanästhesie eine Rolle, die im Folgenden genauer erläutert werden. Diverse Studien haben gezeigt, dass die topische Applikation eines lokalanästhesierenden Gels auf die Wunde eine bessere Anästhesie erreicht als die Injektion (8). Die amerikanische Academy of Pediatrics empfiehlt die Verwendung von topischen Lokalanästhetika für einfache Wunden an Kopf, Hals, Stamm und Extremitäten, die kürzer als 5 cm sind und nicht über das Subkutangewebe hinausreichen (9). Durch ausgedehnte Resorption topischer Anästhetika können systemische Nebenwirkungen auftreten. Dies wird durch die Auswahl der Wunden (keine Schleimhäute, Wunde kleiner als 5 cm) vermieden (10). Das Lokalanästhetikum wird in die Wunde appliziert und mit einer Folie zur besseren Resorption okklusiv abgedeckt (Abbildung 4).
ARS MEDICI 24 ■ 2012 1337
FORTBILDUNG
ab
Abbildung 3: Amputatversorgung
Abbildung 5: Wundrandinfiltration
Abbildung 6: a: Spritze und Kanüle zur Wundirrigation; b: Wundirrigator (Spritze und abgebrochene Kanüle)
Bei der Infiltrationsanästhesie werden
die Wundränder mit einem Lokalanäs-
thestikum (Lidocain, Bubivacain) in-
filtriert. Dabei empfiehlt es sich, zur
Schmerzreduktion dünne Nadeln zu ver-
wenden (27–30 G) und bei nicht ver-
schmutzten Wunden vom Wundrand
her zu infiltrieren, um ein nochmaliges
Durchstechen der Haut zu vermeiden
(Abbildung 5). Studien haben gezeigt,
dass die langsame Injektion angewärm-
ter Flüssigkeit, die mit Natriumbicarbo-
nat gepuffert wurde, den Schmerz der
Abbildung 4: Mit Lokalanästhetikum (LET-Gel) und Folie okklusiv abgedeckte Wunde
Injektion reduziert (11–13). Natriumbicarbonat erhöht die Ausdehnung des Lokalanästhetikums und beschleunigt den Wirkungseintritt. Die Injektion erfolgt am besten in die Subkutis, um
das Spannungsgefühl der Epidermis zu
vermeiden. Die Wirkdauer beträgt bei Lidocain 1 bis 2 Stun-
den und bei Buvivacain 4 bis 8 Stunden (3). Epinephrin
verlängert durch Vasokonstriktion die Wirkdauer, darf aber
nicht an Endstromgebieten wie Fingern, Zehen, Nase und
Penis angewendet werden. Vor der Injektion kann topisches
Lokalanästhetikum in die Wunde aufgetragen werden.
Anschliessend ist eine ausreichende Wartezeit bis zum
vollständigen Wirkungseintritt einzuhalten. In dieser Zeit
kann sehr gut das Wundversorgungsset gerichtet werden,
damit man anschliessend die Wundversorgung speditiv und
zügig durchführen kann.
Das Einwirken topischer Lokalanästhetika benötigt 10 bis
30 Minuten, bei der Infiltrationsanästhesie mit Lidocain oder
Bubivacain zirka 10 Minuten (14).
Je nach Lokalisation kann eine Leitungsblockade durchge-
führt werden, zum Beispiel eine Oberstleitungsanästhesie an
Finger und Zehen, ein volarer Fingerblock, ein Peniswurzel-
block. Es gelten die gleichen Kriterien wie bei der Lokalanästhe-
sie mit vorheriger Analgesie der Haut mittels EMLA®-Pflas-
ters oder -Creme: Verwenden kleiner Nadeln (25–27 G) und
langsames Injizieren von körperwarmem Lokalanästheti-
kum. Das Überprüfen und die Dokumentation der Durch-
blutung, Motorik und Sensibilität vor dem Durchführen der
Leitungsanästhesie sind obligat. Da die Leitungsanästhesie
recht schmerzhaft sein kann und die Kinder häufig vor der
Nadel Angst haben, ist eine Kombination mit der inhalativen
Analgosedation mit Lachgas-Sauerstoff-Gemisch (s. unten)
für die Injektion in Erwägung zu ziehen.
Als Nebenwirkungen der Lokalanästhetika sind ein metallischer Geschmack, Tinnitus, Zuckungen von Lippe und Zunge, Krampfanfall, Agitationen, Rhythmusstörungen und Allergien beschrieben. Sie treten vor allem bei Lokalanästhetika vom Estertyp (Benzocain, Kokain, Tetracain) oder durch Konservierungsstoffe auf. Kreuzreaktionen zwischen Lokalanästhetika vom Estertyp und Amidtyp sind bis heute nicht beschrieben (15). Die Maximaldosen der einzelnen Lokalanästhetika sollten deshalb beachtet werden.
Inhalative Analgosedation Als inhalative Analgosedation bietet sich ein LachgasSauerstoff-Gemisch an (50% Lachgas und 50% Sauerstoff). Es wirkt anxiolytisch, analgetisch sowie sedierend und verflüchtigt sich innert Minuten bei Raumluftatmung. Auch hier braucht es die Kooperation des Kindes, welches durch eine Maske atmen muss. Daher ist dieses Verfahren ab einem Alter von 4 Jahren zu empfehlen. Bei jüngeren Kindern kann allenfalls durch die Applikation eines Sedativums wie Midazolam eine Kooperation erreicht werden. Dabei steigt jedoch die Nebenwirkungsrate, und es ist eine anschliessende Überwachung notwendig. Eine Kombination von zwei Anästhesieverfahren wie Regionalanästhesie und inhalative Analgosedation ist gut möglich und nimmt dem Kind die Angst vor der Injektion (16).
Intravenöse Analgosedation, Vollnarkose Bei ausgedehnten Wunden, starker Verschmutzung, Verdacht auf Fremdkörperreste, Begleitverletzungen von Sehnen, Muskeln, Gelenken und bei einem unkooperativen Kind, welches das Erreichen der oben genannten Ziele der Wundversorgung unmöglich gestaltet, empfiehlt sich die Versorgung in intravenöser Analgosedation beziehungsweise Vollnarkose.
Basisanalgetika nicht vergessen Bei all den oben aufgelisteten Verfahren sollte auch an die Applikation von Basisanalgetika (z.B. Paracetamol, NSAR) gedacht werden, damit die Kinder auch nach dem Eingriff möglichst schmerzfrei sind.
Wundreinigung Generell ist zur Wundreinigung eine ausreichende Analgesie notwendig. Es gibt verschiedene Wundreinigungstechniken, wie beispielsweise mit der feuchten Kompresse, durch Einweichen der Wunde oder die Irrigation der Wundoberfläche mit einem steten Strahl. Welches Verfahren man verwendet, hängt von der Art der Wunde und dem Grad der Verschmutzung ab.
1338 ARS MEDICI 24 ■ 2012
FORTBILDUNG
Einen besonderen Aspekt stellt die Haarent-
Tabelle:
fernung dar. Bei kleinen Wunden ist die
Tetanusprophylaxe bei Verletzungen
Saubere, oberflächliche Wunde
Alle anderen Wunden
Haarentfernung nicht notwendig, falls die Haare nicht die Wunde verunreinigen oder beim Wundverschluss stören. Sie können
Impfschutz
dT-/dTpa-/DTPa-IPV1 Anti-T-IgG2 dT-/dTpa-/DTPa-IPV1 Anti-T-IgG
feucht mit dem Kamm von der Wunde weg-
< 3 Dosen/ unbekannt ≥ 3 Dosen Ja Nein/Ja3 Nein Ja Nein Nein/Ja4 Ja Nein gestrichen werden. Die Rasur bis auf die Haut erhöht das Infektionsrisiko und kann die Wunde zusätzlich verunreinigen (21). Das Rasieren der Augenbrauen ist obsolet, 1Verabreichung eines Kombinationsimpfstoffes mit Diphtherie. Bei Kindern unter 8 Jahren Verabreichung einer Kombination da diese entweder sehr langsam oder gar mit Diphtherie (D, Kinderdosierung), Pertussis (Pa) und Polio (IPV). Bei Kindern im Alter von 8 bis 15 Jahren kann ebenfalls die Verabreichung einer Dosis dTpa angezeigt sein. nicht nachwachsen. 2 Tetanusimmunglobulin 3falls letzte Impfung mehr als 10 Jahre zurückliegt 4falls letzte Impfung mehr als 5 Jahre zurückliegt gemäss Schweizer Impfplan, Januar 2012 Débridement Für die Wundheilung sind vitale und saubere Wundverhältnisse unabdingbar. Mit dem Débridement wird nicht oder schlecht durchblutetes Gewebe mit dem Skalpell oder der Schere entfernt, und die Wundränder werden begra- digt, sodass der Wundverschluss besser durchführbar ist und die primäre Wundheilung verbessert wird (22). Bei Wunden, die primär verschlossen werden sollen, ist das Débridement sofort durchzuführen. Bei sekundärer Wundheilung ist eine Nachkontrolle notwendig und eventuell ein späteres Débridement zu planen. Abbildung 7: Schematische Darstellung der Einzelknopfnaht Mit der feuchten Kompresse und dem Einweichen löst man eingetrockneten Schmutz und verbessert das Milieu der Wunde. Bei stärker verschmutzten Wunden ist eine Wundirrigation für die Reduktion des Infektionsrisikos wichtig, da hiermit kleine Schmutzpartikel, Fremdkörper und Bakterien am besten entfernt werden können (3). Zur Irrigation lässt sich eine Spritze und eine abgebrochene Kanüle verwenden (Abbildung 6). Bezüglich der Wahl der Spülflüssigkeit gibt es in der Literatur unterschiedliche Empfehlungen (3, 17–20). Einigkeit besteht darüber, dass bei unkomplizierten, wenig verunreinigten Wunden mit gut durchblutetem Wundgrund und Wundrand eine ausgedehnte Wundreinigung nicht notwendig ist und isotone Kochsalzlösung oder Hahnenwasser zur Reinigung ausreichen (3, 17, 18). Eine prospektive Studie mit 530 Kindern, bei denen die Wunde entweder mit Kochsalzlösung oder Hahnenwasser gereinigt wurde, zeigte keinen Unterschied bezüglich Wundinfektion (19). Bei stärker verschmutzten Wunden besteht Uneinigkeit, ob die Wundreinigung mit Kochsalzlösung oder Hahnenwasser ausreichend ist, oder ob dafür verdünnte antiseptische Lösungen zu empfehlen sind. Argumente gegen die antiseptischen Lösungen sind deren Gewebetoxizität und die Hemmung der Proliferation von Fibroblasten (17, 18, 20). Tetanusimpfung, Antibiotika und Drainagen Der Tetanusschutz ist immer zu prüfen. Bei Patienten unter 25 Jahren, die mindestens 3 Impfdosen erhalten haben, wird bei sauberen und oberflächlichen Wunden die Auffrischimpfung mit dT-/dTpa (ab 8 Jahre) oder DTPa-IPV (unter 8 Jahren) empfohlen, wenn die letzte Impfung mehr als 10 Jahre zurückliegt. Bei Wunden mit erhöhtem Infektionsrisiko wird die Auffrischimpfung mit dT-/dTpa- (ab 8 Jahren) oder DTPa-IPV (unter 8 Jahren) empfohlen, wenn die letzte Impfung mehr als 5 Jahre zurückliegt. Bei Patienten, die weniger als 3 Impfdosen erhalten haben, oder bei nicht bekanntem oder nicht vorhandenem Tetanusschutz wird die Verabreichung einer Dosis dT-/dTpa (ab 8 Jahren) oder DTPa-IPV (unter 8 Jahren) und ergänzend die Verabreichung von Tetanusimmunglobulin empfohlen. Bei sauberen, oberflächlichen Wunden sind Immunglobuline nicht notwendig. Die Verabreichung von monovalentem T-Impfstoff sollte im Falle einer Verletzung vermieden werden, besonders bei kleinen Kindern, bei denen die Impfung gegen Diphtherie, Pertussis, Hib und Poliomyelitis gemäss Impfplan noch nicht abgeschlossen ist. Bei unvollständiger Impfung ist anschliessend der Impfschutz, unabhängig davon, ob Immunglobuline verabreicht wurden oder nicht, zu vervollständigen (Tabelle) (23). Weder topische noch systemische Antibiotika reduzieren das Infektionsrisiko (17, 24). Das Infektionsrisiko bei Wunden am Kopf beträgt 1,7 Prozent, bei Wunden an der unteren Extremität 23 Prozent (5). Bei tiefen Bisswunden und Bisswunden im Gesicht und an den Händen ist eine prophylaktische Antibiotikagabe jedoch zu erwägen. Bei Wundtaschen und stark kontaminierten Wunden empfiehlt sich die Einlage einer Wunddrainage für mindestens 48 Stunden. 1340 ARS MEDICI 24 ■ 2012 FORTBILDUNG SO MACHE ICH DAS Dr. med. Hansjörg Lang, Eschenz Ein grosses Problem bei der Wundversorgung bei Kindern, vor allem im Kopfbereich oder an der Hand, ist die Ruhigstellung. Die Kinder schlagen mit Armen und Beinen, und eine schöne Naht wird dadurch gefährdet. Ich stelle die Kinder bis etwa 3 Jahren ruhig, indem ich sie einwickle. Die Arme werden längs an den Körper gelegt, und mit einer robusten Decke werden Arme, Beine und Oberkörper eingewickelt. Wie eine Mumie liegt das Kind da, und interessanterweise wird es ruhig, weil es sich nicht bewegen kann. Hält dann eine Assistentin den Kopf oder den Arm, kann sehr schön genäht werden. ❖ Wundverschluss Unter dem Begriff Wundverschluss versteht man die Adaptation der Wundränder zur primären Wundheilung (siehe auch Abbildung 1 und 2). Generell ist zu beachten, dass die Wundränder ohne Stufenbildung adaptiert werden und dass in der Tiefe keine Wundhöhle entsteht. Oberflächliche Wunden, die die Subkutis nicht überschreiten, werden einschichtig, tiefere Wunden mehrschichtig verschlossen. Für die tieferen Schichten ist ein geflochtener resorbierbarer Faden zu empfehlen, zum Verschluss der Haut gibt es verschiedene Materialen wie Fadenmaterial, Wundkleber, Steristrips oder Klammern. Bei Kindern werden wegen des schmerzhaften Entfernens in der Regel keine Klammern verwendet. Lediglich auf dem behaarten Kopf sind sie manchmal hilfreich. Steristrips empfehlen sich für oberflächliche Wunden ohne Spannung. Sie können leicht vom Kind entfernt werden (Gefahr der Wunddehiszenz!). Häufig finden sie Verwendung als Wundverband zur zusätzlichen Reduktion der Spannung. Die Stabilität von Wundklebern (Butylcyanoacrylat, Octylcyanoacrylat) entspricht einem Faden mit der Stärke 5–0. Wundkleber wird bei sauberen, frischen, trockenen und oberflächlichen Wunden verwendet. Die Wundränder sollten ohne Zug adaptierbar sein, und die Wunde sollte im Alltag nicht unter Spannung stehen. Unter dem Hautkleber können sich zwar Wundtaschen bilden, aber das Auftragen ist einfach und schmerzfrei, und er löst sich von alleine mit der Hautschuppung nach 5 bis 10 Tagen ab. Kosmetisch erreichen korrekt angewendeter Wundkleber und Faden vergleichbare Ergebnisse (25). Mögliche Komplikationen sind Wundinfekt, das Aufreissen der Wunde und das Festkleben anderer Strukturen wie der Augenlider oder das Ankleben von Handschuh oder Kompresse bei der Applikation. Das gängigste und häufigste Material zur Wundversorgung ist der Faden. Dabei wird für den Hautverschluss ein monofiler Faden verwendet. Die Fadendicke ist abhängig von der Lokalisation der Wunde, der Spannung der Wundränder und dem Alter des Patienten. Verwendet man nicht resorbierba- ren Faden, ist die Fadenentfernung notwendig, bei resorbierbarem Faden ist die Resorptionszeit länger, bei geflochtenem Faden ist die Fremdkörperreaktion der Wunde stärker. Daher werden bei frischen Wunden vor allem im Gesicht nicht resorbierbare Fäden verwendet, um das beste kosmetische Ergebnis zu erreichen. Die Wundrandadaptation erfolgt in der Regel mit Einzelknopfnähten zur Vermeidung einer Infektion (Abbildung 7). Die Zeit bis zur Wundheilung und Fadenentfernung hängt von der Lokalisation der Wunde ab (Kopf: 5–7 Tage; Stamm: 8–10 Tage; Extremitäten: 10–14 Tage) (3). Bei Kindern verwenden wir bei oberflächlichen Wunden Steristrips, bei Wunden mit geraden Schnitträndern, die keine ausgedehnte Wundhöhle aufweisen und an spannungsarmen Stellen lokalisiert sind (Gesicht), Wundkleber, alle anderen Wunden werden mit Fadenmaterial verschlossen. Als Verband empfiehlt sich einfach aufzutragendes Material, welches möglichst schmerzfrei entfernt werden kann beziehungsweise die Beurteilung der Wunde nicht behindert. Ein feuchtes Milieu begünstigt die Wundheilung und beeinflusst die Narbenbildung. Es beugt der Zelldehydratation und dem Zelltod vor, unterstützt die Angioneogenese und verbessert die Phagozytose, die Ausschüttung von Wachstumsfaktoren sowie die Reepithelialisierung und damit das kosmetische Ergebnis (26). Dabei gilt es jedoch zu beachten, wie häufig die Wunde beurteilt werden soll, das heisst wie oft der Verband gewechselt werden muss (je höher das Infektionsrisiko, desto häufiger der Verbandswechsel). Adjuvante Therapie und Nachsorge Falls nötig, ist eine Ruhigstellung zur Vermeidung der Bean- spruchung der Wunde möglich. Die Häufigkeit der Wund- kontrollen hängt vom Infektionsrisiko ab. Nach der Faden- entfernung besteht ein Badeverbot für 24 Stunden, bis sich die Fadenkanäle verschlossen haben. Bei beginnender Nar- benhypertrophie empfiehlt sich die Behandlung mit silikon- haltigen Pflastern oder Gels (27). Ein guter Sonnenschutz wird bis zu 3 bis 6 Monate nach Abschluss der Wundheilung empfohlen (3). ❖ Korrespondenzadresse: Dr. med. Ulrike Subotic Chirurgische Klinik Universitätskinderspital Zürich Steinwiesstrasse 75 8032 Zürich E-Mail: ulrike.subotic@kispi.uzh.ch Literatur: Die Referenzenliste steht unter www.arsmedici.ch zur Verfügung. Erstpublikation in Pädiatrie 3/2012. ARS MEDICI 24 ■ 2012 1341 FORTBILDUNG Literatur: 1. Janis JE, Kwon RK, Lalonde DH. A practical guide to wound healing. Plast Reconstr Surg 2010; 125 (6): 230e–244e. 2. Barbul A. Wound healing. In: Brunicardi FC, Andersen DK, Billiar TR et al. (eds.) Schwartzs principles of surgery, 8th edn. The McGraw-Hill Companies, Columbus: 165–182. 3. Nicks BA et al. Acute wound management: revisiting the approach to assessment, irrigation and closure considerations. Int J Emerg Med 2010; 3: 399–407. 4. Holander JE, Singer AJ. Comparison of wound care practices in pediatric and adult lacerations repaired in the emergency department. Pediar Emerg Care 1998; 14 (1): 15–18. 5. Lammers RL, Hudson DL, Seaman ME: Prediction of traumatic wound infection with neural network-derived decision model. Am J Emerg Med 2003; 21 (1): 1–7. 6. Percival NJ. Classification of wounds and their management. Surgery 2002; 20 (5): 114–117. 7. Berk WA, Osbourne DD, Taylor DD. Evaluation of the «golden period» for wound repair: 204 cases from a Third World emergency department. Ann Emerg Med 1988; 17 (5): 496–500. 8. Ernst AA et al. Topical lidocaine adrenaline tetracaine (LAT gel) versus injectable buffered lidocaine for local anesthesia in laceration repair. West J Med 1997; 167 (2): 79–81. 9. Zempsky WT, Cravero JP. Relief of pain and anxiety in pediatric patients in emergency medical systems. Pediatrics 2004; 114 (5): 1348–1356. 10. Bonadio WA. Safe and effective method for application of tetracaine, adrenaline and cocaine to oral lacerations. Ann Emerg Med 1996; 28 (4): 396–398. 11. Fatovich DM, Jacobs IG. A randomized controlled trial of buffered lidocaine for local anesthetic infiltration in children and adults with simple lacerations. J Emerg Med 1999; 17 (2): 223–228. 12. Scarfone RJ, Jasani M, Gracely EJ. Pain of local anesthetics: Rate of administration and buffering. Ann Emerg Med 1998; 31 (1): 36–40. 13. Brogan GX, Singer AJ, Valentine SM et al. Comparison of wound infection rates using plain versus buffered lidocaine for anesthesia of traumatic wounds. Am J Emerg Med 1997; 15: 25–28. 14. Kundu S, Achar S. Principles of office anaesthesia: part II. Topical anaesthesia. Am Fam Physician 2002; 66 (1): 99–102. 15. Thyssen JP, Menné T, Elbering J, Plaschke P, Johansen JD. Hypersensitivity to local anesthetics – update and proposal of evaluation algorithm. Contact Dermat 2008; 59 (2): 69–78. 16. Kennedy RM, Luhmann JD. Pharmacological management of pain and anxiety during emergency procedures in children. Paediatr Drugs 2001; 3 (5): 337–354. 17. Morton LM, Phillips TJ. Wound healing update. Semin Cutan Med Surg 2012; 31 (1): 33–37. 18. Hollander JE, Singer AJ. Laceration management. Ann Emerg Med 1999; 34 (3): 356–367. 19. Valente JH et al. Wound irrigation in children: saline solution or tap water? Ann Emerg Med 2003; 41 (5): 609–616. 20. Khan MN, Naqvi AH. Antiseptics, iodine, povidone iodine and traumatic wound cleansing. J Tissue Viability 2006; 16 (4): 6–10. 21. Tang K, Yeh JS, Sgourus S. The influence of hair shave on the infection rate in neurosurgery. A prospective study. Pediatr Neurosurg 2001; 35: 13–17. 22. Lee CK, Hansen SL. Management of acute wounds. Clin Plast Surg 2007; 34: 685–696. 23. Bundesamt für Gesundheit, Eidgenössische Kommission für Impffragen (EKIF). Schweizerischer Impfplan 2012. Richtlinien und Empfehlungen: S. 22. 24. Stamou SC et al. Wound infections after minor limb lacerations: risk factors and the role of antimicrobial agents. J Trauma 1999; 46 (6): 1078–1081. 25. Farion KJ et al. Tissue adhesives for traumatic lacerations: a systematic review of randomized controlled trials. Acad Emerg Med 2003; 10 (2): 110–118. 26. Fonder MA, Mamelak AJ, Lazarus GS, Chanmugam A. Occlusive wound dressings in emergency medicine and acute care. Emerg Med Clin North Am 2007; 25 (1): 235–242. 27. Puri N, Talwar A. The efficacy of silicone gel for the treatment of hypertrophic scars and keloids. J Cutan Aesthet Surg 2009; 2 (2): 104–106. 1342 ARS MEDICI 24 ■ 2012