Transkript
Therapie der Psoriasis
Nicht nur auf die Haut achten!
FORTBILDUNG
Bei der Psoriasis haben sich in den letzten beiden Dekaden sowohl die Wahrnehmung der Erkrankung als auch die Therapieoptionen grundlegend geändert. Die Psoriasis wird heute nicht mehr als blosse Hauterkrankung betrachtet, sondern zu den chronisch-entzündlichen Systemerkrankungen gerechnet. Neue zielgerichtete Therapien, vor allem die Biologika, haben das Therapiespektrum deutlich erweitert.
SANDRA PHILIPP
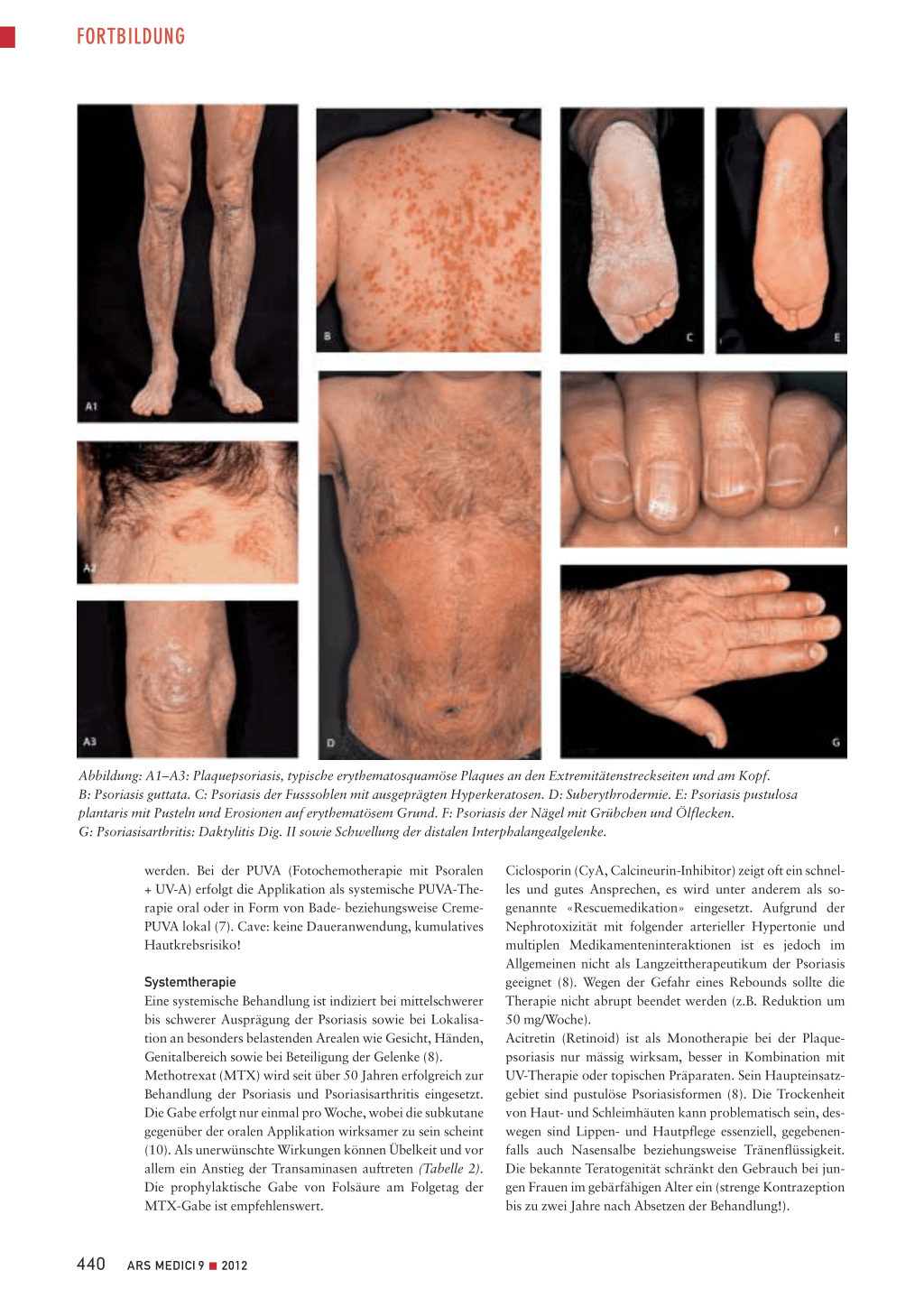
Die Psoriasis gehört mit einer Prävalenz von 2 bis 3 Prozent zu den häufigsten Hauterkrankungen (1) mit allein 1,6 Millionen Betroffenen in Deutschland. Im Vordergrund der Pathogenese steht eine fehlgesteuerte Immunreaktion, die dazu führt, dass eine Entzündungsreaktion sich selbst unterhält und nicht mehr abgeschaltet werden kann. Der dabei produzierte «Cocktail» pro-entzündlicher Botenstoffe verändert die Biologie der Hautzellen (Keratinozyten) und löst eine fehlerhafte sowie überstürzte Reifung der Zellen der Oberhaut (Epidermis) aus. Dadurch kommt es zu den typischen schuppenden rötlichen Psoriasisläsionen. Dabei lassen sich verschiedene Formen unterscheiden (Abbildung). Der Entzündungsprozess scheint jedoch nicht auf die Haut beschränkt zu bleiben, sondern kann auch andere Gewebe betreffen.
Merksätze
❖ Alle Patienten mit Psoriasis sollte man auf Gelenkbeschwerden ansprechen! Typisch sind Morgensteifigkeit oder nächtliche tief sitzende Rückenschmerzen mit Linderung der Beschwerden durch Bewegung.
❖ Patienten mit mittelschwerer bis schwerer Psoriasis sind auf Begleiterkrankungen des metabolischen Formenkreises zu untersuchen. Kontrollen von Gewicht (Hüftumfang!), Blutdruck, Blutglukose, Serumlipiden und EKG können eine frühzeitige Diagnose und Intervention ermöglichen.
Psoriasisarthritis Bei etwa 20 Prozent der Patienten findet sich eine Beteiligung der Gelenke und der Sehnenansätze (Enthesitis) (2). Dabei können die Finger- und Zehengelenke, einzelne bis mehrere grosse Gelenke oder die Wirbelsäule betroffen sein.
Komorbiditäten Des Weiteren finden sich Assoziationen mit anderen chronischentzündlichen Erkrankungen wie zum Beispiel dem M. Crohn sowie Erkrankungen des metabolischen Formenkreises. Untersuchungen zeigen, dass Patienten mit einer mittelschweren bis schweren Psoriasis deutlich häufiger an einer Adipositas, einer Hypertonie, einem Diabetes mellitus oder einer Dyslipidämie leiden als die Vergleichsbevölkerung und somit Risikofaktoren für kardiovaskuläre Erkrankungen aufweisen (3). Einzelne Arbeiten berichten, dass junge Patienten mit schwerer Psoriasis ein dreifach höheres Risiko für einen Herzinfarkt haben (4) beziehungsweise eine ausgeprägte Psoriasis zu einer Verkürzung der Lebenszeit um vier Jahre führen kann (5). Diese ausserhalb der Haut gelegenen Komorbiditäten der Psoriasis unterstreichen die Bedeutung einer interdisziplinären Betreuung der Patienten.
Topische Therapie Bei Patienten mit leichter Psoriasis werden topische Wirkstoffe favorisiert. Basistherapie ist die Hautpflege (z.B. harnstoffhaltige Präparate), um Hauttrockenheit und Juckreiz zu reduzieren. Salicylhaltige Externa unterstützen die Schuppenlösung. Bei trockener Haut sind bevorzugt Salben, bei akuter Entzündung Cremes oder Lotionen anzuwenden. Als Lokaltherapeutikum der ersten Wahl gelten Vitamin-D-Analoga, vor allem in der Erhaltungstherapie. Zu Beginn ist eine Kombination mit topischen Glukokortikoiden (6) möglich (rascheres Ansprechen). Weiterhin kommen Dithranol, teerhaltige Externa sowie Pimecrolimus und Tacrolimus (Cave: off label) zum Einsatz (Tabelle 1).
UV-Therapie Ist die topische Therapie allein nicht ausreichend, kann eine UV-Therapie in Betracht kommen. Die Foto- und Fotochemotherapie ist oft sehr gut wirksam und führt bei etwa drei Viertel der Patienten nach vier bis sechs Wochen zu einer ausreichenden Besserung des Hautbefundes (7). Heute wird häufig die Schmalspektrum-UV-B-Therapie (311 nm) eingesetzt, da diese die Entwicklung von Hautkrebs kaum begünstigt. Dennoch kann zum Beispiel wegen der Beschleunigung der Hautalterung nur über begrenzte Zeitintervalle therapiert
ARS MEDICI 9 ■ 2012 439
FORTBILDUNG
Abbildung: A1–A3: Plaquepsoriasis, typische erythematosquamöse Plaques an den Extremitätenstreckseiten und am Kopf. B: Psoriasis guttata. C: Psoriasis der Fusssohlen mit ausgeprägten Hyperkeratosen. D: Suberythrodermie. E: Psoriasis pustulosa plantaris mit Pusteln und Erosionen auf erythematösem Grund. F: Psoriasis der Nägel mit Grübchen und Ölflecken. G: Psoriasisarthritis: Daktylitis Dig. II sowie Schwellung der distalen Interphalangealgelenke.
werden. Bei der PUVA (Fotochemotherapie mit Psoralen + UV-A) erfolgt die Applikation als systemische PUVA-Therapie oral oder in Form von Bade- beziehungsweise CremePUVA lokal (7). Cave: keine Daueranwendung, kumulatives Hautkrebsrisiko!
Systemtherapie Eine systemische Behandlung ist indiziert bei mittelschwerer bis schwerer Ausprägung der Psoriasis sowie bei Lokalisation an besonders belastenden Arealen wie Gesicht, Händen, Genitalbereich sowie bei Beteiligung der Gelenke (8). Methotrexat (MTX) wird seit über 50 Jahren erfolgreich zur Behandlung der Psoriasis und Psoriasisarthritis eingesetzt. Die Gabe erfolgt nur einmal pro Woche, wobei die subkutane gegenüber der oralen Applikation wirksamer zu sein scheint (10). Als unerwünschte Wirkungen können Übelkeit und vor allem ein Anstieg der Transaminasen auftreten (Tabelle 2). Die prophylaktische Gabe von Folsäure am Folgetag der MTX-Gabe ist empfehlenswert.
Ciclosporin (CyA, Calcineurin-Inhibitor) zeigt oft ein schnelles und gutes Ansprechen, es wird unter anderem als sogenannte «Rescuemedikation» eingesetzt. Aufgrund der Nephrotoxizität mit folgender arterieller Hypertonie und multiplen Medikamenteninteraktionen ist es jedoch im Allgemeinen nicht als Langzeittherapeutikum der Psoriasis geeignet (8). Wegen der Gefahr eines Rebounds sollte die Therapie nicht abrupt beendet werden (z.B. Reduktion um 50 mg/Woche). Acitretin (Retinoid) ist als Monotherapie bei der Plaquepsoriasis nur mässig wirksam, besser in Kombination mit UV-Therapie oder topischen Präparaten. Sein Haupteinsatzgebiet sind pustulöse Psoriasisformen (8). Die Trockenheit von Haut- und Schleimhäuten kann problematisch sein, deswegen sind Lippen- und Hautpflege essenziell, gegebenenfalls auch Nasensalbe beziehungsweise Tränenflüssigkeit. Die bekannte Teratogenität schränkt den Gebrauch bei jungen Frauen im gebärfähigen Alter ein (strenge Kontrazeption bis zu zwei Jahre nach Absetzen der Behandlung!).
440 ARS MEDICI 9 ■ 2012
FORTBILDUNG
Tabelle 1:
Lokale Therapien
Wirkstoffe
Vitamin-D3-Analoga z.B. Calcipotriol, Calcitriol, Tacalcitol
Glukokortikoide topisch z.B. Prednicarbat, Mometasonfuroat, Hydrokortisonbutyrat, Betamethasonvalerat, Clobetasolpropionat Calcineurininhibitoren Pimecrolimus, Tacrolimus Dithranol (Cignolin)
Teerprodukte z.B. Liquor carbonis detergens
Wirkung
Anwendung, Nebenwirkungen, Kommentare
antiproliferativ, antientzündlich
❖ Lokaltherapeutika der 1.Wahl ❖ Langzeittherapie möglich, initial ❖ Kombination mit Glukokortikoiden (rasches Ansprechen) ❖ max. 30% der Körperoberfläche (Resorption!), Hautreizung
antientzündlich, immunsuppressiv, antiproliferativ
❖ häufige Mono- und Kombinationstherapie ❖ rasches Ansprechen, kurzzeitige Anwendung ❖ Cave: Hautatrophie bei Langzeitanwendung, Rezidiv bei abruptem ❖ Absetzen! ❖ differenzierter Einsatz nach Ausprägung und Lokalisation ❖ (therapeutischer Index [6])
antientzündlich, immunsuppressiv
❖ für spezielle Lokalisationen (Gesicht oder Intertrigines), um lokale ❖ Glukokortikoide zu reduzieren ❖ Cave: off label use!
antientzündlich,antiproliferativ
❖ wirksame und sichere Therapie, meist stationär ❖ langsame Dosissteigerung, oft Kombination mit UV-Therapie ❖ Cave: Hautreizung, irreversible Braunfärbung von Kleidung, ❖ Gegenständen
antiproliferativ, juckreizlindernd
❖ heute weniger häufig eingesetzt, v.a. als Shampoo ❖ in Einzelfällen sinnvoll, Kombination mit Salicylsäure, Glukokortikoiden ❖ unangenehmer Geruch
Fumarsäureester (Fumaderm®) gelten in Deutschland als systemische First-Line-Therapie zur Behandlung der mittelschweren bis schweren Psoriasis vulgaris, sind aber in der Schweiz nicht zugelassen (Kasten: Kommentar). Biologika sind gentechnisch hergestellte Proteinmoleküle, die die Wirkung körpereigener Proteine imitieren beziehungsweise blockieren. Sie gelten in Europa zurzeit als SecondLine-Therapeutika (11) und werden eingesetzt, wenn UV-Therapie oder traditionelle systemische Therapien keine ausreichende Wirksamkeit erzielten, unerwünschte Arzneimittelwirkungen aufgetreten sind oder Kontraindikationen bestehen. Aufgrund ihrer Proteinstruktur sind die Substanzen nicht oral verfügbar, sondern müssen parenteral verabreicht werden, das heisst entweder als subkutane Injektionen oder als Infusion. Die Dosierung und Behandlungsintervalle sind je nach Substanz variabel (Tabelle 2). Zwei Klassen von Biologika sind derzeit zur Therapie der Psoriasis zugelassen: die TNF-Inhibitoren und Ustekinumab.
TNFα-Inhibitoren TNFα ist ein Zytokin, das bei chronisch-entzündlichen Erkrankungen eine zentrale Rolle spielt. Die TNFα-Inhibitoren binden an TNFα, blockieren damit seine Wirkung und unterbrechen die Entzündungskaskade. Vier TNF-Inhibitoren (Infliximab, Adalimumab, Etanercept und Golimumab) sind in Europa zur Behandlung der Psoriasis vulgaris und/oder Psoriasisarthritis zugelassen. Die TNF-Inhibitoren weisen eine exzellente Wirksamkeit auf, nach 12 Wochen zeigen
zirka 50 bis 80 Prozent der Patienten eine 75-prozentige Verbesserung des PASI (Psoriasis Area and Severity Index = klinischer Score zur Beurteilung des Schweregrads der Psoriasis) (12). Die Ansprechraten sowie die Zeit bis zum Erreichen des Therapieerfolgs variieren jedoch je nach Substanz und Dosierung. Infliximab führt meist zu einer raschen Besserung des Hautbefundes, ein Teil der Patienten weist jedoch im Langzeitverlauf einen Wirkverlust auf. Dafür werden zum Teil neutralisierende Autoantikörper verantwortlich gemacht, deren Bildung durch zusätzliche Gabe von MTX möglicherweise reduziert werden kann (8). Adalimumab zeigt ebenfalls einen relativ schnellen Rückgang der Hautläsionen (12). Unter Etanercept und Golimumab sprechen die Hautveränderungen etwas langsamer an. Eine initial höhere Dosis von Etanercept (2–50 mg s.c.) in den ersten zwölf Wochen kann das Ansprechen jedoch beschleunigen (12) und ist durchaus üblich. Bei der Psoriasisarthritis zeigen alle TNF-Inhibitoren vergleichbar gute Ansprechraten (12). In Studien konnte gezeigt werden, dass sie auch die Progression der radiologischen Veränderungen aufhalten können. Deshalb sind sie bei gleichzeitiger aktiver Psoriasisarthritis besonders zu empfehlen (8, 11). Sie können eingesetzt werden, wenn NSAR und andere Basistherapien (z.B. MTX) nicht ausreichend wirksam waren. Ustekinumab (UST) ist ein humaner Antikörper gegen die gemeinsame p40-Untereinheit der Zytokine IL-12 und IL-23. Ustekinumab verhindert die Ausreifung bestimmter T-Zellen
ARS MEDICI 9 ■ 2012 441
FORTBILDUNG
Tabelle 2:
Klassische Systemtherapie – mit Auswahl wichtiger unerwünschter Wirkungen, modifiziert nach S3-Leitlinie Therapie der Psoriasis (8)
Medikament
Methotrexat
Wirkmechanismus
Folsäureantagonist antientzündlich, Wirkmechanismus nicht genau bekannt
Ciclosporin
Calcineurininhibitor: T-Zell-Hemmung über IL 2-/IFNγ-Blockade
Fumarsäureester (Fumaderm®
[in der Schweiz
nicht zugelassen])
nicht genau bekannt, u.a. NFκB-Hemmung: T-Zell-Apoptose, Migrationshemmung, Zytokinblockade
Acitretin (Neotigason®)
v.a. Proliferationsinhibition, antiinflammatorisch
Biologika
Etanercept (Enbrel®)
Fusionsprotein aus zwei TNF-Rezeptoren und humanem IgG, TNF-Blockade, HWZ 3 Tage
Adalimumab (Humira®)
humaner monoklonaler Antikörper gegen TNFα, HWZ 14 Tage
Infliximab (Remicade®)
chimärer monoklonaler Antikörper gegen TNFα, HWZ 8–10 Tage
Golimumab (Simponi®)
humaner monoklonaler Antikörper gegen TNFα, HWZ ca. 12 Tage
Ustekinumab (Stelara®)
humaner monoklonaler Antikörper gegen p40, IL-12-/-23-Blockade, HWZ 21 Tage
Anwendung, Nebenwirkungen, Kommentare
❖ auch Psoriasisarthritis ❖ 7,5–25 mg p.o. oder s.c. einmal pro Woche, meist Beginn mit 15 mg ❖ zusätzliche Gabe von Folsäure 5 mg am Folgetag der MTX-Gabe ❖ Haarausfall, Übelkeit, Hepatotoxizität, Arzneimittelinterferenzen, ❖ Infektionen, selten: Knochenmarkdepression, Pneumonitis ❖ Kontrazeption bis fünf Monate nach Ende der Therapie
❖ 2,5–5,0 mg/kg KG pro Tag auf zwei Einzelgaben verteilt ❖ Langzeitanwendung problematisch (1–2 Jahre), ❖ Cave: UV-Therapie → Plattenepithelkarzinom-Risiko! ❖ Nephrotoxizität, Hypertonie, gastrointestinale Symptome, Tremor, ❖ Gingivahyperplasie, Hypertrichose, multiple Arzneimittelinteraktionen, ❖ Rebound bei abruptem Absetzen
❖ Psoriasis vulgaris ❖ gut für die Langzeitanwendung geeignet ❖ einschleichende Dosierung! ❖ gastrointestinale Beschwerden, Flush, transiente Eosinophilie, ❖ Lymphozytopenie, Proteinurie, Transaminasenanstieg
❖ v.a. pustulöse Psoriasis, bei Plaquepsoriasis z.B. in Kombination mit ❖ UV-Therapie ❖ Trockenheit von Haut und Schleimhäuten, Hyperlipidämie, Effluvium, ❖ Muskel- und Gelenkschmerzen, Arzneimittelinterferenzen, Terato❖ genität (sichere Kontrazeption erforderlich!)
❖ initial bei Psoriasis vulgaris 2 × 50 mg s.c. für max. 12 Wo.; ❖ bei Psoriasisarthrithis und Erhaltung 2 × 25 mg oder 1 × 50 mg s.c. ❖ pro Woche ❖ Injektionsreaktionen, meist mild; selten Transaminasenanstieg ❖ Infektionen
❖ Initial 80 mg s.c., nach 1 Wo. 40 mg s.c., dann Erhaltung 40 mg s.c. alle ❖ 2 Wochen ❖ Injektionsreaktionen, meist mild; Haarausfall, Transaminasenanstieg ❖ Infektionen
❖ 5 mg/kg KG i.v. über 2 h, initial an Woche 0, 2 und 6; Erhaltung alle ❖ 8 Wochen ❖ Infusionsreaktionen (ca. 10%), meist mild, selten anaphylaktische ❖ Reaktionen; ggf. Prämedikation (Paracetamol, Prednisolon, Antihist❖ aminikum); Transaminasenanstieg ❖ Infektionen
❖ nur für Psoriasisarthritis zugelassen ❖ 50 mg s.c. alle 4 Wochen ❖ Injektionsreaktionen, Transaminasenanstieg ❖ Infektionen
❖ nur für Psoriasis vulgaris zugelassen ❖ 45 mg s.c. (> 100 kg KG: 90 mg s.c.) initial in Woche 0, Woche 4; ❖ Erhaltung alle 12 Wochen ❖ Kopfschmerzen, selten Arthralgien ❖ Infektionen
442 ARS MEDICI 9 ■ 2012
FORTBILDUNG
KOMMENTAR
Dr. Gisela Stauber-Reichmuth, Dänikon (ZH)
Warum sind Fumarsäureester zur Psoriasistherapie in der Schweiz nicht zugelassen?
Die Derivate der Fumarsäure, einer in Pflanzen vorkommenden Substanz, deren Namen vom gewöhnlichen Erdrauch (Fumaria officinalis) stammt, durchliefen einen bemerkenswerten Werdegang: vom Aussenseiter zum meistverschriebenen Systemtherapeutikum bei Psoriasispatienten in Deutschland. In den Fünfzigerjahren entdeckt und danach in unkontrollierten Rezepturen erhältlich, machten sie neben positiven Einzelberichten von Patienten auch negative Schlagzeilen. Vereinzelt traten schwere nephrotoxische Nebenwirkungen auf bis hin zu Niereninsuffizienz, die aber auf unsachgemässe Anwendung, insbesondere auf Überdosierungen durch Kombination oraler mit topischer Fumarsäuretherapien, zurückzuführen waren (1). Erst in den Achtzigerjahren erfolgte eine systematische Phase-III-Untersuchung an einem standardisierten Gemisch aus vier FumarsäureesterSubstanzen. Ein kleines Schweizer Pharmaunternehmen hatte dieses Medikament entwickelt und erhielt 1994 in Deutschland die Zulassung. Kurz vor Markteinführung sprang ein Lizenzpartner ab, da dieser das Nutzen-Risiko-Potenzial negativ bewertete. Weitere Aktivitäten zur Erlangung von Zulassungen in anderen Ländern unterblieben. Mittlerweile kann man auf 18 Jahre Erfahrung mit Fumarsäureestern in der Psoriasistherapie zurückblicken. Obwohl nur in Deutschland zugelassen, wird das Präparat auch in England oder Italien häufig eingesetzt und muss über Spital- oder internationale Apotheken bezogen werden. In der Schweiz wird es beispielsweise an der dermatologischen
Klinik des Universitätsspitals Zürich bei einigen Patienten angewandt. Heute wird das Präparat Fumaderm® durch Experten positiv bewertet. Dank guter Langzeitwirksamkeit und -verträglichkeit hat es sich in Deutschland vom umstrittenen Präparat zum First-Line-Medikament für die Therapie der mittelschweren oder schweren Psoriasis entwickelt. Den bis heute mit Fumaderm durchgeführten Studien wurde gemäss den deutschen und europäischen S3-Psoriasis-Leitlinien das zweithöchste Evidenzniveau zuerkannt. Weiterführende Studien zu Wirkmechanismen oder anderen Indikationen sind geplant oder wurden kürzlich abgeschlossen (2). Um die häufig auftretenden Nebenwirkungen wie Flushs und gastrointestinale Symptome zu reduzieren, entwickelte die oben erwähnte Schweizer Firma ein weiteres Medikament. BG-12 ist ein Fumarsäurepräparat der zweiten Generation, das die Monosubstanz Fumarsäuredimethylester enthält. Es wurde nicht nur für den Einsatz in der Psoriasistherapie, sondern auch in der Behandlung der multiplen Sklerose (MS) untersucht. 2005 wurden für BG-12 (Panaclar®) Resultate einer Phase-III-Studie zur Psoriasistherapie vorgestellt, in der es sich als verträglicher und wirksamer erwies als Fumaderm. Danach erfolgte in Deutschland ein Zulassungsantrag, der 2007 zugunsten einer europaweiten Zulassung wieder zurückgezogen wurde. Denn mittlerweile (2006) wurde die Schweizer Firma an ein grosses, international tätiges Pharmaunternehmen verkauft. Dieses war bereits seit 2003 an der Weiterentwicklung von BG-12 für die Behandlung von multipler Sklerose beteiligt. Erste klinische Phase-III-Resultate der DEFINE-Studie zur Therapie von schubförmig-remittierender MS mit BG-12 wurden 2011 präsentiert (3). Vor wenigen Wochen hat Biogen den Zulassungsantrag für BG-12 sowohl bei der FDA als auch bei der europäischen Zulassungsbehörde EMA gestellt. ❖
Literatur: 1. Altmeyer P.: Fumarsäureestern, In: H.C. Korting, W. Sterry (Hrsg.) Therapeutische
Verfahren in der Dermatologie, Blackwell Wissenschafts-Verlag, Berlin, Wien 2001; 593–598. 2. Mrowietz U. et. al.: Neue Erkenntnisse zu Fumarsäureestern (Fumaderm®): Ergebnisse eines Experten-Workshop, JDDG Supplement 2011; 4 (9): 1–13. 3. 5th Joint Triennial Congress of the European and Americas Committees for Treatment and Research in Multiple Sclerosis (ECTRIMS/ACTRIMS): Abstracts 95, P1071, P831, P994. Presented October 21, 2011.
(Th1- und Th17-Zellen), die über die Produktion proinflam-
matorischer Zytokine die Entzündungsreaktion unterhalten.
Die Wirksamkeit ist sehr gut. Je nach Dosis (45 vs. 90 mg)
wiesen 67 bis 76 Prozent der Patienten nach 12 Wochen eine
75-prozentige Verbesserung des PASI auf (13, 14).
Biologika weisen kaum Organtoxizitäten auf. Aufgrund
ihres möglichen Einflusses auf das Immunsystem wird als un-
erwünschte Wirkung bei Langzeitbehandlung vor allem ein
erhöhtes Risiko für das Auftreten von Infektionen bezie-
hungsweise von Malignomen diskutiert.
❖
Dr. med. Sandra Philipp Charité Universitätsmedizin Berlin Klinik für Dermatologie und Allergologie D-10117 Berlin
Interessenkonflikte: Referenten- oder Beratertätigkeit für Abbott, Actelion, Biogen, Janssen-Cilag, MSD, Pfizer.
Literatur unter www.allgemeinarzt-online.de/downloads
Diese Arbeit erschien zuerst in «Der Allgemeinarzt» 8/2011. Die für die Schweiz adaptierte Übernahme erfolgt mit freundlicher Genehmigung von Verlag und Autorin.
444 ARS MEDICI 9 ■ 2012