Transkript
PHARMA FORUM
Weidenrindenextrakt überzeugt in der Praxis bei über 4700 Patienten
RENATE WEBER
Während akute Schmerzzustände als Folge von Traumata oder Überbeanspruchung sehr effizient mit nichtsteroidalen Antirheumatika behandelt werden können, muss man bei chronischen rheumatischen Beschwerden neben der zuverlässigen Wirksamkeit auch eine langfristig gute Verträglichkeit fordern. Diesem Anforderungsprofil entspricht das Weidenrindenextrakt-Präparat Assalix®, das seit Mai 2003 in der Schweiz für die Behandlung von rheumatischen Beschwerden wie Kreuzschmerzen, Rücken- und Nackenschmerzen zugelassen und kassenpflichtig ist. Die in klinischen Studien nachgewiesene Wirksamkeit und Verträglichkeit wurde nun im Rahmen einer Anwendungsbeobachtung in Deutschland überprüft und bei über 4700 Patienten bestätigt.
An einer in Deutschland durchgeführten Anwendungsbeobachtung waren 922 Orthopäden, Internisten und Allgemeinpraktiker beteiligt, die 4731 Patienten mit chronischen Rücken- und Gelenkschmerzen über einen Zeitraum von 6 bis 8 Wochen mit Assalix® in unterschiedlicher Dosierung behandelten. Die Resultate wurden anlässlich des Kongresses «Phytopharmaca and Phytotherapy» im Februar 2004 in Berlin vorgestellt.
Situationsanalyse
Bei den Diagnosen dominierten chronische Rückenschmerzen (43%) und Arthrose-bedingte Beschwerden (37,5%). In den vergangenen sechs Monaten waren 86,6 Prozent der Patienten antirheumatisch-analgetisch behandelt worden, davon 40,9 Prozent mit Diclofenac und 16,4 Prozent mit Ibuprofen.
Auf den Inhalt der Beiträge in der Rubrik Pharma Forum nimmt die Redaktion keinen Einfluss. Die Verantwortung trägt der Autor oder die auftraggebende Firma.
Die Umstellung auf Assalix erfolgte bei 56,3 Prozent der Patienten aufgrund von Nebenwirkungen, bei 35,8% wegen unzureichender Wirksamkeit, und bei 8,1 Prozent war mangelnde Compliance der Grund. Die Initialdosis von durchschnittlich 3,4 Dragées wurde im Verlauf auf 3,1 Dragées reduziert. Die durchschnittliche Beobachtungszeit lag bei 8 Wochen.
Resultate der Anwendungsbeobachtung
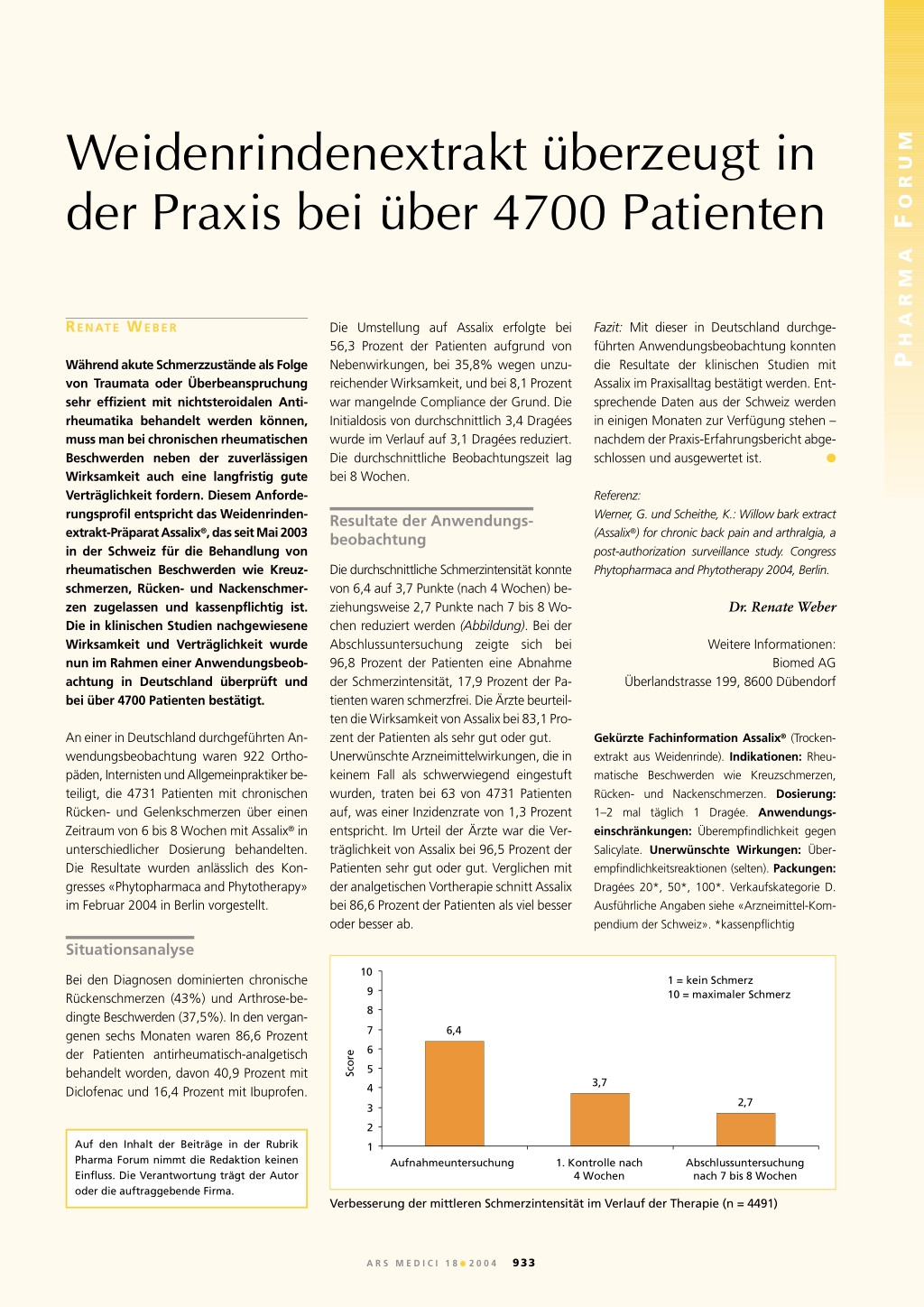
Die durchschnittliche Schmerzintensität konnte von 6,4 auf 3,7 Punkte (nach 4 Wochen) beziehungsweise 2,7 Punkte nach 7 bis 8 Wochen reduziert werden (Abbildung). Bei der Abschlussuntersuchung zeigte sich bei 96,8 Prozent der Patienten eine Abnahme der Schmerzintensität, 17,9 Prozent der Patienten waren schmerzfrei. Die Ärzte beurteilten die Wirksamkeit von Assalix bei 83,1 Prozent der Patienten als sehr gut oder gut. Unerwünschte Arzneimittelwirkungen, die in keinem Fall als schwerwiegend eingestuft wurden, traten bei 63 von 4731 Patienten auf, was einer Inzidenzrate von 1,3 Prozent entspricht. Im Urteil der Ärzte war die Verträglichkeit von Assalix bei 96,5 Prozent der Patienten sehr gut oder gut. Verglichen mit der analgetischen Vortherapie schnitt Assalix bei 86,6 Prozent der Patienten als viel besser oder besser ab.
Fazit: Mit dieser in Deutschland durchge-
führten Anwendungsbeobachtung konnten
die Resultate der klinischen Studien mit
Assalix im Praxisalltag bestätigt werden. Ent-
sprechende Daten aus der Schweiz werden
in einigen Monaten zur Verfügung stehen –
nachdem der Praxis-Erfahrungsbericht abge-
schlossen und ausgewertet ist.
q
Referenz: Werner, G. und Scheithe, K.: Willow bark extract (Assalix®) for chronic back pain and arthralgia, a post-authorization surveillance study. Congress Phytopharmaca and Phytotherapy 2004, Berlin.
Dr. Renate Weber
Weitere Informationen: Biomed AG
Überlandstrasse 199, 8600 Dübendorf
Gekürzte Fachinformation Assalix® (Trockenextrakt aus Weidenrinde). Indikationen: Rheumatische Beschwerden wie Kreuzschmerzen, Rücken- und Nackenschmerzen. Dosierung: 1–2 mal täglich 1 Dragée. Anwendungseinschränkungen: Überempfindlichkeit gegen Salicylate. Unerwünschte Wirkungen: Überempfindlichkeitsreaktionen (selten). Packungen: Dragées 20*, 50*, 100*. Verkaufskategorie D. Ausführliche Angaben siehe «Arzneimittel-Kompendium der Schweiz». *kassenpflichtig
Score
10 9 8 7 6,4 6 5 4 3 2 1 Aufnahmeuntersuchung
1 = kein Schmerz 10 = maximaler Schmerz
3,7 2,7
1. Kontrolle nach 4 Wochen
Abschlussuntersuchung nach 7 bis 8 Wochen
Verbesserung der mittleren Schmerzintensität im Verlauf der Therapie (n = 4491)
A R S M E D I C I 1 8 q 2 0 0 4 933