Transkript
FORTBILDUNG q FORMATION CONTINUE
Medikamentöse Epilepsietherapie
Wie lässt sich die Prognose bestimmen?
THOMAS DORN
Nach der Diagnose einer
Epilepsie stellt sich für den
Betroffenen und seine Ange-
hörigen die Frage, ob und
wenn ja wann mit einer
Anfallsfreiheit zu rechnen ist.
Im Folgenden werden die
Möglichkeiten und Grenzen
einer Prognose der Antiepi-
leptikatherapie erörtert.
Einleitung
Fragen nach dem weiteren Verlauf einer Epilepsie stellen sich vor allem dann, wenn eine progrediente, an sich schon behandlungsbedürftige Hirnerkrankung wie etwa ein Hinrtumor ausgeschlossen wurde. Die Prognose spielt aber nicht allein wegen der ängstlich fragenden Unsicherheit des Betroffenen eine wichtige Rolle, sie hat auch Auswirkungen auf die weitere Behandlungsplanung. In den vergangenen Jahren wurde diese Fragestellung zunehmend wissenschaftlich bearbeitet. Dabei wurde zunächst gefragt, inwieweit die Zuordnung zu den Kategorien fokal versus generalisiert beziehungsweise kryptogen/symptomatisch versus idiopathisch der Klassifikation der Internationalen Liga gegen Epilepsie (ILAE) (1)
eine prognostische Aussage zulässt. Die klinische Erfahrung zeigte, dass besonders bei fokalen Epilepsien – und um die soll es hier vorwiegend gehen – der Verlauf sehr unterschiedlich sein kann. Mit der rasanten Entwicklung der zerebralen Bildgebung in den letzten 10 bis 15 Jahren wurde nun eine erhebliche ätiologische Vielfalt der (fokalen) Epilepsien offenbar. Es kam die Hoffnung auf, dass vielleicht durch eine exakte Bestimmung der Ätiologie eine genauere prognostische Aussage im Einzelfall möglich ist (2). Eine genauere Abschätzung der Prognose fokaler Epilepsien beim einzelnen Patienten hat nämlich vor dem Hintergrund der Möglichkeit einer epilepsiechirurgischen Behandlung auch Auswirkungen auf die Therapiegestaltung bei diesem Patienten. Tatsächlich konnten bestimmte epileptogene Pathologien identifiziert werden, die bei den meisten davon betroffenen Patienten zu pharmakotherapieresistenten Epilepsien führen und deren Diagnose für eine frühe prächirurgische Diagnostik und Therapie spricht, bevor sich nach zeitraubenden Therapieversuchen mit vielen verschiedenen Antiepileptika eine Pharmakotherapieresistenz abzeichnet. Leider erlaubt auch der heutige Stand des Wissens und der Diagnostik in puncto Ätiopathogenese von Epilepsien in den meisten Fällen noch keine eindeutige Aussage bezüglich der Behandlungsprognose zum Zeitpunkt der Erstdiagnose. Wie lässt sich in diesen Fällen aber möglichst früh die Prognose abschätzen? Wann muss hier Pharmakotherapieresistenz angenommen werden? Welche Faktoren neben der Ätiologie bestimmen die pharmakologische Behandlungsprognose? Diesen Fragen widmen sich die folgenden Abschnitte, wobei zunächst noch einmal die Möglichkeiten und Grenzen der syndrom- beziehungsweise ätiologiebezoge-
Merk-
punkte
q Auch die modernen diagnostischen und ätiopathogenetischen Kenntnisse erlauben in den meisten Fällen zum Zeitpunkt der Erstdiagnose noch keine eindeutige Aussage bezüglich der Behandlungsprognose.
q Insbesondere bei fokalen Epilepsien ist die Prognose abhängig von sehr vielen, bisher nur zum Teil bekannten oder messbaren individuellen Determinanten, die neben der Ätiopathogenese die Pharmakokinetik, Pharmakodynamik und Pharmakogenetik betreffen.
q Bei Versagen der ersten Monotherapie sind die Chancen eines Behandlungserfolges mit einem weiteren Medikament minimiert.
q Beim einzelnen Patienten ist jedoch die systematische Erprobung alternativer, bis zur individuellen Toxizitätsgrenze ausdosierter Mono- bzw. Bitherapien angezeigt.
q Bei fokalen Epilepsien ist nach Versagen von zwei bis drei verschiedenen Therapieregimes Pharmakotherapieresistenz anzunehmen und – auch abhängig von der Ätiologie – die chirurgische Behandlungsoption zu prüfen.
nen Prognoseabschätzung aufgezeigt werden, bevor Studien zur Prognose der Pharmakotherapie bei fokalen Epilepsien erörtert werden und dann noch die mögliche Bedeutung pharmakogenetischer Faktoren sowie der Epilepsiedauer und einer allfälligen sekundären Epileptogenese für das Behandlungsergebnis beleuchtet wird. Abschliessend werden die sich aus den dargestellten Befunden ergebenden Kon-
A R S M E D I C I 1 7 q 2 0 0 4 855
FORTBILDUNG q FORMATION CONTINUE
Medikamentöse Epilepsietherapie
sequenzen für die Gestaltung der Pharmakotherapie zusammengefasst, die nicht nur für den Neurologen, sondern auch für den zuweisenden Allgemeinarzt von Bedeutung sind.
Grenzen der Prognoseabschätzung
Eine jüngere Studie (3) mit 2200 Patienten eines Zentrums, die über ein bis sieben Jahre beobachtet wurden, liefert Anhaltspunkte zur Behandlungsprognose von Epilepsien bezogen auf die Kategorien der ILAE-Klassifikation (Tabelle 1). Während 80 Prozent der Patienten mit idiopathisch generalisierten Epilepsien mit einer Pharmakotherapie für mindestens ein Jahr anfallsfrei werden, ist dies bei kryptogenen respektive symptomatisch generalisierten Epilepsien (u.a. Lennox-Gastaut-Syndrom) nur zu 27 Prozent der Fall. Bei den kryptogenen beziehungsweise symptomatischen fokalen Epilepsien liegt diese Zahl bei 35 respektive 45 Prozent. Die Kategorie «idiopathisch fokal», die vollständigkeitshalber in Tabelle 1 mit aufgeführt ist, wurde von den Autoren nicht untersucht, da diese in den allermeisten Fällen spontan ausheilenden benignen Partialepilepsien des Kindesalters oft gar keiner medikamentösen Behandlung bedürfen (4). Bei den nichtidiopathischen fokalen Epilepsien beleuchten die Autoren die Bedeutung der Ätiologie für das Behandlungsergebnis und führen aus, dass nur 11 Prozent der Patienten mit einer mesiotemporalen Sklerose mindestens ein Jahr anfallsfrei werden. Noch weniger, nämlich nur 3 Prozent mit einer im MRI darstellbaren dualen Pathologie (d.h. einer mesiotemporalen Sklerose plus einer anderen zerebralen Läsion, zum Beispiel einer kortikalen Dysplasie), wurden mit Antiepileptika anfallsfrei. Da diese Patienten oft durch einen epilepsiechirurgischen Eingriff anfallsfrei werden können (2), kann die frühe und exakte Bestimmung der Ätiologie eine Odyssee durch eine Reihe frustraner, zeitraubender und vielleicht auch nebenwirkungsträchtiger Pharmakotherapien verhindern. Aber auch bezogen auf eine bestimmte Ätiologie, zum Beispiel ein im MRI darstell-
Tabelle 1: Prognose bezüglich Anfallsfreiheit bei v e r s c h i e d e n e n E p i l e p s i e f o r m e n nach (3) und (4)
idiopathisch
kryptogen symptomatisch
fokal
nahezu 100% anfallsfrei Spontanheilung
35*–45**% anfallsfrei
generalisiert
80% anfallsfrei
* = kryptogen, ** = symptomatisch
27% anfallsfrei
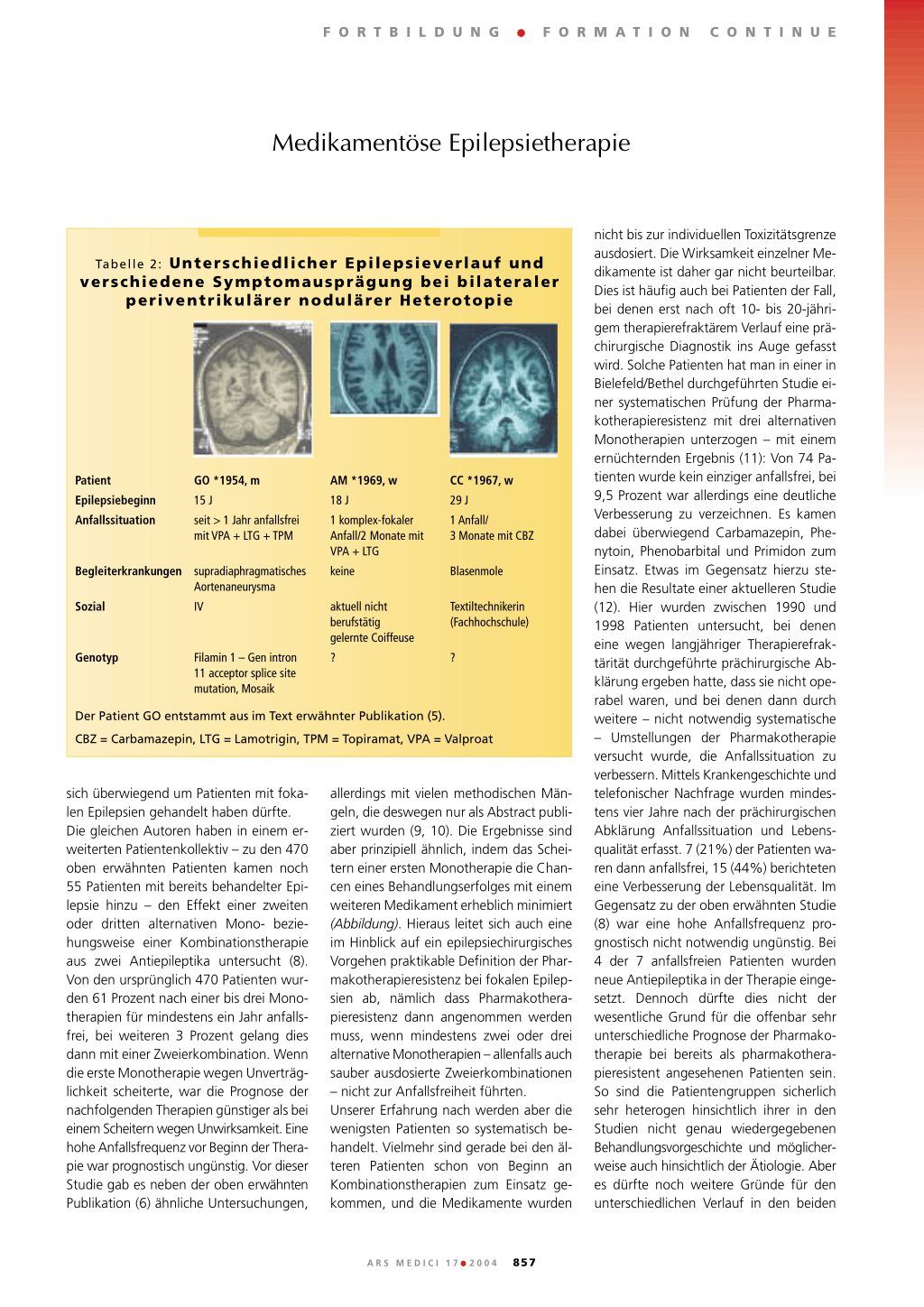
bares Hirnmissbildungssyndrom, können Verlauf und Behandlungsergebnis eine erhebliche Streubreite aufweisen. Dies mögen die in Tabelle 2 dargestellten drei PatientInnen aus unserem Zentrum mit bilateraler periventrikulärer nodulärer Heterotopie (BPNH) verdeutlichen. Während der Patient mit einer ausgeprägten Pathologie im MRI und auch extrazerebralen Syndrommanifestationen inzwischen anfallsfrei ist, erleiden die beiden Patientinnen mit deutlich weniger periventrikulären Noduli grauer Substanz immer noch Anfälle. Möglicherweise liefert der im Fall der beiden Patientinnen noch unklare Genotyp bei diesem sehr wahrscheinlich nicht nur auf sehr unterschiedliche Mutationen im Filamin1-Gen zu beziehenden Syndrom eine Erklärung (5). Die Grenzen solcher Betrachtungen liegen aber natürlich vor allem darin, dass es sich um keine epidemiologischen Studien handelt und eine Ansammlung von Patienten mit schwer behandelbaren Epilepsien an dem eine solche Studie durchführenden Zentrum anzunehmen ist. So ist die ganze prognostische Bandbreite – das heisst möglicherweise auch viel günstigere Behandlungsverläufe – bei einem bestimmten Syndrom nicht erkennbar. Zu berücksichtigen ist aber auch, dass bei der oben erwähnten Studie (3) kein fester Behandlungsalgorithmus gewählt wurde.
Prognose der Pharmakotherapie fokaler Epilepsien
Vor dem Hintergrund der in der Regel doch erheblichen Unschärfe, die sich bei
der Ableitung einer prognostischen Aussage aus der Ätiologie ergibt, macht es Sinn, sich unabhängig von der Ätiologie mit der Prognose einer antiepileptischen Pharmakotherapie zu befassen beziehungsweise nach mehr pharmakologischen Prädiktoren für ein gutes oder schlechtes Ansprechen auf eine Therapie zu suchen. Die erste hierzu wichtige Aussage ergibt sich aus einer Studie von 1987 (6): Die Prognose eines Behandlungsversuches ist unabhängig von der Auswahl des Medikamentes. Es wird daher empfohlen, sich bei der Ersttherapie vor allem am Nebenwirkungsprofil zu orientieren, wobei dies heute bezüglich unterschiedlicher Patientengruppen und Komorbiditäten sehr differenziert zu sehen ist. Erst in jüngerer Zeit gelang es, die Prognose der Pharmakotherapie von Epilepsien methodisch einigermassen akzeptabel zu untersuchen. So wurde die Prognose einer ersten Monotherapie angeschaut (7), indem 470 Patienten, die nach ersten Anfällen zwischen 1984 und 1987 behandelt wurden, unter einer ersten Monotherapie (überwiegend mit Valproat, Carbamazepin oder Lamotrigin) beobachtet wurden. 47 Prozent der Patienten wurden mit einer ersten Monotherapie für mindestens ein Jahr anfallsfrei. Für das Scheitern der Therapie waren Unverträglichkeiten und ungenügende Wirksamkeit gleichermassen von Bedeutung. Anfallsfreiheit stellte sich meist schon bei geringen bis mittleren Dosierungen ein. Schwachpunkt dieser Studie ist, dass die Epilepsiesyndrome nicht klar bestimmt wurden; es ist aber anzunehmen, dass es
856 A R S M E D I C I 1 7 q 2 0 0 4
FORTBILDUNG q FORMATION CONTINUE
Medikamentöse Epilepsietherapie
Tabelle 2: Unterschiedlicher Epilepsieverlauf und verschiedene Symptomausprägung bei bilateraler
periventrikulärer nodulärer Heterotopie
Patient Epilepsiebeginn Anfallssituation
GO *1954, m
15 J
seit > 1 Jahr anfallsfrei mit VPA + LTG + TPM
Begleiterkrankungen supradiaphragmatisches Aortenaneurysma
Sozial
IV
Genotyp
Filamin 1 – Gen intron 11 acceptor splice site mutation, Mosaik
AM *1969, w 18 J 1 komplex-fokaler Anfall/2 Monate mit VPA + LTG keine
aktuell nicht berufstätig gelernte Coiffeuse ?
CC *1967, w 29 J 1 Anfall/ 3 Monate mit CBZ
Blasenmole
Textiltechnikerin (Fachhochschule)
?
Der Patient GO entstammt aus im Text erwähnter Publikation (5). CBZ = Carbamazepin, LTG = Lamotrigin, TPM = Topiramat, VPA = Valproat
sich überwiegend um Patienten mit fokalen Epilepsien gehandelt haben dürfte. Die gleichen Autoren haben in einem erweiterten Patientenkollektiv – zu den 470 oben erwähnten Patienten kamen noch 55 Patienten mit bereits behandelter Epilepsie hinzu – den Effekt einer zweiten oder dritten alternativen Mono- beziehungsweise einer Kombinationstherapie aus zwei Antiepileptika untersucht (8). Von den ursprünglich 470 Patienten wurden 61 Prozent nach einer bis drei Monotherapien für mindestens ein Jahr anfallsfrei, bei weiteren 3 Prozent gelang dies dann mit einer Zweierkombination. Wenn die erste Monotherapie wegen Unverträglichkeit scheiterte, war die Prognose der nachfolgenden Therapien günstiger als bei einem Scheitern wegen Unwirksamkeit. Eine hohe Anfallsfrequenz vor Beginn der Therapie war prognostisch ungünstig. Vor dieser Studie gab es neben der oben erwähnten Publikation (6) ähnliche Untersuchungen,
allerdings mit vielen methodischen Mängeln, die deswegen nur als Abstract publiziert wurden (9, 10). Die Ergebnisse sind aber prinzipiell ähnlich, indem das Scheitern einer ersten Monotherapie die Chancen eines Behandlungserfolges mit einem weiteren Medikament erheblich minimiert (Abbildung). Hieraus leitet sich auch eine im Hinblick auf ein epilepsiechirurgisches Vorgehen praktikable Definition der Pharmakotherapieresistenz bei fokalen Epilepsien ab, nämlich dass Pharmakotherapieresistenz dann angenommen werden muss, wenn mindestens zwei oder drei alternative Monotherapien – allenfalls auch sauber ausdosierte Zweierkombinationen – nicht zur Anfallsfreiheit führten. Unserer Erfahrung nach werden aber die wenigsten Patienten so systematisch behandelt. Vielmehr sind gerade bei den älteren Patienten schon von Beginn an Kombinationstherapien zum Einsatz gekommen, und die Medikamente wurden
nicht bis zur individuellen Toxizitätsgrenze ausdosiert. Die Wirksamkeit einzelner Medikamente ist daher gar nicht beurteilbar. Dies ist häufig auch bei Patienten der Fall, bei denen erst nach oft 10- bis 20-jährigem therapierefraktärem Verlauf eine prächirurgische Diagnostik ins Auge gefasst wird. Solche Patienten hat man in einer in Bielefeld/Bethel durchgeführten Studie einer systematischen Prüfung der Pharmakotherapieresistenz mit drei alternativen Monotherapien unterzogen – mit einem ernüchternden Ergebnis (11): Von 74 Patienten wurde kein einziger anfallsfrei, bei 9,5 Prozent war allerdings eine deutliche Verbesserung zu verzeichnen. Es kamen dabei überwiegend Carbamazepin, Phenytoin, Phenobarbital und Primidon zum Einsatz. Etwas im Gegensatz hierzu stehen die Resultate einer aktuelleren Studie (12). Hier wurden zwischen 1990 und 1998 Patienten untersucht, bei denen eine wegen langjähriger Therapierefraktärität durchgeführte prächirurgische Abklärung ergeben hatte, dass sie nicht operabel waren, und bei denen dann durch weitere – nicht notwendig systematische – Umstellungen der Pharmakotherapie versucht wurde, die Anfallssituation zu verbessern. Mittels Krankengeschichte und telefonischer Nachfrage wurden mindestens vier Jahre nach der prächirurgischen Abklärung Anfallssituation und Lebensqualität erfasst. 7 (21%) der Patienten waren dann anfallsfrei, 15 (44%) berichteten eine Verbesserung der Lebensqualität. Im Gegensatz zu der oben erwähnten Studie (8) war eine hohe Anfallsfrequenz prognostisch nicht notwendig ungünstig. Bei 4 der 7 anfallsfreien Patienten wurden neue Antiepileptika in der Therapie eingesetzt. Dennoch dürfte dies nicht der wesentliche Grund für die offenbar sehr unterschiedliche Prognose der Pharmakotherapie bei bereits als pharmakotherapieresistent angesehenen Patienten sein. So sind die Patientengruppen sicherlich sehr heterogen hinsichtlich ihrer in den Studien nicht genau wiedergegebenen Behandlungsvorgeschichte und möglicherweise auch hinsichtlich der Ätiologie. Aber es dürfte noch weitere Gründe für den unterschiedlichen Verlauf in den beiden
A R S M E D I C I 1 7 q 2 0 0 4 857
FORTBILDUNG q FORMATION CONTINUE
Medikamentöse Epilepsietherapie
Polymorphismen eine funktionelle Bedeutung haben dürften. So wurde unlängst gezeigt, dass ein genetischer Polymorphismus des so genannten ABCB1-Transporter-Gens Pharmakotherapieresistenz mit determinieren könnte (16).
Abbildung: Vergleich von vier verschiedenen Studien zur Prognose alternativer Pharmakotherapieregimes bei fokalen Epilepsien*, deren Autoren jeweils unterhalb des entsprechenden Diagramms angegeben sind (nach 6, 8, 9, 10): MT = Monotherapie, PT = Polytherapie (PT als drittes Therapieregime nur bei [6, 10]). Die Patientenzahlen sind 100 (10), 622 (6), 40 (9) beziehungsweise 470 (8). Nur bei der jüngsten Studie (8) kamen neuere Antiepileptika zum Einsatz. *Beachte, dass bei dieser Studie auch einige Patienten mit generalisierten Epilepsien berücksichtigt wurden.
Studien beziehungsweise bei Epilepsiepatienten mit der gleichen Hirnpathologie geben. Heute gelingt es zunehmend, die Bedingungen zu analysieren, die neben der ohnehin schon vielfältigen Ätiologie die Behandlungsprognose einer Epilepsie determinieren. Hierzu zählen vor allem pharmakogenetische Gegebenheiten und die Behandlungsdauer beziehungsweise wahrscheinlich auch die so genannte sekundäre Epileptogenese.
Pharmakogenetik – multiple Drug Resistance (MDR)-Gene
In der Pharmakogenetik wird untersucht, inwieweit genetische Faktoren Pharmakodynamik und Pharmakokinetik eines Medikamentes beeinflussen. Schon lange ist bekannt, dass eine bestimmte Dosis eines Medikamentes beziehungsweise Antiepileptikums in verschiedenen Patienten zu sehr unterschiedlichen Serumkonzentrationen und damit auch unterschiedlichen pharmakologischen Effekten führt (13). Neben der zum Beispiel von Begleitmedikamenten und nutritiven Faktoren abhängigen Enzyminduktion wurden auch
genetische Determinanten des Antiepileptikametabolismus erkannt. So ist der Phenytoinmetabolismus über die Zytochrom-P-450-Isoenzyme zum Teil genetisch determiniert. Eine kleine Gruppe von Patienten sind «slow metabolizers» und bauen bei einer gegebenen Dosis deutlich höhere Serumkonzentrationen mit der Gefahr einer Intoxikation auf als die übrigen (14). Die Geschwindigkeit des Antiepileptikametabolismus sollte aber die Prognose nicht wesentlich bestimmen, da die Variabilität der Natur durch die entsprechende Wahl der Dosis kompensiert werden kann. Schwieriger wird dies, wenn der Transport der Substanz zum Zielorgan beziehungsweise Zielrezeptor erschwert ist. Es gibt mehrere Familien von Transportproteinen – auf die man vor allem in der Onkologie aufmerksam wurde –, die körperfremde Substanzen und somit auch Antiepileptika aus den Organen zurück ins Blut oder in Galle und Urin transportieren; diese könnten an der Entstehung von Pharmakotherapieresistenz bei Epilepsien beteiligt sein (15). Diese Transporter werden durch polymorphe Gene determiniert, wobei einzelne
Bedeutung der Krankheitsdauer für die Prognose
In letzter Zeit wird zunehmend die Frage untersucht, inwieweit die Dauer einer Epilepsie beziehungsweise auch die Zahl der bisher aufgetretenen Anfälle die Prognose beeinflussen – auch wenn die zugrunde liegende Pathologie nicht progredient ist. Möglicherweise können epileptische Anfälle zumindest bei bestimmten Epilepsieformen zu Umbauvorgängen im Gehirn führen, die die Wahrscheinlichkeit für das Auftreten weiterer Anfälle begünstigen. Seit den späten Sechzigerjahren taucht in diesem Zusammenhang auch der Begriff «sekundäre Epileptogenese» auf. So wird angenommen, dass durch epileptische Aktivität in einem durch eine Läsion verursachten epileptischen Herd in anderen, primär gesunden Hirnarealen ebenfalls autochthone epileptische Herde induziert werden können (17). Ein von Löscher (18) vorgeschlagenes Modell geht davon aus, dass es im Gefolge einer Läsion des Kortex zu einer Kaskade von Umbauvorgängen kommen kann, die zunächst zum Auftreten pharmakologisch behandelbarer Anfälle, im weiteren Verlauf dann aber durch Mechanismen, die von den Anfällen selbst induziert werden, wie zum Beispiel Neurodegeneration, zu einer pharmakotherapierefraktären Epilepsie führen. Dieser Ansatz führt auch zur Forderung, unser gegenwärtiges Arsenal antikonvulsiv wirkender Medikamente, also die so genannten Antiepileptika, durch antiepileptogen wirkende Substanzen respektive krankheitsmodifizierende Therapieverfahren zu ergänzen. Dieser Ansatz bedeutet auch, dass Anfallsfreiheit möglichst zügig durch systematische Therapieführung angestrebt werden und im Fall von Pharmakotherapieresistenz die operative Behandlungsoption abgeklärt werden muss.
858 A R S M E D I C I 1 7 q 2 0 0 4
FORTBILDUNG q FORMATION CONTINUE
Medikamentöse Epilepsietherapie
Fazit
1. Gerade bei fokalen Epilepsien ist die Therapieprognose abhängig von sehr vielen, bisher nur zum Teil bekannten oder messbaren individuellen Determinanten, die neben der Ätiopathogenese die Pharmakokinetik, Pharmakodynamik und Pharmakogenetik betreffen.
2. Beim einzelnen Patienten ist also die systematische Erprobung alternativer, bis zur individuellen Toxizitätsgrenze ausdosierter Mono- beziehungsweise Bitherapien angezeigt. Auch wenn aufgrund der Studie von Kwan und Brodie (6) gefolgert werden könnte, dass das Ausdosieren bis zur Toxizitätsgrenze nicht mehr viel bringt, wenn sich bei niedrigen bis mittleren Dosierungen keine Anfallsfreiheit eingestellt hat, halte ich an dem obigen Prinzip fest, da einzelne Patienten eben doch davon profitieren
und man deshalb ohne Ausdosieren Gefahr läuft, später nach einem allfälligen Scheitern weiterer Therapien erneut vor der Frage zu stehen, ob das früher verworfene Medikament nicht doch noch einmal eingesetzt werden sollte. Solche Reexpositionen sind aber aufgrund pharmakokinetischer Interaktionen, die das Umstellen der Therapie erheblich erschweren können, häufig dann sehr schwierig und langwierig. 3. Bei fokalen Epilepsien ist nach Versagen von zwei bis drei verschiedenen Therapieregimes Pharmakotherapieresistenz anzunehmen, und es gilt – auch abhängig von der Ätiologie –, die chirurgische Behandlungsoption zu prüfen. 4. Eine Pharmakotherapieresistenz-Prüfung sollte aus psychosozialen und wahrscheinlich auch biologischen Gründen – Stichwort sekundäre Epileptogenese – nicht länger als zwei Jahre dauern.
5. Als ceterum censeo sei angemerkt, dass
Pseudotherapieresistenz bei Non-Com-
pliance kein seltenes Phänomen auf dem
oft langwierigen Weg zur optimalen
Therapie ist und deshalb im Auge be-
halten und mit dem Patienten offen
thematisiert werden muss (19).
q
Das Literaturverzeichnis kann beim Verlag angefordert werden (info@rosenfluh.ch)
Anschrift des Autors: Dr. Thomas Dorn Leitender Arzt
Schweizerisches Epilepsie-Zentrum Bleulerstrasse 60, 8008 Zürich Tel. 01-387 63 43 Fax 01-387 63 97
E-Mail: Thomas.Dorn@swissepi.ch Internet: www.swissepi.ch
Interessenkonflikte: keine