Transkript
Im Fokus: Multiples Myelom und maligne Lymphome
Ersttherapie des multiplen Myeloms beim jüngeren Patienten
Stellenwert neuer Therapiekonzepte
Bei Patienten mit Erstdiagnose eines multiplen Myeloms muss nach wie vor evaluiert werden, ob sie für eine Behandlungsintensifikation mittels Hochdosis-Chemotherapie (HDT) und anschliessender autologer Stammzelltransplantation (ASZT) qualifizieren. Durch eine Reihe kürzlich publizierter Studien konnten der Stellenwert, die optimale Zusammensetzung und die Therapiedauer der verschiedenen Behandlungsschritte (Induktion, Intensifikation, Konsolidation, Erhaltung) nun klarer definiert werden.
PANAGIOTIS SAMARAS, CHRISTOPH RENNER
SZO 2019; 2: 6–8.
Panagiotis Samaras Christoph Renner
HDT und ASZT nach mindestens partiellem Ansprechen auf eine Induktionstherapie bleiben dabei auch im Zeitalter neuer Substanzen wesentliche Eckpfeiler in der Erstlinienbehandlung jüngerer Patienten.
Ist die Hochdosis-Chemotherapie im Zeitalter neuer Substanzen noch notwendig?
Die Frage, ob durch verschiedene Kombinationen neuer Substanzen eine Hochdosis-Chemotherapie mit Melphalan unnötig wird, wurde in verschiedenen klinischen Studien gestellt. Bereits vor einigen Jahren wurden die Ergebnisse einer randomisierten italienischen Studie publiziert, in der nach Induktionsbehandlung entweder 1 bis 2 HDT/ASZT oder eine Konsolidation mit Melphalan, Prednison und Lenalidomid (MPR) durchgeführt wurden. Die Patienten mit intensiver Behandlung (HDT + ASZT) hatten dabei ein deutlich besseres Gesamtüberleben (OS). Allerdings muss einschränkend erwähnt werden, dass die Patienten in dieser Studie lediglich Lenalidomid und
ABSTRACT
First line treatment in younger patients with multiple myeloma
Younger and biologically fit patients should receive an active induction treatment, ideally containing a proteasome inhibitor and an immunomodulatory drug as first line treatment. High dose chemotherapy with subsequent autologous stem cell transplantation (ASCT) after achievement of at least partial response with the induction treatment is still considered standard of care for these patients. Progression free and overall survival may be further improved with a maintenance treatment with lenalidomide after ASCT for at least two years or until progression. Alternatively, the proteasome inhibitors bortezomib or ixazomib may be used as maintenance drugs in patients not tolerating lenalidomide. Importantly, cost coverage must be obtained from the health insurance for the different treatment steps beforehand.
Keywords: Multiple myeloma, proteasome inhibitor, immunomodulatory drug, autologous stem cell transplantation.
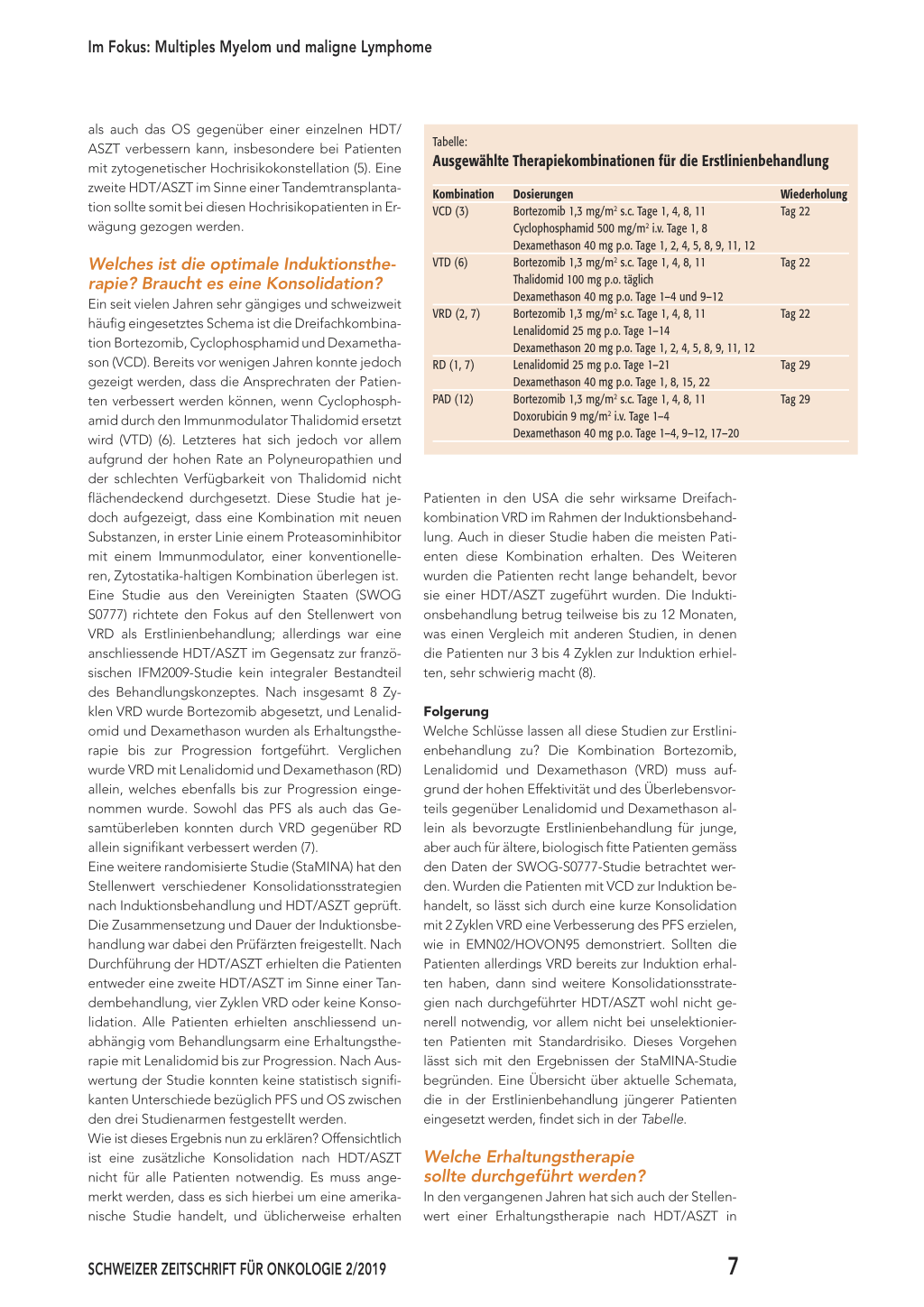
Prednison als Induktion erhalten haben, was sicherlich weniger effektiv ist als eine Dreifachkombination (1). Dieses Manko wurde in der französischen Studie IFM2009 behoben, da in dieser randomisierten Phase-III-Studie die Patienten eine Dreierkombination aus Bortezomib, Lenalidomid und Dexamethason (VRD) als Induktion und nach 3 Zyklen entweder eine Intensifikation mit HDT/ASZT, und dann 2 weitere Zyklen VRD, oder nur VRD für insgesamt 8 Zyklen erhielten. Alle Patienten wurden im Anschluss mit Lenalidomid als Erhaltungstherapie über ein Jahr behandelt. Die Behandlung mit Hochdosis-Chemotherapie und ASZT führte zu einem signifikant längeren progressionsfreien Überleben (PFS) im Vergleich zum konventionellen Behandlungsarm mit VRD allein (50 vs. 36 Monate; HR: 0,65; p < 0,001). Das Gesamtüberleben konnte jedoch nicht verlängert werden, und die Autoren folgern daraus, dass die Hochdosistherapie eventuell auch für eine spätere Therapielinie aufgehoben werden kann, um den Patienten ein besseres Langzeitüberleben zu ermöglichen (2). Erst kürzlich wurden die Daten der internationalen europäischen Studie EMN02/HOVON95 präsentiert. Dabei wurde der Stellenwert von einer oder zwei Hochdosistherapien mit ASZT nach Induktion mit Bortezomib, Cyclophosphamid und Dexamethason (VCD) gegenüber einer konventionell dosierten Zusatzbehandlung mit Bortezomid, Melphalan und Prednison (VMP) nach VCD geprüft. Zusätzlich prüfte die Studie auch die Effektivität einer kurzen Konsolidation mit 2 Zyklen VRD nach HDT/ASZT oder VMP. Die Behandlung mit HDT/ASZT sowie eine kurze Konsolidation mit VRD resultierten in einer Verbesserung des PFS gegenüber einer konventionellen Behandlung mit VCD, der VMP folgte (3, 4). In einer sehr aktuellen Analyse dieser Studie konnte gezeigt werden, dass eine Tandem-HDT/ASZT sowohl das PFS 6 SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 2/2019 Im Fokus: Multiples Myelom und maligne Lymphome als auch das OS gegenüber einer einzelnen HDT/ ASZT verbessern kann, insbesondere bei Patienten mit zytogenetischer Hochrisikokonstellation (5). Eine zweite HDT/ASZT im Sinne einer Tandemtransplantation sollte somit bei diesen Hochrisikopatienten in Erwägung gezogen werden. Welches ist die optimale Induktionstherapie? Braucht es eine Konsolidation? Ein seit vielen Jahren sehr gängiges und schweizweit häufig eingesetztes Schema ist die Dreifachkombination Bortezomib, Cyclophosphamid und Dexamethason (VCD). Bereits vor wenigen Jahren konnte jedoch gezeigt werden, dass die Ansprechraten der Patienten verbessert werden können, wenn Cyclophosphamid durch den Immunmodulator Thalidomid ersetzt wird (VTD) (6). Letzteres hat sich jedoch vor allem aufgrund der hohen Rate an Polyneuropathien und der schlechten Verfügbarkeit von Thalidomid nicht flächendeckend durchgesetzt. Diese Studie hat jedoch aufgezeigt, dass eine Kombination mit neuen Substanzen, in erster Linie einem Proteasominhibitor mit einem Immunmodulator, einer konventionelleren, Zytostatika-haltigen Kombination überlegen ist. Eine Studie aus den Vereinigten Staaten (SWOG S0777) richtete den Fokus auf den Stellenwert von VRD als Erstlinienbehandlung; allerdings war eine anschliessende HDT/ASZT im Gegensatz zur französischen IFM2009-Studie kein integraler Bestandteil des Behandlungskonzeptes. Nach insgesamt 8 Zyklen VRD wurde Bortezomib abgesetzt, und Lenalidomid und Dexamethason wurden als Erhaltungstherapie bis zur Progression fortgeführt. Verglichen wurde VRD mit Lenalidomid und Dexamethason (RD) allein, welches ebenfalls bis zur Progression eingenommen wurde. Sowohl das PFS als auch das Gesamtüberleben konnten durch VRD gegenüber RD allein signifikant verbessert werden (7). Eine weitere randomisierte Studie (StaMINA) hat den Stellenwert verschiedener Konsolidationsstrategien nach Induktionsbehandlung und HDT/ASZT geprüft. Die Zusammensetzung und Dauer der Induktionsbehandlung war dabei den Prüfärzten freigestellt. Nach Durchführung der HDT/ASZT erhielten die Patienten entweder eine zweite HDT/ASZT im Sinne einer Tandembehandlung, vier Zyklen VRD oder keine Konsolidation. Alle Patienten erhielten anschliessend unabhängig vom Behandlungsarm eine Erhaltungstherapie mit Lenalidomid bis zur Progression. Nach Auswertung der Studie konnten keine statistisch signifikanten Unterschiede bezüglich PFS und OS zwischen den drei Studienarmen festgestellt werden. Wie ist dieses Ergebnis nun zu erklären? Offensichtlich ist eine zusätzliche Konsolidation nach HDT/ASZT nicht für alle Patienten notwendig. Es muss angemerkt werden, dass es sich hierbei um eine amerikanische Studie handelt, und üblicherweise erhalten Tabelle: Ausgewählte Therapiekombinationen für die Erstlinienbehandlung Kombination VCD (3) VTD (6) VRD (2, 7) RD (1, 7) PAD (12) Dosierungen Bortezomib 1,3 mg/m2 s.c. Tage 1, 4, 8, 11 Cyclophosphamid 500 mg/m2 i.v. Tage 1, 8 Dexamethason 40 mg p.o. Tage 1, 2, 4, 5, 8, 9, 11, 12 Bortezomib 1,3 mg/m2 s.c. Tage 1, 4, 8, 11 Thalidomid 100 mg p.o. täglich Dexamethason 40 mg p.o. Tage 1–4 und 9–12 Bortezomib 1,3 mg/m2 s.c. Tage 1, 4, 8, 11 Lenalidomid 25 mg p.o. Tage 1–14 Dexamethason 20 mg p.o. Tage 1, 2, 4, 5, 8, 9, 11, 12 Lenalidomid 25 mg p.o. Tage 1–21 Dexamethason 40 mg p.o. Tage 1, 8, 15, 22 Bortezomib 1,3 mg/m2 s.c. Tage 1, 4, 8, 11 Doxorubicin 9 mg/m2 i.v. Tage 1–4 Dexamethason 40 mg p.o. Tage 1–4, 9–12, 17–20 Wiederholung Tag 22 Tag 22 Tag 22 Tag 29 Tag 29 Patienten in den USA die sehr wirksame Dreifachkombination VRD im Rahmen der Induktionsbehandlung. Auch in dieser Studie haben die meisten Patienten diese Kombination erhalten. Des Weiteren wurden die Patienten recht lange behandelt, bevor sie einer HDT/ASZT zugeführt wurden. Die Induktionsbehandlung betrug teilweise bis zu 12 Monaten, was einen Vergleich mit anderen Studien, in denen die Patienten nur 3 bis 4 Zyklen zur Induktion erhielten, sehr schwierig macht (8). Folgerung Welche Schlüsse lassen all diese Studien zur Erstlinienbehandlung zu? Die Kombination Bortezomib, Lenalidomid und Dexamethason (VRD) muss aufgrund der hohen Effektivität und des Überlebensvorteils gegenüber Lenalidomid und Dexamethason allein als bevorzugte Erstlinienbehandlung für junge, aber auch für ältere, biologisch fitte Patienten gemäss den Daten der SWOG-S0777-Studie betrachtet werden. Wurden die Patienten mit VCD zur Induktion behandelt, so lässt sich durch eine kurze Konsolidation mit 2 Zyklen VRD eine Verbesserung des PFS erzielen, wie in EMN02/HOVON95 demonstriert. Sollten die Patienten allerdings VRD bereits zur Induktion erhalten haben, dann sind weitere Konsolidationsstrategien nach durchgeführter HDT/ASZT wohl nicht generell notwendig, vor allem nicht bei unselektionierten Patienten mit Standardrisiko. Dieses Vorgehen lässt sich mit den Ergebnissen der StaMINA-Studie begründen. Eine Übersicht über aktuelle Schemata, die in der Erstlinienbehandlung jüngerer Patienten eingesetzt werden, findet sich in der Tabelle. Welche Erhaltungstherapie sollte durchgeführt werden? In den vergangenen Jahren hat sich auch der Stellenwert einer Erhaltungstherapie nach HDT/ASZT in SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 2/2019 7 Im Fokus: Multiples Myelom und maligne Lymphome mehreren Studien herauskristallisiert. Ursprünglich hatten drei randomisierte Studien Lenalidomid in diesem Setting geprüft. Die Therapiedauer ging entweder über 2 Jahre oder bis zur Progression der Erkrankung. In allen Studien konnte zwar eine deutliche Verbesserung des PFS als primärem Endpunkt aufgezeigt werden, aber nicht in allen auch eine Verbesserung des Gesamtüberlebens, da sie dafür nicht ausreichend viele Patienten eingeschlossen hatten. Die entsprechenden drei Studien (CALGB 100104, GIMEMA RV-MM-PI-209, IFM 2005-02) wurden nun in eine Metaanalyse integriert, die letztlich einen Überlebensvorteil nach längerem Follow-up nachweisen konnte. Bei Patienten mit erhöhter Laktatdehydrogenase, Niereninsuffizienz und Hochrisiko-Zytogenetik konnte der Überlebensvorteil hingegen nicht bestätigt werden, dies wohl zum Teil auch, weil nicht für alle Patienten ausreichende Daten aus allen drei Studien verfügbar waren (9). Mehr Klarheit in dieser Frage wurde durch die britische Myeloma-XI-Studie herbeigeführt. In dieser Studie wurden verschiedene Behandlungsansätze in der Erstlinientherapie geprüft. Eine wesentliche Fragestellung betraf auch die mögliche Effektivität einer Erhaltungstherapie mit Lenalidomid bis zur Progression gegenüber einer reinen Nachbeobachtung der Patienten. Im Rahmen dieser Studie konnte ein Überlebensvorteil durch Lenalidomid in allen Patientensubgruppen gezeigt werden, einschliesslich der Patienten mit HochrisikoZytogenetik (10). Wie lange therapien? Zur Frage der optimalen Dauer einer Erhaltungstherapie mit Lenalidomid sind mittlerweile ebenfalls nützliche Studiendaten verfügbar. In der deutschen Studie GMMG-MM5 haben Patienten Lenalidomid entweder über 2 Jahre oder nur bis zum Erreichen einer kompletten Remission erhalten. In der Studie hatten diejenigen Patienten ein längeres Gesamt- Merkpunkte I Eine Hochdosis-Chemotherapie mit anschliessender ASZT kann auch weiterhin als Standardtherapie für jüngere und «fitte» Patienten angesehen werden. I Die Kombination aus Bortezomib, Lenalidomid und Dexamethason (VRD) ist das bevorzugte Regime für die Erstlinienbehandlung sowohl jüngerer, transplantationsfähiger Patienten als auch älterer nicht transplantierbarer Patienten, die aber sonst körperlich «fit» sind. I VRD kann auch als kurze Konsolidation die Resultate verbessern, sofern die Patienten es nicht bereits im Rahmen der Induktionstherapie erhalten haben. I Eine Erhaltungstherapie mit Lenalidomid über einen Zeitraum von mindestens 2 Jahren nach HDT/ASZT kann generell empfohlen werden. Bortezomib oder Ixazomib sind mögliche Alternativen für Patienten, die Lenalidomid nicht vertragen oder die nicht darauf angesprochen haben. I Patienten mit Hochrisiko-Zytogenetik sollten für eine Tandemtransplantation in Erwägung gezogen werden. überleben, die die Therapie über die volle Dauer von 2 Jahren eingenommen hatten (11). Somit sollten gemäss derzeitiger Datenlage Patienten eine Lenalid- omid-Erhaltungstherapie zumindest über einen Zeit- raum von 2 Jahren durchführen. Die Frage, ob eine Behandlung darüber hinaus bis zur Progression noch wirksamer ist, wird in den kommenden Jahren durch die DETERMINATION-Studie endgültig geklärt wer- den. Im Gegensatz zu Lenalidomid sind für Proteasom- Inhibitoren weniger Studiendaten verfügbar. In der europäischen HOVON-65/GMMG-HD4-Studie ha- ben Patienten vor und nach HDT/ASZT Bortezomib erhalten, vorher als Induktion in Kombination mit Do- xorubicin und Dexamethason (PAD) und hinterher se- parat über 2 Jahre als Erhaltung. Im Vergleichsarm er- hielten die Patienten das klassische VAD (Vincristin, Doxorubicin, Dexamethason) als Induktion und die Erhaltungstherapie mit Thalidomid. Der Einsatz von Bortezomib hat in dieser Studie zu einer klaren Ver- besserung des Gesamtüberlebens geführt (12). Eine erst kürzlich publizierte internationale Phase-III- Studie (TOURMALINE-MM3) hat den Stellenwert von Ixazomib, einem Proteasominhibitor der zweiten Ge- neration, als Erhaltungstherapie über 2 Jahre ge- genüber Plazebo geprüft. Wesentliche Vorteile von Ixazomib sind die orale Verfügbarkeit und die nur einmal wöchentliche Einnahme. Die Studie konnte eine Verbesserung des PFS mit Ixazomib, primärer Endpunkt der Studie, zeigen. Ob eine Verbesserung des Gesamtüberlebens nach längerem Follow-up demonstriert werden kann, ist fraglich, da die hierfür notwendige Fallzahl eventuell zu klein ist (13). In beiden Studien haben auch Patienten mit Hochri- siko-Zytogenetik von dem Einsatz des Proteasom- Inhibitors als Erhaltungstherapie profitiert, sodass so- wohl Bortezomib als auch Ixazomib als Bestandteil einer Erhaltungstherapie in Betracht gezogen wer- den können, insbesondere für Patienten, die Lenalid- omid nicht vertragen oder die im Vorfeld nicht darauf angesprochen haben. I PD Dr. med. Panagiotis Samaras E-Mail: psamaras@onkozentrum.ch und Prof Dr. med. Christoph Renner E-Mail: Christoph.Renner@hirslanden.ch Onkozentrum Hirslanden Klinik Hirslanden 8032 Zürich Interessenkonflikte: keine. 8 SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 2/2019 Im Fokus: Multiples Myelom und maligne Lymphome Quellen: 1. Palumbo A, Cavallo F, Gay F, Di Raimondo F, Ben Yehuda D, Petrucci MT, et al.: Autologous transplantation and maintenance therapy in multiple myeloma. N Engl J Med. 2014; 371(10): 895–905. 2. Attal M, Lauwers-Cances V, Hulin C, Leleu X, Caillot D, Escoffre M, et al.: Lenalidomide, bortezomib, and dexamethasone with transplantation for myeloma. N Engl J Med. 2017; 376(14): 1311–1320. 3. Cavo M, Beksac M, Dimopoulos M, Pantani L, Gay F, Hájek R, et al.: Intensification therapy with bortezomib-melphalan-pPrednisone versus autologous stem cell transplantation for newly diagnosed multiple myeloma: An intergroup, multicenter, phase III study of the European Myeloma Network (EMN02/HO95 MM Trial). Blood. 128(22): 673. 4. Sonneveld P, Beksac M, van der Holt B, Dimopoulos MA, Carella AM, Ludwig H, et al.: Consolidation followed by maintenance therapy versus maintenance alone in newly diagnosed, transplant eligible patients with multiple myeloma (MM): A Randomized Phase 3 Study of the European Myeloma Network (EMN02/HO95 MM Trial). Blood. 128(22): 242. 5. Cavo M, Gay F, Patriarca F, Zamagni E, Montefusco V, Dozza L, et al.: Double autologous stem cell transplantation significantly prolongs progression-free survival and overall survival in comparison with single autotransplantation in newly diagnosed multiple myeloma: an analysis of phase 3 EMN02/H095 study. ASH 2017. Abstract 401. 6. Moreau P, Hulin C, Macro M, Caillot D, Chaleteix C, Roussel M, et al.: VTD is superior to VCD prior to intensive therapy in multiple myeloma: results of the prospective IFM2013-04 trial. Blood. 2016; 127(21): 2569-2574. 7. Durie BGM, Hoering A, Abidi MH, Rajkumar SV, Epstein J, Kahanic SP, et al.: Bortezomib with lenalidomide and dexamethasone versus lenalidomide and dexamethasone alone in patients with newly diagnosed myeloma without intent for immediate autologous stem-cell transplant (SWOG S0777): a randomised, open-label, phase 3 trial. Lancet. 2017; 389(10068): 519–527. 8. Stadtmauer EA, Pasquini MC, Blackwell B, Knust K, Bashey A, Devine SM, et al.: Comparison of autologous hematopoietic cell transplant (autoHCT), bortezomib, lenalidomide (len) and dexamethasone (RVD) consolidation with len maintenance (ACM), tandem autohct with len Maintenance (TAM) and autohct with len maintenance (AM) for up-front treatment of patients with multiple myeloma (MM): primary results from the randomized phase III trial of the Blood and Marrow Transplant Clinical Trials Network (BMT CTN 0702 – StaMINA Trial). Blood. 2016; 128 (LBA-1). 9. McCarthy PL, Holstein SA, Petrucci MT, Richardson PG, Hulin C, Tosi P, et al.: Lenalidomide Maintenance After Autologous Stem-Cell Transplantation in Newly Diagnosed Multiple Myeloma: A Meta-Analysis. J Clin Oncol 2017; 35(29): 3279– 3289. 10. Jackson G, Davies FE, Pawlyn C, Cairns D, Striha A, Collett C, et al.: Lenalidomide maintenance versus observation for patients with newly diagnosed multiple myeloma (Myeloma XI): a multicentre, open-label, randomised, phase 3 trial. Lancet Oncol 2019; 20: 57–73. 11. Goldschmidt H, Mai EK, Dürig J, Scheid C, Weisel KC, Kunz C, et al.: ResponseAdapted Lenalidomide Maintenance in Newly Diagnosed, Transplant-Eligible Multiple Myeloma: Results from the Multicenter Phase III GMMG-MM5 Trial. ASH 2017. Abstract 400. 12. Goldschmidt H, Lokhorst HM, Mai EK, van der Holt B, Blau IW, Zweegman S, et al.: Bortezomib before and after high-dose therapy in myeloma: long-term results from the phase III HOVON-65/GMMG-HD4 trial. Leukemia. 2018; 32(2): 383–390. 13. Dimopoulos M, Gay F, Schjesvold FH, Beksac M, Hajek R, Weisel K, et al.: Maintenance Therapy with the Oral Proteasome Inhibitor (PI) Ixazomib Significantly Prolongs Progression-Free Survival (PFS) Following Autologous Stem Cell Transplantation (ASCT) in Patients with Newly Diagnosed Multiple Myeloma (NDMM): Phase 3 Tourmaline-MM3 Trial. ASH 2018. Abstract 301. SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 2/2019 9