Transkript
Im Fokus: Prostatakarzinom und Nierenzellkarzinom
Die Systemtherapie des fortgeschrittenen Prostatakarzinoms
Aktuelle onkologische Optionen
Die Systembehandlung des fortgeschrittenen Prostatakarzinoms beinhaltet in erster Linie hormonelle Therapien und supportive Massnahmen. In späteren Therapielinien kommen Zytostatika, dann zielgerichtete sowie immunologische Ansätze mit unterschiedlichen Wirkansätzen dazu. In den letzten Jahren erfolgten wichtige Therapiestudien; neue Behandlungsmöglichkeiten zeichnen sich ab.
RUDOLF MORANT
Rudolf Morant
14
Hormontherapien
Die Grundsätze der Hormontherapie beim fortgeschrittenen Prostatakarzinom sind in den letzten Jahren unverändert geblieben. Prostatakarzinomzellen sind zumindest anfänglich für ihr Überleben auf eine kontinuierliche Testosteronwirkung über die nukleären Androgenrezeptoren angewiesen. Eine Unterbrechung dieser Stimulation, sei es durch chemische oder chirurgische Kastration oder durch Hemmung der Androgenrezeptoren, kann somit bei den meisten Prostatakarzinomzellen eine Apoptose auslösen. Dies zeigt sich klinisch durch fallende PSA-Werte, schwindende tumorbedingte Schmerzen, einen besseren Allgemeinzustand und messbare Verkleinerungen von Tumormanifestationen. Bei fortgeschrittenen Prostatakarzinomen tritt jedoch – meist im Mittel zwischen 12 und 18 Monaten – eine Resistenz gegen eine Testosteronablation auf. Die hormonelle Ablation erfolgt meistens durch LHRH-Agonisten wie Goserelin, Leuprolid oder Buserelin, deren Wirkung gleichwertig, aber nicht besser oder nebenwirkungsärmer ist als eine Orchiektomie. Die verschiedenen Formulierungen besitzen unterschiedliche Wirkungsdauer und Galenik, zeigen aber bezüglich Wirksamkeit keine eindeutigen Unterschiede. Nach Orchiektomie ist ein zusätzlicher Einsatz von LHRH-Agonisten nicht indiziert. Um einen initialen Anstieg von Testosteron und damit einhergehende klinische Symptomverschlechterung («flare-up») zu vermeiden, wird anfänglich eine
Kombination mit einem Androgenrezeptorhemmer verabreicht. LHRH-Antagonisten wie Degarelix (Firmagon®) wirken – im Gegensatz zu den oben aufgeführten LHRHAgonisten – direkt über eine Hemmung der Hypophysenaktivität und senken den Testosteronspiegel entsprechend schnell innert weniger Tage. Sie können somit zu einer schnelleren und, wie es scheint, teilweise besseren PSA-Kontrolle führen als LHRHAgonisten (1).
Spezielle Strategien und Begleitmassnahmen Da viele Patienten mit behandeltem Prostatakrebs heute länger als vor Jahrzehnten leben, werden die mittel- bis langfristigen Nebenwirkungen einer Androgenentzugstherapie bedeutsamer. Zunehmend rücken sie ins Bewusstsein der behandelnden Ärzte: Neben dem Verlust von Libido und Potenz, dem Auftreten von störenden Hitzewallungen, Schwitzen und psychischen Veränderungen gehören verschiedene Stoffwechselveränderungen wie Gewichtszunahme bei gleichzeitigem Verlust von Knochen- und Muskelmasse, verschlechterten Werten von Serumlipiden und Blutzucker (2) und erhöhter kardialer Morbidität zu diesen Begleiterscheinungen. Diese Veränderungen ähneln denen des metabolischen Syndroms. Entsprechende Kontrollen, Therapien und Beratungen, zu denen die Einnahme von Kalzium, die Ernährungsberatung und körperliche Bewegung gehören, ergänzen die Hormontherapien. Eine intermittierende Hormontherapie ist zwar noch
SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 4/2010
Im Fokus: Prostatakarzinom und Nierenzellkarzinom
keine allgemein anerkannte Strategie, diese kann jedoch einen Teil der Nebenwirkungen durch die Therapiepausen erträglicher machen und möglicherweise zudem die Zeit bis zum Auftreten einer Resistenz auf den Androgenentzug verlängern (3). In mehreren Studien konnte bis jetzt keine signifikante Verschlechterung des Überlebens gegenüber einer kontinuierlichen Ablation gezeigt werden (4). Auch wenn unter der Therapie das Tumorzellwachstum grösstenteils weiterhin testosteronabhängig bleibt, reagieren die Karzinomzellen bereits sensibler auf sehr niedrige Hormonspiegel, was fortgesetzte hormonelle Massnahmen sinnvoll macht. Die molekularbiologischen Ursachen der verstärkten Empfindlichkeit auf Androgene können unterschiedlich sein, hierzu gehören: Amplifikation des Gens für den Androgenrezeptor, dessen Überexpression oder gar Mutation oder auch die Expression des antiapoptotischen Bcl-2-Gens (u.a.), welche sich nicht gegenseitig ausschliessen müssen. Die Möglichkeiten einer Mehrlinienhormontherapie führten auch zur Änderung der klinischen Bezeichnungen. Bei einem Wiederansteigen des PSA unter Testosteronentzug wurde das Prostatakarzinom früher als «hormonrefraktär» bezeichnet, was jedoch wegen der möglichen Zweit- und Drittlinientherapien nicht mehr adäquat ist und deshalb als «kastrationsrefraktäres Prostatakarzinom» (CRPC) bezeichnet wird. Die generelle klinische Empfehlung nach Auftreten eines kastrationsrefraktären Zustands ist deshalb, auch nach Auftreten einer Androgenresistenz die früher durchgeführte Androgenablation auf unbeschränkte Zeit fortzusetzen. In einer randomisierten Studie bei Patienten mit CRPC waren die klinischen Unterschiede zwischen Fortführen versus Absetzen der Hormontherapie jedoch eher gering und statistisch nicht signifikant.
Sekundäre hormonelle Massnahmen Hormonelle Zweitlinientherapien beim CRPC versuchen die Bildung von Testosteron in der Nebenniere zu hemmen oder die Rezeptoraktivität im Tumor direkt zu blockieren. Neben den seit Längerem bekannten Antiandrogenen wie Bicalut-
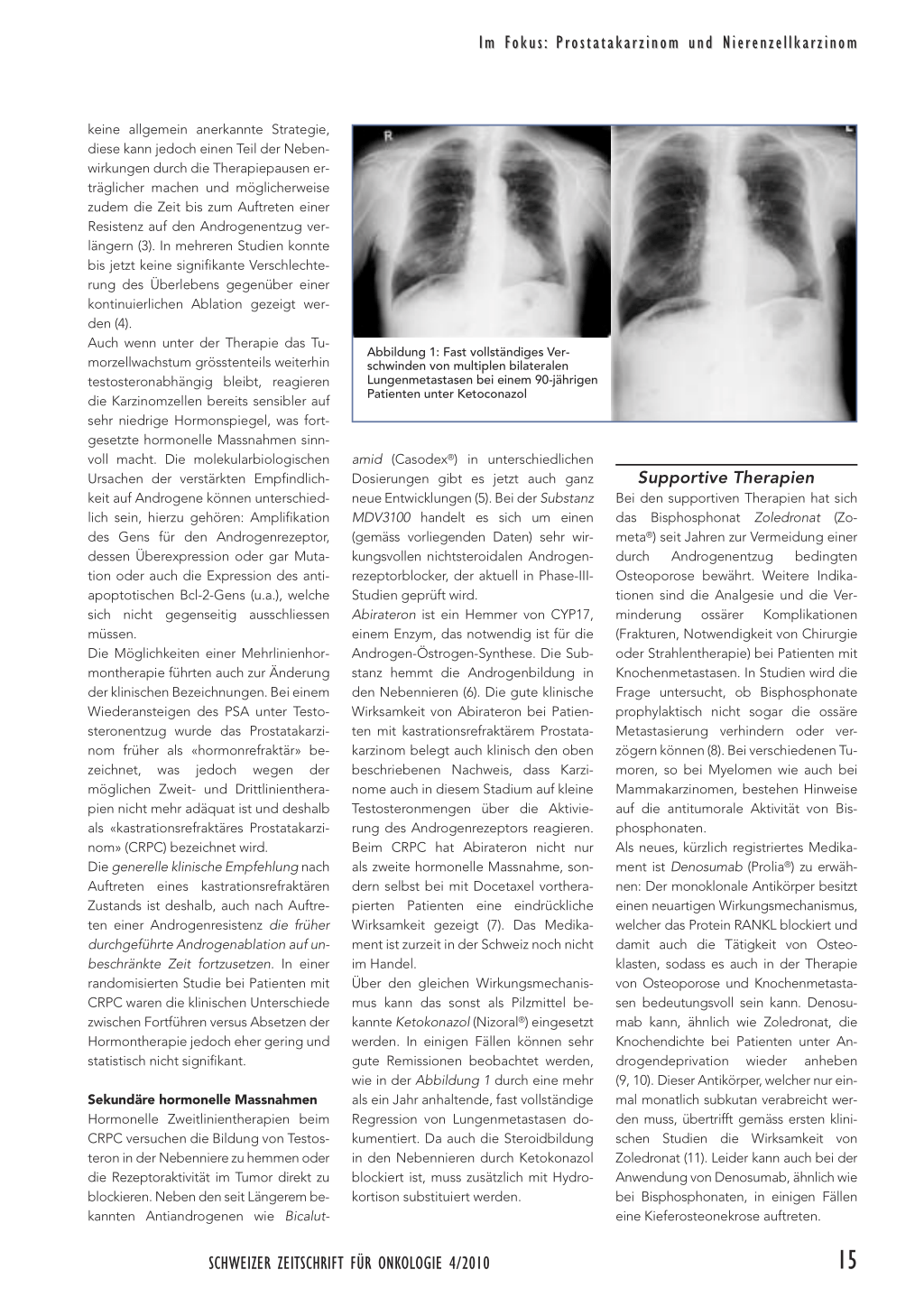
Abbildung 1: Fast vollständiges Verschwinden von multiplen bilateralen Lungenmetastasen bei einem 90-jährigen Patienten unter Ketoconazol
amid (Casodex®) in unterschiedlichen Dosierungen gibt es jetzt auch ganz neue Entwicklungen (5). Bei der Substanz MDV3100 handelt es sich um einen (gemäss vorliegenden Daten) sehr wirkungsvollen nichtsteroidalen Androgenrezeptorblocker, der aktuell in Phase-IIIStudien geprüft wird. Abirateron ist ein Hemmer von CYP17, einem Enzym, das notwendig ist für die Androgen-Östrogen-Synthese. Die Substanz hemmt die Androgenbildung in den Nebennieren (6). Die gute klinische Wirksamkeit von Abirateron bei Patienten mit kastrationsrefraktärem Prostatakarzinom belegt auch klinisch den oben beschriebenen Nachweis, dass Karzinome auch in diesem Stadium auf kleine Testosteronmengen über die Aktivierung des Androgenrezeptors reagieren. Beim CRPC hat Abirateron nicht nur als zweite hormonelle Massnahme, sondern selbst bei mit Docetaxel vortherapierten Patienten eine eindrückliche Wirksamkeit gezeigt (7). Das Medikament ist zurzeit in der Schweiz noch nicht im Handel. Über den gleichen Wirkungsmechanismus kann das sonst als Pilzmittel bekannte Ketokonazol (Nizoral®) eingesetzt werden. In einigen Fällen können sehr gute Remissionen beobachtet werden, wie in der Abbildung 1 durch eine mehr als ein Jahr anhaltende, fast vollständige Regression von Lungenmetastasen dokumentiert. Da auch die Steroidbildung in den Nebennieren durch Ketokonazol blockiert ist, muss zusätzlich mit Hydrokortison substituiert werden.
Supportive Therapien
Bei den supportiven Therapien hat sich das Bisphosphonat Zoledronat (Zometa®) seit Jahren zur Vermeidung einer durch Androgenentzug bedingten Osteoporose bewährt. Weitere Indikationen sind die Analgesie und die Verminderung ossärer Komplikationen (Frakturen, Notwendigkeit von Chirurgie oder Strahlentherapie) bei Patienten mit Knochenmetastasen. In Studien wird die Frage untersucht, ob Bisphosphonate prophylaktisch nicht sogar die ossäre Metastasierung verhindern oder verzögern können (8). Bei verschiedenen Tumoren, so bei Myelomen wie auch bei Mammakarzinomen, bestehen Hinweise auf die antitumorale Aktivität von Bisphosphonaten. Als neues, kürzlich registriertes Medikament ist Denosumab (Prolia®) zu erwähnen: Der monoklonale Antikörper besitzt einen neuartigen Wirkungsmechanismus, welcher das Protein RANKL blockiert und damit auch die Tätigkeit von Osteoklasten, sodass es auch in der Therapie von Osteoporose und Knochenmetastasen bedeutungsvoll sein kann. Denosumab kann, ähnlich wie Zoledronat, die Knochendichte bei Patienten unter Androgendeprivation wieder anheben (9, 10). Dieser Antikörper, welcher nur einmal monatlich subkutan verabreicht werden muss, übertrifft gemäss ersten klinischen Studien die Wirksamkeit von Zoledronat (11). Leider kann auch bei der Anwendung von Denosumab, ähnlich wie bei Bisphosphonaten, in einigen Fällen eine Kieferosteonekrose auftreten.
SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 4/2010
15
Im Fokus: Prostatakarzinom und Nierenzellkarzinom
Zur supportiven Therapie von schmerzhaften Knochenmetastasen zählen – neben medikamentöser Schmerztherapie, chirurgischen Interventionen und perkutaner Strahlentherapie – besonders in fortgeschrittenen Fällen mit ausgedehnter ossärer Metastasierung auch eine nuklearmedizinische Behandlung mit den Betastrahlern Strontium-89, Samarium153 oder weiteren Isotopen. Die Dauer der analgetischen Wirkung dieser nuklearmedizinischen Massnahme ist allerdings sehr unterschiedlich.
Zytostatische Therapien
Im Vergleich zur bisher üblichen Chemotherapie mit Mitoxantron konnte im Jahr 2004 unter randomisierten Studienbedingungen erstmals ein Überlebensvorteil von 2,4 Monaten durch die Chemotherapie mit Docetaxel (Taxotere®) in metastasierten Stadien gezeigt werden. Docetaxel, alle drei Wochen verabreicht, zeigte ein besseres Ansprechen (48 vs. 35% PSA-Ansprechen) sowie eine bessere Schmerzkontrolle und führte sogar zu einem längeren Überleben (18,9 vs. 16,5 Monate). Seither hat sich der früher nur sporadisch und oft auch umstrittene Einsatz von Zytostatika bei CRPC breit durchgesetzt. Docetaxel in Kombination mit Prednison bleibt bis heute die erste und meisteingesetzte zytostatische Therapie bei Patienten mit fortgeschrittenem CRPC. Ausserdem konnte gezeigt werden, dass ein fallendes PSA um mehr als 30% ein verlängertes Überleben voraussagt.
Die Behandlung mit Docetaxel Eine wichtige, nur teilweise beantwortete Frage ist, zu welchem Zeitpunkt der Erkrankung mit dem Einsatz von Docetaxel begonnen werden sollte. Empfehlenswert ist hier folgendes Vorgehen: Bei langsam steigendem PSA-Wert eines asymptomatischen Patienten kann es durchaus sinnvoll sein, mit der Chemotherapie noch zuzuwarten und so dem Patienten die Nebenwirkungen einer solchen Behandlung zu ersparen. Bei Auftreten von Symptomen, die durch Chemotherapie vermindert werden, ist deren Einsatz meist gut zu vertreten; er wird auch meistens von den Patienten akzeptiert. Jedoch sollte nicht so lange mit dieser Therapie gewartet werden bis die Pa-
Punkte Alter KPS Hämoglobin PSA LDH ALK Albumin Gesamtpunkte Ein-Jahres-Überlebenswahrscheinlichkeit Zwei-Jahres-Überlebenswahrscheinlichkeit durchschnittliche Überlebensdauer
Abbildung 2: Nomogramm zur Abschätzung des Überlebens von Patienten mit progredientem kastrationsrefraktärem Prostatakarzinom (CRPC) (adaptiert nach 20)
tienten stark symptomatisch sind oder gar schwere Komplikationen wie Frakturen oder Lähmungen aufgetreten sind. In zu fortgeschrittenen Situationen kann eine klinische Besserung allerdings nur langsam oder auch kaum mehr möglich sein. Ein langsam steigender PSA-Wert bei asymptomatischen Patienten mit CRPC kann dagegen ein guter Zeitpunkt für Studien mit neuen Medikamenten sein. Hinweise auf die Aktivität des Tumors und damit die Prognose können neben dem Wissen um die bisherige Entwicklung und den aktuellen Ausbreitungsgrad des Tumors der Gleason Score und die PSA-Verdoppelungszeit geben. Auch ein prognostischer Index für Patienten mit CRPC in Form eines Nomogramms kann nützlich sein (vgl. Abbildung 2). Bezüglich des eingesetzten Regimes ist gemäss den vorliegenden Studienresultaten von 2004 ein dreiwöchentliches Regime in Kombination mit 10 mg Prednison täglich einer wöchentlichen Gabe von Docetaxel vorzuziehen. Die optimale Dauer einer wirksamen Chemotherapie ist weiterhin unklar. Oft werden 6 bis 10 Zyklen verabreicht. Wichtig ist, bei fehlendem Abfallen des PSA-Spiegels nach dem ersten Zyklus noch nicht gleich die Behandlung abzubrechen, denn der PSA-Abfall kann verzögert auftreten. Die Toxizität einer Therapie mit Docetaxel kann beträchtlich, auch kumulativ sein und Dosismodifikationen zur Folge haben, gelegentlich sogar den Therapieabbruch erzwingen. Kli-
nisch störend sind oft Probleme mit Hauttoxizität und Finger- respektive Zehennägelstörungen. Der prophylaktische Einsatz von kühlenden Handschuhen während der Chemotherapie kann hier vorbeugend wirken.
Weitere und neueste Chemotherapeutika Neben Docetaxel gibt es eine Vielzahl anderer Medikamente, die eine gewisse Wirksamkeit beim Prostatakarzinom zeigen, so Vinorelbine, Gemcitabine, Capecitabine, Carboplatin und andere, wie unter anderen in sequenziellen Phase-IIStudien der SAKK gezeigt worden ist. Auch Mitoxantron wird weiter eingesetzt, bei dem als erstem Medikament randomisiert ein positiver Einfluss auf die Lebensqualität gezeigt wurde (12). Die Therapie mit Docetaxel wird oft nach einer festgelegten Anzahl von Zyklen oder wegen zu hoher Toxizität sistiert, nicht wegen aufgetretener Tumorresistenz. Klinisch hat sich gezeigt, dass – nach anfänglichem Ansprechen auf Docetaxel – bei erneuter Tumorprogression eine Wiederaufnahme der gleichen Therapie wiederum zu einem Ansprechen führen kann. Verschiedene Medikamente können auf der Grundlage von Phase-II-Studien in der Zweitlinientherapie wirksam sein, so die Kombination von Carboplatin mit Paclitaxel (13). Auch andere Kombinationen wie Oxaliplatin und Capecitabine zeigten ein gutes Ansprechen in einer Zweitlinienindikation nach Docetaxel (14).
16 SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 4/2010
Im Fokus: Prostatakarzinom und Nierenzellkarzinom
Bis vor Kurzem gab es jedoch keine wirksame Zweitlinientherapie nach Docetaxelgabe, die das Überleben nachweislich verlängert. An der ASCO-Jahrestagung 2010 konnte hierzu erstmals eine randomisierte Studie einen Fortschritt zeigen: Das Medikament Cabazitaxel (Jevtana®) konnte im Vergleich zu Mitoxantron bei Patienten, die auf Docetaxel nicht mehr angesprochen hatten, das Überleben von 12,7 auf 15,1 Monate verlängern (15). Dieses neue Taxan wurde von der FDA im Juni 2010 registriert, und andere Länder erwarten in Kürze die Zulassung.
Neue Ansätze in der Diskussion
Manche in Phase-II-Studien vielversprechenden Resultate und Therapieansätze zeigten im weiteren Verlauf der klinischen Prüfungen ernüchternde Resultate. Hierzu gehören: Vitamin D respektive dessen Mangel scheinen auf der Grundlage epidemiologischer Daten eine wichtige Rolle bei der Entstehung von Prostatakrebs zu haben. In-vitro- wie auch erste klinische Daten legten eine Wirksamkeit auch in der Therapie von Prostatakarzinom nahe. Eine grosse Phase-III-Studie, die Calcitriol zusammen mit Docetaxel prüfte, musste allerdings wegen Nichterreichen des Studienziels frühzeitig geschlossen werden, nachdem im Studienarm sogar mehr Todesfälle als in der Kontrollgruppe beobachtet worden waren (16). Rezeptoren für den Epidermis Growth Factor (EGFR) sind in einem Teil der Prostatakarzinome überexprimiert. Der Einsatz des monoklonalen Anti-EGFRAntikörpers Cetuximab (Erbitux®) wurde in einer SAKK-Studie in Kombination mit Docetaxel für die Zweitlinientherapie eingesetzt (17). Ein Ansprechen wurde in 31% bei 38 Patienten gesehen, und es wurden auch länger dauernde Stabilisierungen beobachtet. Weitergehende Folgerungen könnten allerdings nur in randomisierten Studien erhoben werden. HER-2 ist hingegen nur selten überexprimiert, sodass der Einsatz von Trastuzumab (Herceptin®) schon aus präklinischer Sicht nicht sinnvoll ist, was inzwischen auch klinisch gezeigt worden ist. Die Hemmung der Neoangiogenese mit verschiedenen Tyrosinkinasehemmern
wie auch mit dem monoklonalen Anti-
körper Bevacizumab (Avastin®) hat sich
bei verschiedenen Tumoren in der Klinik
bewährt, darunter beim metastasierten
Kolonkarzinom und Nierenkarzinom.
Studien beim Prostatakarzinom zeigten
eine Verlängerung des progressions-
freien Überlebens von 7,5 auf 9,9 Mo-
nate, allerdings keinen signifikanten
Überlebensvorteil, sodass der Einsatz
von Bevacizumab zurzeit nicht reif für die
Klinik ist (18).
Ganz neue Ansatzpunkte sind Thera-
pien, die über das Immunsystem wirken.
So wurde im April 2010 Supuleucel-T
(Provenge®) in den USA registriert; es
handelt sich um eine aufwendige im-
muntherapeutische Methode auf der Ba-
sis von patienteneigenen mononu-
kleären Zellen. Bei asymptomatischen
Patienten mit CRPC konnte randomisiert
eine Überlebensverlängerung gezeigt
werden (19).
In der Systemtherapie des fortgeschritte-
nen Prostatakarzinoms sind in den letz-
ten Jahren mehrere bedeutsame Fort-
schritte gemacht worden; die
gegenwärtig laufenden Studien sowie
neue Medikamente in der Entwicklung
lassen auf weitere klinisch relevante Sub-
stanzen in der Zukunft hoffen.
▲
Dr. med. Rudolf Morant Brust- und Tumorzentrum ZeTuP St. Gallen, Chur und Rapperswil Alte Jonastrasse 24 8640 Rapperswil E-Mail: rudolf.morant@zetup.ch
Interessenkonflikte: keine deklariert
Quellen:
1. Shore ND, Crawford E, Olesen T, Persson B: Long-term prostate-specific antigen (PSA) control in prostate cancer (PCa) patients switched from leuprolide to degarelix or receiving continuous degarelix treatment. J Clin Oncol 2010; 28: Abstract 4673.
2. Saylor PJ, Smith MR: Metabolic complications of androgen deprivation therapy for prostate cancer. J Urol 2009; 181: 1998–2006.
3. Gleave M, Klotz L, Taneja SS: The continued debate: intermittent vs. continuous hormonal ablation for metastatic prostate cancer. Urol Oncol 2009; 27: 81–6.
4. Calais da Silva FE, Bono AV, et al.: Intermittent androgen deprivation for locally advanced and metastatic prostate cancer: results from a randomised phase 3 study of the South European Uroncological Group. Eur Urol 2009; 55: 1269–77.
Merkpunkte
▲ Eine Hormontherapie ist die erste Sys-
temtherapie beim fortgeschrittenen Prostatakarzinom.
▲ Beim kastrationsrefraktären Prostata-
karzinom (CRPC) gibt es zunehmend Möglichkeiten endokriner Zweitlinientherapien (z.B. mit Abirateron).
▲ Die Indikation zu einer Chemotherapie
mit Docetaxel ist beim fortgeschrittenen symptomatischen CRPC gegeben.
▲ Cabazitaxel ist eine Zweitlinienchemo-
therapie mit nachgewiesener Verlängerung des Überlebens.
▲ Supportive Therapien mit Zoledronat
(bzw. in Kürze auch mit Denosumab) sind ein wichtiger Pfeiler der Systemtherapie beim ossär metastasierten Prostatakarzinom.
5. Sharifi N: New agents and strategies for the hormonal treatment of castration-resistant prostate cancer. Expert Opin Investig Drugs 2010; 19: 837–46.
6. Attard G, Reid AH, A’Hern R, et al.: Selective inhibition of CYP17 with abiraterone acetate is highly active in the treatment of castration-resistant prostate cancer. J Clin Oncol 2009; 27: 3742–8.
7. Vogiatzi P, Claudio PP: Efficacy of abiraterone acetate in post-docetaxel castration-resistant prostate cancer. Expert Rev Anticancer Ther 2010; 10: 1027–30.
8. Neville-Webbe HL, Coleman RE: Bisphosphonates and RANK ligand inhibitors for the treatment and prevention of metastatic bone disease. Eur J Cancer 2010; 46: 1211–22.
9. Smith MR, Saad F, et al.: Effects of denosumab on bone mineral density in men receiving androgen deprivation therapy for prostate cancer. J Urol 2009; 182: 2670–5.
10. Neville-Webbe HL, Gnant M, Coleman RE: Potential anticancer properties of bisphosphonates. Semin Oncol 2010; 37 Suppl 1: S53–65.
11. Fizazi K: A randomized phase III trial of denosumab versus zoledronic acid in patients with bone metastases from castration-resistant prostate cancer. J Clin Oncol 2010; 28: LBA 4507.
12. Tannock IF, Osoba D, et al.: Chemotherapy with mitoxantrone plus prednisone or prednisone alone for symptomatic hormone-resistant prostate cancer: a Canadian randomized trial with palliative end points. J Clin Oncol 1996; 14: 1756–64.
13. Jeske S, Tagawa ST, et al.: Carboplatin plus paclitaxel therapy after docetaxel in men with metastatic castrate resistant prostate cancer. Urol Oncol 2010 (in press). doi:10.1016/j.urolonc. 2009.12.023
14. Blesa JM, Marco VG, et al.: Phase II Trial of Oxaliplatin and Capecitabine After Progression to First-Line Chemotherapy in Androgen-Indepen-
SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 4/2010
17
Im Fokus: Prostatakarzinom und Nierenzellkarzinom
dent Prostate Cancer Patients. Am J Clin Oncol 2010 (in press).
15. De Bono JS, Oudard S, Ozguroglu M et al.: for the TROPIC Investigators: Cabazitaxel or mitoxantrone with prednisone in patients with metastatic castration-resistant prostate cancer (mCRPC) previously treated with docetaxel: Final results of a multinational phase III trial (TROPIC). J Clin Oncol 2010; 28: 15s; 28: 15s: abstr 4508.
16. Scher HI, Chi KN, De Wit R, et al.: Docetaxel (D) plus high-dose calcitriol versus D plus prednisone (P) for patients (Pts) with progressive castrationresistant prostate cancer (CRPC): Results from the phase III ASCENT2 trial. J Clin Oncol 2010; 28: 15s: suppl. abstr 4509.
17. Cathomas R, Rothermundt C, von Moos R, Betticher DC, Winterhalder RC, Droege C et al.: Cetuximab in combination with docetaxel in patients (pts) with metastatic castration resistant (mCRPC) and docetaxel-refractory prostate cancer: A multicenter phase II trial (SAKK 08/07). J Clin Oncol 2010; 28: 15s:abstr 4666.
18. Kelly WK, Halabi S, Carducci MA, et al.: A randomized, double-blind, placebo-controlled phase III trial comparing docetaxel, prednisone, and placebo with docetaxel, prednisone, and bevacizumab in men with metastatic castration-resistant prostate cancer (mCRPC): Survival results of CALGB 90401. J Clin Oncol 2010; 28: 18s:suppl; abstr LBA4511.
19. Higano CS, Schellhammer PS, et al.: Integrated data from 2 randomized, double-blind, placebo-controlled, phase 3 trials of active cellular immunotherapy with sipuleucel-T in advanced prostate cancer. Cancer 2009; 115: 3670–9.
20. Smaletz O SH, Small EJ, et al.: Nomogram for overall survival of patients with progressive metastatic prostate cancer after castration. J Clin Oncol 2002; 20: 3972–82.
18 SCHWEIZER ZEITSCHRIFT FÜR ONKOLOGIE 4/2010