Transkript
25. SCHWEIZERISCHE TAGUNG FÜR PHYTOTHERAPIE, BADEN, 25. NOVEMBER 2010
Pflanzliche Vielstoffgemische – eine rationale Option zur Bekämpfung lästiger Viren?
Jürgen Reichling
Einleitung
Viren sind infektiöse Partikel, die keine Zellstruktur und keinen eigenen Stoffwechsel besitzen. Als Nukleinsäure (Genom) enthalten sie entweder DNA oder RNA, die von einer Proteinkapsel, dem Kapsid, umgeben sind. Einige Viren verfügen noch über eine Lipidhülle, in der viruseigene Proteine lokalisiert sind. Anders als Bakterien, die frei lebende Mikroorganismen darstellen, ist das Virus ein Zellparasit, der die Wirtszelle zur Vermehrung benötigt. Viren haben verschiedene Strategien entwickelt, um eine Wirtszelle zu infizieren. Jedes Virus besitzt spezifische Oberflächenproteine, mit deren Hilfe es sich an Rezeptoren der Zelloberfläche anheften und so in die Wirtszelle eindringen kann. In der Wirtszelle nutzen Viren die zelleigene Energie- und Enzymausstattung, um sich zu vermehren. Der Erfolg der Viren stützt sich auf verschiedene Eigenschaften: ◆ hohe genetische Variabilität ◆ Unterschiede hinsichtlich ihrer Übertra-
gungswege ◆ effiziente Replikation in der Wirtszelle ◆ Täuschung beziehungsweise Überwin-
dung der wirtszelleigenen Abwehr ◆ Fähigkeit, in der Wirtszelle zu überleben
beziehungsweise zu persistieren. Die Konsequenz davon ist, dass sich Viren in vielen Zellen vermehren und ganz unterschiedliche Organismen befallen können. Da die Vermehrung der Viren eng mit dem zellulären Metabolismus verbunden ist, besteht die Schwierigkeit, dass man die intrazelluläre Replikation der Viren meist nicht ohne schwerwiegende Nebenwirkungen für den Gesamtorganismus bekämpfen kann.
Neben der Impfung, wo immer möglich, stellen synthetische antivirale Substanzen (Chemotherapeutika) das Rückgrat einer effizienten antiviralen Bekämpfung dar. Um aufkommende Resistenzen zu überwinden, wird weltweit nach antiviralen Substanzen mit möglichst neuen Wirkmechanismen gesucht. Vor diesem Hintergrund sind auch phyto-antivirale Substanzen in den Mittelpunkt der Forschung geraten. In der Vergangenheit wurden viele Hundert Arzneipflanzen und pflanzliche Drogen schon auf ihre potenziellen antiviralen Eigenschaften untersucht. Dabei wurde eine grosse Vielfalt unterschiedlicher phyto-antiviraler Substanzen entdeckt, wie zum Beispiel Alkaloide, Katechine, Cumarine, Lignane, Flavonoide, Saponine, Terpene. Im Folgenden möchte ich auf zwei prominente virale Infektionskrankheiten eingehen, nämlich Lippenherpes (verursacht durch Herpes-simplex-Viren) und Echte Grippe (verursacht durch Influenzaviren), und die Möglichkeit erörtern, inwieweit pflanzliche Vielstoffgemische in diesen Fällen bei der Bekämpfung der viralen Infektion beziehungsweise bei der Linderung der mit der Infektion verbundenen Symptome hilfreich sein können.
Ätherische Öle mit Anti-Herpes-Wirkung in In-vitro-Studien
Ätherische Öle sind komplexe, aromatisch duftende Gemische aus verschiedenen Komponenten mit niedrigem Molekulargewicht und unterschiedlichster chemischer Struktur. Überwiegend handelt es sich bei den Einzelsubstanzen um Monoterpene, Sesquiterpene und Phenylpropanderivate. Durch Wasserdampfdestillation können ätherische Öle aus verschiedenen Pflanzenteilen gewonnen werden. Neben antimikrobiellen Eigenschaften zeichnen
sich diese Öle auch durch entzündungshemmende, antirheumatische, immunmodulatorische und sedative Effekte aus. Herpes-simplex-Viren (HSV) sind weltweit verbreitet und gehören mit zu den häufigsten Krankheitserregern beim Menschen. Es handelt sich um behüllte Viren mit doppelsträngiger DNA, von denen man zwei Serotypen, HSV-1 und HSV-2, unterscheidet. In den Industrieländern beträgt die Kontamination der Bevölkerung mit HSV-1 etwa 80 bis 90 Prozent, mit HSV-2 etwa 20 bis 30 Prozent. Eine Infektion durch HSV-1 ist durch virushaltige Bläschen im Bereich der Lippen oder Mundschleimhaut (Lippenherpes; Herpes labialis) gekennzeichnet, während HSV-2 in der Regel Infektionen im Genitalbereich (Herpes genitalis) verursacht. Die Viren persistieren in den Nervenganglien, und die Symptome treten periodisch an der Stelle der ehemaligen Infektion immer wieder auf. In der Komplementärmedizin und Aromatherapie werden ätherische Öle vor allem bei Lippenherpes traditionell angewendet. In verschiedenen In-vitro-Studien haben wir ätherische Öle auf ihre potenzielle antiherpale Wirkung gegen HSV-1 und HSV-2 untersucht. Als Testsystem verwendeten wir einen Plaquereduktionstest und als Wirtszellen Affennierenzellen. Die Zellen werden zunächst mit Viren (100–300 pfu/ml) infiziert und anschliessend für drei Tage bei 37° C inkubiert. Anschliessend werden die Zellen mit 10 Prozent Formalin fixiert und mit Kristallviolett gefärbt. Bei infizierten Zellen kommt es durch Zelllyse zur Bildung von Plaques (Löcher im Zellrasen), die als weisse Stellen vor einem violetten Hintergrund gut zu erkennen sind. Durch Verwendung von antiviralen Substanzen kann die Plaquebildung (Infektiosität) reduziert werden. Die Plaquereduktion wird in Prozent der Kontrolle ausgedrückt. Stellvertretend soll im Folgenden näher auf die
thema22
PHYTOTHERAPIE
1/2011
25. SCHWEIZERISCHE TAGUNG FÜR PHYTOTHERAPIE, BADEN, 25. NOVEMBER 2010
Anti-HSV-1-Wirkung von Melissenöl, Pfef-
ferminzöl, Thymianöl, Kamillenöl und Tee-
Tabelle 1:
baumöl eingegangen werden (11). Der HSV-Infektionszyklus ist durch die Ab-
Anti-HSV-1-Wirkung ausgewählter ätherischer Öle (Dosis-Wirkungs-Beziehung)
folge von koordinierten Regulationsvorgängen in der Wirtszelle charakterisiert:
Ätherisches Öl Kamillenöl
EC50 (g/ml) 0,3
CC50 (g/ml) 30,0
SI 100,0
◆ Adsorption des Virus an die Zellmem-
Melissenöl
4,0
30,0 7,5
bran
Teebaumöl
9,0
60,0
6,7
◆ Penetration des Virus beziehungsweise
Thymianöl
10,0
70,0
7,0
der Virus-DNA in die Zelle
Pfefferminzöl
20,0
140,0
7,0
◆ intrazelluläre Replikation der Virus-DNA und Proteine
EC50: effektive Konzentration; CC50: zytotoxische Konzentration; SI: Selektivitätsindex CC50/EC50
◆ intrazellulärer Zusammenbau komplet-
ter Viruspartikel
◆ Freisetzung der Viren aus der Wirtszelle. rend der dreitägigen Inkubationszeit mit Wert von 0,3 g/ml und einem SI-Wert von
Durch Zugabe der ätherischen Öle zu ver- den Testölen behandelt, dann konnte keine 100 als ausserordentlich wirksam. Der SI-
schiedenen Zeiten des HSV-Infektionszy- Reduktion der Plaquebildung beobachtet Wert (Selektivitätsindex) ist ein relatives
klus sollte geprüft werden, welcher Schritt werden. Diese Resultate bedeuten, dass die Mass für die Spanne zwischen zytotoxi-
im Infektionszyklus durch die ätherischen antiherpale Wirkung der Testöle auf einer scher und antiviraler Wirkung. Experi-
Öle gehemmt wird. Bei den Experimenten direkten Interaktion der ätherischen Öle mente zur Zell-zu-Zell-Übertragung von
wurden jeweils die maximalen nicht zytoto- mit den zellfreien Viruspartikeln beruht. HSV-1 haben zudem gezeigt, dass ätheri-
xischen Konzentrationen der ätherischen Interessanterweise erwiesen sich die ge- sche Öle in der Lage sind, die Verbreitung
Öle (z.B. Pfefferminzöl: 100 g/ml; Thy- nannten ätherischen Öle auch wirksam ge- des Virus von einer infizierten Zelle zu einer
mianöl: 50 g/ml; Teebaumöl: 30 g/ml; gen acyclovirresistente Herpesstämme, da nicht infizierten Zelle mithilfe einer Plas-
Melissenöl: 20 g/ml; Kamillenöl: 10 g/ml) das Wirkungsprinzip dieser Stoffe sich mabrücke (unter Umgehung des Immun-
verwendet. Wurden die zellfreien Viren vor grundlegend vom Wirkungsmechanismus systems) zu unterbinden. Darüber hinaus
der Infektion der Wirtszellen eine Stunde der synthetischen Produkte unterscheidet ist die antivirale Wirkung der ätherischen
lang mit den Testölen vorbehandelt, dann (Abbildung).
Öle zeitabhängig und hängt zudem von
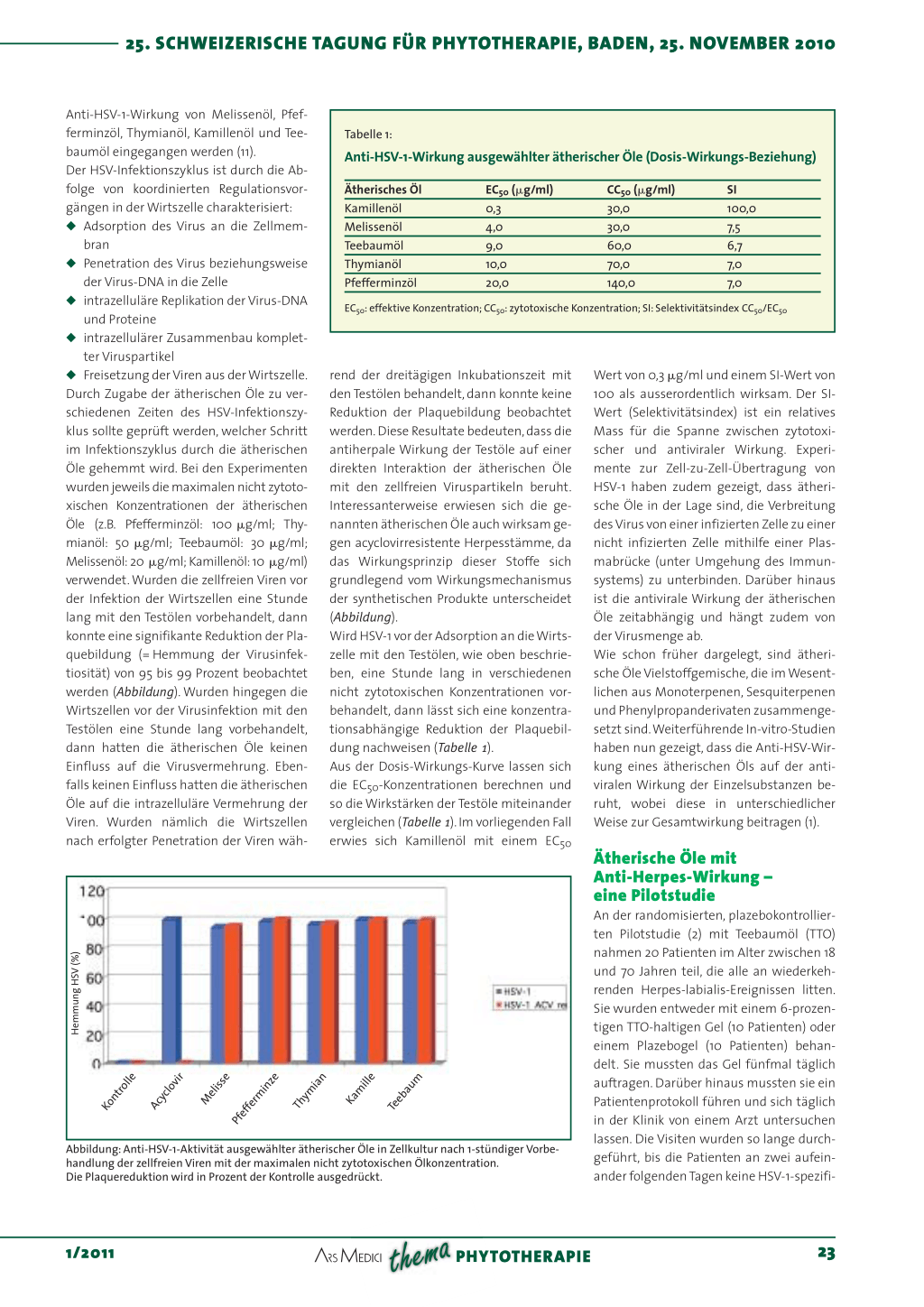
konnte eine signifikante Reduktion der Pla- Wird HSV-1 vor der Adsorption an die Wirts- der Virusmenge ab.
quebildung (= Hemmung der Virusinfek- zelle mit den Testölen, wie oben beschrie- Wie schon früher dargelegt, sind ätheri-
tiosität) von 95 bis 99 Prozent beobachtet ben, eine Stunde lang in verschiedenen sche Öle Vielstoffgemische, die im Wesent-
werden (Abbildung). Wurden hingegen die nicht zytotoxischen Konzentrationen vor- lichen aus Monoterpenen, Sesquiterpenen
Wirtszellen vor der Virusinfektion mit den behandelt, dann lässt sich eine konzentra- und Phenylpropanderivaten zusammenge-
Testölen eine Stunde lang vorbehandelt, tionsabhängige Reduktion der Plaquebil- setzt sind. Weiterführende In-vitro-Studien
dann hatten die ätherischen Öle keinen dung nachweisen (Tabelle 1).
haben nun gezeigt, dass die Anti-HSV-Wir-
Einfluss auf die Virusvermehrung. Eben- Aus der Dosis-Wirkungs-Kurve lassen sich kung eines ätherischen Öls auf der anti-
falls keinen Einfluss hatten die ätherischen die EC50-Konzentrationen berechnen und viralen Wirkung der Einzelsubstanzen be-
Öle auf die intrazelluläre Vermehrung der so die Wirkstärken der Testöle miteinander ruht, wobei diese in unterschiedlicher
Viren. Wurden nämlich die Wirtszellen vergleichen (Tabelle 1). Im vorliegenden Fall Weise zur Gesamtwirkung beitragen (1).
nach erfolgter Penetration der Viren wäh-
erwies sich Kamillenöl mit einem EC50
Ätherische Öle mit Anti-Herpes-Wirkung – eine Pilotstudie
An der randomisierten, plazebokontrollier-
ten Pilotstudie (2) mit Teebaumöl (TTO)
Hemmung HSV (%)
nahmen 20 Patienten im Alter zwischen 18
und 70 Jahren teil, die alle an wiederkeh-
renden Herpes-labialis-Ereignissen litten.
Sie wurden entweder mit einem 6-prozen-
tigen TTO-haltigen Gel (10 Patienten) oder
einem Plazebogel (10 Patienten) behan-
delt. Sie mussten das Gel fünfmal täglich
Kontrolle Acyclovir Melisse Pfefferminze Thymian Kamille Teebaum
auftragen. Darüber hinaus mussten sie ein
Patientenprotokoll führen und sich täglich
in der Klinik von einem Arzt untersuchen
Abbildung: Anti-HSV-1-Aktivität ausgewählter ätherischer Öle in Zellkultur nach 1-stündiger Vorbehandlung der zellfreien Viren mit der maximalen nicht zytotoxischen Ölkonzentration. Die Plaquereduktion wird in Prozent der Kontrolle ausgedrückt.
lassen. Die Visiten wurden so lange durchgeführt, bis die Patienten an zwei aufeinander folgenden Tagen keine HSV-1-spezifi-
1/2011
thema PHYTOTHERAPIE
23
25. SCHWEIZERISCHE TAGUNG FÜR PHYTOTHERAPIE, BADEN, 25. NOVEMBER 2010
Tabelle 2:
Antivirale Aktivität von ausgewählten Polyphenolen gegen Influenza-A-Viren in Zellkultur
Polyphenole
CC50 (g/ml) EC50 (g/ml) SI
Quercetin Apigenin (+) Catechin (–) Epicatechin Kaffeesäure Epicatechingallat Epigallocatechingallat
60,0 60,0 100,0 120,0 150,0 232,5 126,1
12,2 4,1 8,3 12,0 12,5 11,7 13,0
*bezogen auf die einmalige Einnahme von 50 mg Polyphenole
4,9 14,6 12,0 10,0 12,0 19,9 9,7
Plasmakonzentration Mensch (g/ml)* 0,3 – 0,12 0,12 0,18 0,45 0,05
sche DNA mehr aufwiesen und die Reepithelisierung eingesetzt hatte. Die mittlere Zeitspanne vom Auftreten der ersten Läsionen in der Vesikel- beziehungsweise Bläschenphase bis zur Reepithelisierung betrug in der TTO-Gruppe 9 Tage und in der Plazebogruppe 12,5 Tage. Die Unterschiede waren aufgrund der geringen Patientenzahl nicht statistisch signifikant. Trotz dieser Einschränkung entsprachen die Ergebnisse denen aus einer ähnlichen Untersuchung, die mit Acyclovir durchgeführt worden war. Die Ergebnisse aus den In-vitro-Studien und der humanen Beobachtungsstudie bestätigen die aus anekdotischen Berichten von Patienten postulierte antiherpale Wirkung von ätherischen Ölen und deren potenziellen Nutzen in der lokalen Behandlung von Lippenherpes. Patienten mit wieder-
kehrenden Lippenherpes-Attacken berichten zudem, dass durch die Behandlung mit ätherischen Ölen am Ort der Infektion einerseits der Juckreiz und die Entzündungen stark gemindert und andererseits mögliche bakterielle Infektionen verhindert oder zumindest deutlich minimiert werden.
Polyphenole mit Anti-Influenza-Wirkung – In-vitro-Studien
Influenzaviren sind Orthomyxoviren und werden in die Typen A, B und C unterteilt. Für den Menschen sind nur Influenza-Aund Influenza-B-Viren von Interesse. Während es bei Influenza-B-Viren keine Subtypen gibt, können Influenza-A-Viren anhand ihrer Oberflächenproteine Hämagglutinin (HA) und Neuraminidase (NA) verschiedenen Subtypen zugeordnet werden (z.B.
H1N1, H3N2). Influenza-A-Viren und Influenza-B-Viren sorgen jedes Jahr weltweit für schwerwiegende Infektionskrankheiten (Influenza-Grippe, Echte Grippe), die vor allem bei Problemgruppen, wie zum Beispiel älteren Menschen, Schwangeren und Menschen mit chronischen Grunderkrankungen, zu schwerwiegenden Komplikationen bis hin zum Tode führen können. Eine Influenzagrippe darf nicht mit einer banalen viralen Infektion der oberen Atemwege (grippaler Infekt) verwechselt werden. Die Influenzaviren dringen über die Schleimhäute der oberen Atemwege, des Mundes und der Augen in den Körper ein. Das Influenzavirus ist ein behülltes Virus mit negativer Einzelstrang-RNA (Minus-Polarität), die in acht separate Einzelstrangsegmente unterteilt ist. Sie bilden zusammen mit den Nukleoproteinen das helikale Nukleokapsid. Als Prophylaxe steht eine jährliche Influenzaimpfung zur Verfügung und bei erfolgter Infektion kommt (innerhalb von 48 Stunden) der Einsatz von spezifischen Chemotherapeutika infrage, wie zum Beispiel die Neuraminidasehemmer Oseltamivir und Zanamivir sowie die beiden M2-Ionenkanalprotein-Hemmer Amantadin und Rimantadin. Inwieweit Arzneipflanzen und ihre speziellen Zubereitungen zur Prophylaxe oder zur symptomatischen Behandlung typischer Beschwerdebilder (z.B. Husten, Fieber, Kopfund Muskelschmerzen) geeignet sind, ist derzeit unklar und wird kontrovers diskutiert. Derzeit werden polyphenolhaltige Pflanzenextrakte aus Camelia sinensis (Teestrauch), Cistus incanus ssp. tauricus
Tabelle 3:
Spezialextrakt aus Cistus incanus (CYSTUS052) appliziert oral oder als Aerosol in einem experimentellen Influenza-AMausmodell (H7N7)
Weibliche Mäuse wurden in einem Inhalationskäfig mit 2 ml Aerosol (Cystus052-Extrakt 10 mgl; H2O als Kontrolle) 10 Minuten lang 3 x am Tag behandelt. Die Behandlung dauerte insgesamt 5 Tage. 10 Minuten nach der ersten Behandlung wurden die anästhesierten Mäuse mit dem Influenza-A-Virus (H7N7) infiziert. Die Experimente wurden 3 x wiederholt.
Behandlung
CYSTUS052® H2O-Kontrolle CYSTUS052® H2O-Kontrolle
Applikationsweg
Aerosol Aerosol Oral Oral
Anzahl der Versuchstiere
15 15 10 10
Tiere mit Krankheitssymptomen
0(2)/15 13/15 10/10 10/10
Auftreten der Symptome (Tage nach der Infektion) (8) 7 7 7
Überlebende Tiere
15(13)/15 7/15 2/10 2/10
6 Tage nach der Virusinfektion wurden in der Lunge von Kontrolltieren 240 Hämagglutinin-Einheiten/ml und von mit CYSTUS052 Aerosol behandelten Tieren lediglich noch 40 Hämagglutinin-Einheiten/ml nachgewiesen.
Droebner et al. (2007) Antiviral Research 76: 1–10.
thema24
PHYTOTHERAPIE
1/2011
25. SCHWEIZERISCHE TAGUNG FÜR PHYTOTHERAPIE, BADEN, 25. NOVEMBER 2010
Tabelle 4: Ergebnisse der Studie (Kalus et al. 2009)
Gemessene Parameter Symptomen-Summenscore (SSS) Tag 1 Tag 4 Tag 5 Tag 6 Tag 7 Entzündungsmarker CRP Tag 1 Tag 4 Tag 7
CYSTUS052 SSS-Mittelwert über alle Patienten (0–30) 22 17 10 7 4 (mg/l) 37,6 36,4 8,8
Plazebo SSS-Mittelwert über alle Patienten (0–30) 22 20 18 15 11 (mg/l) 34,8 39,4 17,7
(behaarte Zistrose), Geranium sanguineum (Blutstorchschnabel) und Punica granatum (Granatapfelbaum) als mögliche Kandidaten diskutiert. Stellvertretend sollen die In-vitro- und In-vivo-Studien mit einem polyphenolhaltigen Spezialextrakt (CYSTUS052) aus der behaarten Zistrose vorgestellt und diskutiert werden. In-vitro-Studien mit isolierten Polyphenolen in Zellkultur (MDCK-Zellen = Hundenierenzellen; Plaquereduktionstest) haben gezeigt, dass bei gleichzeitiger Inkubation der Wirtszellen mit Viren und Testsubstanzen (in nicht zytotoxischen Konzentrationen) für eine Stunde (anschliessend wird das Inokulum entfernt und die Zellkultur für 3 bis 4 Tage bei 33° C weiterkultiviert) eine signifikante konzentrationsabhängige Plaquereduktion nachgewiesen werden konnte (Tabelle 2) (3–5). Dieser Befund korreliert mit den Ergebnissen aus den Studien zur antiviralen Wirkung von ätherischen Ölen und macht deutlich, dass diese Substanzen direkt auf die zellfreien Viren einwirken. Elektronenmikroskopische Studien haben gezeigt, dass Polyphenole an virale Oberflächenproteine (Hämagglutinin) binden. Dadurch werden die Viren ähnlich wie durch Antikörper agglutiniert, wodurch die Adsorption der Viruspartikel an die Zelloberfläche verhindert wird (3). Polyphenole können auch mit Wirtszellrezeptoren interagieren und dadurch die Anheftung der Viren an die Zelloberfläche unterbinden. Dadurch wird in beiden Fällen verhindert, dass die Viren in die Wirtszelle eindringen können. Hingegen wurde die intrazelluläre Virusvermehrung durch die Polyphenole nicht beeinflusst.
Polyphenolhaltiger Extrakt (Cystus052) mit Anti-Influenza-A-Wirkung – In-vivoStudie (Mausmodell)
In einem Zellkultursystem mit Lungenepithelzellen zeigte der Spezialextrakt CYSTUS052 (Zistrosenextrakt) nach einstündiger Vorbehandlung der zellfreien Influenzaviren eine signifikante, dosisabhängige Reduktion der Plaquebildung. In einer Konzentration von 50 g/ml hemmte der Extrakt in vitro die Zellplaquebildung (Virusinfektiosität), hervorgerufen von aviären INF-Viren (H5N1 und H7N7) als auch von humanen INF-Viren (H1N1), zu 90 bis 100 Prozent. In der wirksamen Konzentration veränderte der Zistrosenextrakt weder die Zellmorphologie noch beeinflusste er das Wachstum und die Vitalität der Epithelzellen negativ. Er löste auch keine Apoptose aus und induzierte auch keine rezeptorvermittelten intrazellulären Vorgänge, wie zum Beispiel die Aktivierung von Transkriptionsfaktoren (6). Basierend auf diesen Ergebnissen wurden Mäuse mit dem hochpathogenen aviären Influenzavirus (H7N7) infiziert und mit einem CYSTUS052-Extrakt oral oder in Form eines Aerosols im Vergleich zu den entsprechenden Wasserkontrollen behandelt (Tabelle 3) (7). Sieben Tage nach der Infektion entwickelten die Mäuse in beiden Wasserkontrollgruppen klinische Symptome (z.B. Rückgang der Körpertemperatur und der Körperaktivität, gesträubtes Fell) sowie eine signifikante Reduktion ihres Körpergewichts. In der Wasseraerosolgruppe verstarben etwa 53 Prozent der Kontrolltiere, in der Kontrollgruppe, die oral Wasser ver-
abreicht bekommen hatte, verstarben sogar 80 Prozent der Kontrolltiere. In der CYSTUS052-Aerosolgruppe entwickelten in einem der drei unabhängigen Versuchsansätze lediglich zwei Tiere Krankheitssymptome, an denen sie dann auch verstarben (Tabelle 3). Alle anderen Tiere zeigten keine krankheitsspezifischen Symptome und auch keine signifikanten Gewichtsverluste. Die orale Gabe von CYSTUS052 hatte hingegen keinen Einfluss auf den Krankheitsverlauf. Alle Tiere erkrankten, wovon 80 Prozent (wie bei der Kontrollgruppe) anschliessend verstarben. Dieses Ergebnis überrascht nicht, da Polyphenole aus dem Gastrointestinaltrakt nur in sehr geringen Mengen resorbiert werden (Tabelle 2) und somit keine antivirale Wirkung am Infektionsort entfalten können. Das Ergebnis der hier vorgestellten tierexperimentellen Studie ist vergleichbar mit dem Ergebnis aus ähnlichen tierexperimentellen Studien, die mit anderen polyphenolhaltigen Pflanzenextrakten (z.B. aus Geranium sanguineum) durchgeführt wurden (8).
Polyphenolhaltiger Extrakt (Cystus052) zur Linderung von Symptomen einer banalen Infektion der oberen Atemwege (grippaler Infekt)
Studientyp: prospektive, randomisierte, plazebokontrollierte Studie. Eingeschlossene Patienten: insgesamt 160 Patienten mit durch Rachenabstrich nachgewiesenen Infekten; 92 Patienten wiesen eine virale und 67 eine bakterielle Infektion auf. Behandlungsbeginn: 1 Tag nach der ersten Visite. Verum-/Plazebotherapie: täglich 6 x 2 CYSTUS052-Lutschpastillen (etwa 260 mg Polyphenole) oder Plazebolutschpastillen. Therapie- und Beobachtungszeitraum: 7 Tage. Bewertung von fünf subjektiven Symptomen auf ihren Schweregrad: Schmerz, Hustenintensität, Hustenfrequenz, Auswurf und Schnupfen. Bewertungsgrundlage: 0 = nicht vorhanden; 2 = schwach; 4 = mild; 6 = stark. Symptomen-Summenscore: Aus der Addition der bewerteten Symptome errechnet sich der jeweilige Symptomen-Summenscore; er kann pro Patient zwischen 0 (keine Symptome) und 30 (starke Symptome) Punkte betragen.
1/2011
thema PHYTOTHERAPIE
25
25. SCHWEIZERISCHE TAGUNG FÜR PHYTOTHERAPIE, BADEN, 25. NOVEMBER 2010
Entzündungsmarker: In den Blutproben wurde auch der Entzündungsmarker (C-reaktives Protein) bestimmt. Bei der Studie von Kalus et al. (9) nahm über einen Beobachtungszeitraum von sieben Tagen der Symptomen-Summenscore in der Verumgruppe, unabhängig von der zugrunde liegenden Pathogengruppe, von 22 auf 4 ab, während er in der Plazebogruppe lediglich von 22 auf 11 zurückging (Tabelle 4). Gleichzeitig nahm der Entzündungsmarker CRP im Blut der Verumgruppe von 37,6 auf 8,8 mg/l ab, während er sich in der Plazebogruppe von 34,6 auf 17,7 mg/l verringerte. Die Unterschiede in beiden Studienarmen waren statistisch signifikant. Dieses Ergebnis ist ein erster Hinweis darauf, dass der polyphenolhaltige Pflanzenextrakt CYSTUS052 in der Lage ist, die Begleitsymptome eines banalen grippalen Infekts im Vergleich zu Plazebo in kürzerer Zeit signifikant zu bessern und den Heilungsprozess zu beschleunigen. Ähnliche Ergebnisse wurden mit einem polyphenolhaltigen Extrakt aus grünem Tee erzielt, wobei dort der Extrakt in Form von Kapseln oral eingenommen wurde (10). Beide Studien sind aufgrund der unterschiedlichen Extraktzubereitungen der verwendeten Pflanzen und Applikationsform der Extrakte nur bedingt miteinander vergleichbar. Daher müssen weitere Studien zeigen, ob Patienten mit banalen Infekten der oberen Atemwege tatsächlich einen Vorteil durch die beschriebenen Therapieformen haben. Bei der Studie von Kalus et al. (9) handelt es sich um eine symptomatische Behandlung eines banalen grippalen Infekts (Erkältung) und nicht um eine primäre Bekämpfung und Elimination der dem Infekt zugrunde liegenden Bakterien und Viren. Die Symptome einer Erkältung (z.B. Husten, Auswurf, Schnupfen) sind kein direktes Resultat von viralen oder bakteriellen zytopa-
thischen Effekten, sondern das Resultat der
Bildung von proinflammatorischen Zytoki-
nen und Chemokinen, die in Viren oder
Bakterien infizierten Epithelzellen gebildet
und anschliessend sezerniert werden. Sie
stimulieren entzündungsrelevante Leuko-
zyten. Daher ist die Verwendung von ent-
zündungshemmenden Stoffen ein proba-
tes Mittel, um die Begleitsymptome einer
banalen Erkältungskrankheit erfolgreich
zu bekämpfen. Zubereitungen aus Cistus
incanus werden in Griechenland traditio-
nell als entzündungshemmende Mittel
verwendet.
Aufgrund der oben beschriebenen experi-
mentellen Tierstudien und den wenigen
klinischen Studien mit Patienten mit bana-
len viralen Atemwegsinfektionen wird
spekuliert, ob sich polyphenolhaltige Pflan-
zenextrakte als Prophylaktikum zur Verhin-
derung einer Influenzainfektion eignen
könnten. Bisher gibt es keine einzige valide
klinische Humanstudie, die eine solch ge-
wagte Spekulation rechtfertigen würde.
Zudem sind die Applikationsformen der
Extrakte in den Tierstudien und klinischen
Humanstudien völlig anders und nicht
miteinander vergleichbar. Zu prüfen wäre
allerdings, ob Problemgruppen in der Be-
völkerung nach erfolgter Influenzaimp-
fung von einer Begleittherapie mit poly-
phenolhaltigen Extrakten in Form von
Mund- und Nasensprays zusätzlich profi-
tieren könnten, zum Beispiel durch Ver-
hinderung oder Abschwächung eines grip-
palen Infekts beziehungsweise einer In-
fluenzagrippe und/oder durch Linderung
der Begleitsymptome.
◆
Anschrift des Referenten Prof. Dr. Jürgen Reichling Institut für Pharmazie und Molekulare Biotechnologie, Abt. Biologie Universität Heidelberg Im Neuenheimer Feld 364 D-69120 Heidelberg Juergen.reichling@t-online.de
Literatur:
1. Astani A., Reichling J., Schnitzler P.: Comparative study on the antiviral activity of selected monoterpenes derived from essential oils. Phytotherapy Research 2010; 23: 673–679.
2. Carson C.F., Ashton L., Dry L., Smith D.W., Riley T.V. Melaleuca alternifolia (tea tree) oil gel (6 percent) for the treatment of recurrent herpes labialis. Journal of Antimicrobial Chemotherapy 2001; 48: 445–458.
3. Nakayama M., Suzuki K., Toda M., Okubo S., Hara Y., Shimamura T. Inhibition of the infectivity of influenza virus by tea polyphenols. Antiviral Research 1993; 21: 289–299.
4. Song J.-M., Lee K.-H., Seong B.-L. Antiviral effect of catechins in green tea on influenza virus. Antiviral Research 2005; 68: 66–74.
5. Pantev A., Ivancheva S., Staneva L., Serkedjieva J. Biologically active constituents of a polyphenol extract from Geranium sanguineum L. with anti-Influenza activity. Zeitschrift für Naturforschung 2006; 61c: 508–516.
6. Ehrhardt C., Hrincius E.R., Korte V. et al. A polyphenol-rich plant extract, CYSTUS052, exerts anti-influenza virus activity in cell culture without toxic side effects or the tendency to induce viral resistance. Antiviral Research 2007; 76: 38–47.
7. Droebner K., Erhardt C., Poetter A., Ludwig S., Planz O. CYSTUS052, a polyphenol-rich plant extract, exerts anti-inluenza virus activity in mice. Antiviral Research 2007; 76: 1–10.
8. Serkedjieva J., Gegova G., Mladenova K. Protective efficacy of an aerosol preparation, obtained from Geranium sanguineum L., in experimental influenza infection. Pharmazie 2008; 63: 160–163.
9. Kalus U., Grigorov A., Kadecki O., Jamsen J.-P., Kiesewetter H., Radtke H. Cistus incanus (CYSTUS052) for treating patients with infection of the upper respiratory tract. A prospective, randomised, placebocontrolled clinical study. Antiviral Research 2009; 84: 267–271.
10. Rowe C.A., Nantz M.P., Bukowski J.F., Percival S.S. Specific formulation of Camellia sinensis prevents cold and flu symptoms and enhances ␥␦ T cell functions: a randomized, double-blind, placebo-controlled study. Journal of the American College of Nutrition 2007; 26: 445–452.
11. Reichling J., Schnitzler P., Suschke U., Saller R. Essential oils of aromatic plants with antimicrobial, antifungal, antiviral, and cytotoxic properties – an overview. Forschende Komplementärmedizin 2009; 16: 79–90.
thema26
PHYTOTHERAPIE
1/2011