Transkript
BERICHT
Neues zur Behandlung von Patienten mit gastrointestinalen Karzinomen
Adjuvante und palliative Chemotherapie
Die Diagnostik und Behandlung von Patienten mit gastrointestinalen Tumorerkrankungen rückt mit zunehmender Inzidenz immer mehr in den Mittelpunkt sowohl der internistischen Onkologie, der Gastroenterologie, der Viszeralchirurgie als auch anderer Fachgebiete, die an der Versorgung von onkologischen Patienten beteiligt sind. Gemäss den am diesjährigen ASCO-Kongress vorgestellten neuen Daten gibt der folgende Artikel eine Übersicht über aktuelle Entwicklungen der adjuvanten und palliativen Chemotherapie bei gastrointestinalen Tumorerkrankungen. Mit Abstand die wichtigste Neuheit war in diesem Jahr die Etablierung von KRAS als erstem Biomarker bei der palliativen Behandlung von Patienten mit kolorektalem Karzinom.
JÖRG TROJAN
Kolorektales Karzinom MMR-Status und Therapieansprechen Ein defekter DNA-Mismatch-Reparaturmechanismus (MMR) geht im Zellkulturmodell mit einer 5-FU-Resistenz einher. Sargent ging der Frage nach, ob der Nachweis einer defekten MMR, die bei etwa 15 Prozent aller kolorektalen Karzinome nachweisbar ist, einen Einfluss auf den Erfolg einer alleinigen 5-FUTherapie im Stadium II und III hat (1). Retrospektiv wurde hierzu der MMRStatus aus Tumorgewebe von 341 Patienten, die innerhalb von randomisierten Studien mit 5-FU/Folinsäure oder Levamisol adjuvant behandelt beziehungsweise überwacht wurden, mittels Immunhistochemie (Verlust der Expression von hMLH1 im Tumorgewebe)
untersucht. Es zeigte sich, dass nur Patienten mit intakter MMR von einer 5-FU-haltigen adjuvanten Therapie profitieren, nicht jedoch die Patienten mit defekter MMR. Insbesondere im Falle einer alleinigen adjuvanten Therapie mit 5-FU (z.B. Patienten mit Stadium II oder Kontraindikationen für die Gabe von Oxaliplatin) ist die Bestimmung des MMR-Status empfehlenswert.
Adjuvante Therapie im Stadium III Standard der adjuvanten Therapie im Stadium III ist die Behandlung mit einem infusionalen 5-FU-Regime in Kombination mit Oxaliplatin (z.B. FOLFOX4-Schema). Allegra berichtete die ersten Ergebnisse der NSABP-C-08-Studie in Bezug auf Sicherheit (2). In dieser randomisierten Phase-III-Studie wird geprüft, ob durch eine 12-monatige ad-
Kongress der American Society of Clinical Oncology (ASCO) in Chicago/Illinois, USA, vom 30. Mai bis 3. Juni 2008; mit über 30 000 Teilnehmern aus Klinik, Forschung und Industrie ist die ASCO-Tagung der grösste und bedeutendste Krebskongress. Die Zusammenfassungen der vorgestellten Präsentationen sind frei zugänglich unter www.asco.org.
juvante Therapie mit Bevacizumab zusätzlich zu FOLFOX6 über 6 Monate eine weitere Verbesserung der Prognose erzielt werden kann. Bevacizumab ist ein humanisierter monoklonaler Antikörper, der über Hemmung des vaskulären endothelialen Wachstumsfaktors (vascular endothelial growth factor, VEGF) die Angiogenese des Tumors hemmt. Eine Zulassung liegt nur für die palliative Therapie vor. Im Zeitraum September 2004 bis Oktober 2006 wurden insgesamt 2710 Patienten in die Studie eingeschlossen. Es zeigte sich in der Gruppe der zusätzlich mit Bevacizumab behandelten Patienten eine geringgradig erhöhte Inzidenz von Wundheilungsstörungen und peripherer Neuropathie. Komplikationen wie Blutungen, gastrointestinale Perforationen oder Thrombosen traten im Bevacizumab-Arm nicht gehäuft auf. Daten zur Wirksamkeit werden frühestens für 2010 vorliegen, bis dahin sollte Bevacizumab nicht in der adjuvanten Situation eingesetzt werden.
Optionen zur palliativen Therapie In der palliativen Situation stehen in der Erstlinientherapie derzeit mit 5-FU beziehungsweise Capecitabin, Oxaliplatin, Irinotecan und Bevacizumab eine Reihe denkbarer Kombinationsmöglichkeiten
954 ARS MEDICI 21 ■ 2008
NEUES ZUR BEHANDLUNG VON PATIENTEN MIT GASTROINTESTINALEN KARZINOMEN
A
B
C
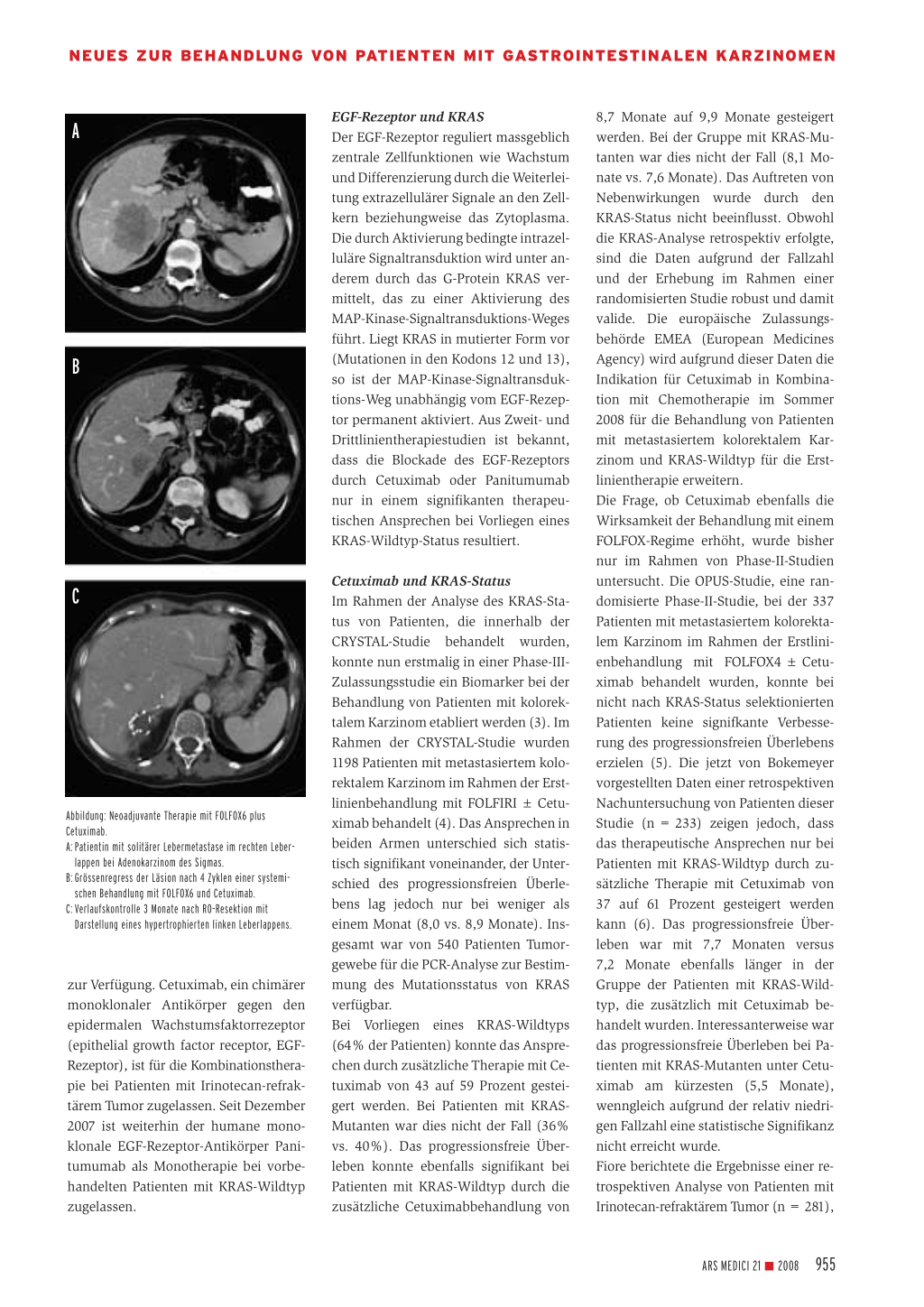
Abbildung: Neoadjuvante Therapie mit FOLFOX6 plus Cetuximab. A: Patientin mit solitärer Lebermetastase im rechten Leber-
lappen bei Adenokarzinom des Sigmas. B: Grössenregress der Läsion nach 4 Zyklen einer systemi-
schen Behandlung mit FOLFOX6 und Cetuximab. C: Verlaufskontrolle 3 Monate nach R0-Resektion mit
Darstellung eines hypertrophierten linken Leberlappens.
zur Verfügung. Cetuximab, ein chimärer monoklonaler Antikörper gegen den epidermalen Wachstumsfaktorrezeptor (epithelial growth factor receptor, EGFRezeptor), ist für die Kombinationstherapie bei Patienten mit Irinotecan-refraktärem Tumor zugelassen. Seit Dezember 2007 ist weiterhin der humane monoklonale EGF-Rezeptor-Antikörper Panitumumab als Monotherapie bei vorbehandelten Patienten mit KRAS-Wildtyp zugelassen.
EGF-Rezeptor und KRAS Der EGF-Rezeptor reguliert massgeblich zentrale Zellfunktionen wie Wachstum und Differenzierung durch die Weiterleitung extrazellulärer Signale an den Zellkern beziehungweise das Zytoplasma. Die durch Aktivierung bedingte intrazelluläre Signaltransduktion wird unter anderem durch das G-Protein KRAS vermittelt, das zu einer Aktivierung des MAP-Kinase-Signaltransduktions-Weges führt. Liegt KRAS in mutierter Form vor (Mutationen in den Kodons 12 und 13), so ist der MAP-Kinase-Signaltransduktions-Weg unabhängig vom EGF-Rezeptor permanent aktiviert. Aus Zweit- und Drittlinientherapiestudien ist bekannt, dass die Blockade des EGF-Rezeptors durch Cetuximab oder Panitumumab nur in einem signifikanten therapeutischen Ansprechen bei Vorliegen eines KRAS-Wildtyp-Status resultiert.
Cetuximab und KRAS-Status Im Rahmen der Analyse des KRAS-Status von Patienten, die innerhalb der CRYSTAL-Studie behandelt wurden, konnte nun erstmalig in einer Phase-IIIZulassungsstudie ein Biomarker bei der Behandlung von Patienten mit kolorektalem Karzinom etabliert werden (3). Im Rahmen der CRYSTAL-Studie wurden 1198 Patienten mit metastasiertem kolorektalem Karzinom im Rahmen der Erstlinienbehandlung mit FOLFIRI ± Cetuximab behandelt (4). Das Ansprechen in beiden Armen unterschied sich statistisch signifikant voneinander, der Unterschied des progressionsfreien Überlebens lag jedoch nur bei weniger als einem Monat (8,0 vs. 8,9 Monate). Insgesamt war von 540 Patienten Tumorgewebe für die PCR-Analyse zur Bestimmung des Mutationsstatus von KRAS verfügbar. Bei Vorliegen eines KRAS-Wildtyps (64% der Patienten) konnte das Ansprechen durch zusätzliche Therapie mit Cetuximab von 43 auf 59 Prozent gesteigert werden. Bei Patienten mit KRASMutanten war dies nicht der Fall (36% vs. 40%). Das progressionsfreie Überleben konnte ebenfalls signifikant bei Patienten mit KRAS-Wildtyp durch die zusätzliche Cetuximabbehandlung von
8,7 Monate auf 9,9 Monate gesteigert werden. Bei der Gruppe mit KRAS-Mutanten war dies nicht der Fall (8,1 Monate vs. 7,6 Monate). Das Auftreten von Nebenwirkungen wurde durch den KRAS-Status nicht beeinflusst. Obwohl die KRAS-Analyse retrospektiv erfolgte, sind die Daten aufgrund der Fallzahl und der Erhebung im Rahmen einer randomisierten Studie robust und damit valide. Die europäische Zulassungsbehörde EMEA (European Medicines Agency) wird aufgrund dieser Daten die Indikation für Cetuximab in Kombination mit Chemotherapie im Sommer 2008 für die Behandlung von Patienten mit metastasiertem kolorektalem Karzinom und KRAS-Wildtyp für die Erstlinientherapie erweitern. Die Frage, ob Cetuximab ebenfalls die Wirksamkeit der Behandlung mit einem FOLFOX-Regime erhöht, wurde bisher nur im Rahmen von Phase-II-Studien untersucht. Die OPUS-Studie, eine randomisierte Phase-II-Studie, bei der 337 Patienten mit metastasiertem kolorektalem Karzinom im Rahmen der Erstlinienbehandlung mit FOLFOX4 ± Cetuximab behandelt wurden, konnte bei nicht nach KRAS-Status selektionierten Patienten keine signifkante Verbesserung des progressionsfreien Überlebens erzielen (5). Die jetzt von Bokemeyer vorgestellten Daten einer retrospektiven Nachuntersuchung von Patienten dieser Studie (n = 233) zeigen jedoch, dass das therapeutische Ansprechen nur bei Patienten mit KRAS-Wildtyp durch zusätzliche Therapie mit Cetuximab von 37 auf 61 Prozent gesteigert werden kann (6). Das progressionsfreie Überleben war mit 7,7 Monaten versus 7,2 Monate ebenfalls länger in der Gruppe der Patienten mit KRAS-Wildtyp, die zusätzlich mit Cetuximab behandelt wurden. Interessanterweise war das progressionsfreie Überleben bei Patienten mit KRAS-Mutanten unter Cetuximab am kürzesten (5,5 Monate), wenngleich aufgrund der relativ niedrigen Fallzahl eine statistische Signifikanz nicht erreicht wurde. Fiore berichtete die Ergebnisse einer retrospektiven Analyse von Patienten mit Irinotecan-refraktärem Tumor (n = 281),
ARS MEDICI 21 ■ 2008 955
BERICHT
die mit Irinotecan und Cetuximab behandelt wurden (7). Bei Patienten mit KRAS-Wildtyp zeigte sich ein verlängertes progressionsfreies Überleben (5,5 Monate vs. 2,7 Monate) und Gesamtüberleben (13,2 Monate vs. 8,0 Monate) gegenüber Patienten, bei denen eine KRAS-Mutante vorlag.
Panitumumab und KRAS-Status Mit Panitumumab steht seit Kurzem ein komplett humaner EGF-Rezeptor-Antikörper zur Verfügung. Eine Prämedikation ist nicht notwendig, das Auftreten von seltenen beobachteten Infusionsreaktionen ist noch unwahrscheinlicher. Derzeit ist Panitumumab nur nach Versagen einer Oxaliplatin- und Irinotecanhaltigen Chemotherapie als Monotherapie bei Patienten mit KRAS-Wildtyp zugelassen (8). Siena berichtete die ersten Ergebnisse zur Sicherheit von Panitumumab in Kombination mit FOLFOX6 im Rahmen einer randomisierten PhaseIII-Studie (n = 903) bei der Erstlinientherapie von Patienten mit metastasiertem kolorektalem Karzinom (9). Die Phase-III-Sicherheitsdaten im Rahmen der Zweitlinientherapie in Kombination mit FOLFIRI wurden von Peeters vorgestellt (10). In beiden Studien traten keine unerwarteten Nebenwirkungen auf. Mit den ersten Ergebnissen zur Wirksamkeit ist in ein bis zwei Jahren zu rechnen. In einer Zweitlinientherapie-Studie (Phase II, einarmig, n = 109) mit Panitumumab in Kombination mit FOLFIRI zeigte sich bei Patienten mit KRAS-Wildtyp in Analogie zu Cetuximab ein ebenfalls längeres progressionsfreies Überleben und Gesamtüberleben als bei Patienten mit KRAS-Mutanten (6,1 Monate vs. 3,7 Monate bzw. 9,1 Monate vs. 7,2 Monate) (11).
Strategien gegen Oxaliplatin-induzierte periphere Neuropathie Die chronische Oxaliplatin-induzierte periphere Neuropathie ist mit zunehmender Therapiedauer ein klinisch relevantes Problem. Im Alltag führt die Neuropathie nicht selten zum Therapieabbruch, bevor eine messbare Krankheitsprogression vorliegt. Wenngleich die CONCePT-Studie, die von Grothey vorgestellt wurde (12), vorzeitig abge-
brochen wurde, liegen nun valide Daten vor, die zeigen, dass die intermittierende Therapie mit Oxaliplatin bei fortgeführter Erhaltungstherapie mit 5-FU/Bevacizumab ein praktikabler Ansatz ist, der mit deutlich weniger chronischer Neurotoxizität einhergeht als die kontinuierliche Oxaliplatingabe bis zum Progress. Die Studie wurde vorzeitig abgebrochen, weil befürchtet wurde, dass sich das therapeutische Ansprechen durch Magnesium/Kalzium-Infusionen, die einige Patienten als Teil der Studie erhielten, verschlechtert. Dies hat sich jedoch nicht bestätigt. Im Rahmen einer NCCGT-Studie wurde zudem erstmalig im randomisierten Phase-III-Vergleich gezeigt, dass durch die Gabe von Magnesium/Kalzium (jeweils 1 g vor und nach der Oxaliplatingabe) das Auftreten der chronischen Neurotoxizität deutlich vermindert werden kann (13).
Bevacizumab plus Chemotherapie Die BRiTE-Studie ist eine grosse Anwendungsbeobachtung an 1953 Patienten, die im Rahmen der Erstlinientherapie mit einem Bevacizumab-haltigen Chemotherapieregime behandelt wurden. Es zeigte sich nur eine geringe Rate an schwerwiegenden Wundheilungsstörungen und Blutungsereignissen, sodass bei Beachtung der Kontraindikationen, wie zum Beispiel ein 5- bis 6-wöchiger Abstand zu operativen Eingriffen, ein sicherer Einsatz möglich ist (14, 15). Auf dem letzten ASCO-Kongress berichtete Falcone die finalen Ergebnisse einer Phase-III-Studie (n = 244) zur Behandlung mit FOLFIRI versus FOLFOXIRI, das heisst einer Kombination von 5-FU/Folinsäure mit Oxaliplatin und Irinotecan. Die Ansprechraten im FOLFOXIRI-Arm waren deutlich besser als im FOLFIRI-Arm (60% vs. 34%) und resultierten in einer höheren Rate an potenziell kurativen (R0) Leberteilresektionen (15% vs. 6%) (16). Im Rahmen der Anschlussstudie (Phase II) wurden bisher 51 auswertbare Patienten mit FOLFOXIRI plus Bevacizumab behandelt (17). Hierdurch konnte die Ansprechrate auf 75 Prozent gesteigert werden. Von bisher 30 Patienten, die eine auf die Leber begrenzte Meta-
stasierung aufwiesen, konnten 8 Patienten leberteilreseziert werden (R0-Resektion bei 7 Patienten). Weitere Daten müssen zeigen, ob sich dieses Schema bei Patienten mit primär nicht resektablen Lebermetastasen als ein Standard erweist. Nach kurativer Leberteilresektion ist aufgrund der derzeitigen Datenlage die adjuvante Behandlung mit FOLFIRI nicht sinnvoll (18).
Pankreaskarzinom Nach Resektion eines Pankreaskarzinoms ist in Europa die 6-monatige Behandlung mit Gemcitabin in vielen Praxen und Kliniken Standard. In der Originalpublikation der CONKO-001Studie (19) war zwar das rezidivfreie Überleben deutlich verbessert (6,9 Monate vs. 13,4 Monate), der primäre Endpunkt der Studie, das Gesamtüberleben, war jedoch (noch) nicht statistisch signifikant verlängert. Mit längerer Nachbeobachtung ist dieser Endpunkt mittlerweile signifikant durch die Behandlung mit Gemcitabin verlängert (20,2 Monate vs. 22,8 Monate). Obwohl der mediane absolute Unterscheid auf den ersten Blick scheinbar gering ausfällt, so zeigt sich bei Betrachtung der KaplanMeier-Kurve ein eindeutiger, mit zunehmender Nachbeobachtungszeit sicherlich noch weiter zunehmender Effekt. In der palliativen Situation konnte abgesehen von einer Subgruppe von Patienten, die unter Behandlung mit Gemcitabin/ Erlotinib ein Hautexanthem ≥ Grad 2 entwickeln (20), in den letzten Jahren kein therapeutischer Fortschritt erzielt werden. In diesem Jahr wurden von Kindler die Ergebnisse einer Therapie mit Gemcitabin in Kombination mit zwei molekulargezielten Therapeutika (Gemcitabin/Bevacizumab/Cetuximab vs. Gemcitabin/Bevacizumab/Erlotinib) im Rahmen einer randomisierten PhaseII-Studie (n = 139) vorgestellt (21). Die Ergebnisse waren negativ, somit wird eine weitere Entwicklung dieses Ansatzes im Rahmen einer Phase-III-Studie nicht stattfinden.
Magenkarzinom Bei der palliativen Therapie des Magenkarzinoms stehen in Europa mit Doce-
956 ARS MEDICI 21 ■ 2008
BERICHT
taxel und seit Kurzem dem oralen Fluoropyrimidin-Derivat Capecitabin neue Therapieoptionen zur Verfügung. In Japan und anderen Ländern Südostasiens wird seit Jahren S1, ein weiteres orales Fluoropyrimidin-Derivat, bei der Therapie des Magenkarzinoms eingesetzt. Eine dreiarmige, randomisierte Phase-III-Studie aus China (n = 224) lieferte den Vergleich von S1 versus S1/Cisplatin versus 5-FU/Cisplatin (22). Hierbei zeigte sich der S1/Cisplatin-Arm in Bezug auf Ansprechrate (35% vs. 25% vs. 19%), progressionsfreies Überleben (5,3 Monate vs. 4,2 Monate vs. 2,8 Monate) und Gesamtüberleben (14,2 Monate vs. 8,9 Monate vs. 10,3 Monate) dem S1- und dem 5-FU/Cisplatin-Arm deutlich überlegen. Eine randomisierte koreanische Phase-II-Studie (n = 80) untersuchte, ob die Kombination von S1/Docetaxel der Kombination von Docetaxel/Cisplatin überlegen ist. Hierbei zeigten sich ebenfalls erhebliche Vorteile im S1/Docetaxel-Arm mit einer Ansprechrate von 46 versus 22 Prozent, einem progressionsfreien Überleben von 7,3 Monaten versus 4,9 Monate und einem Gesamtüberleben von bemerkenswerten 21,1 Monaten vs. 8,2 Monate. Wenngleich diese Daten noch im Rahmen eines Phase-III-Konzeptes mit Einschluss westlicher Patienten bestätigt werden müssen, so könnte sich durch eine solche Kombinationstherapie eine erhebliche Prognoseverbesserung erzielen lassen.
Hepatozelluläres Karzinom Der duale Tyrosinkinase-Hemmstoff Sorafenib (MAP-Kinase-Signaltransduktionsweg und VEGF-Rezeptor) ist seit Oktober 2007 bei der Behandlung von Patienten mit hepatozellulärem Karzinom zugelassen (23). An der Zulassungsstudie (SHARP-Studie) nahmen nur westliche Zentren teil. In Asien wurde eine separate plazebokontrollierte Phase-III-Studie (n = 226) durchgeführt, deren Ergebnisse jetzt vorliegen (24). Sowohl die Krankheitskontrollrate
(Krankheitsstabilisierung und Ansprechen: 35% vs. 16%) als auch progressionsfreies Überleben (2,8 Monate vs. 1,4 Monate) und Gesamtüberleben (6,5 Monate vs. 4,1 Monate) konnten durch die Behandlung mit Sorafenib verbessert werden. Hand-Fuss-Syndrom (10%), Durchfall (6%) und Fatigue (3%) waren erwartungsgemäss die häufigsten schwerwiegenden Nebenwirkungen.
Maligner Aszites Wiederholte Parazentesen sind die Standardbehandlung bei malignem Aszites. Daneben ist keine medikamentöse Therapie hinreichend etabliert. Im Rahmen einer randomisierten Phase-II/III-Studie (n = 258) wurde untersucht, ob bei einem Kollektiv von Patienten mit Ovarialkarzinom und peritoneal metastasierten, vor allem gastrointestinalen Tumoren die intraperitoneale Behandlung mit dem Antikörper Catumaxomab wirksam ist (25). Catumaxomab ist gegen das epitheliale Adhäsionsmolekül EpCAM und den Lymphozytenmarker CD3 gerichtet und resultiert in einer Aktivierung von Killerzellen. Als primärer Endpunkt wurde das mediane punktionsfreie Überleben definiert. Durch die viermalige intraperitoneale Gabe von Catumaxomab konnte das punktionsfreie Überleben von 11 auf 46 Tage gesteigert werden. Die mediane punktionsfreie Zeit wurde von 13 auf 72 Tage verlängert.
Fazit Ein wissenschaftlicher Schwerpunkt der aktuellen ASCO-Tagung war die Therapie des kolorektalen Karzinoms: ■ Mit KRAS steht der erste Biomarker bei
dieser Erkrankung zur Verfügung, der es erlaubt, Patienten eine individualisierte Therapie anzubieten. Aufgrund der hohen Ansprechraten von 60 Prozent könnte sich eine Cetuximabbasierte Kombinationstherapie insbesondere für Patienten mit begrenzter Lebermetastasierung als potenzielle neoadjuvante Therapieoption etablieren.
■ Die Anwendung von Bevacizumab in Kombination mit einer Chemotherapie ist gut verträglich, insbesondere dann, wenn ein entsprechender Abstand von 5 bis 6 Wochen zu einer operativen Therapie eingehalten wird.
■ Die Verträglichkeit von Panitumumab in Kombination mit Chemotherapie ist ebenfalls gut, Phase-III-Daten zur Wirksamkeit werden mit Spannung erwartet.
■ Eine schwerwiegende Oxaliplatininduzierte chronische Neuropathie kann durch geplante Oxaliplatinpausen und Fortführung einer Erhaltungstherapie sowie durch Magnesium/ Kalzium-Gabe verhindert werden.
Wenngleich die adjuvante Behandlung
mit Gemcitabin aufgrund der Datenlage
spätestens jetzt Standard sein sollte, gibt
es bei der palliativen Therapie des Pan-
kreaskarzinoms leider keine wesentli-
chen Fortschritte zu berichten. Ansätze
für eine individualisierte Therapie
werden in dieser Indikation dringend
benötigt.
Die intraperitoneale Therapie mit Catu-
maxomab könnte bei Patienten mit ma-
lignem Aszites ein neuer Therapiestan-
dard werden.
■
Korrespondenzadresse: Priv.-Doz. Dr. med. Jörg Trojan Oberarzt der Medizinischen Klinik I Schwerpunkt Gastroenterologie und
Hepatologie Klinikum der Johann-Wolfgang-
Goethe-Universität Theodor-Stern-Kai 7
D-60590 Frankfurt Tel. 0049-(0)69-6301-7860 Fax 0049-(0)69-6301-83776 E-Mail: trojan@em.uni-frankfurt.de
Interessenkonflikte: keine
Literaturliste auf Anfrage beim Verlag erhältlich: info@rosenfluh.ch
958 ARS MEDICI 21 ■ 2008